24 липня, 2017
Современные аспекты проблемы гемолитической болезни плода и новорожденного
(Клиническая лекция)
 Проблема иммунологического конфликта матери и плода остается актуальной в Украине, несмотря на современные достижения в мировой медицинской практике, которые позволили в несколько раз снизить заболеваемость гемолитической болезнью плода и новорожденного, исключить перинатальные потери в связи с изосенсибилизацией по системе групп крови АВ0 и резус-фактору (Rh). В развитых странах предупреждение сенсибилизации D-негативных женщин проведено путем внедрения соответствующих государственных программ.
Проблема иммунологического конфликта матери и плода остается актуальной в Украине, несмотря на современные достижения в мировой медицинской практике, которые позволили в несколько раз снизить заболеваемость гемолитической болезнью плода и новорожденного, исключить перинатальные потери в связи с изосенсибилизацией по системе групп крови АВ0 и резус-фактору (Rh). В развитых странах предупреждение сенсибилизации D-негативных женщин проведено путем внедрения соответствующих государственных программ.
Мировая медицинская практика подтверждает безусловный, гарантированный положительный исход снижения перинатальной заболеваемости и смертности новорожденных, ассоциированных с последствиями изоиммунизации. Механизм действия антител против Rh схематически представлен на рисунке 1.
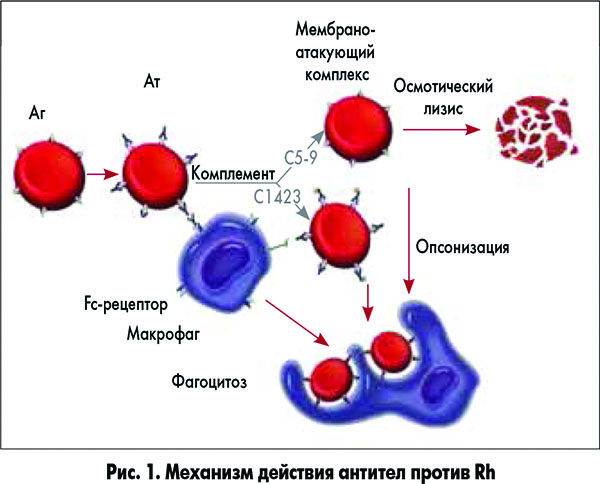 Женщины с отрицательным Rh (Rh–) составляют группу высокого риска по перинатальным потерям. При наличии титра антител в крови у них достоверно чаще регистрируются: самопроизвольные выкидыши (10%), мертворождаемость (14,3%), ранняя неонатальная смертность (11,8%).
Женщины с отрицательным Rh (Rh–) составляют группу высокого риска по перинатальным потерям. При наличии титра антител в крови у них достоверно чаще регистрируются: самопроизвольные выкидыши (10%), мертворождаемость (14,3%), ранняя неонатальная смертность (11,8%).
Перинатальные потери до внедрения системы рутинной профилактики в различных странах составляли: в Великобритании – 76 случаев на 100 000 живорождений; в Австралии – 91 и в США – 89 соответственно (NICE, 2008).
В Украине на сегодняшний день отсутствуют основания считать проблему предупреждения гемолитической болезни плода (ГБП) и гемолитической болезни новорожденного (ГБН) при резус-несовместимой беременности решенной. На протяжении последнего времени частота случаев резус-конфликтной беременности не имеет тенденции к снижению и составляет 1,2-1,5%. В 2013 г. в Украине было зарегистрировано 7,4% случаев ГБП и ГБН на 1000 живых новорожденных. Во всех регионах ежегодно стабильно регистрируются случаи перинатальных потерь, связанных с ГБП и ГБН. В странах ЕС уровень резус-сенсибилизированных женщин на порядок ниже и составляет 0,1-0,2%. Такие показатели – результат повсеместного внедрения программы анти-D-иммунопрофилактики. По данным Харьковского городского перинатального центра, за 2014-2016 гг. частота ГБН составила 1,7%.
Еще в 1939 г. Levine и Stetson обнаружили в сыворотке крови женщины, которая родила мертвого ребенка с асцитом, антитела, взаимодействующие с эритроцитами крови отца ребенка. Последующие открытия позволили понять причину гибели плода в таких случаях и разработать соответствующие методы диагностики, лечения и, самое главное, профилактики данных состояний. C 1971 г. Всемирной организацией здравоохранения (ВОЗ) рекомендован к использованию анти-D-иммуноглобулин внутримышечно в дозировке 25 мкг, что соответствует 125 МЕ, в расчете на каждый миллилитр эритроцитарной массы резус-позитивного плода, попадающей в Rh– кровоток матери. В 1998 г. были обозначены сроки проведения иммунопрофилактики, а именно: в 28 недель всем Rh– несенсибилизированным пациенткам необходимо ввести анти-D-иммуноглобулин в рекомендуемой дозировке.
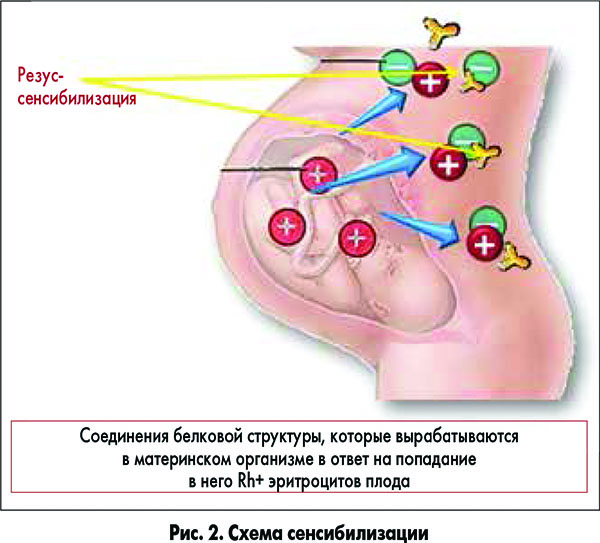
Гемолитическая болезнь плода и новорожденного развивается в результате иммунизации материнского организма эритроцитами плода, содержащими антигены, которые отсутствуют у матери (рис. 2). В мировой популяции существует более 10 изосерологических систем эритроцитарных антигенов. Наиболее часто встречается иммунизация, обусловленная системой Rh (95%), значительно реже данные заболевания связаны с системой АВ0. Антигенные системы крови человека представлены несколькими видами. Rh – это белковый антигенный комплекс, расположенный на внутренней поверхности эритроцитов, реже – в лейкоцитах и тромбоцитах. Антигены системы резуса начинают формироваться с 7-8 недель беременности. В системе резус различают 5 антигенов. Наиболее иммуногенным является антиген D, наличие которого и определяет положительный Rh (Rh+). Rh+ люди могут быть как гомозиготными (DD), так и гетерозиготными (Dd). Гомозиготные Rh+ мужчины составляют 40-45%. Все дети от гомозиготного отца наследуют ген, ответственный за синтез резус-белка, и будут Rh+. При гетерозиготности (Dd) отца Rh+ дети родятся в 50% случаев. Из Rh антигенов наиболее распространенные 3 вида, но существует более 6 аллелей антигенов (C, D, E и c, d, e). D (Rh) имеется у 85% людей, C (Rh) – у 70%, Е (Rh) – у 30%. Наличие на эритроцитах хоть одного из них делает человека Rh+. До настоящего времени в антигенной детерминанте Dd антиген d не подтвержден, также не идентифицирован ген, ответственный за синтез d. Символ d используется в иммуногематологии для обозначения отсутствия антигена D на эритроцитах. Распространенность антигена D в крови у представителей разных этнических групп различна. В европейской популяции носители антигена D составляют около 86%, соответственно, доля Rh– людей, у которых отсутствует антиген D, составляет около 14%.
 AB0-конфликт проявляется чаще, если у матери – 0 (l) группа крови, а у плода – А (II) или В (III) группа. Более легкое течение ГБП и ГБН при групповой несовместимости А (II) и В (III), в сравнении с резус-конфликтом, связано с меньшей иммуногенностью факторов как группы А (II), так и группы B (III), а также защитной ролью плацентарного барьера и околоплодных вод, которые адсорбируют комплексы антиген-антитело. Группа крови А (II) является более сильной в антигенном отношении, чем группа В (III).
AB0-конфликт проявляется чаще, если у матери – 0 (l) группа крови, а у плода – А (II) или В (III) группа. Более легкое течение ГБП и ГБН при групповой несовместимости А (II) и В (III), в сравнении с резус-конфликтом, связано с меньшей иммуногенностью факторов как группы А (II), так и группы B (III), а также защитной ролью плацентарного барьера и околоплодных вод, которые адсорбируют комплексы антиген-антитело. Группа крови А (II) является более сильной в антигенном отношении, чем группа В (III).
Основным условием развития ГБП и ГБН является попадание эритроцитов плода, отличных по антигенному составу, через плаценту в кровоток матери. Первичный контакт эритроцитов плода с кровью матери приводит к образованию полных антител, относящихся к классу IgM. Эти антитела имеют большие размеры, мало переходят к плоду и не представляют для него опасности. Вторичными являются неполные антитела, блокирующие и агглютинирующие эритроциты, они относятся к классам IgG, IgA.
Блокирующие антитела могут действовать на эритроцитах без их агглютинации. IgG относительно малого размера и могут проходить через плаценту, приводя к развитию гемолитической болезни. Существует два основных класса IgG (неполных антител): IgG1 и IgG3. IgG3 имеют большую тропность к ретикулоэндотелиоцитам и легко связываются с ними, вызывая гемолиз. Треть женщин не имеют IgG3, поэтому риск развития резус-конфликта у них снижен.
Некоторые антитела, включая анти-D, анти-К, анти-С, связаны со значительными фетальными и перинатальными рисками, прежде всего анемией, желтухой или перинатальными потерями. Существуют также множество антител, которые не оказывают существенного влияния на плод.
Иммунные антитела в организме женщины могут появиться в результате переливания несовместимой крови либо беременности, завершенной родами или абортом с несовместимыми по антигенному составу системами крови матери и плода. В ряде случаев еще до беременности у женщин определяются антитела после повторных профилактических вакцинаций. Это связано с тем, что некоторые вакцины выращиваются на питательных средах, содержащих А-фактор.
Развитие ГБП и ГБН под влиянием антител матери связано не только с гемолизом эритроцитов плода, но и с угнетением эритропоэза плода антителами матери.
Частота резус-D-иммунизации во время или после первой беременности Rh+ плодом составляет около 10%. Риск и степень изоиммунизации по Rh зависят от величины так называемой фетоматеринской геморрагии (ФМГ) и следующих факторов: внематочной беременности (1%), самопроизвольного аборта (3-4%), искусственного аборта (если прерывание беременности произошло после 7-8 недель); переливания Rh+ крови (2-5%). Некоторые клинические состояния приводят к большей фетоматеринской геморрагии. Примерно 99% женщин имеют фетоматеринскую геморрагию <4 мл на один случай нормальных родов, 50% из них – >4 мл. Увеличивают ФМГ кесарево сечение, ручное удаление плаценты, мертворождение, травма живота во время III триместра, многоплодная беременность (интранатально). Титр изоиммунных антител изменяется при повторном попадании антигена в кровоток матери, он зависит от количества антигена и способности материнского организма продуцировать антитела. При вынашивании Rh+ ребенка, несовместимого по системе АВ0, снижается риск иммунизации по Rh.
Патогенез развития гемолитической болезни плода и новорожденного достаточно хорошо изучен, особенности его не зависят от вида антигена, вызвавшего гемолитическую болезнь. При попадании в кровоток матери антирезусные антитела сначала блокируют, а затем вызывают агглютинацию эритроцитов плода, иногда она происходит и без их блокирования. При разрушении комплексов эритроцитов выделяется гемоглобин, который во внеклеточном пространстве превращается в непрямой билирубин, клинически это проявляется анемией различной степени тяжести и гипербилирубинемией. Непрямой билирубин токсичен, является жирорастворимым, легко проникает в жировую ткань, подавляет ферментные процессы, вызывает некрозы. Он проникает в митохондрии и приводит к нарушению в них: дыхания и окислительного фосфорилирования, синтеза белка, потока ионов калия через мембрану клетки и органелл. Это отрицательно сказывается на состоянии нервной системы, вызывая у детей, перенесших ГБ, ряд характерных неврологических симптомов. Непрямой билирубин может проникать через гематоэнцефалический барьер, действует на клетки базальных ядер головного мозга, вызывает гипербилирубинемическую токсическую энцефалопатию (ядерную желтуху). Значительно чаще ядерная желтуха развивается у недоношенных детей. Энцефалопатия в дальнейшем проявляется нарушением умственного развития с поздним развитием основных функций и навыков. Анемия усиливает функцию костного мозга по выработке молодых незрелых форм эритроцитов, увеличиваются очаги эритропоэза в печени, сгущается желчь и расширяются желчные протоки, развивается спленомегалия, гепатомегалия с нарушением функции этих органов. Последствиями этого являются гипопротеинемия, портальная гипертензия, асцит и генерализованные отеки. Предпринимаются попытки прогнозировать с помощью ультразвуковых маркеров токсический гепатит у новорожденных, перенесших тяжелые формы гемолитической болезни с заменным переливанием крови. Самые тяжелые формы ГБП и ГБН проявляются асцитом, который развивается как результат гипертензии в портальной и пупочной венах из-за увеличения и анатомических изменений в печени. Вследствие эритропоэза в печеночной ткани развивается гипопротеинемия из-за печеночной недостаточности с дисфункцией отечной плаценты (нарушений в переносе аминокислот и пептидов). Первоначально считалось, что асцит у плода – это результат сердечной недостаточности на фоне тяжелой анемии и гиперволемии. Последствия осложнений резус-конфликта следующие: органопатии (спленомегалия, гепатомегалия), интоксикационный синдром, гипоксия плода (в том числе острая), энцефалопатии с нарушением когнитивных функций, внутриутробная гибель плода. Таким образом, вопросы предотвращения тяжелейших осложнений аллоиммунизации для плода вплоть до его гибели становятся первоочередными.
Rh– беременным, вынашивающим Rh– детей, нет необходимости проводить антенатальную анти-D-иммунопрофилактику. В популяции Rh– женщины европеоидной расы вынашивают около 38% Rh– детей, им антенатальная анти-D-иммунопрофилактика не показана.
С 2002 г. используется молекулярно-генетический метод полимеразной цепной реакции (ПЦР) в реальном масштабе времени (NIPT) для неинвазивного антенатального определения Rh плода по фетальной ДНК. Возможные сроки проведения теста – с 11 недель беременности. Точность определения резус-принадлежности плода по крови матери возрастает с увеличением срока беременности и достигает почти 100% с 23 недель при ложноотрицательных результатах, которые составляют 0,1-0,3%. В Украине проводится стандартная рутинная антенатальная профилактика анти-D-иммуноглобулином вне зависимости от резус-принадлежности плода и постнатальная при рождении Rh+ ребенка, регламентированные клиническими протоколами (Приказ МЗ Украины от 15.07.2011 № 417 «Об организации амбулаторной акушерско-гинекологической помощи в Украине» и Приказ МЗ Украины от 31.12.2004 № 676 «Об утверждении клинических протоколов по акушерской и гинекологической помощи»).
Учитывая дороговизну метода NIPT, его рутинное проведение для определения резус-принадлежности плода всем Rh– женщинам, вынашивающим детей от Rh+ отцов, считается нецелесообразным.
Со времени открытия феномена антигенной несовместимости крови матери и плода уже достаточно много известно о проблеме иммуноконфликтной беременности по системе Rh и системе АВ0. Клинический опыт, основанный на разработках ведущих мировых клиник, представлен в виде практических рекомендаций и опубликован в 2014 г. британским Королевским колледжем акушеров-гинекологов (RCOG). Создание обновленного руководства было обусловлено необходимостью определения клинически значимого потенциала эритроцитарных антител для развития ГБП и ГБН и возможности их предотвращения. При этом были приняты во внимание недавние события в медицине плода, такие как широко распространенное использование неинвазивного ультразвукового допплеровского мониторинга анемии плода по среднемозговой артерии (СМА) вместе с определением генотипа плода по ДНК плода в образцах материнской крови во многих потенциальных случаях развития ГБП и ГБН.
Тематичний номер «Гінекологія, Акушерство, Репродуктологія» № 2 (26), червень-липень 2017 р.


