6 серпня, 2017
Вибір неседативного антигістамінного препарату
Кропив’янка – поширене шкірне захворювання, що характеризується нестерпним свербежем і появою на шкірі блідо-рожевих пухирів, схожих на пухирі від жалення кропивою. Гостра кропив’янка обумовлена зазвичай дією на організм екзогенних факторів та алергенів, а хронічна є або вторинним проявом низки інших соматичних захворювань, або не має встановленої причини. В останньому випадку говорять про хронічну ідіопатичну кропив’янку (ХІК), і саме ця клінічна форма нині домінує в структурі цього захворювання. Згідно з останніми даними, частота ХІК у загальній популяції становить 1-3% (Greiwe J., Bernstein J. A. et al., 2017).
Це захворювання істотно погіршує якість життя пацієнтів, оскільки для нього характерне часте, рецидивуюче виникнення на шкірі еритематозних пухирів, що супроводжується вираженим свербежем та спостерігається протягом ≥6 тижнів. При цьому надійне усунення симптомів ХІК є складним клінічним завданням, вирішення якого потребує від лікаря індивідуального підходу та урахування таких факторів, як гістопатологічні особливості ураження шкіри, вік пацієнта, супутні захворювання, а також фармакологічні характеристики та доказова база обраних лікарських засобів. Основою лікування ХІК є застосування Н1-антигістамінних препаратів (АГП). Однак, попри наявність на фармацевтичному ринку широкого асортименту сучасних лікарських засобів цього класу, приблизно у 10% пацієнтів з ХІК перебіг захворювання не вдається контролювати навіть при їх використанні в дуже високих дозах, що перевищують стандартні зареєстровані (Asero R. et al., 2015). Чи може лікар на основі знань про особливості фармакокінетики та фармакодинаміки конкретних АГП прогнозувати клінічну ефективність цих засобів та які з них переконливо підтвердили здатність усувати свербіж та пухирі на шкірі в експериментальних та клінічних дослідженнях за участю пацієнтів із кропив’янкою? Саме про це буде йти мова в цьому огляді.
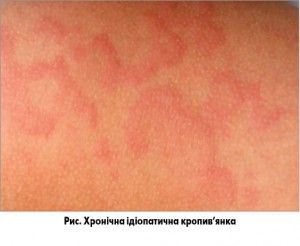 Як відомо, головним медіатором у патогенезі виникнення симптомів кропив’янки є гістамін, який виділяється тучними клітинами шкіри та досягає в ній дуже високих тканинних концентрацій. Саме тому базисними засобами медикаментозного лікування ХІК (рис.) є АГП. При цьому безперечна перевага сьогодні надається сучасним неседативним АГП II покоління, які на відміну від АГП I покоління забезпечують більш тривалу дію і позбавлені багатьох побічних ефектів з боку центральної нервової системи. Однак у сучасних настановах відсутні дані щодо порівняльної ефективності АГП при кропив’янці і, відповідно, немає чітких рекомендацій стосовно вибору того чи іншого препарату. Тож спробуємо розібратися в цьому питанні за допомогою аналізу фармакології, активності in vivo і клінічної ефективності трьох найбільш вивчених у порівняльних дослідженнях АГП II покоління – дезлоратадину, фексофенадину і левоцетиризину.
Як відомо, головним медіатором у патогенезі виникнення симптомів кропив’янки є гістамін, який виділяється тучними клітинами шкіри та досягає в ній дуже високих тканинних концентрацій. Саме тому базисними засобами медикаментозного лікування ХІК (рис.) є АГП. При цьому безперечна перевага сьогодні надається сучасним неседативним АГП II покоління, які на відміну від АГП I покоління забезпечують більш тривалу дію і позбавлені багатьох побічних ефектів з боку центральної нервової системи. Однак у сучасних настановах відсутні дані щодо порівняльної ефективності АГП при кропив’янці і, відповідно, немає чітких рекомендацій стосовно вибору того чи іншого препарату. Тож спробуємо розібратися в цьому питанні за допомогою аналізу фармакології, активності in vivo і клінічної ефективності трьох найбільш вивчених у порівняльних дослідженнях АГП II покоління – дезлоратадину, фексофенадину і левоцетиризину.
Фармакокінетика і фармакодинаміка АГП
Для попереднього прогнозування ефективності того чи іншого АГП необхідно знати два основні параметри: його афінність (спорідненість) до Н1-рецепторів гістаміну та концентрацію, яку він створює в рецепторних ділянках in vivo. Результати експериментальних досліджень in vitro з радіоактивним мепіраміном щодо оцінки конкурентного зв’язування з рецепторами засвідчили, що значення показника афінності (Ki) до клонованих Н1-рецепторів в ізольованих клітинах у дезлоратадину, левоцетиризину і фексофенадину становлять 0,4; 3 і 10 нм відповідно.
Іншим важливим параметром є концентрація препарату в місці його дії – тобто безпосередньо в шкірі. Але чи можна розрахувати цей показник та спрогнозувати клінічну ефективність АГП на підставі знання лише плазмових концентрацій цих лікарських засобів? Щоб відповісти на питання, слід докладніше зупинитися на патофізіології кропив’янки та її провідних симптомів – висипу і свербежу. На фоні захворювання гістамін вивільняється з мастоцитів, які знаходяться в тканинах поза кровоносних судин. Цей процес можна відтворити шляхом внутрішньошкірного введення гістаміну. Головною патофізіологічною подією при кропив’янці є вазодилатація, описана Lewis 1927 року як почервоніння шкіри в місці ін’єкції гістаміну. Ця відповідь опосередковується стимуляцією Н1-рецепторів гладеньких м’язів кровоносних судин. У подальшому гістамін із тканин потрапляє в кровоток і стимулює Н1-рецептори на поверхні післякапілярних венулярних ендотеліоцитів, що підвищує проникність судин і спричиняє висип та набряк. Оскільки вазодилатація є первинною і домінуючою шкірною відповіддю, ефективність АГП при кропив’янці визначається концентрацією препарату в позасудинних шарах шкіри і меншою мірою залежить від плазмової концентрації. Крім того, свербіж виникає внаслідок стимуляції Н1-рецепторів на чутливих нервах виключно поза судинами.
Отже, висип і свербіж пригнічуються лише молекулами препарату, які перебувають у позасудинних шарах шкіри, а не в системній циркуляції. Виходячи з цього важливим фактором, який визначає клінічну ефективність АГП, є тканинна концентрація препарату.
Відомо, що плазмова концентрація левоцетиризину стає максимальною приблизно через 1 год після його прийому, тоді як зменшення висипу і свербежу досягає максимальних рівнів через 2 год. Це свідчить про те, що дифузія вільного препарату з плазми в позасудинний простір є стримуючим фактором дії АГП. Левоцетиризин діє довше, ніж це можна було б очікувати на підставі плазмових концентрацій. Отже, препарат захоплюється шкірою і потрапляє в «пастку», ймовірно, завдяки зв’язуванню з білками, абсорбції всередину клітин або розчиненню в ліпідах.
Докази того, що АГП накопичуються в шкірі, були отримані в ході дослідження Frossard і співавт. Було встановлено, що через 24 год після однократного перорального прийому левоцетиризину в дозі 5 мг загальна концентрація препарату в шкірі вдвічі перевищує його загальну плазмову концентрацію (40±19 нг/г у шкірі порівняно з 20±8 нг/мл у плазмі).
АГП можуть накопичуватись у шкірі декількома шляхами. По-перше, АГП зв’язуються з Н1-рецепторами гістаміну впродовж тривалого часу. Встановлено, що напівперіод дисоціації від Н1-рецепторів для левоцетиризину, фексофенадину і дезлоратадину становить 142, 62 і 5 хв відповідно. По-друге, АГП залишаються в позаклітинному просторі і можуть взаємодіяти з Н1-рецепторами. По-третє, АГП у залишковій кількості можуть перебувати в шкірі у фармакологічно неактивній формі внаслідок зв’язування з білками або екстрацелюлярним матриксом, потрапляння всередину клітин або абсорбцію в жирову тканину. Відомо, що інгібування пухирів і еритеми дезлоратадином і фексофенадином є значно меншим через 24 год порівняно з максимальним пригніченням через 3-4 год після прийому.
Загалом ці дані свідчать, що клінічну ефективність Н1-блокаторів не можна прогнозувати, базуючись тільки на даних про їх спорідненість з Н1-рецепторами та активність, отриманими в дослідженнях in vitro, оскільки на ефективність АГП in vivo впливають й інші важливі фактори, зокрема метаболізм, екскреція, розчинність у ліпідах, ступінь і міцність зв’язування з білками і структурними елементами, проникнення і накопичення в тканинах тощо. Отже, для реальної клінічної практики вагомим аргументом при виборі того чи іншого АГП є результати досліджень in vivo та клінічних досліджень за участю пацієнтів із кропив’янкою.
Дослідження in vivo
Провокаційна проба з гістаміном (оцінка пухиря та еритеми після внутрішньошкірного введення гістаміну) тривалий час вважалася основним тестом in vivo для прогнозування клінічної ефективності АГП. Проте чи є ця проба дійсно прогностичною? Два великих огляди літератури дають негативну відповідь на це питання. Monroe і співавт. у 1997 р. проаналізували дослідження АГП I і II покоління і дійшли висновку, що хоча провокаційна проба з гістаміном може слугувати корисним клініко-фармакологічним тестом для оцінки дозозалежної відповіді на АГП, проте вона не корелює з клінічною відповіддю, і, отже, цю модель не можна використовувати як прогнозування або порівняння клінічної ефективності АГП при сезонному алергічному риніті або ХІК. Пізніше, 2007 року, Devillier і Bousquet провели огляд літератури за період 1980-2006 рр. стосовно 16 АГП I і II покоління і встановили, що препарати відрізнялися за своєю здатністю пригнічувати гістамініндуковане утворення пухиря й еритеми, але ці відмінності не корелювали з різницею в клінічній ефективності при алергічному риніті або хронічній кропив’янці. Однак слід зазначити, що в цьому огляді не були достатньо представлені два сучасні АГП для лікування пацієнтів з кропив’янкою – дезлоратадин і левоцетиризин.
До нового огляду, проведеного 2017 року, включили 10 досліджень, у яких порівнювалася відповідь на однократний прийом дезлоратадину, фексофенадину або левоцетиризину в провокаційній шкірній пробі з гістаміном. Результати показали, що за силою ефекту фексофенадин і левоцетиризин були значно кращими, ніж дезлоратадин. Крім того, після прийому левоцетиризину відповідь наставала швидше (через 1 год) порівняно з дезлоратадином.
Максимальний ефект усіх трьох препаратів спостерігався приблизно через 4 год після прийому. Проте, коли провокаційну пробу виконали через 24 год після прийому, у 3 із 4 досліджень левоцетиризин виявився значно ефективнішим, ніж фексофенадин. Це свідчить про більш тривалу антигістамінну дію левоцетиризину.
Ефективність у клінічних дослідженнях при кропив’янці
Існує 3 дослідження, у яких безпосередньо порівнювалися левоцетиризин і дезлоратадин у пацієнтів з ХІК. На жаль, досліджень ефективності фексофенадину порівняно з левоцетиризином або дезлоратадином не проводилося.
Порівняння ефективності левоцетиризину (в дозі 5 мг/добу) і дезлоратадину (в дозі 5 мг/добу) при лікуванні ХІК було проведено в багатоцентровому рандомізованому подвійному сліпому дослідженні, в якому взяли участь 886 пацієнтів: 438 приймали левоцетиризин, а 448 – дезлоратадин (Potter P. C. et al., 2009). Результати показали, що застосування левоцетиризину протягом 1-го і 4-го тижня терапії супроводжувалося статистично більш значним зменшенням тяжкості свербежу (первинна кінцева точка), ніж при використанні дезлоратадину. Зменшення середніх показників вираженості свербежу на 1-му тижні становило 53,4% у групі левоцетиризину і 46,9% у групі дезлоратадину (p<0,001), а на 4-му тижні – 62,4 і 57,6% відповідно (p<0,004). Крім того, у групі хворих, які отримували левоцетиризин, спостерігався достовірно більш тривалий період зменшення свербежу та проявів кропив’янки, ніж у групі хворих, які отримували дезлоратадин, – як протягом 1-го тижня (р=0,002 і р<0,005 відповідно), так і протягом усього періоду дослідження (р=0,009 і р<0,05 відповідно). Задоволеність лікуванням через 1 і 4 тиж була значно вищою в групі пацієнтів, які отримували левоцетиризин (р=0,012 і р<0,021 відповідно). Таким чином, левоцетиризин, демонструючи швидку і тривалу протиалергічну дію, виявився більш ефективним, ніж дезлоратадин.
У другому рандомізованому подвійному сліпому дослідженні пацієнтів з ХІК обстежували кожні 2 тиж протягом 6 тиж (Hong J. B. et al., 2010). Багатомірний аналіз із поправкою на вік, стать, індекс маси тіла, ниркову і печінкову функцію, загальний стан здоров’я, зміни схеми лікування, супутню терапію та інші параметри показав, що левоцетиризин незалежно асоціювався з кращою терапевтичною відповіддю, ніж дезлоратадин (р=0,0468).
Метою третього рандомізованого подвійного сліпого дослідження тривалістю 4 тиж було порівняти ефективність левоцетиризину (n=40) і дезлоратадину (n=40) у дозах, що до 4 разів перевищували стандартні, у пацієнтів з резистентною до лікування кропив’янкою (Staevska M. et al., 2010). Дози препаратів збільшували щотижня. При застосуванні дози 5 мг симптоми були відсутні в 30 пацієнтів (9 у групі левоцетиризину vs 4 у групі дезлоратадину) порівняно з 28 пацієнтами в разі використання більш високих доз – 10 мг (8 vs 7 відповідно) і 20 мг (5 vs 1 відповідно). Крім того, перехід на левоцетиризин дозволив повністю нівелювати симптоми в 7 з 20 пацієнтів, які не відповіли на терапію дезлоратадином у дозі 20 мг. І, навпаки, жоден з пацієнтів, які не відповіли на терапію левоцетиризином у дозі 20 мг, не отримав користі від переведення на дезлоратадин. Аналіз оцінок за візуальною аналоговою шкалою дискомфорту також показав, що левоцетиризин був ефективнішим за дезлоратадин (р<0,03).
Висновки
Кропив’янка (особливо її хронічна ідіопатична форма) є розповсюдженим і досить часто – стійким до лікування захворюванням, яке значно погіршує якість життя пацієнтів. Отже, для її базисної терапії лікарі повинні обирати ефективні АГП. Дані експериментальних та клінічних досліджень, представлені в цьому огляді, свідчать, що левоцетиризин швидко й ефективно зменшує прояви кропив’янки і, отже, може розглядатися як оптимальний неседативний АГП для лікування пацієнтів із цим захворюванням.
Non-sedating H1-antihistamines are the mainstay of treatment for urticaria (Editorial). Pharmacy
Magazine, 2017 (April): 35-40.
Стаття друкується в скороченні.
Переклав з англ. Олексій Терещенко
Медична газета «Здоров’я України 21 сторіччя» № 13-14 (410-411), липень 2017 р.


