2 липня, 2017
Міжнародна конференція «Досягнення неврології» (6-8 квітня, м. Київ). Майстер-класи
Нейропротекція в комплексній реабілітації при органічних ураженнях головного мозку:
досвід польських колег
 Президент і керівник Польського центру функціональної реабілітації «Votum» (м. Краків) Павел Адамкевич поділився досвідом відновного лікування та реабілітації пацієнтів після інсультів і черепно-мозкових травм (ЧМТ). Доповідач розповів про застосування концепції Bobath у нейрореабілітації. Концепція Bobath є проблемно-орієнтованим підходом до оцінки й лікування пацієнтів із порушеннями рухових функцій і постурального контролю внаслідок ураження центральної нервової системи. Обґрунтування цієї концепції засновано на сучасних знаннях про управління рухом, моторне навчання, нервову та м’язову пластичність, а також на знанні біомеханічних особливостей людини та її рухів. Клінічна реалізація концепції Bobath передбачає застосування індивідуального набору втручань. Концепція прагне до 24-годинного міждисциплінарного підходу до ведення пацієнта, коли сам хворий, його родина, всі члени мультидисциплінарної команди (невролог, реабілітолог, психолог, фізіотерапевт, логопед) працюють разом для досягнення поставлених цілей. Фармакологічне лікування після інсультів і ЧМТ спрямоване на корекцію метаболічних процесів, які відбуваються в пошкодженій мозковій тканині. Серед нейропротекторів, з яким польські фахівці мають досвід роботи, лектор зазначив холіну альфосцерат (препарат Гліатилін). Холіну альфосцерат є донором холіну, з якого утворюється ацетилхолін, і попередником для синтезу фосфатидилхоліну – основного компонента клітинних мембран. Ацетилхолін є критично необхідним нейромедіатором для реалізації всіх когнітивних функцій (пам’яті, мислення, уваги), тому Гліатилін передусім відзначається виразними прокогнітивними ефектами, а також як регулятор рівня свідомості. Гліатилін захищає від пошкодження нейрональні мембрани, підвищує рівень свідомості, сприяючи виходу з коми («пробуджувальний ефект»), підтримує альтернативні способи спілкування до відновлення мови. Багаторазово доведено його позитивний вплив на функції пам’яті, уваги, мислення та засвоєння нової інформації. Підвищення здатності до навчання та активувальний ефект важливі для залучення пацієнта до участі в реабілітаційних програмах.
Президент і керівник Польського центру функціональної реабілітації «Votum» (м. Краків) Павел Адамкевич поділився досвідом відновного лікування та реабілітації пацієнтів після інсультів і черепно-мозкових травм (ЧМТ). Доповідач розповів про застосування концепції Bobath у нейрореабілітації. Концепція Bobath є проблемно-орієнтованим підходом до оцінки й лікування пацієнтів із порушеннями рухових функцій і постурального контролю внаслідок ураження центральної нервової системи. Обґрунтування цієї концепції засновано на сучасних знаннях про управління рухом, моторне навчання, нервову та м’язову пластичність, а також на знанні біомеханічних особливостей людини та її рухів. Клінічна реалізація концепції Bobath передбачає застосування індивідуального набору втручань. Концепція прагне до 24-годинного міждисциплінарного підходу до ведення пацієнта, коли сам хворий, його родина, всі члени мультидисциплінарної команди (невролог, реабілітолог, психолог, фізіотерапевт, логопед) працюють разом для досягнення поставлених цілей. Фармакологічне лікування після інсультів і ЧМТ спрямоване на корекцію метаболічних процесів, які відбуваються в пошкодженій мозковій тканині. Серед нейропротекторів, з яким польські фахівці мають досвід роботи, лектор зазначив холіну альфосцерат (препарат Гліатилін). Холіну альфосцерат є донором холіну, з якого утворюється ацетилхолін, і попередником для синтезу фосфатидилхоліну – основного компонента клітинних мембран. Ацетилхолін є критично необхідним нейромедіатором для реалізації всіх когнітивних функцій (пам’яті, мислення, уваги), тому Гліатилін передусім відзначається виразними прокогнітивними ефектами, а також як регулятор рівня свідомості. Гліатилін захищає від пошкодження нейрональні мембрани, підвищує рівень свідомості, сприяючи виходу з коми («пробуджувальний ефект»), підтримує альтернативні способи спілкування до відновлення мови. Багаторазово доведено його позитивний вплив на функції пам’яті, уваги, мислення та засвоєння нової інформації. Підвищення здатності до навчання та активувальний ефект важливі для залучення пацієнта до участі в реабілітаційних програмах.
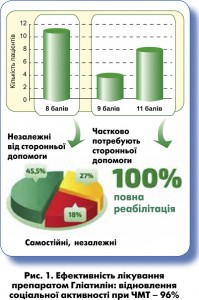
Т. Мандат і співавт. під керівництвом професора Я.К. Підгорського в неврологічній клініці WAM (м. Варшава) протягом 2000-2001 років проводили дослідження ефектів холіну альфосцерату в пацієнтів із ЧМТ різного ступеня тяжкості – гострими субдуральними гематомами, мультифокальним забиттям головного мозку, струсом головного мозку. Покращення відзначали в 96% випадків (рис. 1). Показано, що лікування Гліатиліном істотно підвищувало ефективність реабілітаційних заходів і сприяло швидшому відновленню мови, когнітивних функцій і моторики. Як зауважив лектор, фармакологічна нейропротекція створює необхідне підґрунтя для активації процесів нейропластичності, на яких базуються всі методи фізичної реабілітації – рання мобілізація, ерготерапія, Bobath-терапія тощо.
Загадки посттравматичного головного болю
 Завідувач кафедри неврології, нейрохірургії та психіатрії Ужгородського національного університету, доктор медичних наук Михайло Михайлович Орос здійснив цікавий розбір клінічного випадку, на якому продемонстрував труднощі диференційної діагностики цервікокраніалгії.
Завідувач кафедри неврології, нейрохірургії та психіатрії Ужгородського національного університету, доктор медичних наук Михайло Михайлович Орос здійснив цікавий розбір клінічного випадку, на якому продемонстрував труднощі диференційної діагностики цервікокраніалгії.
Пацієнтка 56 років звернулася зі скаргами на періодичний пульсуючий біль голови в потилиці, в лівій руці, шиї та скроні, частіше однобічний, що супроводжується епізодами головокружіння, нудоти, осцилопсії, часто з фотофобією. Тривалість нападу – від кількох годин до 2 діб, частота – 1-2 рази на місяць.
Анамнез хвороби. Вважає себе хворою протягом року. Неодноразово лікувалася в невролога, оториноларинголога, мануального терапевта та травматолога. Прийом бетагістину ефекту не давав. Є нетривалий ефект від нестероїдних протизапальних препаратів (НПЗП), напади болю та головокружіння знімає парентеральними аналгетиками.
Анамнез життя. Росла та розвивалася в нормальних умовах. Має троє дітей, роди природні. Перенесена пневмонія у 23 роки, хронічний холецистит. Потрапила в дорожньо-транспортну пригоду 1,5 року тому (зі слів, без наслідків). У молоді роки страждала на мігрень без аури, після менопаузи періодично відзначала незначний головний біль.
Неврологічний статус. Вогнищевої симптоматики не виявлено. Виявлено болючі точки в м’язах шиї, спини та верхніх кінцівок, але без іррадіації болю.
Параклінічні обстеження (загальний аналіз крові та аудіометрія) відхилень від норми не виявили. Рентгенографія в боковій проекції та магнітно-резонансна томографія шиї структурної патології не виявили.
Попередній діагноз – цервікокраніалгія, або цервікогенний головний біль (ЦГБ). Але що послужило його причиною?
Лектор нагадав діагностичні критерії ЦГБ (за F. Antonaci, 2001):
1. Однобічний головний біль без зміни сторони болю.
2. Біль спричиняють: різкі рухи в шиї, незручне положення шиї та голови, зовнішній тиск на шию й потилицю; біль обмежує рухи в шиї.
3. Епізодичні болі різної інтенсивності та тривалості.
4. Відсутній пульсуючий характер болю, біль помірний.
5. Біль починається з шиї й поширюється на скроню та чоло.
6. Блокади з використанням місцевих анестетиків можуть привести до зникнення болю.
7. Характерні різні вегетативні супутники нападу болю: нудота, набряк, почервоніння обличчя, головокружіння, фоно- та фотофобії, нечіткість контурів предметів у іпсилатеральному бічному полі зору.
Існують також діагностичні критерії ЦГБ Міжнародного товариства з вивчення головного болю (IHS, 2004), які за змістом дуже схожі, але додатково містять критерій зникнення болю протягом 3 міс після того, як було проведено успішне лікування захворювання чи пошкодження шийних структур, розціненого як причина болю.
Як правило, джерелом цервікогенного болю є структури шийного відділу хребта, а саме добре іннервована задня поздовжня зв’язка. Механізм її подразнення пов’язаний з особливостями біомеханіки шиї: під час повороту голови виникає обертальний момент навколо передньої частини міжхребцевого диска, тоді як задня його частина перерозтягується та може пошкоджуватися.
За характеристиками та локалізаціями ЦГБ може імітувати специфічні больові синдроми, такі як мігрень і тригемінальна невралгія. Це пояснюється взаємодією перших трьох спинномозкових нервів (C1-C3) із трійчастим нервом на рівні ядер спінального трійчастого тракту. Тому ЦГБ рідко має якусь одну визначену локалізацію. Якщо біль відчувається лише в потиличній ділянці, то він спричинений подразненням потиличного нерва.
Для лікування ЦГБ із різною ефективністю застосовують мануальну терапію, лікувальну фізкультуру, черезшкірну електростимуляцію нервів, блокаду великого потиличного нерва, введення кортикостероїдів у суглоб С2-С3, радіочастотну нейротомію, хондропротектори. Лектор наголосив на тому, що НПЗП можуть полегшувати головний біль, але вони не лікують цервікогенну причину болю.
Дещо докладніше лектор прокоментував можливості застосування хондропротекторів, до яких належать препарати глюкозаміну/хондроїтину й препарати неомилюваних сполук авокадо та сої (Піаскледин). Північноамериканська
асоціація ортопедів заявляє про їхню ефективність за даними багатьох досліджень при різних суглобових синдромах від 5 до 10%, і про це слід повідомляти пацієнтів. Інше питання: що безпечніше – НПЗП чи хондропротектори? Пацієнта можна запевнити, що лікування Піаскледином буде безпечним. Окрім того, на відміну від НПЗП, Піаскледин має доведені трофічні властивості – підвищує експресію факторів росту хрящової й кісткової тканини. При цьому пригнічується низка прозапальних цитокінів і молекул пошкодження хрящової тканини – інтерлейкіни 1, 6 та 8, колагеназа, стромелізин, простагландин Е2. Отже, терапія Піаскледином сприяє відновленню балансу катаболічних і анаболічних процесів у хрящовій тканині, що може застосовуватися в терапії артропатій різного походження. Зазначені механізми дії зумовлюють власний протибольовий ефект препарату.
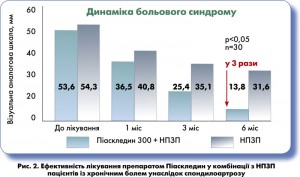
У відкритому рандомізованому дослідженні Н.А. Шостака та Н.Г. Правдюка (2008) вивчали ефективність і безпечність препарату Піаскледин 300 у комбінації з НПЗП порівняно з НПЗП у двох паралельних групах пацієнтів із хронічним болем у нижній частині спини, що був пов’язаний зі спондилоартрозом. На тлі комбінованої терапії з використанням Піаскледину спостерігали зменшення виразності больового синдрому, який пацієнти оцінювали за візуальною аналоговою шкалою. Протибольовий ефект зростав у міру збільшення тривалості прийому препарату. З третього місяця лікування достовірне зменшення болю відзначали лише в групі комбінованої терапії, а на шостому місяці виразність болю була практично в 3 рази меншою в групі Піаскледин + НПЗП порівняно з групою, де застосовували лише НПЗП (рис. 2). Клінічну ефективність відзначено у 89,2% хворих: у них значно знизилися показники болю в спині, покращився функціональний стан хребта, що поєднувалося з доброю переносимістю препарату.
Повертаючись до розгляду клінічного випадку, лектор зазначив, що скарги та результати обстеження пацієнтки не задовольняють діагностичним критеріям ЦГБ. Для цього типу болю не типовий пульсуючий характер, про який говорить пацієнтка. Рухи шиї, за словами хворої, не посилюють біль. До того ж, незважаючи на різноманітні методи лікування, больовий синдром не зник протягом 3 міс, і пацієнтка зазначає, що хворіє вже протягом року.
Зрештою можна було запідозрити міофасціальний синдром (МФС) – варіант неспецифічного м’язово-скелетного болю з тригерними точками в м’язах і фасціях шиї. Він є причиною близько половини всіх випадків ЦГБ. Типові локалізації тригерних точок – у m. sternocleidomastoideus, верхній частині трапецієвидного м’яза, косих м’язах шиї. Для кожної групи м’язів описано характерні патерни іррадіації болю в різні ділянки голови.
Діагностичні критерії МФС поділяють на «великі» (обов’язкові) та «малі» (додаткові).
До великих критеріїв належать:
– скарги на регіональний біль;
– наявність тугого тяжу в м’язі при пальпації;
– ділянки підвищеної чутливості в межах тяжу;
– характерний патерн відображеного болю чи розладів чутливості (парестезій);
– обмеження обсягу рухів;
Малі критерії (можуть змінюватися, але необхідна наявність хоча б одного з трьох):
– виникнення болю чи розладів чутливості під час стимуляції (пальпації) тригерних точок;
– локальне м’язове скорочення під час пальпації тригерних точок;
– зменшення болю при розтягненні м’яза чи при ін’єкції в тригерну точку.
Проте діагноз МФС також відкинули, тому що наявна симптоматика не відповідала обов’язковим критеріям. Хвора скаржиться на регіональний біль, але не виявлено спастичного тяжу в м’язах під час пальпації. Знайдено болючі точки в м’язах шиї, спини та верхніх кінцівок, але немає характерного для МФС патерну іррадіації болю.
Розглядали також синдром Barre-Lieou («шийна мігрень»), що, як вважалося раніше, виникає при подразненні вертебральної артерії. Це застарілий діагноз, правомірність якого ставлять під сумнів експерти IHS. У експериментальних дослідженнях показано, що вертебральна артерія дуже слабо реагує на електростимуляцію вертебрального нерва Франка (N. Bogduk et al., 2008) і на введення вазоактивних речовин (G.N. Lambert et al., 1984). Тобто якщо немає значної механічної компресії вертебральної артерії, то будь-яке її подразнення не зумовлює порушень мозкового кровообігу.
Із даних анамнезу звертає на себе увагу те, що пацієнтка вважає себе хворою протягом року, а 1,5 року тому перенесла ДТП. Тому є всі підстави пов’язати симптоми з хлистовою травмою шиї. Це різновид гострої травми, яка спричиняє миттєве перерозтягнення в м’язах, зв’язках, сухожиллях, нервах та інших структурах шиї внаслідок раптового неочікуваного імпульсу, який викликає ривок голови спочатку назад (гіперекстензія), а потім уперед (гіперфлексія). Хлистова травма шиї типова для незначних ДТП при поштовху нерухомого автомобіля ззаду, а також для деяких видів спорту (бокс, дзюдо, карате, регбі).
Довготривалі прогнози щодо частоти виникнення й тяжкості розладів, пов’язаних із хлистовою травмою, дуже неоднозначні. За даними A.L. Young і співавт., лише 12% людей, які перенесли хлистову травму, залишаються безсимптомними протягом 10 років. Відсутні чітке визначення синдрому, радіологічні критерії та специфічна терапія. Спочатку травма може бути не поміченою. Кілька діб триває «світлий проміжок». Згодом можуть спостерігати різноманітні симптоми. Описано також пізній синдром хлистової травми, який розвивається через кілька місяців.
R. Ferrari і співавт. (2005) вивчали частоту різних симптомів у осіб, які перенесли хлистову травму в ДТП, а також окремо в жінок і чоловіків. Найбільш стійким і повторюваним виявився біль у шиї чи в плечі (100%), за ним – головний біль, на який дещо частіше скаржилися жінки (86,1 проти 78,4% у чоловіків). Цікаво, що після хлистової травми шиї багато учасників дослідження почали скаржитися на біль у попереку (62-65%). Інші симптоми (парестезії в кінцівках, запаморочення, нудота, дзвін у вухах) траплялися з частотою менше 50% і практично однаково в чоловіків і жінок.
Тривалість симптомів та ймовірність хронізації наслідків хлистової травми визначається комплексною взаємодією біологічних, психосоціальних, економічних, юридичних факторів (можливість отримати страхове відшкодування).
Стратегія лікування передбачає усунення гострого нападу болю та профілактику хронізації больового синдрому й психоемоційних розладів. Для фармакотерапії застосовують аналгетики, НПЗП, опіоїди, інші препарати зі знеболювальним ефектом (міорелаксанти, триптани при мігренозному характері болю).
Для фізіотерапії цервікокраніалгії використовують холодні та гарячі компреси, електронейростимуляцію, гідротерапію, комірець Шанца (не більш як на 7 днів для уникнення хронізації), постізометричну релаксацію, ін’єкції в тригерні точки, остеопатію (але мануальну терапію протипоказано!). Пацієнту слід рекомендувати рухати шиєю як зазвичай, наскільки це можливо для запобігання закріпленню больової поведінки.
Профілактика хлистової травми полягає в правильному регулюванні підголівників у автомобілі: верхній край підголівника має бути на 6 см нижче маківки голови; сидіння слід регулювати таким чином, щоб підголівник був якомога ближче за головою. За даними американських авторів, які досліджували різні аспекти хлистової травми, три з чотирьох підголівників мають неоптимальне положення відносно голови, тому не запобігають травмі шиї, хоча спеціально для цього призначені.
Цілком імовірно, що больовий синдром у пацієнтки з клінічного прикладу являє собою віддалені наслідки хлистової травми шиї. Прицільна рентгенографія С1-С2-сегментів виявила асиметрію між зубом і латеральними масами атланта, а також асиметрію просторів міжхребцевих суглобів, що підтверджує наявність травми. Проте не можна виключити
й коморбідність із мігренню, на що вказує згадування про напади мігрені в молодості. Характеристики болю та тривалість нападів цілком укладаються в діагностичні критерії мігрені. Тобто, можливо, в цьому випадку легка травма шиї (яка минула непоміченою для пацієнтки) стала тригерним фактором для поновлення мігренозних атак. Тому для усунення нападів обґрунтовано застосування триптанів, а для лікування наслідків травми – фізіотерапевтичних методів.
Отже, цей клінічний приклад демонструє, що причина ЦГБ не завжди очевидна, клінічна картина може нагадувати специфічні цефалгії, не виключено співіснування двох і більше механізмів розвитку та хронізації больового синдрому, в тому числі з віддаленими наслідками травм, які здавалися пацієнту незначними.
Підготував Дмитро Молчанов