27 липня, 2017
Тецентрик® – история прорыва
В последние три года инновационная иммунотерапия рака является наиболее обсуждаемым в мировом медицинском сообществе достижением клинической онкологии. Тецентрик® (атезолизумаб) – моноклональное антитело, которое связывается с PD-L1 и блокирует его взаимодействие с рецепторами PD-1 и B7.1, а также включает активацию противоопухолевого иммунного ответа, приводя к уменьшению опухолевого роста. Тецентрик® одобрен к применению при уротелиальной карциноме и немелкоклеточном раке легкого (НМРЛ) и в настоящее время активно изучается при опухолях целого ряда локализаций. Рассмотрим историю появления этого препарата.
Первоосновы
Спонтанное излечение от рака – явление, которое наблюдалось в течение сотен лет. Все это время оно было предметом ожесточенных споров, но на сегодняшний день считается неоспоримым фактом. Практически все отчеты отмечают связь регрессии опухоли с перенесенными пациентом инфекциями, включая дифтерию, гонорею, гепатит, грипп, малярию, корь, оспу, сифилис, туберкулез и т.д.
 Под спонтанной регрессией подразумевается частичное или полное исчезновение злокачественной опухоли «без какой-либо очевидной причины». Спонтанная регрессия встречается при большинстве типов рака и упоминается в медицинской литературе начиная с 1742 г.
Под спонтанной регрессией подразумевается частичное или полное исчезновение злокачественной опухоли «без какой-либо очевидной причины». Спонтанная регрессия встречается при большинстве типов рака и упоминается в медицинской литературе начиная с 1742 г.
Однако явление спонтанной регрессии наблюдалось и ранее: оно известно как синдром Святого Перегрина. Молодой священник Перегрин Лациози (1265-1345) страдал запущенным раком голени, требующим ампутации ноги. Но ко времени, на которое была назначена операция, опухоль исчезла и впоследствии не возвращалась, что позволило церкви признать исцеление чудом.
В 1891 г. молодой американский хирург Уильям Коули разработал первую терапевтическую противоопухолевую вакцину, которая по разным причинам была предана забвению. Фактически вакцина Коули вызывала у пациентов воспаление и высокую температуру, подвергая организм серьезному стрессу и стимулируя работу иммунной системы. Этот подход был сопряжен с определенными рисками, но позволял некоторым больным с распространенными стадиями полностью излечиться от рака. Ценность этих исследований заключается в том, что они заложили основы современной иммунотерапии, подтвердив замечательный факт, что рак не является необратимым процессом.
У. Коули указал несколько моментов, имеющих решающее значение для выживания пациента. Ключевым фактором была симуляция естественной острой инфекции, сопровождавшейся существенным повышением температуры. Инъекции вводили ежедневно или через день в течение первого месяца или двух. Чтобы избежать иммунной толерантности к вакцине, дозировка постепенно увеличивалась с течением времени в зависимости от реакции пациента. Вакцину вводили непосредственно в первичную опухоль и (по возможности) в метастазы. Для предотвращения рецидива соблюдался последующий 6-месячный курс еженедельных инъекций. Последний случай использования вакцины Коули был зафиксирован в Китае в 1980-х гг.: ее вводили в качестве первичной терапии мужчине с терминальной стадией рака печени. Пациент получил 68 инъекций токсинов Коули за 34 недели. К концу этого периода все опухолевые очаги полностью регрессировали.
Спонтанная регрессия – реальность и мифы
Стандартное определение спонтанной регрессии было предложено в 1960-е гг. и включает в себя требование о том, что наличие рака изначально должно быть подтверждено микроскопическим исследованием тканей. Спонтанная регрессия злокачественных опухолей не является исключительно редким феноменом: только за 2002 г. медицинские журналы опубликовали более 4 посвященных этой теме статей. По имеющимся данным, средняя частота такой регрессии составляет 1 случай на 80 000 больных. Чаще всего регрессия происходит при опухолях у детей, раке молочной железы, хорионэпителиоме, аденокарциноме почки, нейробластоме, меланоме, саркомах, раке мочевого пузыря и кожи.
Сравнительная редкость спонтанных регрессий в настоящее время может быть следствием иммуносупрессивного характера традиционной противоопухолевой терапии. Процессу роста и метастазирования опухоли также способствует нарушение целостности опухоли при биопсии или хирургическом лечении, вследствие чего значительное количество опухолевых клеток попадает в системный кровоток, в то время как большинство препаратов (особенно используемых в химиотерапии) подавляют иммунную систему.
 Фактически спонтанная регрессия не так уж спонтанна и беспричинна. Она связана с активацией иммунной системы в условиях серьезного стресса для организма. Острые инфекции и повышение температуры тела вызывают немедленный и эффективный иммунный ответ, воздействующий одновременно на инфекционный агент и опухоль.
Фактически спонтанная регрессия не так уж спонтанна и беспричинна. Она связана с активацией иммунной системы в условиях серьезного стресса для организма. Острые инфекции и повышение температуры тела вызывают немедленный и эффективный иммунный ответ, воздействующий одновременно на инфекционный агент и опухоль.
Тот же У. Коули указывал, что симптомом, наиболее связанным с регрессией опухоли, была сильная фебрильная реакция. Ретроспективное исследование пациентов с неоперабельными саркомами мягких тканей, проведенное У. Коули, показало, что 5-летняя выживаемость достигала 60% у пациентов, температура тела которых поднималась на фоне введения вакцины в среднем до 38-40 °C, но не превышала 20% у пациентов, лечение которых не сопровождалось сильной фебрильной реакцией.
 Современные исследования показывают, что основным препятствием к спонтанному исцелению от рака является дисфункция иммунной системы, связанная как с ускользанием опухоли от иммунного надзора, так и с любым существующим у пациента видом иммунного дефицита.
Современные исследования показывают, что основным препятствием к спонтанному исцелению от рака является дисфункция иммунной системы, связанная как с ускользанием опухоли от иммунного надзора, так и с любым существующим у пациента видом иммунного дефицита.
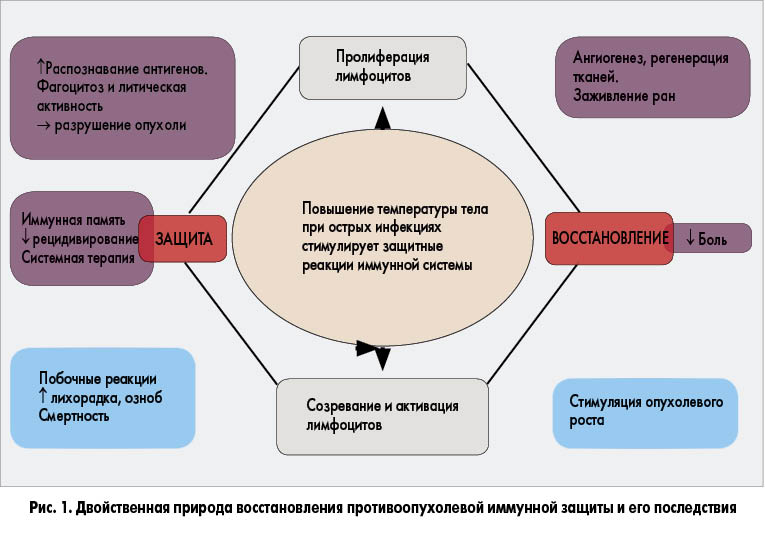
В то же время спонтанная регрессия связана с целым рядом изменений в иммунной системе. Это активация антиген-презентирующих дендритных клеток, приводящая к улучшению распознавания опухолевых антигенов и токсинов, а также активация и пролиферация цитотоксических Т-лимфоцитов и натуральных киллеров, инфильтрирующих опухоль (рис. 1).
Большинство современных методов борьбы с раком не используют потенциал собственной иммунной системы пациентов и даже подавляют ее активность. Все эти факты привели ученых к пониманию того, что идеальная комплексная противоопухолевая терапия включает в себя воздействие на иммунную систему пациента.
Воздействие на механизм запрограммированной смерти
Ускользание раковых клеток от иммунного надзора связано с патологическим воздействием опухоли на иммунные контрольные точки – сигнальные молекулы, которые регулируют защитные реакции организма и могут как подавлять, так и активировать иммунную систему.
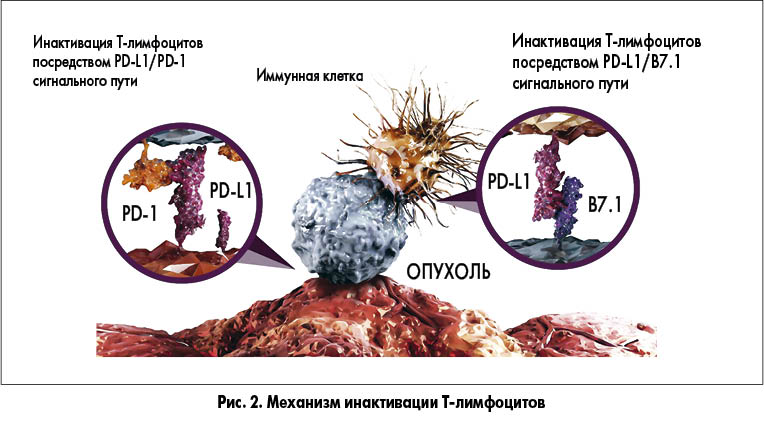
Рецептор программируемой гибели клеток PD‑1 на поверхности Т-лимфоцитов подавляет активность Т-лимфоцитов в периферических тканях, с тем чтобы избежать аутоиммунных реакций, т.е. он отвечает за отрицательную регуляцию сигнала и взаимодействует с двумя лигандами – PD-L1 и PD-L2.
Для воздействия на механизм запрограммированной смерти были разработаны два класса препаратов – ингибиторов иммунных контрольных точек, которые воздействуют соответственно на PD‑1 и PD-L1, предотвращая ускользание опухоли от иммунного надзора. Предполагалось, что использование PD-L1 в качестве терапевтической мишени будет сопровождаться меньшей токсичностью благодаря модуляции иммунного ответа селективно в микроокружении опухоли. Дальнейшие исследования подтвердили это предположение: блокирование PD‑1 и PD-L1 дает сходные клинические результаты, но блокирование PD-L1 связано с меньшим риском аутоиммунных реакций, поскольку остается активным PD‑1/PD-L2 путь регуляции иммунной системы. Связываясь с PD-L1, Тецентрик® предотвращает взаимодействие этого белка с PD‑1 и В7.1 на поверхности Т-лимфоцитов и приводит к восстановлению противоопухолевого иммунитета.
 Тецентрик® (атезолизумаб) – первый препарат на основе моноклональных антител, специфичных к белку PD-L1, который экспрессируется на клетках опухоли и иммунных клетках, инфильтрирующих опухоль.
Тецентрик® (атезолизумаб) – первый препарат на основе моноклональных антител, специфичных к белку PD-L1, который экспрессируется на клетках опухоли и иммунных клетках, инфильтрирующих опухоль.
За счет ингибирования PD-L1 Тецентрик® активирует Т-лимфоциты, восстанавливая их способность эффективно обнаруживать и атаковать злокачественные клетки. Данный препарат вводится внутривенно в фиксированной дозировке 1200 мг в течение 60 мин каждые 3 недели. Высокий уровень экспрессии PD-L1 опухолью коррелирует с повышенным ответом на атезолизумаб.
 Появление иммунотерапии положило начало новой стратегии в лечении рака – воздействию на клетки иммунной системы, а не на опухоль. Этот подход сделал возможным применение одного препарата при разных видах опухолей, ткани которых инфильтрированы лимфоцитами и используют сигнальный путь PD‑1/PD-L1 для ускользания от иммунного ответа.
Появление иммунотерапии положило начало новой стратегии в лечении рака – воздействию на клетки иммунной системы, а не на опухоль. Этот подход сделал возможным применение одного препарата при разных видах опухолей, ткани которых инфильтрированы лимфоцитами и используют сигнальный путь PD‑1/PD-L1 для ускользания от иммунного ответа.
История атезолизумаба
12 июля 2015 г. в рамках основного исследования II фазы IMvigor 210 было установлено, что предложенная компанией Genentech анти-PD-L1 иммунотерапия уменьшает размеры опухоли у пациентов с распространенной уротелиальной карциномой.
16 августа 2015 г. исследование II фазы BIRCH показало, что атезолизумаб эффективен при НМРЛ.
26 августа 2015 г. компания Syndax Pharmaceuticals инициировала совместное с компанией Roche клиническое исследование фазы Ib/II, в котором Тецентрик® применяется совместно с энтиностатом (малой молекулой, воздействующей на мицелоидные супрессорные клетки и регуляторные Т-лимфоциты) у пациентов с трижды негативным раком грудной железы.
8 января 2016 г. компания Roche представила обновленные результаты исследования атезолизумаба при уротелиальной карциноме.
4 марта 2016 г. FDA предоставило атезолизумабу статус «прорыв в терапии» для приоритетного рассмотрения в терапии уротелиальной карциномы.
10 апреля 2016 г. атезолизумаб получил от FDA статус приоритетного рассмотрения при НМРЛ. В первом исследовании III фазы OAK применение атезолизумаба у пациентов с НМРЛ, ранее получавших лечение, привело к значимому увеличению общей выживаемости (ОВ) по сравнению со стандартной химиотерапией.
18 мая 2016 г. атезолизумаб впервые одобрен FDA для лечения больных с местнораспространенной или метастатической уротелиальной карциномой, у которых заболевание прогрессирует во время или после проведения неоадъювантной или адъювантной химиотерапии, содержащей препараты платины. Атезолизумаб стал первым лекарственным средством в классе ингибиторов PD‑1/PD-L1, одобренным для лечения уротелиального рака.
18 октября 2016 г. атезолизумаб был одобрен FDA для лечения пациентов с метастатическим НМРЛ, прогрессирующим во время или после платиносодержащей химиотерапии без тестирования экспрессии PD-L1.
Это решение принято на основании результатов исследования OAK, где у пациентов с максимальной экспрессией PD-L1 медиана выживаемости в группе атезолизумаба достигла 20,5 мес против 8,9 в группе доцетаксела. Даже у PD-L1-негативных пациентов на фоне атезолизумаба ОВ была на 25% выше, чем у тех, кто принимал доцетаксел (медиана ОВ составила 12,6 против 8,9 мес в группе доцетаксела). Улучшение показателей ОВ было сходным у больных с плоскоклеточным и неплоскоклеточным раком.
17 апреля 2017 г. по процедуре ускоренного рассмотрения FDA одобрило Тецентрик® в качестве стартовой терапии для лечения пациентов с прогрессирующей местнораспространенной или метастатической уротелиальной карциномой, которые не могут получать химиотерапию цисплатином.
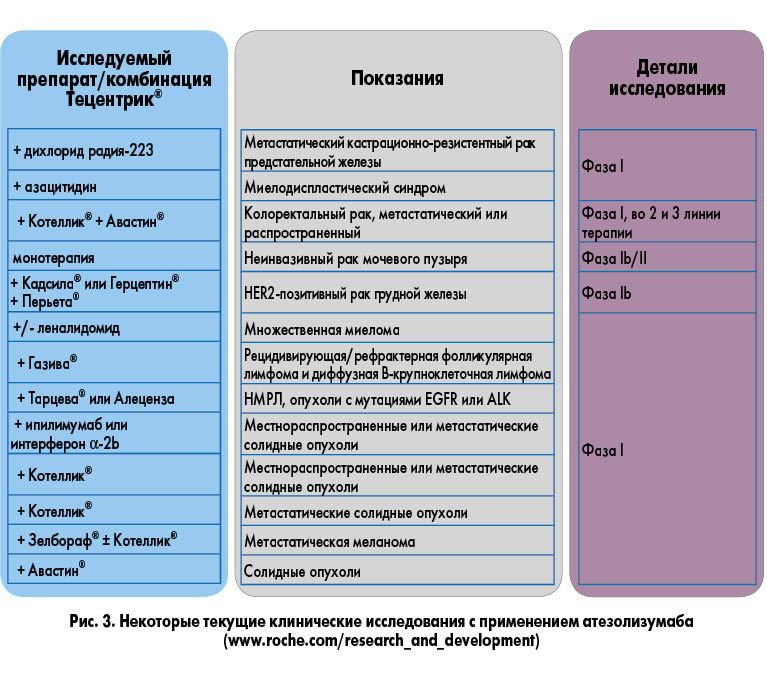
В настоящее время Тецентрик® исследуется в разных комбинациях и в монотерапии при целом ряде онкологических заболеваний (рис. 2). Большинство исследований находятся в I фазе (рис. 3).
Изменяя картину будущего для пациентов
В публикациях, посвященных результатам терапии пациентов, принимавших участие в исследованиях, указывается, что Тецентрик® «меняет правила игры», модифицируя прогноз заболевания. Среди участвовавших в клинических исследованиях пациентов, у которых опухоль реагировала на атезолизумаб, 84% все еще отвечали на лечение через год терапии. Речь идет о больных с метастатической уротелиальной карциномой, которые ранее получали химиотерапию.
 Мемориальный онкологический центр Слоан-Кеттеринг (США) опубликовал историю пациента Крейга Брауна, который получал Тецентрик® как участник клинического исследования. В начале 2014 г. у него был диагностирован рак мочевого пузыря стадии IV, который метастазировал в кости ребер. Пациент получал химиотерапию на основе препарата платины 1 раз в неделю в течение почти 6 мес, но достиг лишь частичной ремиссии и прогрессия заболевания началась сразу после прекращения терапии.
Мемориальный онкологический центр Слоан-Кеттеринг (США) опубликовал историю пациента Крейга Брауна, который получал Тецентрик® как участник клинического исследования. В начале 2014 г. у него был диагностирован рак мочевого пузыря стадии IV, который метастазировал в кости ребер. Пациент получал химиотерапию на основе препарата платины 1 раз в неделю в течение почти 6 мес, но достиг лишь частичной ремиссии и прогрессия заболевания началась сразу после прекращения терапии.
Крейг Браун получал атезолизумаб с октября 2014 г. Ответ на лечение развивался быстро, заметных побочных эффектов не наблюдалась в течение 19 мес. На момент публикации материала (конец мая 2016 г.) пациент все еще получал Тецентрик® и пребывал в состоянии полной ремиссии.
Список литературы находится в редакции.
Подготовила Катерина Котенко
Сообщения в прессе
 Уже в ходе первых исследований атезолизумаб показал впечатляющие результаты, которые получили широкое освещение в прессе. Большинство мировых научных изданий, цитируя позицию FDA, объявили данный препарат прорывом в лечении опухолей, которое ранее представляло собой большую проблему.
Уже в ходе первых исследований атезолизумаб показал впечатляющие результаты, которые получили широкое освещение в прессе. Большинство мировых научных изданий, цитируя позицию FDA, объявили данный препарат прорывом в лечении опухолей, которое ранее представляло собой большую проблему.
На уротелиальную карциному приходится большинство всех случаев рака мочевого пузыря, также он поражает мочеточники и почечную лоханку, а НМР является наиболее распространенным типом рака легкого. Все эти опухоли тяжело поддаются лечению стандартными методами, особенно на поздних стадиях.
Продолжается серьезная работа над тем, чтобы обеспечить доступ к препарату Тецентрик® как можно большему количеству больных и максимально быстро получить новые результаты исследований.
Также опубликованы впечатляющие клинические случаи, в которых Тецентрик® вызывает регрессию опухолей у пациентов с запущенными стадиями рака. В частности, указывается, что заметный клинический эффект может развиваться даже после первых инфузий.
Ключевые результаты исследований были опубликованы и активно обсуждались на всех профильных мировых конгрессах.
 «Наряду с утверждением атезолизумаба FDA также утвердила тест для определения уровней экспрессии белка PD-L1 на иммунных клетках, инфильтрирующих опухоль, чтобы помочь врачам выяснить, какие пациенты могут получить наибольшие преимущества от лечения этим препаратом».
«Наряду с утверждением атезолизумаба FDA также утвердила тест для определения уровней экспрессии белка PD-L1 на иммунных клетках, инфильтрирующих опухоль, чтобы помочь врачам выяснить, какие пациенты могут получить наибольшие преимущества от лечения этим препаратом».
5 июля 2016 г.
 «Тецентрик® предлагает новую терапевтическую стратегию второй линии для пациентов с НМРЛ, независимо от статуса PD-L1 опухоли. Интересно отметить, что исследование также показало улучшение ОВ даже у пациентов без экспрессии PD-L1, что означает – у нас есть проблема с использованием отрицательности PD-L1 в качестве фактора исключения лечения».
«Тецентрик® предлагает новую терапевтическую стратегию второй линии для пациентов с НМРЛ, независимо от статуса PD-L1 опухоли. Интересно отметить, что исследование также показало улучшение ОВ даже у пациентов без экспрессии PD-L1, что означает – у нас есть проблема с использованием отрицательности PD-L1 в качестве фактора исключения лечения».
9 октября 2016 г.
 «Новый препарат Тецентрик® был одобрен FDA для лечения рака легкого. Некоторые пациенты, участвовавшие в первых клинических испытаниях этого препарата, уже седьмой год живут без каких-либо признаков заболевания; следующий интересующий нас вопрос – будет ли это заболевание возвращаться».
«Новый препарат Тецентрик® был одобрен FDA для лечения рака легкого. Некоторые пациенты, участвовавшие в первых клинических испытаниях этого препарата, уже седьмой год живут без каких-либо признаков заболевания; следующий интересующий нас вопрос – будет ли это заболевание возвращаться».
2 декабря 2016 г.
 «Тецентрик® продемонстрировал обнадеживающие показатели длительности ответа, выживаемости и переносимости, что поддерживает его терапевтическое применение при ранее не леченном метастатическом уротелиальном раке».
«Тецентрик® продемонстрировал обнадеживающие показатели длительности ответа, выживаемости и переносимости, что поддерживает его терапевтическое применение при ранее не леченном метастатическом уротелиальном раке».
7 января 2017 г.
 «Недавно рандомизированное исследование III фазы (ОАК) оценивало атезолизумаб во второй линии НМРЛ независимо от гистологии опухолей или экспрессии PD-L1; однако в соответствии с экспрессией PD-L1 проводилась стратификация. Медиана ОВ составила 20,5 мес в группе атезолизумаба и 8,9 мес в группе доцетаксела... Интересно, что анти-PD-L1 стал первым ингибитором иммунных контрольных точек, показавшим статистически значимое улучшение ОВ у пациентов с PD-L1-отрицательным статусом».
«Недавно рандомизированное исследование III фазы (ОАК) оценивало атезолизумаб во второй линии НМРЛ независимо от гистологии опухолей или экспрессии PD-L1; однако в соответствии с экспрессией PD-L1 проводилась стратификация. Медиана ОВ составила 20,5 мес в группе атезолизумаба и 8,9 мес в группе доцетаксела... Интересно, что анти-PD-L1 стал первым ингибитором иммунных контрольных точек, показавшим статистически значимое улучшение ОВ у пациентов с PD-L1-отрицательным статусом».
10 марта 2017 г.
 «Тецентрик®, также известный как атезолизумаб, получил одобрение по программе ускоренного утверждения FDA в качестве терапии первой линии для пациентов с прогрессирующим раком мочевого пузыря, которым не показана стандартная химиотерапия цисплатином. Этот препарат был ранее одобрен для использования у пациентов с прогрессирующим или метастатическим раком мочевого пузыря, чье состояние ухудшилось в течение года после химиотерапии. Одобрение, которое появилось через шесть месяцев после одобрения препарата Тецентрик® FDA в терапии НМРЛ, является стимулом для швейцарской фармацевтической компании расширить показания к применению этого препарата».
«Тецентрик®, также известный как атезолизумаб, получил одобрение по программе ускоренного утверждения FDA в качестве терапии первой линии для пациентов с прогрессирующим раком мочевого пузыря, которым не показана стандартная химиотерапия цисплатином. Этот препарат был ранее одобрен для использования у пациентов с прогрессирующим или метастатическим раком мочевого пузыря, чье состояние ухудшилось в течение года после химиотерапии. Одобрение, которое появилось через шесть месяцев после одобрения препарата Тецентрик® FDA в терапии НМРЛ, является стимулом для швейцарской фармацевтической компании расширить показания к применению этого препарата».
17 апреля 2017 г.