27 липня, 2017
Нові можливості в терапії гормоночутливого раку
«Буквально вся біологія ґрунтується
на здатності клітин до поділу.
Нам вдалося виявити ключові молекули,
що скеровують даний процес».
Ліленд Хартуелл
 На науково-практичній конференції «Зміна стандартів лікування поширеного і метастатичного раку молочної залози», яка відбулася 9 червня в м. Львові, обговорювалися оновлені дані стосовно можливостей лікування цього серйозного захворювання. Перегляду стандартів лікування гормоночутливого раку молочної залози (РМЗ) присвятив свою доповідь завідувач відділу хіміотерапії Львівського державного онкологічного регіонального лікувально-діагностичного центру, доцент, кандидат медичних наук Ярослав Васильович Шпарик.
На науково-практичній конференції «Зміна стандартів лікування поширеного і метастатичного раку молочної залози», яка відбулася 9 червня в м. Львові, обговорювалися оновлені дані стосовно можливостей лікування цього серйозного захворювання. Перегляду стандартів лікування гормоночутливого раку молочної залози (РМЗ) присвятив свою доповідь завідувач відділу хіміотерапії Львівського державного онкологічного регіонального лікувально-діагностичного центру, доцент, кандидат медичних наук Ярослав Васильович Шпарик.
Починаючи свій виступ, Я.В. Шпарик згадав слова Жан-Мартена Шарко про те, що захворювання старе і нічого в ньому не змінюється – змінюємося ми завдяки нашій здатності розпізнавати те, що було недоступним нашому розумінню. І хоча відомий французький лікар не мав на увазі РМЗ, це твердження повною мірою можна до нього застосувати. Останнім часом істотно змінилися погляди на це захворювання і можливості його лікування – спостерігається колосальний розрив між поточним станом клінічної онкології і ситуацією ще кілька років тому. Щорічно в Україні приблизно у 14 000 жінок уперше діагностують РМЗ. Більше половини з них ризикують померти від цього захворювання, оскільки пухлина виявляється на пізній стадії, і це невигідно відрізняє Україну від розвинених зарубіжних країн. Украй важливим є запровадження скринінгу, роль якого у зниженні поширеності запущених стадій захворювання є очевидною. І хоча в організації скринінгу існують певні суперечності, актуальність поліпшення ранньої діагностики не викликає сумнівів.
Смертність до року з моменту встановлення діагнозу досягає 15% серед українських жінок, хворих на РМЗ. Якщо в США і розвинених країнах Європи 5-річна виживаність при РМЗ становить близько 85%, то в нашій країні цей показник нижчий за 50%. Таким чином, протягом першого року в Україні від РМЗ помирає приблизно така ж частка хворих жінок, як у США протягом 5 років. Українки віком до 35 років складають лише 3% пацієнток з РМЗ – найчастіше до онколога потрапляють жінки, старші за 50 років. Структура захворюваності РМЗ співставна з такою за кордоном, більш ніж у 3/4 жінок це захворювання розвивається в постменопаузі, з них приблизно у 60-66% наявна експресія гормональних рецепторів.
Для жінок з метастатичним РМЗ медикаментозний метод лікування є основним. При гормон-рецептор-позитивному захворюванні стандартом лікування визнана гормонотерапія. Першим препаратом для гормональної терапії РМЗ став тамоксифен, який був впроваджений у клінічну практику у 1973 р. Далі з’явилися інгібітори ароматази (спочатку анастрозол, згодом летрозол та екземестан), а потім фулвестрант – перший представник нового класу стероїдних антиестрогенів, який застосовується як препарат другої лінії терапії. Усі перераховані препарати – класичні «гравці» сучасної гормонотерапії РМЗ.
Дослідження, проведені на рубежі XX і XXI ст., в яких тамоксифен використовувався як препарат порівняння, показали, що ефективність інгібіторів ароматази трохи вища та дозволяє збільшити час до прогресування метастатичного РМЗ (6-8 міс проти 10-11). Таким чином, якщо пацієнтка розпочинає паліативну гормонотерапію з тамоксифену, існує велика імовірність того, що через 6 міс захворювання почне прогресувати і потрібно буде змінити лікування; на тлі терапії інгібіторами ароматази очікуваний період без прогресування буде трохи довшим.
Як зазначив Я.В. Шпарик, ще нещодавно гормональну терапію не наважувалися призначати в паліативному режимі, віддаючи перевагу хіміотерапії. На сьогодні такі погляди зазнали істотних змін. Для значної групи пацієнток, старших за 35 років, у яких захворювання прогресує повільно і відсутнє метастатичне ураження життєво важливих органів (печінка, легені), гормонотерапія може бути перспективною. Наявність препаратів різних груп дозволяє проводити до 4 ліній гормонотерапії, але слід пам’ятати, що з кожною подальшою лінією зменшується період до прогресування захворювання. Інгібітори ароматази мають деякі переваги перед тамоксифеном при призначенні в першій лінії. При паліативній гормонотерапії у жінок в репродуктивному віці і в пременопаузі небажано використовувати аналоги гонадотропін-рилізинг-гормону для тимчасового пригнічення функції яєчників. Неоад’ювантна гормонотерапія загалом зрідка використовується.
Принципових інновацій у класичній гормонотерапії РМЗ найближчим часом не очікується. Подальші перспективи науковці пов’язують з появою таргетних препаратів, наприклад таких, як палбоцикліб – родоначальник групи циклібів, що першим почав використовуватись за межами клінічних досліджень.
Палбоцикліб є інгібітором циклінзалежних кіназ (CDK), що беруть участь у поділі клітини. За дослідження механізмів регуляції клітинного циклу, що уможливили створення палбоциклібу, трьом ученим – Ліленду Хартуеллу, Тімоті Ханту і Полу Нерсу – у 2001 р. була присуджена Нобелівська премія в галузі фізіології й медицини.
Як нагадав Я.В. Шпарик, перший період клітинного циклу (G1) характеризується активним ростом і функціонуванням клітини. У другому (S) періоді відбувається реплікація ДНК з подвоєнням генетичного матеріалу хромосом. У постсинтетичному періоді (G2) клітина готується до поділу та синтезує необхідні білки. Далі вона вступає в період мітозу (М), коли хромосоми розходяться в дочірні клітини, кожна з яких починає власний життєвий цикл. У фазі G1 існує «точка неповернення», проходячи яку клітина неминуче вступить в мітоз. Циклінзалежні кінази стимулюють проходження цього етапу, ініціюючи перехід клітини від фази G1 до фази, пов’язаної з реплікацією ДНК; їх блокування робить мітоз неможливим.
Таким чином, вибірково інгібуючи CDK 4 і 6, палбоцикліб призводить до блокади проліферації пухлинних клітин. Було встановлено, що патологічна гіперактивація CDK4/6 часто спостерігається при РМЗ, що експресує рецептори естрогену (ER+). У результаті доклінічних досліджень з’ясувалося, що подвійне інгібування CDK4/6 і сигнального шляху ER має ефект синергії та пригнічує ріст клітинних ліній ER+ РМЗ у фазі G1.
Ранні дослідження показали перспективність нового препарату – палбоциклібу, після чого було ініційовано міжнародне рандомізоване дослідження II фази PALOMA-1, в якому вивчалася ефективність палбоциклібу в комбінації з летрозолом у першій лінії терапії. На етапі відбору це дослідження було розділене на дві когорти. У першу входили жінки в постменопаузі з метастатичним ER+ РМЗ і відсутністю експресії рецепторів епідермального фактору росту (HER2-), у другу – пацієнтки з інших країн – учасниць дослідження з цим же підтипом РМЗ, але додатково з підтвердженою ампліфікацією CCND1 і/або видаленням p16. Як зауважив доповідач, дослідники з часом відмовилися від пошуку мутацій, оскільки це не впливало на результати лікування, але обмежувало набір пацієнток і потребувало дороговартісного обстеження. Усі учасниці дослідження були рандомізовані 1:1 для отримання комбінації летрозолу з палбоциклібом (125 мг 1 раз на добу курсом 21 день, потім 7 днів перерви) або летрозолу і плацебо відповідно.
Я.В. Шпарик зазначив, що Україна також брала участь у проведенні дослідження PALOMA-1: було включено в цілому близько 20 хворих, з них 5 отримували лікування на базі Львівського державного онкологічного регіонального лікувально-діагностичного центру.
Дослідження показало, що комбінація палбоциклібу з летрозолом достовірно збільшує виживаність без прогресування (ВБП) порівняно з монотерапією летрозолом. У жінок, що отримували комбіновану терапію палбоциклібом і летрозолом, медіана ВБП досягала 20,2 міс, тоді як на тлі летрозолу цей показник відповідав даним попередніх досліджень і складав 10,2 міс. Ці дані були представлені на щорічній конференції Американської асоціації з дослідження раку (AACR) у м. Сан-Дієго у квітні 2014 р.
Ґрунтуючись на результатах проміжного аналізу дослідження PALOMA-1, у квітні 2013 р. Управління з контролю якості харчових продуктів і лікарських препаратів США (FDA) надало палбоциклібу статус пріоритетного розгляду. У лютому 2015 р. палбоцикліб (Ібранс) був дозволений до застосування в першій лінії терапії в жінок з поширеним і метастатичним ER+ HER2- РМЗ. Це рідкісний приклад того, як підставою для ухвалення FDA стали результати дослідження II, а не III фази.
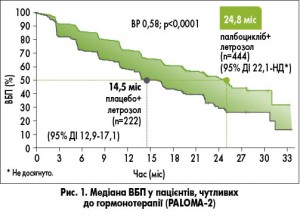
Минулого року були опубліковані результати дослідження III фази PALOMA-2 за участю 666 пацієнток (із них 13 – з України). Дизайн був аналогічним дослідженню II фази, але рандомізація в групи палбоцикліб + летрозол і летрозол + плацебо проведена у співвідношенні 2:1. У цьому дослідженні показник ВБП був навіть вищим – у групі палбоциклібу з летрозолом він склав 24,8 міс проти 14,5 у групі летрозолу (рис. 1).
Основним і найбільш поширеним побічним ефектом палбоциклібу була нейтропенія, яка розвивалася у 79,5% пацієнток у групі палбоциклібу з летрозолом проти 6,3 у групі летрозолу. Фебрильна нейтропенія не спостерігалася в дослідженні PALOMA-1, а в PALOMA-2 була рідкісним явищем (2,5%). Я.В. Шпарик підкреслив, що нейтропенія, спровокована терапією палбоциклібом, істотно відрізняється від нейтропенії, пов’язаної з хіміотерапією: вона менш тривала і характеризується меншим ступенем тяжкості. На тлі летрозолу цей побічний ефект розвивається вкрай рідко, практично не впливає на якість життя пацієнта і легко піддається корекції. При нейтропенії 1-2 ступеня немає необхідності модифікувати лікування; при нейтропенії 3 ступеня слід відстрочити на 1 тиждень початок наступного курсу палбоциклібу. За наявності інфекції на тлі нейтропенії необхідно перервати терапію палбоциклібом до поліпшення стану (нейтропенії 1-2 ступеня) і згодом знизити дозу палбоциклібу. У цілому краще відкласти початок наступного курсу палбоциклібу, аніж знижувати дози. Таким чином, палбоцикліб у комбінації з летрозолом не тільки добре переноситься, але і значно збільшує медіану ВБП.
У дослідженні PALOMA-3 вивчалася ефективність комбінації палбоциклібу з фулвестрантом у другій лінії терапії у 521 пацієнтки після прогресування РМЗ на попередній лінії гормонотерапії. З України були включені 3 пацієнтки. Дизайн цього дослідження припускав можливість включення пацієнток у пременопаузі, але за умови пригнічення функції яєчників аналогами гонадотропін-
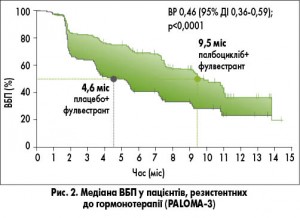
рилізинг-гормону. При проміжному аналізі медіана ВБП у цьому дослідженні склала 9,2 міс у групі палбоциклібу й фулвестранту проти 3,8 міс у групі фулвестранту і плацебо; за результатами остаточного аналізу дослідників ці показники склали 9,5 міс проти 4,6 відповідно, а за результатами центральної оцінки – 9,5 міс проти 5,5, але в усіх випадках палбоцикліб забезпечував значну перевагу перед монотерапією фулвестрантом у другій лінії гормонотерапії при прийнятному профілі безпеки (рис. 2).
За результатами дослідження PALOMA-3 палбоцикліб у поєднанні з фулвестрантом затверджений FDA до застосування в другій лінії терапії при поширеному або метастатичному ER+ HER2- РМЗ.
На конгресі ASCO-2017 були озвучені результати загальної виживаності (ЗВ) в дослідженні PALOMA-1. Медіана ЗВ у групі палбоциклібу і летрозолу склала 37,5 міс проти 33,3 у групі летрозолу (когорта в США) або 35,1 і 35,7 міс (в інших країнах, що брали участь у дослідженні). Різниця в ЗВ була статистично недостовірною. Я.В. Шпарик підкреслив, що після завершення дослідження отримували системну терапію 78,6% пацієнток у групі комбінованого лікування і 86,4 у групі летрозолу. Окрім того, у групі летрозолу більша кількість пацієнток отримувала ≥3 лінії терапії (37 проти 18), у тому числі фулвестрант у поєднанні з палбоциклібом. Тривалість періоду до переходу на другу лінію терапії була більшою в групі палбоциклібу.
Крім того, на ASCO-2017 були представлені результати аналізу підгруп дослідження PALOMA-2 – показані достовірні переваги додавання палбоциклібу до летрозолу в усіх підгрупах.
Палбоцикліб у комбінації з гормонотерапією показав значні переваги порівняно з однією лише гормонотерапією в першій і другій лінії при поширеному або метастатичному ER+ HER2- РМЗ і на сьогодні включений у міжнародні рекомендації за всіма цими показаннями.
Підготувала Катерина Котенко
Посилання доступні за запитом у редакції.
Надруковано за підтримки Представництва
«Файзер Ейч.Сі.Пі. Корпорейшн» в Україні.
WUKIBR0317012