27 липня, 2017
Рибоциклиб как препарат первой линии терапии HR+ распространенного рака грудной железы

Согласно результатам промежуточного анализа исследования MONALEESA‑2, в котором оценивались эффективность и безопасность сочетания рибоциклиба с летрозолом в качестве стартовой терапии пациенток с распространенным гормон-рецептор-положительным (HR+) и HER2-отрицательным (HER2-) раком грудной железы (РГЖ), при комбинированной терапии наблюдалась более длительная выживаемость без прогрессирования (ВБП) по сравнению с монотерапией летрозолом.
Более чем у 75% больных РГЖ на поверхности опухолевых клеток присутствуют рецепторы эстрогенов и прогестерона (HR+ опухоли). Стандартом первой линии терапии женщин с HR+ и HER2- распространенным РГЖ являются ингибиторы ароматаз, однако к ним у большинства пациенток через некоторое время развивается резистентность. Разработка эффективных методов, введение схем альтернативного ступенчатого лечения, повышающих чувствительность к гормональной терапии, является важной задачей для клиницистов. Ингибирование циклинзависимых киназ 4 и 6 (CDK 4/6) теоретически способно преодолеть или снизить устойчивость к эндокринной терапии пациенток с HR+ распространенным РГЖ при отсутствии экспрессии рецептора эпидермального фактора роста (HER2-).
Известно, что цикл деления клетки регулируют киназы CDK 4/6 и их белковый регулятор циклин D1 (CCND1), являющийся непосредственной транскрипционной мишенью сигнального пути рецепторов эстрогенов. Основными маркерами устойчивости к гормональной терапии являются повышенная экспрессия CDK 4/6 и амплификация гена ССND1, которые часто встречаются у пациенток с HR+ РГЖ. Эффективной стратегией в первой линии терапии было торможение каскада реакций, вовлекающих циклин D1, CDK 4/6, ингибитор CDK 4 и белок ретинобластомы, которое применялось не только у пациенток с HR+ распространенным РГЖ, но и при прогрессировании заболевания на фоне гормональной терапии.
Рибоциклиб представляет собой пероральный селективный низкомолекулярный ингибитор CDK 4/6, который блокирует фосфорилирование белка ретинобластомы, тем самым препятствуя делению клетки и индуцируя остановку клеточного цикла в фазе G1. Ранее было доказано, что рибоциклиб проявляет противоопухолевую активность в отношении эстроген-рецептор-положительной модели ксенотрансплантатов РГЖ как при самостоятельном применении, так и в сочетании с летрозолом и ингибитором фосфадитилинозитол‑3-киназы. В исследовании IВ фазы у женщин в постменопаузе с эстроген-рецептор-положительным и HER2- РГЖ при одновременном применении с летрозолом рибоциклиб имел приемлемый профиль безопасности и продемонстрировал клиническую активность.
Методы
Рандомизированное двойное слепое плацебо-контролируемое исследование III фазы MONALEESA‑2 проводилось в 29 странах с участием 223 клинических баз. Пациенток разделили на две группы для получения селективного ингибитора СDK 4/6 рибоциклиба + летрозол или плацебо + летрозол. Авторы выбрали дозу рибоциклиба 600 мг/день на основании результатов исследования I фазы. Рандомизация была стратифицирована в соответствии с наличием или отсутствием метастазов в легких и печени. Пациентки получали лечение до прогрессирования заболевания, развития неприемлемой токсичности, летального исхода или прекращения приема рибоциклиба или летрозола по любой другой причине.
В исследование были включены 668 женщин в постменопаузе с HR+ и HER2- рецидивировавшим или метастатическим РГЖ на поздней стадии, которые ранее не получали системной терапии по поводу заболевания поздней стадии. Первичной конечной точкой была медиана ВБП; вторичные конечные точки включали общую выживаемость, суммарную эффективность лечения и безопасность. Пациентки имели измеряемые проявления заболевания (согласно критериям оценки объективного ответа при солидных опухолях REGISТ) или как минимум единичное поражение кости, функциональный статус по ECOG 0 или 1 при сохранных функциях органов и костного мозга.
Из исследования исключались пациентки с прогрессирующим заболеванием, которые ранее получали терапию ингибиторами CDK 4/6, систематическую химио- или гормональную терапию, в том числе адъювантную или неоадъювантную терапию нестероидным ингибитором ароматаз. Также к исследованию не допускались пациентки с воспалительным РГЖ, метастазами в центральной нервной системе, сердечно-сосудистым заболеванием в анамнезе, нарушением функции желудочно-кишечного тракта, при которой изменялась абсорбция препарата. Не допускалось использование сопутствующих препаратов, удлиняющих интервал QT, а также наличие пируэтной желудочковой тахикардии в анамнезе. Характеристики пациенток на момент включения были сбалансированы между двумя группами.
Средний возраст составил 62 года. У всех больных был HR+ распространенный РГЖ, и все, кроме 2 пациенток (по 1 в каждой группе), имели HER2- заболевание. В общей сложности у 227 пациенток (34%) прогрессирующее или метастатическое заболевание было диагностировано впервые (34,1% в группе рибоциклиба и 33,8% – в группе плацебо). У 397 пациенток (59,4%) предшествующий безрецидивный период составил более 24 мес. У 393 пациенток (58,8%) наблюдалось поражение внутренних органов (включая метастазы в печени, легких и других внутренних органах), а у 147 (22%) – единичное поражение костей.
Пациентки основной группы получали рибоциклиб перорально (600 мг/день на протяжении 3 недель с недельным перерывом в 28-дневном цикле) в сочетании с летрозолом (2,5 мг в сутки), больные контрольной группы принимали плацебо с летрозолом. Снижение дозы рибоциклиба (с 600 до 400 или 200 мг/день) было разрешено для уменьшения частоты побочных явлений, связанных с терапией; доза летрозола оставалась неизменной. Пациентки, которые прекращали прием рибоциклиба или плацебо, продолжали получать летрозол. Какие-либо другие изменения терапии были запрещены.
Результаты
Средняя продолжительность лечения рибоциклибом и плацебо составляла 13,0 и 12,4 мес соответственно. Наиболее распространенными причинами прекращения лечения были:
- прогрессирование заболевания у 87 пациенток (26,0%) в группе рибоциклиба и 146 (43,7%) в группе плацебо;
- решение пациентки или врача в 22 (6,6%) и 26 случаях (7,8%) соответственно;
- побочные эффекты у 25 (7,5%) и 7 (2,1%) пациенток соответственно.
Медиана продолжительности наблюдения составила 15,3 мес. Медиана относительной интенсивности дозы составляла 100% для летрозола в двух группах, 100% для плацебо и 87,5% для рибоциклиба. Перерыв в приеме рибоциклиба произошел у 257 пациенток (76,9%) и летрозола – у 132 (39,5%) в группе рибоциклиба. Из 330 участниц второй группы по причине безопасности плацебо перестали получать 134 (40,6%) пациентки, а летрозол – 107 (32,4%). Снижение дозы препарата производилось у 53,9% пациенток в группе рибоциклиба и у 7,0% пациенток в группе плацебо, чаще всего по причине побочных эффектов (у 50,6 и 4,2% соответственно). Наиболее частым побочным эффектом, приводившим к снижению дозы, была нейтропения (у 104 пациенток, получавших рибоциклиб, и ни у одной из пациенток, получавших плацебо).
Эффективность рибоциклиба в комбинации с летрозолом
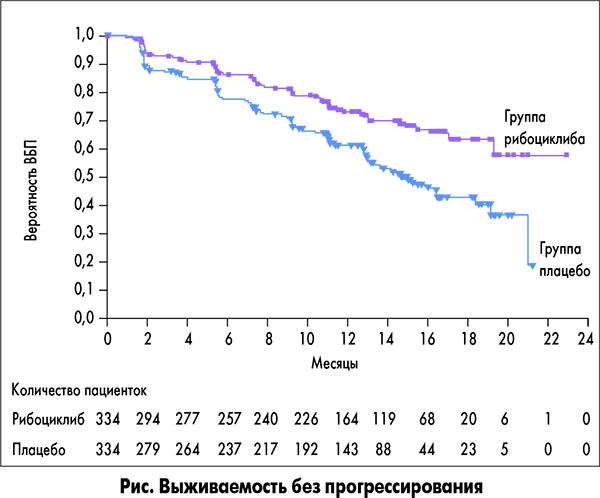
Промежуточный анализ был проведен после того, как по крайней мере у 211 пациенток отмечено прогрессирование заболевания или смертельный исход. Медиана продолжительности ВБП (рис.) не была достигнута в группе рибоциклиба (95% доверительный интервал – ДИ – от 19,3 до «не достигнуто»), тогда как в группе плацебо (отношение рисков 0,56; 95% ДИ 0,43-0,72; р=3,29×10–6) она составила 14,7 мес (95% ДИ 13,0-16,5). Локально оцениваемая ВБП была значительно выше в группе рибоциклиба, чем в группе плацебо. Через 12 мес ВБП составила 72,8% (95% ДИ 67,3-77,6) в группе рибоциклиба и 60,9% (95% ДИ 55,1-66,2) в группе плацебо. После 18 мес показатель ВБП в группах составил 63,0% (95% ДИ 54,6-70,3) и 42,2% (95% ДИ 34,8-49,5) соответственно. Результаты центрального анализа ВБП независимым комитетом подтвердили оценку первичной эффективности с отношением рисков 0,59 (95% ДИ 0,41-0,85; р=0,002).
Суммарная эффективность терапии составляла 40,7% в группе рибоциклиба и 27,5% в группе плацебо в популяции intention-to-treat, а также 52,7% и 37,1% соответственно среди пациенток с исходно измеримым заболеванием (р<0,001 для обоих сравнений). Клинические преимущества лечения достигнуты у 79,6% пациенток в группе рибоциклиба и 72,8% больных в группе плацебо в популяции intention-to-treat, а также у 80,1 и 71,8% соответственно среди пациенток с исходно измеримым заболеванием (р=0,02 для обоих сравнений). Результаты общей выживаемости не были готовы на момент промежуточного анализа; зафиксировано 43 случая смерти (23 в группе рибоциклиба и 20 в группе плацебо). Для оценки общей выживаемости исследование продолжается с сохранением слепого дизайна.
Безопасность
При оценке безопасности (у 334 пациенток в группе рибоциклиба и 330 в группе плацебо) побочными эффектами, которые наблюдались по крайней мере у 35% участниц обеих групп, были:
- нейтропения (74,3% в группе рибоциклиба и 5,2% в группе плацебо);
- тошнота (51,5 и 28,5% соответственно);
- инфекции (50,3 и 42,4% соответственно);
- усталость (36,5 и 30,0% соответственно);
- диарея (35,0 и 22,1% соответственно).
Тошнота, инфекции, усталость, диарея преимущественно были 1 и 2 степени. Наиболее распространенными побочными эффектами 3 или 4 степени (которые встречались у ≥5% пациенток обеих групп) были нейтропения (59,3% в группе рибоциклиба и 0,9% в группе плацебо), лейкопения (21,0 и 0,6% соответственно), артериальная гипертензия (9,9 и 10,9%), повышение уровня аланинаминотрансферазы (9,3 и 1,2%) и аспартатаминотрансферазы (5,7 и 1,2%), лимфопения (6,9 и 0,9%). Фебрильная нейтропения наблюдалась у 5 пациенток (1,5%) в группе рибоциклиба; в группе плацебо таких случаев не было.
Инфекции были зарегистрированы у 168 пациенток (50,3%) в группе рибоциклиба и у 140 (42,4%) в группе плацебо. Наиболее распространенными были инфекции мочевых путей (10,8 и 8,2% соответственно), а также верхних дыхательных путей (10,5 и 10,6%), преимущественно 1 или 2 степени. Сообщалось о единственном инфекционном осложнении 3 степени в группе рибоциклиба – инфекции мочевых путей у 2 пациенток (0,6%). В обеих группах не было инфекционных осложнений 4 степени. Увеличение интервала QTcF более чем на 60 мс в сравнении с исходными данными произошло у 9 пациенток (2,7%) в группе рибоциклиба и ни у одной пациентки в группе плацебо. В группе рибоциклиба у 11 пациенток (3,3%) отмечался по меньшей мере один средний QTcF интервал более 480 мс (в том числе 1 пациентка с изначальной патологией сердечно-сосудистой системы и 6 больных, у которых имело место увеличение интервала более чем на 60 мс от исходного уровня). Большинство из этих пациенток смогли продолжить лечение рибоциклибом в дозе 600 мг без прерывов. У одной пациентки (0,3%) в группе плацебо был средний интервал QTcF более 480 мс по сравнению с первоначальным.
Серьезные побочные эффекты были отмечены у 71 пациентки (21,3%) в группе рибоциклиба и у 39 (11,8%) в группе плацебо. Из них 25 (7,5%) в группе рибоциклиба и 5 (1,5%) в группе плацебо считались связанными с курсом лечения. Было 4 случая смерти: 3 (0,9%) в группе рибоциклиба и 1 (0,3%) в группе плацебо во время лечения. По одной пациентке в каждой из групп умерли от прогрессирования РГЖ. Оставшиеся 2 летальных исхода в группе рибоциклиба были вызваны внезапной смертью и смертью по неизвестной причине. Случай внезапной смерти считался связанным с рибоциклибом, произошел на 11-й день второго цикла и сопровождался гипокалиемией 3 степени (корригированной пероральными препаратами калия) и пролонгацией интервала QTcF в 1-й день второго цикла. Во время первого цикла эта пациентка принимала запрещенный сопутствующий препарат (метадон) с известным риском пролонгации интервала QT. Пациентка, которая умерла от неизвестной причины, получала рибоциклиб в течение 4 дней до отзыва информационного согласия и прекращения терапии. Летальных исход наступил через 19 дней и не был расценен исследователями как связанный с рибоциклибом.
Выводы
Рандомизированное исследование III фазы MONALEESA‑2 показало значительное увеличение показателя ВБП и уровня объективного ответа при применении комбинации рибоциклиба с летрозолом по сравнению с монотерапией летрозолом в первой линии лечения у женщин в постменопаузе с распространенным HR+ и HER2- РГЖ. То, что добавление рибоциклиба к летрозолу обеспечивает значительное повышение показателей общего ответа, согласуется с результатами предшествующих наблюдений. Увеличение безрецидивной выживаемости было сопряжено с более высокой частотой миелосупрессии у пациенток группы рибоциклиба, но в целом комбинированное лечение имеет приемлемый уровень безопасности. Большинство негематологических осложнений в группе рибоциклиба были 1 или 2 степени; побочные эффекты 3-4 степени были обратимы при временном прекращении лечения или снижении дозы, что позволяло большинству пациенток продолжать лечение.
Список литературы находится в редакции.
Статья печатается в сокращении.
Hortobagyi G.N., Stemmer S.M., Burris H.A. et al.
Ribociclib as First-Line Therapy for HR-Positive,
Advanced Breast Cancer. N Engl J Med 2016; 375: 1738-48.
Перевела с англ. Алена Юшинова