27 липня, 2017
Брентуксимаб ведотин як консолідуюча терапія після аутологічної трансплантації стовбурових клітин у пацієнтів з лімфомою Ходжкіна з ризиком рецидиву або прогресування: дослідження AETHERA
Рання консолідація брентуксимабом ведотином (БВ) після аутологічної трансплантації стовбурових клітин (АТСК) збільшує виживаність без прогресування (ВБП) захворювання в пацієнтів з лімфомою Ходжкіна (ЛХ) з факторами ризику розвитку рецидиву або прогресування після трансплантації. Таке лікування є важливою терапевтичною опцією для пацієнтів, яким проводиться АТСК.
Високодозова терапія з подальшою АТСК є стандартом медичної допомоги для пацієнтів з рецидивуючою або первинно-рефрактерною ЛХ. Два рандомізованих дослідження показали значне поліпшення ВБП після АТСК; декілька масштабних досліджень довели, що ця процедура може забезпечити виліковування приблизно 50% пацієнтів. Фактори ризику були ретельно вивчені з метою виявлення пацієнтів, для яких АТСК, найімовірніше, буде корисною. Серед факторів, що зазвичай пов’язуються з негативним прогнозом, – первинно-рефрактерна ЛХ, тривалість початкової ремісії менше 1 року, а також наявність екстранодальних вогнищ або пізньої стадії хвороби на момент рецидиву.
Розглядалися різні стратегії лікування з метою поліпшення результату після АТСК, у тому числі ПЕТ-адаптовані підходи, інтенсифікації режиму кондиціонування, опромінення до або після трансплантації, тандемна трансплантація і консолідуюча терапія після трансплантації. У попередніх дослідженнях, присвячених консолідуючій терапії, дослідники стикалися з проблемою забезпечення ефективної терапії, що добре переноситься, у ранні строки після АТСК, коли терапевтичний ефект може бути найбільшим.
Брентуксимаб ведотин – це кон’югат анти-CD30 антитіла з лікарським засобом, який доставляє антинеопластичний агент до CD30-позитивних пухлинних клітин, що призводить до їх апоптотичної загибелі.
Брентуксимаб ведотин показав значну ефективність, у тому числі частоту об’єктивної відповіді 75% і повну відповідь 34%, у базовому дослідженні II фази за участю пацієнтів із CD30‑позитивною ЛХ, для яких високодозова терапія і АТСК були неефективними. Тривале спостереження показало медіану загальної виживаності (ЗВ) 40,5 міс (95% довірчий інтервал – ДІ – 28,7 – не визначено). Дослідження AETHERA було проведене для того, щоб визначити, чи покращує застосування БВ ВБП захворювання в пацієнтів з рецидивуючою або первинно-рефрактерною ЛХ при використанні його як ранньої консолідуючої терапії після АТСК.
Методи
Це рандомізоване плацебо-контрольоване подвійне сліпе дослідження III фази проводилося у 78 центрах у Північній Америці та Європі. У ньому брали участь пацієнти (віком ≥18 років) з гістологічно підтвердженою класичною ЛХ, які перенесли високодозову хіміотерапію та трансплантацію аутологічних стовбурових клітин до рандомізації. Придатні до включення пацієнти мали принаймні один з таких факторів ризику прогресування після АТСК:
- первинно-рефрактерна ЛХ (недосягнення повної ремісії, визначене дослідником);
- рецидивуюча ЛХ з початковою тривалістю ремісії <12 міс;
- екстранодальні ураження на початку передтрансплантаційної сальвадж-терапії.
Крім того, пацієнти повинні були перебувати у стані повної ремісії, часткової ремісії або стабілізації захворювання після передтрансплантаційної сальвадж-терапії та мати збережену функцію печінки, нирок, а також кісткового мозку за результатами гематологічних і хімічних лабораторних досліджень. Пацієнтів, які раніше отримували БВ, виключили. Пацієнти, які перенесли більше однієї АТСК, були допущені до участі.
Пацієнти з несприятливими факторами ризику з рецидивуючою або первинно-рефрактерною класичною лімфомою Ходжкіна, які перенесли АТСК, були випадковим чином розподілені за допомогою рандомізації фіксованими блоками за послідовністю випадкових чисел, генерованих комп’ютером, в групи брентуксимабу ведотину (16 циклів по 1,8 мг/кг) або плацебо, що призначали внутрішньовенно раз на 3 тижні, починаючи з 30-45 дня після трансплантації.
Учасники були випадковим чином розподілені (1:1) за допомогою рандомізації фіксованими блоками за послідовністю випадкових чисел, генерованих комп’ютером, у групи БВ або плацебо, що призначали внутрішньовенно. Рандомізацію стратифіковано за кращою клінічною відповіддю після завершення сальвадж-терапії (повна відповідь – часткова відповідь – стабілізація захворювання), а також за первинною рефрактерною ЛХ порівняно з рецидивом хвороби менш ніж через 12 міс після завершення першої лінії терапії, порівняно з рецидивом через ≥12 міс після завершення лікування. Ні пацієнти, ні дослідники не були обізнані щодо призначеного лікування.
Брентуксимаб ведотин або плацебо вводили протягом 30 хв на 1-й день кожного 21-денного циклу (кожні 3 тижні) до 16 циклів. Якщо в пацієнтів, за визначенням дослідника, було виявлено радіографічні критерії прогресування захворювання, призначене лікування могло бути розкрите, і пацієнти у групі плацебо отримували можливість лікування БВ у рамках окремого дослідження доти, поки той не буде комерційно доступним (ClinicalTrials.gov, номер NCT0 1196208).
Прогресування оцінювалося за переглянутими критеріями відповіді на лікування пацієнтів зі злоякісними лімфомами; КТ проводилася на початку і через 3, 6, 9, 12, 18 і 24 міс після введення першої дози. Оцінка безпеки включала в себе реєстрацію побічних реакцій, у тому числі серйозних, супутніх препаратів, фізичний огляд і лабораторні аналізи. Тяжкість побічних реакцій оцінювалася за критеріями загальної термінології Національного інституту раку для побічних явищ (версія 4). Безпека контролювалася незалежним комітетом з моніторингу даних.
Первинною кінцевою точкою була ВБП за висновком незалежної експертизи, що визначається як час від рандомізації до першого підтвердженого прогресування захворювання або смерті. Вторинними кінцевими точками були загальна виживаність і безпека.
Результати
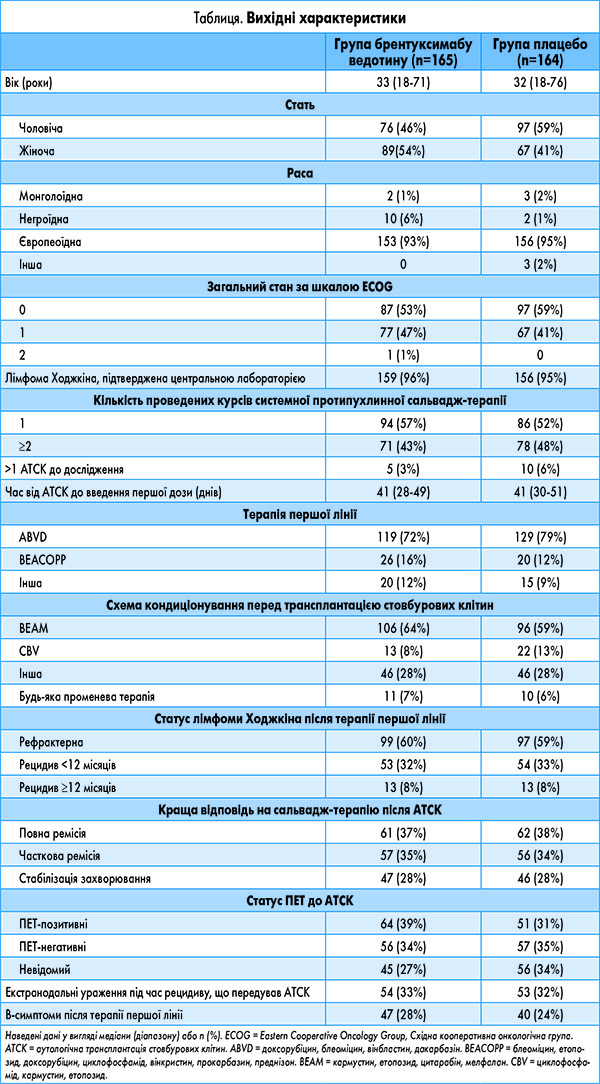
З 6 квітня 2010 р. по 21 вересня 2012 р. 329 пацієнтів були рандомізовані у групи БВ (n=165) або плацебо (n=164). Усі пацієнти припинили лікування станом на 25 липня 2013 р., і датою завершення збору даних для первинного аналізу ефективності було 18 серпня 2014 р. До групи БВ увійшло трохи більше пацієнтів жіночої статі і негроїдної раси; решта вихідних характеристик були в цілому аналогічні для обох груп (табл.). Усі пацієнти припинили лікування на момент завершення збору даних для первинного аналізу; 251 пацієнт залишився у програмі довгострокового спостереження: 122 (74%) пацієнти в групі БВ і 129 (79%) пацієнтів у групі плацебо. Причинами припинення лікування були: завершення 16 циклів терапії – 78 (47%) пацієнтів, які отримували БВ, і 81 (49%), які отримували плацебо; прогресування захворювання – 24 (15%) і 69 (42%) пацієнтів відповідно; побічні явища – 54 (33%) і 10 (6%) пацієнтів відповідно, а також рішення пацієнта – 9 (5%) і 4 (2%) хворих відповідно.
Найчастішими побічними явищами, що призвели до припинення лікування БВ, були периферична сенсорна та моторна нейропатія (дані не представлені).
Через 30 міс медіани часу спостереження (діапазон від 0 до 50 міс) первинна кінцева точка – ВБП згідно з незалежною оцінкою – значно поліпшувалася у пацієнтів групи БВ (відносний ризик – 0,57; 95% ДІ 0,40-0,81; p=0,0013), що еквівалентно зниженню вірогідності настання події на 43%. Медіана ВБП у групі БВ склала 42,9 міс (95% ДІ 30,4-42,9) порівняно з 24,1 міс (11,5 – не визначено) у групі плацебо. Розрахункова 2-річна ВБП за незалежною оцінкою склала 63% (95% ДІ 55‑70) у групі БВ і 51% (95% ДІ 43‑59) у групі плацебо. ВБП за остаточною оцінкою дослідників також покращувалася в пацієнтів у групі БВ. Розрахункова 2-річна ВБП за оцінкою дослідників склала 65% (95% ДІ 57-72) у групі БВ порівняно з 45% (95% ДІ 37-52) у групі плацебо.
Проміжний аналіз ЗВ свідчить про відсутність значущих відмінностей між групами терапії. Важливо, що 72 (85%) з 85 пацієнтів групи плацебо, яким після виникнення прогресування призначалося подальше лікування за рамками даного дослідження, отримували БВ. Крім цього, алогенна трансплантація стовбурових клітин пацієнтам групи плацебо виконувалася частіше, ніж пацієнтам групи БВ (n=23 проти n=12). При post-hoc аналізі в пацієнтів, що були відібрані за більшою кількістю факторів ризику, відзначалося значно більш виражене підвищення показників ВБП на тлі консолідації БВ порівняно з плацебо. Аналогічна картина спостерігалася з точки зору ЗВ: зменшення відносного ризику для ЗВ у пацієнтів, що мали більше одного фактора ризику.
Популяція аналізу безпеки включала 167 пацієнтів, які отримували БВ, і 160 пацієнтів, які отримували плацебо.
Найчастішою побічною реакцією в групі БВ була периферична сенсорна нейропатія. Виникнення периферичної нейропатії після початку лікування відзначалося у 112 (67%) пацієнтів у групі БВ і у 31 (19%) – у групі плацебо. Периферична нейропатія була причиною припинення терапії БВ у 38 (23%) пацієнтів і потребувала модифікації дози у 51 (31%) хворого. З 51 пацієнта з периферичною нейропатією, яким була потрібна модифікація дози, 13 (25%) припинили лікування через периферичну нейропатію, а 29 (57%) завершили всі 16 циклів терапії. У пацієнтів, які завершили менш ніж 16 циклів терапії, медіана кількості циклів лікування в групі БВ склала 10,5 (діапазон від 2 до 15). Нейтропенія частіше виникала в пацієнтів у групі БВ, ніж у групі плацебо. Нейтропенія ступеня тяжкості ≥3 зафіксована у 49 (29%) пацієнтів групи БВ; тільки в одного (1%) пацієнта цієї групи була фебрильна нейтропенія. Нейтропенія призводила до відстрочення введення дози у 36 (22%) пацієнтів групи БВ, але не потребувала зменшення дози або припинення лікування. Підтримувальну терапію колонієстимулюючим фактором отримували 42 (25%) пацієнти у групі БВ і 17 (11%) – у групі плацебо. Важкі інфекції (ступінь тяжкості ≥3) виникали у 11 (7%) пацієнтів у групі БВ і у 9 (6%) – у групі плацебо.
У цілому у 13 (4%) з 327 пацієнтів після початку лікування виникли легеневі токсичні явища: у 8 (5%) – у групі БВ і у 5 (3%) – у групі плацебо. До проведення аналізу померли 53 (16%) пацієнти: 28 (17%) у групі БВ і 25 (16%) у групі плацебо. Частка пацієнтів, які померли внаслідок захворювання, була подібною в обох групах лікування: 18 (11%) випадків смерті в групі БВ і 17 (11%) – у групі плацебо.
Обговорення
Результати дослідження свідчать про те, що, порівняно з плацебо, консолідуюча терапія БВ сприяє статистично і клінічно значущому зростанню ВБП згідно з незалежною оцінкою і оцінкою дослідників. За незалежною оцінкою, розрахункова частка пацієнтів, що вижили й не мали ознак прогресування захворювання до 24 міс, склала 63% при застосуванні БВ і 51% на тлі плацебо. Згідно з оцінкою дослідників, розрахункова частка пацієнтів до 24 міс становила відповідно 65 і 45%. Після періоду оцінки в 24 міс, що сумарно охоплює 108 пацієнто-років спостереження, було зареєстровано лише 4 події, пов’язані з ВБП.
У попередніх дослідженнях продемонстровано, що рецидив або прогресування після АТСК зазвичай мають місце рано: 71% випадків прогресування відбуваються протягом 1 року після трансплантації, а 90% – протягом 2 років. Ці дані свідчать на користь того, що багато хто з пацієнтів, у яких не виявлялося ознак прогресування до 24 міс, можуть бути вилікувані, проте необхідно подальше спостереження за їх виживаністю. На додаток до стійкого клінічного ефекту консолідації БВ у цьому дослідженні більшість пацієнтів групи плацебо потребували подальшої протипухлинної терапії, включаючи майже удвічі більшу потребу в алогенній трансплантації стовбурових клітин порівняно з групою БВ.
Відзначено стійкий позитивний вплив БВ на ВБП в усіх підгрупах дослідження, у тому числі у пацієнтів з первинною рефрактерністю і рецидивом менш ніж через 12 міс після першої лінії терапії. Ефективність трохи зменшується в пацієнтів, ПЕТ-негативних перед АТСК; однак інтерпретація цього спостереження обмежена в зв’язку з тим, що ПЕТ не передбачалася протоколом дослідження як обов’язкова процедура і протокол не потребував об’єктивних критеріїв для інтерпретації знімків.
При короткостроковому періоді подальшого спостереження в цьому дослідженні припускалося, що проміжний аналіз ЗВ не виявить відмінностей між групами терапії, зважаючи на малу кількість подій і вплив на аналіз високої частоти переходу пацієнтів з групи плацебо.
Порівняно з літературними даними про виживаність пацієнтів з ЛХ з групи високого ризику, які перенесли АТСК, трирічна ЗВ в цьому дослідженні, що перевищує 80%, є значною і може свідчити про клінічну користь БВ як консолідуючої терапії та терапії «порятунку». Пацієнти, у яких виникло прогресування захворювання після АТСК, живуть із хронічною формою ЛХ, і більшість з них помруть від захворювання або ускладнень терапії; але з появою нових препаратів, у тому числі БВ, становище таких хворих поліпшується. Дані довгострокового подальшого спостереження пацієнтів з рецидивом або прогресуванням ЛХ свідчать про досягнення на тлі терапії БВ медіани ЗВ, що дорівнює 40,5 міс (95% ДІ 28,7 – не визначено). Отже, у групі БВ може бути показаний сприятливий вплив на виживаність, однак для цього потрібен довший період подальшого спостереження, який і передбачено дослідженням. Рання консолідація БВ сприяла зменшенню числа подій прогресування захворювання і виліковуванню більшої кількості пацієнтів.
Терапія БВ, як правило, добре переноситься, і профіль безпеки відповідає результатам попередніх досліджень. Майже половина пацієнтів у групі БВ завершили всі 16 циклів терапії. Периферична нейропатія була найбільш поширеною побічною реакцією, при цьому в більшості пацієнтів мало місце завершення або поліпшення симптомів на час аналізу. Слід зазначити, що третина пацієнтів в групі БВ припинили лікування через токсичні явища, головним чином, нейропатію. Нейтропенія піддавалася контролю колонієстимулюючим фактором чи відтермінуванням введення дози. Важливо, що терапія БВ мала сприятливий профіль переносимості в ранній період після АТСК і не супроводжувалася розвитком серйозних інфекцій, що вказує на можливість раннього початку застосування БВ після АТСК, коли вплив пухлини мінімальний і консолідація може дати найбільший ефект.
Брентуксимаб ведотин як консолідуюча терапія в цілому добре переносився безпосередньо після АТСК і забезпечував стійкий позитивний вплив на ВБП у пацієнтів з ЛХ з групи високого ризику рецидиву або прогресування після АТСК. Консолідуюча терапія БВ може збільшити ймовірність виліковування або сприяти уникненню подальших курсів токсичної хіміотерапії і видається ефективною у хворих на рак, особливо в популяції пацієнтів молодого віку, де існує висока потреба в ефективному лікуванні.
Список літератури знаходиться в редакції.
Стаття друкується у скороченні.
Moskowitz Craig H., Nademanee Auayporn, Masszi Tamas, Agura Edward, Holowiecki Jerzy, Abidi Muneer H., Chen Andy I., Stiff Patrick, Gianni Alessandro M., Carella Angelo, Osmanov Dzhelil, Bachanova Veronika, Sweetenham John, Sureda Anna, Huebner Dirk, Sievers Eric L., Chi Andy, Larsen Emily K., Hunder Naomi N., Walewski Jan для AETHERA Study Group.
Перекладено та адаптовано
з Lancet 2015; 385: 1853-62
За підтримки ТОВ «Такеда Україна»
UA/ADC/0717/0022


