27 липня, 2017
Наночасточки сквалену, поєднані з гемцитабіном, – новий підхід до забезпечення цільової доставки хіміопрепарату
30 травня 2017 р. у журналі Nature Communications вийшла друком стаття «Кон’югація сквалену з гемцитабіном як унікальний підхід до доправлення ліків, що використовує ендогенні ліпопротеїни». Одним з її співавторів у складі великого міжнародного колективу дослідників є провідний науковий співробітник відділу фізики біологічних систем Інституту фізики НАН України, доктор фізико-математичних наук Семен Єсилевський.
Наукову роботу виконано в галузі наномедицини – міждисциплінарного наукового напряму на перетині медицини, молекулярної біології, біофізики, біохімії та фармакології, який займається застосуванням наночасточок з лікувальною та діагностичною метою.
Значною проблемою лікування пацієнтів з онкологічними захворюваннями є адресна доставка токсичних лікарських речовин безпосередньо до пухлини з мінімізацією їхнього впливу на здорові тканини та організм у цілому. Інертні наночасточки можуть використовуватися як контейнери, здатні переносити лікарський препарат до клітин-мішеней, вивільняючи його лише там, де необхідно. Зазначене завдання є складним для безпосередньої реалізації, адже потребує складних міжгалузевих досліджень на перетині медицини, молекулярної біології, біофізики, біохімії та фармакології.
Зокрема, для успішного створення онкологічного нанопрепарату необхідно розробити:
- методи отримання наночасточок різного походження;
- способи з’єднання наночасточок з лікарським препаратом;
- способи адресної доставки до злоякісних (або інших) клітин;
- методи контрольованого вивільнення хіміопрепарату в пухлинні клітини;
- шляхи забезпечення утилізації наночасточок організмом тощо.
Наразі вирішити всі поставлені завдання в повному обсязі ще не вдалося. Дослідження, присвячені нанотехнологіям в онкологічній практиці, проводяться в багатьох наукових центрах по всьому світу, мають міждисциплінарний та часто міжнародний характер, оскільки потребують об’єднання зусиль та досвіду фахівців різних спеціальностей.
За майже 30 років існування наномедицини було запропоновано величезну кількість варіантів терапевтичних наночасточок: їх виготовляли на основі різноманітних полімерів, ліпосом (ліпідних пухирців), металевих наночасточок (заліза, золота, срібла, міді), карбонових матеріалів (фулеренів, нанотрубок, графену), багатьох інших матеріалів та їх комбінацій. Жоден із цих варіантів не увійшов до широкої медичної практики.
Сьогодні вважається, що для досягнення бажаного ефекту найкраще підходять наночасточки з нетоксичних біосумісних матеріалів, які можуть розпадатися й утилізуватися в організмі, не завдаючи шкоди здоровим органам і тканинам.
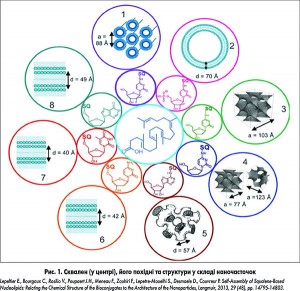
Одним з перспективних біосумісних матеріалів є сквален – жиророзчинна речовина, що постійно синтезується в клітинах нашого організму як попередник у синтезі холестеролу та стероїдних гормонів (рис. 1). Сквален – нейтральна речовина, яка давно широко використовується у парфумерії та косметології. Фахівці групи професора Патріка Кувре (Patrick Couvreur) з Університету Парі-Зюд (м. Париж, Франція) є піонерами у використанні сквалену для створення терапевтичних наночасточок. Вони зокрема розробили технологію хімічної модифікації низки лікарських препаратів скваленовими «хвостами», після якої утворені агрегати починають формувати наночасточки різної форми й розміру.
Відомо, що скваленові наночасточки нетоксичні та можуть бути введені безпосередньо у кров, яка успішно транспортує їх до відповідних тканин-мішеней. Водночас не було досліджено, як саме такі часточки взаємодіють з різноманітними компонентами плазми крові. Власне, з’ясування цих механізмів і стало метою дослідження, в якому взяв участь С. Єсилевський. Роботи проводилися шляхом поєднання експериментальних методик та комп’ютерного моделювання. Останніми роками комп’ютерне моделювання стало своєрідним золотим стандартом для біомедичних досліджень.
Оскільки сквален є жиророзчинною речовиною, то окрему увагу науковці приділили вивченню його взаємодії з ліпопротеїнами плазми крові. Ліпопротеїни – це складні білкові молекули, синтезовані людським організмом для транспорту не розчинних у воді речовин, зокрема ліпідів і холестеролу. Самі ліпіди у крові не розчиняються, але в поєднанні з ліпопротеїдами можуть транспортуватися з током крові. Особливу роль у цьому процесі відіграє фракція ліпопротеїнів низької щільності, надлишок яких часто спостерігається в осіб, хворих на атеросклероз. Спрощено ліпопротеїни можна описати як нанорозмірні жирові краплі, вкриті поверхневим шаром білків.
Під час дослідження виявилося, що у плазмі крові скваленові наночасточки дуже активно взаємодіють з ліпопротеїнами низької щільності. Комплекс протипухлинного препарату гемцитабіну зі скваленом (гемцитабін-сквален) вбудовується в ліпопротеїнові часточки та разом з ними транспортується в межах організму (рис. 2). Скваленовий «хвіст» при цьому виконує функцію якоря: завдяки своїй жиророзчинності він проникає всередину ліпопротеїнової жирової краплі, втягуючи за собою приєднану молекулу гемцитабіну. Без скваленового «хвоста» цей водорозчинний препарат не проникає в ліпопротеїнові часточки та швидко деградує в плазмі крові, не досягаючи клітин-мішеней.

Можливість вбудовування гемцитабін-сквалену в ліпопротеїни є важливою ще й з огляду на те, що клітини злоякісних пухлин часто мають підвищену потребу в холестеролі й захоплюють із крові значно більшу кількість ліпопротеїнів, ніж здорові клітини. Таким чином, лікарський препарат у високих концентраціях буде адресно надходити до клітин-мішеней і активно споживатися ними.
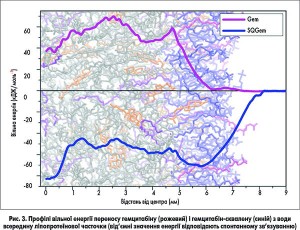
Дослідницька група професора П. Кувре виконувала основну експериментальну частину роботи. Український вчений С. Єсилевський разом з професором Крістофом Рамзеєром (Christophe Ramseyer) з Університету Бурґонь-Франш-Комте (м. Безансон, Франція) проводили комп’ютерне моделювання процесу вбудовування гемцитабін-сквалену в ліпопротеїни низької щільності за допомогою методу молекулярної динаміки. Розглядалася модельна система з кількох сотень тисяч атомів, яка складалася з молекули гемцитабін-сквалену й частини ліпідного ядра ліпопротеїнової часточки (рис. 3). Обраховувалися всі фізичні міжатомні взаємодії та рух усіх атомів у такій системі. Було доведено, що для молекули гемцитабін-сквалену проникнення в ліпопротеїнову часточку є енергетично вигідним, тоді як сам гемцитабін усередину не проникає. Розрахунки достовірно підтвердили експериментальні дані.
Таким чином, скваленові наночасточки можуть бути носієм для хіміопрепарату. Природні властивості сквалену дозволяють використовувати ендогенні ліпопротеїни для транспорту хіміопрепаратів та підвищувати вибіркове поглинання лікарського препарату злоякісними пухлинними клітинами. Зазначена робота пояснює лише одну з численних деталей складної картини поведінки скваленових наночасточок у живому організмі. Однак саме такі деталі є важливими для створення нових ефективних лікарських засобів, придатних для використання в онкології.
Sobot D., Mura S., Yesylevskyy S.O. et al. Conjugation of squalene to gemcitabine as unique approach exploiting endogenous lipoproteins for drug delivery. Nature Communications 8, Article number: 15678 (2017).
Підготувала Катерина Котенко
Підготовлено за підтримки прес-служби НАН України