27 липня, 2017
Клинический случай лечения редкой гигантской гастроинтестинальной стромальной опухоли пищевода
Термин «гастроинтестинальные стромальные опухоли» (GIST – Gastrointestinal Stromal Tumors) был впервые предложен в 1983 г. для описания неэпителиальных опухолей желудочно-кишечного тракта, которые по своим иммуногистохимическим и ультраструктурным характеристикам отличаются от опухолей истинно нейрогенного и гладкомышечного происхождения [1, 2]. Верификация GIST основана на использовании иммуногистохимического определения гиперэкспрессии клетками GIST тирозинкиназного рецептора с-kit (CD117) и его гиперактивации [4, 10, 11, 13].
По разным данным, гастроинтестинальные стромальные опухоли составляют от 0,1 до 3% от всех злокачественных новообразований желудочно-кишечного тракта и являются наиболее часто встречающимися мезенхимальными опухолями данной локализации [1]. Однако описания гастроинтестинальных стромальных опухолей пищевода встречаются крайне редко, не более 2% от всех GIST, тем более отсутствует достоверная статистика их встречаемости в популяции [1].
В зависимости от преобладания того или иного компонента при морфологическом исследовании выделяют веретеноклеточный (70%), эпителиоидный (20-25%) и смешанный варианты GIST. Большинство опухолей на этапе их первичного диагностирования при отсутствии диссеминации и инфильтрации органов/тканей выглядят как доброкачественные новообразования (до 70%). Однако морфологи предпочитают не использовать термин «доброкачественный», поскольку считается, что практически все GIST имеют злокачественный потенциал и, вероятно, при длительном периоде наблюдения опухоль приобретает черты «злокачественного» новообразования [3, 8, 9, 12, 13].
В настоящее время к GIST относят мезенхимальные опухоли гастроинтестинального тракта, позитивные по CD117, а результаты иммуногистохимического анализа на наличие экспрессии CD117 являются определяющими в проведении дифференциальной диагностики. Другими маркерами, которые помогают дифференцировать GIST от других опухолей желудочно-кишечного тракта мезенхимального происхождения, являются CD34-антиген, S‑100 протеин, гладкомышечный актин (SMA) и десмин. Таким образом, иммуногистохимическое исследование является неотъемлемой частью диагностического процесса и должно проводиться в специализированном лечебном учреждении при всех мезенхимальных новообразованиях желудочно-
кишечного тракта и забрюшинного пространства [1, 2, 8, 9, 13].
Описание клинического случая
Пациент C., 61 год, поступил в 1-е хирургическое отделение Харьковской городской больницы скорой и неотложной медицинской помощи, являющееся клинической базой кафедры торакоабдоминальной хирургии ХМАПО с клиникой дисфагии, с выраженной общей слабостью, дискомфортом за грудиной.
Из анамнеза: болеет в течение 10-12 лет, когда впервые отметил наличие дисфагии, длительное время наблюдался и проходил консервативное лечение по месту жительства, где больному проводилась консервативная терапия с периодическими плановыми обследованиями по поводу ахалазии пищевода, на которых рентгенологически выявляли признаки дилатационной эзофагопатии, эндоскопически – явления застойного эзофагита. Последняя госпитализация была связана с клиникой пищеводного кровотечения (по данным ФГДС, имели место кровотечение из язвенного дефекта пищевода). После остановки кровотечения больной был направлен для дальнейшего дообследования в клинику кафедры торакоабдоминальной хирургии ХМАПО для уточнения диагноза и решения вопроса об оперативном лечении.
При поступлении больной предъявлял жалобы на наличие дисфагии 1 степени (нарушение проходимости для грубой пищи) с задержкой пищи и неприятными ощущениями в области верхней трети грудной клетки. Объективно – правильного телосложения, удовлетворительного питания, дефицита массы тела нет. Данные рентгенологического исследования представлены на рисунке 1.
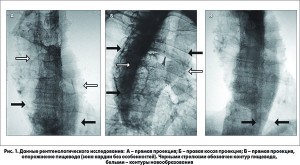
Определялось расширение пищевода до 10-15 см в верхне- и среднегрудном отделах пищевода, в просвете определяются округлые массы. При этом длительной задержки бариевой взвеси в пищеводе и при прохождении через кардию, что было бы характерно для ахалазии пищевода 3-4 стадии, при рентгенологическом обследовании не выявлено. При опорожнении пищевода определялись контуры новообразования пищевода, что позволяло заподозрить наличие новообразования пищевода. При этом наличие злокачественной опухоли таких больших размеров представлялось маловероятным ввиду относительно удовлетворительного состояния пациента.
При эндоскопическом исследовании в просвете пищевода выявлены бугристые разрастания с обширными изъязвлениями, протяженностью от 20 до 30 см от резцов просвет пищевода щелевидно сужен, на протяжении 30 см от резцов определялись бугристые разрастания хрящевой плотности, а на протяжении от 30 до 35 см от резцов проходимость для эндоскопа была сохранена, желудок и двенадцатиперстная кишка без особенностей. Заподозрено наличие злокачественной опухоли пищевода. Взята биопсия: в одном из биоптатов выявлены фрагменты лейомиомы пищевода, покрытой плоским эпителием.
Для уточнения диагноза больному выполнена 64-срезовая компьютерная томография (СКТ) с контрастированием. По данным СКТ выявлено гигантское полиповидное образование на ножке, исходящее из левой заднебоковой стенки шейного отдела пищевода на уровне С V – C VI, свободно свисающее в просвет пищевода с наличием зон деструкции, кальцификации и изъязвления (рис. 2).
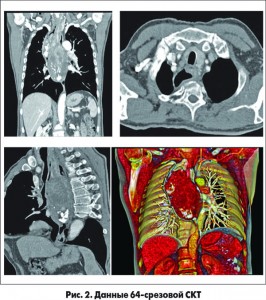
При этом нельзя было полностью исключить сращение образования с левой боковой стенкой пищевода в зоне верхней трети внутригрудного отдела пищевода. Также выявлены сосуды, кровоснабжающие образование из бассейна левой нижней щитовидной артерии и проходящие магистрально через ножку опухоли.
Клинический анализ крови: гемоглобин – 118 г/л, эритроциты – 3,92×1012/л, лейкоциты – 17,1×109/л, гематокрит – 0,315, тромбоциты – 390×109/л, лимфоциты – 19,1%, моноциты – 6,2%, гранулоциты – 74,7%. Биохимический анализ крови: белок – 59 г/л, билирубин общий – 7,0 мкмоль/л, глюкоза крови – 5,5 ммоль/л, АЛТ – 19 МЕ/л, АСТ – 14 МЕ/л, амилаза – 59 МЕ/л, мочевина – 4,39 мкмоль/л, креатинин – 91,5 мкмоль/л. Коагулограмма: ПТИ – 90 с, фибриноген – 3,99 г/л, АЧР – 60 с. На основании полученных данных установлен диагноз – гигантская лейомиома шейного отдела пищевода с явлениями кальцификации и распада, вторичная дилатационная эзофагопатия. Больному предложено оперативное лечение.
Оперативное вмешательство выполнено левосторонним шейным и правосторонним торакотомным доступом. Из левостороннего шейного доступа произведена мобилизация шейного отдела пищевода с перевязкой левой нижней щитовидной артерии для деваскуляризации образования и уменьшения риска кровотечения после удаления опухоли (рис. 3А). Основной этап выполнен из правостороннего переднебокового торакотомного доступа в 5 межреберьи (рис. 3Б).
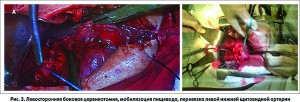
При ревизии обращало на себя внимание значительное расширение пищевода в области верхней и средней трети внутригрудного отдела с гипертрофией стенки и наличием объемного образования больших размеров в просвете пищевода (рис. 4А). После выполнения продольной эзофаготомии извлечена большая опухоль размерами 18×10×12 см (рис. 4Б).
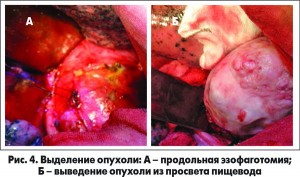
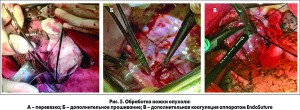
После выведения опухоли получен доступ к ее ножке, фиксированной в области шейного отдела пищевода (рис. 5).
Ножка опухоли была дважды лигирована (рис. 5А), а после отсечения опухоли прошита атравматической нитью (рис. 5Б) с дополнительной коагуляцией аппаратом EndoSuture (рис. 5В). Произведена продольная эзофагография непрерывным швом рассасывающейся нитью, в желудок проведен трансназальный зонд для питания, плевральная полость дренирована по Бюлау.
Шейный доступ и торакотомный разрез ушиты. Окончательный вид удаленного препарата представлен на рисунке 6.
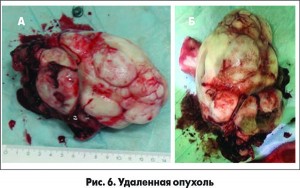
В послеоперационном периоде проводилось зондовое питание с 2-х по 5-е сутки, трансназальный зонд удален на 4-е сутки после операции. На 5-е сутки отмечалось формирование экссудативного левостороннего реактивного плеврита (проведена пункция – эвакуировано 400 мл серозного экссудата). Больной выписан в удовлетворительном состоянии на 7-е сутки после операции. Наблюдение в течение 4 мес не выявило данных относительно рецидива опухоли, дисфагии нет.
Гистологическое исследование
Для морфологического исследования иссеченные фрагменты опухоли фиксировали в 10% растворе формалина на 24 ч. После фиксации кусочки ткани заливали в парафин, срезы окрашивали гематоксилином и эозином. Для изучения гистогенетических особенностей новообразования иммуногистохимическим методом применяли панель моноклональных антител (МКАТ), включающую: общий эпителиальный маркер – Cytokeratin pan AE1/AE3; гладкомышечный актин (Smooth Muscle Actin 1A4); маркер эндотелиальных клеток (CD34); маркер клеток нейронального происхождения – нейронспецифическая энолаза (NSE (BBS/NC/V1-H14)); маркера клеток гистиоцитарного происхождения CD68 KP 1; CD117 c-kit протоонкоген, ассоциированный с опухолевыми клетками GIST; маркера пролиферации Ki-67 (MIB1). Использовались первичные моноклональные антитела фирмы DAKO (Дания), Ready-to-Use. В качестве хромогена использовался DAB (диаминобензидин). Комплекс морфологических и морфометрических исследований проводился на микроскопе Primo Star (Carl Zeiss) с использованием программ AxioCam (ERc 5s).
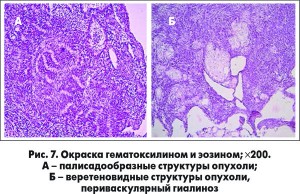
При микроскопическом исследовании было установлено, что новообразование имело четкую связь с мышечным слоем стенки пищевода, не имело собственной капсулы. Гистологическая структура опухоли оказалась неоднородной. Отдельные ее участки состояли из вытянутых клеток с различной эозинофилией цитоплазмы, со слабо различимыми границами. Ядра сигарообразные, расположены центрально, содержали мелкодисперсный или мелкопузырчатый хроматин. В единичных клетках обнаруживалась выраженная вакуолизация цитоплазмы, в результате они приобретали перстневидную структуру. Группы клеток формировали пучки различной длины, короткие вихреобразные или палисадообразные структуры, напоминающие лейомиому или нейриному (рис. 7А).
Очагово определялись светлые овальные или округлые клетки, складывающиеся в клеточные гнезда или альвеолярные структуры, преимущественно вокруг кровеносных сосудов. Опухоль отличалась высокой степенью васкуляризации, местами приобретая вид ангиолейомиомы. В опухолевой строме обнаруживались поля гиалиноза, особенно периваскулярно. Миксоидные изменения чередовались с обширными полями кровоизлияний и массивными некрозами. Преимущественно в подслизистой основе выявлялась очагово-диффузная лимфоцитарная инфильтрация (рис. 7Б).
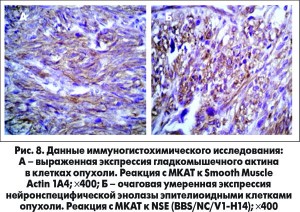
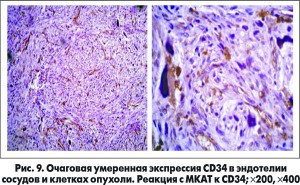
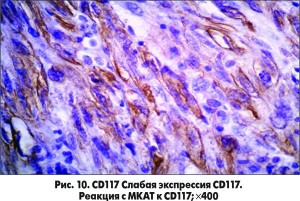
С предварительным морфологическим диагнозом «ангиолейомиома пищевода» материал направлен на иммуногистохимическое исследование (табл.). Его объем и результаты представлены и на рисунках 8-10.
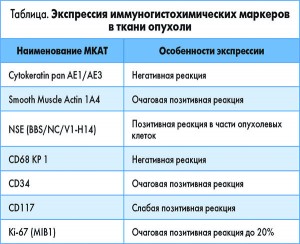
Важной фенотипической особенностью опухолевых клеток является способность экспрессировать как гладкомышечные, так и нейрональные и эндотелиальные иммуногистохимические маркеры. Таким феноменальным свойством обладают так называемые GIST, что позволило установить данный патоморфологический диагноз.
Обсуждение
Пищеводная локализация GIST составляет 0,01-0,03% от всей злокачественной патологии ЖКТ [7, 8]. Особенности роста опухоли и ее клинические проявления позволяют ей вырастать до гигантских размеров без значительного изменения общего состояния пациента. Заподозрить GIST позволяют ее большие размеры, отсутствие соединительнотканной капсулы с наличием, однако, четкой границы со здоровыми тканями, что сближает ее с доброкачественными опухолями, и наличие зон некроза и кальцификации. Также для GIST характерно отсутствие лимфогенной диссеминации, что делает ненужным выполнение местной и регионарной лимфодиссекции, а также позволяет выполнять оперативные вмешательства с сохранением пораженного органа.
Развиваются эти опухоли из интерстициальных клеток Кахаля, которые занимают промежуточное положение между гладкомышечной и нервной тканью. Эти опухоли не всегда прорастают слизистую, что и не всегда позволяет поставить диагноз по результатам эндоскопической биопсии. Кроме того, опухоль при окраске гематоксилин-эозином по гистологической структуре похожа на лейомиому пищевода, что также является причиной диагностических ошибок.
Важной фенотипической особенностью опухолевых клеток, связанной с их ростом из клеток Кахаля, является способность экспрессировать как гладкомышечные, так и нейрональные и эндотелиальные иммуногистохимические маркеры. Поэтому идентификация гистологической принадлежности GIST представляет сложную диагностическую задачу [2, 4] и, согласно рекомендациям ВОЗ, возможна лишь с помощью иммуногистохимического метода [3].
Своевременная диагностика и лечение этой категории больных с применением современных методов диагностики возможна при вовлечении в диагностический процесс высококвалифицированной команды врачей различных специальностей.
Таким образом, данное клиническое наблюдение свидетельствует о разнообразии морфологических типов и клинических проявлений GIST и необходимости тщательного подхода к лечению и дальнейшему наблюдению за такими больными на основании таких прогностических факторов, как: размеры опухоли, иммунофенотип, митотический индекс, радикализм оперативного вмешательства. Хирургический метод является ведущим в лечении GIST и позволяет надеяться на полное выздоровление. В нашем случае удалось провести обработку ножки пищевода в пределах здоровых тканей, что позволило уменьшить травматичность операции и сохранить функцию органа.
Выводы
Анализ данных литературы и описанного выше клинического случая показывает, что наличие у больного гигантской GIST пищевода является серьезной диагностической и лечебной задачей. Комплексное обследование больного с применением современных томографических методов позволяет разрешить диагностические противоречия, возникающие при анализе традиционных методов обследования, и определить тактику дальнейшего хирургического лечения. Обязательным для подтверждения гистологической принадлежности GIST является иммуногистохимическое исследование.
Литература
1. Гастроинтестинальные стромальные опухоли (диагностика, лечение) // Практические рекомендации. Под ред. проф. И.Ф. Поддубной. – Москва, 2008. – 54 с.
2. Серяков А.П. Гастроинтестинальные стромальные опухоли // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. – 2010. – Т. 20. – № 4. – С. 49-57.
3. Benjamin R., Rankin C., Fletcher C. et al. Phase III dose-randomized study of imatinib mesylate (STI571) for GIST: intergroup S0033 early results // Proc. Am. Soc. Clin. Oncol. – 2003. – V. 22. – P. 3271.
4. Crossby J., Catton C., Davis A. et al. // Malignant gastrointestinal stromal tumors of the small intestine: a review of 50 cases from prospective database. Ann Surg Oncol. – 2001. – V. 8. – P. 50-59.
5. De Matteo R., Lewis J., Leung D. et al. // Two hundred gastrointestinal stromal tumors: recurrence patterns and prognostic factors for survival. – Ann Surgery. – 2000. – V. 231. – P. 51-58.
6. Demetri G., von Mehren M., Blanke C. et al. // Efficacy and safety of imatinib mesylate in advanced gastrointestinal stromal tumors // N Engl J Med. – 2002. – V. 347. – P. 472-480.
7. Dougherty M., Compton C., Talbert M. et al. // Sarcomas of the gastrointestinal tract. Separation into favorable and unfavorable prognostic groups by mitotic count. – Annal. Surg. – 1991. – V. 214. – P. 569-574.
8. Fletcher C., Berman J., Corless C. et al. // Diagnosis of gastrointestinal stromal tumors: a consensus approach // Human Pathology. – 2002. – V. 33. – № 5. – P. 459-465.
9. Fletcher J., Corless C., Dimitrijevic S. et al. // Mechanisms of resistance to imatinib mesylate in advanced gastrointestinal stromal tumors // Proc. Am. Soc. Clin. Oncol. – 2003. – V. 22. – P. 3275.
10. Heikki J. Стратификация больных с гастроинтестинальными стромальными опухолями по группам риска // Human pathology. – 2008. – vol. 39. – № 10. – С. 1-9.
11. Miettinen M., Lasota J. Gastrointestinal stromal tumors – definition, clinical, histological, immunohistochemical, and molecular genetic features and differential diagnoses // Virchows. Arch. – 2001. – V. 438. – P. 1-12.
12. Oosterom A.T., Judson I.R., Verweij J. et al. Update of phase I study of imatinib (STI571) in advanced soft tissue sarcomas and gastrointestinal stromal tumors: a report of the EORTC Soft Tissue and Bone Sarcoma Group // Eur J Cancer. – 2002. – V. 38. – Suppl. 5. – P. 83-87.
13. Singer S., Rubin B., Fletcher A. et al. // Prognostic value of kit mutation type, mitotic activity, and histological subtype in gastrointestinal stromal tumors. – J. of Clin. Oncol. – 2002. – V. 20. – № 18. –
P. 3898-3905.