27 липня, 2017
Современные подходы к терапии глиобластом
Прогрессирование при глиобластоме (ГБМ), наиболее распространенном первичном раке головного мозга (ГМ), сопровождается ухудшением нейрокогнитивной функции, снижением функционального статуса (ФС) и прогрессирующим снижением качества жизни, связанного со здоровьем. После хирургической резекции, стандартного лечения пациентов с впервые диагностированной ГБМ, и при наличии хорошего показателя по шкале Карновского (≥70) проводится одновременно лучевая терапия (ЛТ) и химиотерапия (ХТ) темозоломидом с его последующим приемом в адъювантном режиме. Прогноз остается неблагоприятным даже после внедрения в общую практику сочетания ЛТ + темозоломид в 2005 г., поскольку заболевание характеризуется высоким риском возникновения рецидивов. ГБМ характеризуется избыточной экспрессией фактора роста эндотелия сосудов А (VEGF-A), ключевого регулятора опухолевого ангиогенеза; для этого типа опухолей характерна высокая васкуляризация, что делает целесообразным применение бевацизумаба – антитела, которое специфически связывается с VEGF и блокирует его активность.
Согласно данным Национального канцер-регистра Украины за 2015 г., злокачественные новообразования ГМ были диагностированы в 3,5 и 4,9 случаях на 100 тыс. населения среди женщин и мужчин соответственно. В то же время смертность от злокачественных опухолей ГМ составила 2,5 случая среди женщин и 3,3 – среди мужчин на 100 тыс. населения. Наиболее частой и наиболее злокачественной формой опухоли головного мозга является ГБМ (IV степень злокачественности согласно классификации ВОЗ), которая составляет 54% от всех глиом и характеризуется высокой летальностью. Только треть пациентов преодолевают порог 1-летней выживаемости, а менее 5% – 5-летней.
Опухоли высокой степени злокачественности диффузно инфильтрируют окружающие ткани и зачастую вовлекают в патологический процесс контралатеральную часть ГМ. Хотя ГБМ представляет собой инвазивную опухоль с высокой склонностью клеток к миграции, для этого типа опухоли не характерно распространение за пределы ЦНС, а отдаленные метастазы практически отсутствуют [1].
Патологический процесс может долгое время протекать бессимптомно. Первыми признаками заболевания могут быть симптомы, связанные с повышенным внутричерепным давлением (ВЧД), судороги или локальная неврологическая симптоматика, которые зависят от размера и локализации опухоли или зоны перифокального отека. К неспецифическим симптомам относятся головные боли распирающего характера, боли в спине, головокружение, потеря аппетита, рвота утром натощак, потеря массы тела, повышенная утомляемость, потеря концентрации, изменение поведения. Причиной этих симптомов, как правило, является сдавление внутренних структур ГМ опухолью или вследствие отека.
Очаговые проявления зависят от конкретной локализации опухоли и включают нарушения речи, зрения, изменения психической сферы, снижение памяти, невозможность совершать сложные действия. Обычно этот тип опухоли не ассоциирован с возникновением кровоизлияний или кальцификатов. В то же время, после проведения внутривенного контрастного исследования в 96% случаев усиливаются отек и давление на окружающие ткани.
Пациенты с опухолями ЦНС должны быть обследованы комплексно, с обязательной оценкой общего статуса, неврологической симптоматики, степени внутричерепной гипертензии по офтальмоскопической картине глазного дна, с проведением электроэнцефалографии и нейровизуализации. Общий статус оценивается по шкале Карновского. Диагноз супратенториальной ГБМ устанавливается на основании данных нейровизуализации – МРТ в трех режимах (Т1, Т2 и FLAIR) или КТ.
В основе постановки диагноза лежит визуализация ГМ, оптимальным является проведение магнитно-резонансной томографии (МРТ). Спинной мозг и цереброспинальная жидкость (ЦСЖ) обычно не оцениваются при отсутствии клинических симптомов. Изучение тканей – обязательная процедура, которая обычно проводится путем стереотаксической биопсии или после резекции опухоли. Молекулярные маркеры являются полезными дополнительными инструментами в диагностике и лечении и приобретают все большее значение в повседневной практике.
Степень резекции опухоли и явления остаточного заболевания следует оценивать после операции. В послеоперационном периоде обязательно выполнение КТ с контрастированием и без такового, а также выполнение МРТ без контрастного усиления и с таковым, однако эта оценка должна проводиться в течение 24-48 ч, чтобы отличить усиление контраста после оперативного вмешательства от остаточной опухоли. Благоприятными прогностическими факторами являются радикальная резекция опухоли, возраст <50 лет, более высокий функциональный статус и ненарушенная неврологическая функция. Определение молекулярных маркеров позволяет идентифицировать пациентов с более благоприятным прогнозом или более высокой вероятностью ответа на химиотерапию алкилирующими агентами [2].
К основным методам лечения ГБМ относятся хирургическое вмешательство, ЛТ, ХТ и системная терапия.
Хирургическое лечение
Оперативное вмешательство проводится с целью верификации диагноза, уменьшения симптомов, связанных с повышенным ВЧД и компрессией окружающих тканей, увеличения выживаемости и уменьшения потребности в кортикостероидах. Выполняется полная резекция, что обеспечивает более длительную выживаемость, в особенности у пациентов с хорошим функциональным статусом. Показания к хирургическому лечению зависят от возраста пациента, его общего статуса, а также анатомического расположения самой опухоли и ее хирургической доступности. К сожалению, инфильтративная природа высокозлокачественных астроцитом часто усложняет проведение тотальной резекции. При проведении операции должен сводиться к минимуму риск функциональных осложнений и снижения качества жизни пациентов.
Практически всегда после хирургического лечения происходит рецидив заболевания. У некоторых пациентов проведение повторной резекции может улучшить исход. Согласно анализу, проведенному Park и соавт., расположение опухоли в критически важных функциональных зонах ГМ, большой объем опухоли, а также низкий функциональный статус по шкале Карновского ассоциированы с неблагоприятными исходами при проведении повторной резекции.
Лучевая терапия
Дистанционная фракционированная ЛТ (ДФЛТ) является стандартом адъювантной терапии у пациентов с высокозлокачественными астроцитомами. Проведение ЛТ увеличивает общую выживаемость (ОВ) практически в два раза по сравнению с лучшей поддерживающей терапией.
Стандартная суммарная очаговая доза (СОД) – 60 Гр, при этом разовая доза – 1,8-2,0 Гр. У пожилых пациентов эффективно применение меньших доз: СОД – 34 Гр, 10 фракций, СОД – 40,05 Гр, 15 фракций или СОД – 50 Гр, 20 фракций. При рецидиве возможно проведение повторной ЛТ с использованием высокоточных современных методик, таких как фракционная стереотаксическая ЛТ, у пациентов с хорошим ФС или небольшим размером опухоли.
Химиотерапия и системная терапия
Традиционно ХТ имела минимальное значение в терапии пациентов с впервые выявленной глиомой. Химиолучевая терапия стала новым стандартом у пациентов молодого и среднего возраста (при условии хорошего ФС) с анапластической олигодендроглиомой или олигоастроцитомой при наличии делеции 1р/19q. Темозоломид, препарат алкилирующего типа действия, является стандартом в терапии ГБМ у молодых пациентов с хорошим ФС. Рекомендовано проведение комбинированного химиолучевого лечения с использованием темозоломида – ежедневный прием темозоломида в течение ЛТ с последующими поддерживающими курсами ХТ темозоломидом.
Данный подход привел к увеличению ОВ в сравнении с проведением только ЛТ после удаления опухоли (14,6 против 12,2 мес). Энзим MGMT, отвечающий за репарацию ДНК, способен вызвать резистентность к алкилирующим препаратам. Высокий уровень этого энзима при ГБМ уменьшает чувствительность опухолевых клеток к действию алкилирующих агентов и ухудшает результаты терапии. Было выявлено, что при ГБМ эффективность комбинированного лечения с темозоломидом значимо выше в группе пациентов с метилированным геном-промотором MGMT, который приводит к инактивации MGMT, чем без него.
Некоторым пациентам после удаления опухоли в ГМ могут быть имплантированы биополимерные пластины, содержащие химиотерапевтический препарат. Через несколько недель эти пластины рассасываются с высвобождением лекарственного вещества, уничтожающего раковые клетки. Данная методика продемонстрировала увеличение выживаемости у пациентов с рецидивирующей ГБМ (31 против 23 недель), в результате чего Управление по контролю качества пищевых продуктов и лекарственных препаратов США (FDA) одобрило применение кармустиновых пластин для этой группы пациентов. Кроме того, в исследовании III фазы у пациентов с впервые выявленной ГБМ поддерживающая терапия кармустином в виде имплантированных пластин по сравнению с плацебо увеличила медиану ОВ с 11,2 до 13,9 мес. Данная методика демонстрировала свою эффективность через 2 и 3 года после установки, импортируемые пластины для поддерживающей терапии кармустином были одобрены в качестве начальной терапии при злокачественных глиомах.
Режим PCV (прокарбазин, ломустин, винкристин) рекомендован для использования у больных с анапластической астроцитомой, анапластической олигодендроглиомой, анапластической олигоастроцитомой в качестве ХТ после удаления опухоли и ЛТ. Данный режим может быть применен в качестве первой линии терапии, особенно при подтверждении делеции 1p/19q.
К сожалению, доступные методы лечения недостаточно эффективны, у пациентов закономерно происходит прогрессирование или рецидив заболевания. Поэтому применение новых препаратов, в частности антиангиогенного действия, является перспективным направлением.
Бевацизумаб, впервые одобренный в 2004 г. для лечения метастатического колоректального рака, стал первым антиангиогенным препаратом, широко доступным для лечения онкологических больных с распространенными формами заболевания. Сегодня этот препарат продолжает преобразовывать подход в лечении онкологических заболеваний, демонстрируя преимущества в увеличении ОВ и/или ВБП. Таким образом, антиангиогенная терапия в настоящее время стала одной из основных методик лечения рака.
В Украине бевацизумаб уже зарегистрирован для лечения колоректального рака, рака молочной железы, немелкоклеточного рака легкого, почечноклеточного рака, рака яичника, фаллопиевой трубы и первичного рака брюшины, рака шейки матки и теперь получил регистрацию для терапии ГБМ, рецидивировавшей после лечения темозоломидом.
В мае 2009 г. FDA одобрило применение бевацизумаба для лечения ГБМ, прогрессировавшей на фоне первичной терапии. Одобрение было дано на основании данных исследований BRAIN и NCI.
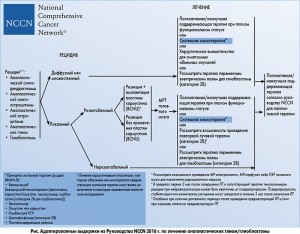
Авастин® – антитело, специфически связывающееся с VEGF и блокирующее его. Известно, что VEGF является основным фактором, запускающим ангиогенез в опухоли – процесс формирования и поддержания кровеносных сосудов, необходимых для роста и метастазирования опухоли. Таргетный механизм воздействия препарата позволяет контролировать рост и метастазирование опухоли с благоприятным профилем безопасности ХТ. В рекомендациях NCCN Авастин® одобрен в качестве монотерапии у пациентов с рецидивирующей ГБМ (рис.).
Исследование BRAIN – многоцентровое исследование II фазы с участием 167 пациентов с гистологически подтвержденной ГБМ, прогрессировавшей после первичного лечения темозоломидом и ЛТ. Основными критериями эффективности исследования BRAIN были ВБП в течение 6 мес, а также частота общего ответа – ЧОО (оценка при помощи МРТ в трех режимах – Т1, Т2 и FLAIR). Дополнительными критериями эффективности были ОВ и ВБП, продолжительность ответа на лечение и безопасность. В исследовании BRAIN оценивалось действие бевацизумаба при введении дозы 10 мг/кг каждые 2 недели в качестве монотерапии или в сочетании с иринотеканом.
У большинства пациентов, продемонстрировавших объективный ответ или ВБП в течение 24 недель, наблюдалось долговременное снижение дозы стероидов при получении бевацизумаба. В группе монотерапии бевацизумабом ЧОО составила 25,9%, а медиана продолжительности ответа – 4,2 мес. В группе монотерапии ВБП в течение 6 мес составила 42,6%, а в группе комбинированной терапии – 50,3%, в то же время медиана ОВ была выше в группе монотерапии – 9,2 vs 8,7 мес соответственно [3]. Дополнительным преимуществом стало то, что пациентам в группе бевацизумаба требовалось меньшее количество кортикостероидов, что может быть следствием улучшения контроля над опухолью (уменьшения объема опухоли), а также снижения проницаемости сосудистой сетки.
Функциональный статус по шкале Карновского ≥70 указывает, что пациент способен к самообслуживанию, но не может осуществлять нормальную деятельность или выполнять работу. Способность к самообслуживанию является важным аспектом в лечении ГБМ. Пациенты, принявшие участие в исследовании, имели исходно высокий показатель функциональной независимости (по шкале Карновского ≥70), который сохранился во время лечения и до прогрессирования [4, 5].
Первичная терапия
У пациентов с клинической и радиологической картиной ГБМ решается вопрос о проведении максимально полной и безопасной резекции. Хирургическая тактика зависит от возраста пациента и оценки по шкале Карновского, локализации опухоли, возможности уменьшения масс-эффекта с помощью агрессивной хирургической тактики, резектабельности опухоли, времени с момента последнего оперативного вмешательства у пациентов с рецидивами. Оптимальным решением является тотальная резекция опухоли. Стереотаксическая биопсия должна быть использована при затрудненном дифференциальном диагнозе, в особенности при подозрении на лимфому ГМ, а также в случаях, когда хирургическое удаление невозможно или нецелесообразно.
Если ГБМ подтверждена интраоперационным исследованием замороженных срезов, рекомендована имплантация пластины с кармустином. В случае частичной резекции обязательно проведение МРТ без контрастирования или с таковым в течение 72 ч после операции. Если максимальная резекция опухоли сопряжена с высоким риском нарастания неврологической симптоматики, т.е. фактически невозможна, необходимо выполнить стереотаксическую или открытую биопсию.
Адъювантная терапия
Дальнейшая терапия зависит от гистологической характеристики опухоли, статуса локуса 1р/19q и ФС пациента. У пациентов с ГБМ дальнейшая лечебная тактика преимущественно зависит от ФС. При высоком ФС (≥60) пациентам в возрасте <70 лет рекомендовано проведение ДФЛТ параллельно с приемом темозоломида. Пациентам в возрасте ≥70 лет рекомендовано проведение ДФЛТ в сочетании с темозоломидом (категория 2В), проведение низкодозовой ДФЛТ (категория 1) или ХТ с отстроченной ЛТ. Пациенты, которым рекомендована ХТ, должны получать темозоломид при наличии метилированного гена-промотора MGMT. Назначение ЛТ и ХТ пациентам с низким ФС по шкале Карновского (≤60) после операции осуществляется индивидуально, может быть рекомендована ДФЛТ, ХТ или паллиативная терапия.
Дальнейшее ведение пациентов и терапия при рецидиве заболевания
Пациентам назначают контрольную МРТ на 2-6-й неделе после ЛТ, а в дальнейшем каждые 2-4 мес в течение 2-3 лет. Так как ЛТ способна спровоцировать дисфункцию ГЭБ, то может возникнуть потребность в усилении терапии кортикостероидами. Раннее проведение МРТ позволяет титровать дозу кортикостероидов в зависимости от масс-эффекта или наличия отека. В дальнейшем МРТ выполняется для диагностики рецидива опухоли. Раннее выявление рецидивов важно, так как существуют различные варианты лечения пациентов с рецидивами. Для выявления лучевого некроза или псевдопрогрессии могут быть выполнены МРТ-перфузия, МРТ-спектроскопия или ПЭТ. Терапия в случае рецидива включает в себя проведение повторного оперативного вмешательства, ХТ, ЛТ, системной или паллиативной терапии и зависит от течения самого заболевания и ФС пациента. При локальном рецидиве возможно проведение повторной резекции с постановкой пластины с химиопрепаратом в послеоперационное ложе или без таковой. При повторной резекции или в случае неоперабельной опухоли пациентам с плохим ФС следует назначать паллиативную/наилучшую поддерживающую терапию без дальнейшего активного лечения. При высоком показателе ФС проводится системная терапия и ЛТ. У пациентов с диффузным поражением возможными опциями могут быть: лучшая поддерживающая терапия, оперативное вмешательство, системная терапия или электротерапия.
Таким образом, ГБМ является наиболее распространенной первичной опухолью ГМ и характеризуется высокой степенью летальности. Прогрессирование заболевания сопровождается нарушением нейрокогнитивной функции, снижением ФС и прогрессирующим снижением качества жизни. К основным методам лечения ГБМ относятся ЛТ, ХТ и оперативное вмешательство. Поскольку ГБМ характеризуются избыточной экспрессией VEGF-A и повышенной васкуляризацией, перспективным в терапии ГБМ является применение антител, блокирующих VEGF. В настоящее время Авастин® зарегистрирован в Украине в качестве терапии рецидивировавшей ГБМ. Данный препарат в проведенных исследованиях продемонстрировал увеличение ВБП и возможность поддержания качества жизни. Прицельный механизм воздействия бевацизумаба позволяет контролировать рост и метастазирование опухоли.
Литература
1. NCCN guidelines: Central nervous system cancers, 2016.
2. Stupp R. et al., High-Grade Malignant Glioma: ESMO Clinical Practice Guidelines, 2014.
3. Friedman H.S. et al., Bevacizumab Alone and in Combination With Irinotecan in Recurrent Glioblastoma, 2009.
4. Narita Y., Bevacizumab for glioblastoma, 2015.
Подготовили Екатерина Марушко и Катерина Котенко