10 липня, 2017
Фармакоэкономические аспекты применения различных лекарственных форм препарата Мабтера® (ритуксимаб)
Лимфомы – одно из немногих онкологических заболеваний, при которых полного излечения возможно добиться, используя высокотехнологичные лекарственные препараты и современные схемы терапии. До появления таргетных препаратов на основе моноклональных антител лишь 20% больных лимфомой имели шанс на стойкую ремиссию после лечения. Применение препаратов направленного действия позволяет достичь значительно лучших результатов – после этого пациенты живут и работают в течение 9-10 лет. Согласно данным мировой статистики, благоприятный прогноз возможен для 80% пациентов, получающих своевременное и полноценное лечение современными препаратами [3, 6].
В последние годы заболеваемость злокачественными лимфомами в Украине растет. Эти опухоли все чаще поражают людей работоспособного возраста. С учетом мирового опыта в Украине разработаны и утверждены приказом Министерства здравоохранения клинические протоколы по оказанию медицинской помощи больным с лимфомами, предусматривающие применение современных препаратов целенаправленного действия. Одним из таких препаратов является ритуксимаб, без которого трудно представить современное лечение лимфом. Ритуксимаб входит в состав схем начальной и поддерживающей терапии, может применяться в виде монотерапии и в комбинации с различными схемами химиотерапии [6].
Наряду с высокой эффективностью для ритуксимаба характерны определенные сложности с процедурой введения: необходим доступ к периферической вене; инфузия занимает длительное время (3-4 ч); процедура должна проводиться в условиях стационара в отдельном помещении, оборудованном специальными креслами или кроватями, при обязательном присутствии медицинского персонала (врача и медицинской сестры) и осуществлении мониторинга состояния больного во время и после завершения инфузии [2, 5]. Существенно упростить процедуру введения ритуксимаба позволяет новая лекарственная форма инновационного препарата Мабтера® для подкожного (п/к) введения. В ходе рандомизированных клинических исследований (РКИ) доказаны равные клинические эффективность и безопасность его различных (п/к и внутривенных – в/в) лекарственных форм [9-12]. Учитывая то, что Мабтера® – препарат дорогостоящий, актуальным является анализ экономической целесообразности применения его п/к лекарственной формы в условиях украинского фармацевтического рынка, который и был положен в основу исследования.
Материал и методы
Проведена фармакоэкономическая оценка полихимиотерапии (ПХТ) с добавлением ритуксимаба (схема R-CHOP) пациентов с неходжкинскими лимфомами при применении различных лекарственных форм препарата Мабтера®. Использовались методы «общая стоимость заболевания», «минимизация затрат» и «влияние на бюджет». Метод минимизации затрат (costminimization analysis – СМА) применяется при доказанной равной клинической эффективности и безопасности альтернативных лекарственных препаратов (ЛП), сравнивает стоимость их эквивалентных доз и позволяет выбрать наиболее дешевый ЛП [7, 13]. Общая стоимость заболевания (cost of illness) – метод, который учитывает все затраты, связанные с процессом применения определенного ЛП (лечения пациента с определенным заболеванием). В расчет принимались затраты на соответствующую лекарственную форму препарата Мабтера®, другие ЛП, входящие в схему ПХТ, услуги медицинского персонала, пребывание в стационаре. Анализ влияния на бюджет (budget impact analysis – BIA) позволяет определить, сколько средств государственного (регионального) бюджета может быть сэкономлено (или дополнительно потрачено) при замене одного ЛП на другой. При проведении расчетов стоимость ЛП Мабтера® принималась в соответствии с задекларированными ценами, других ЛП – с оптовыми ценами дистрибьютора «БаДМ» по состоянию на 22.03.2017 [2].
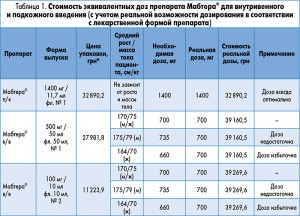
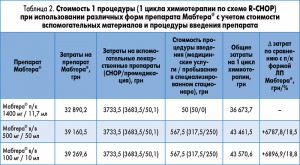
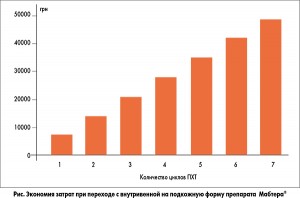
На первом этапе анализа была рассчитана стоимость эквивалентных доз препарата Мабтера® для обеих лекарственных форм. Согласно инструкции, дозирование в/в лекарственной формы зависит от площади поверхности тела (ППТ) и составляет 375 мг/м2. Средняя масса тела и рост пациентов принимались в соответствии с данными Госкомстата Украины о среднем росте и массе тела взрослого населения. Мабтера® для в/в введения на фармацевтическом рынке представлена в двух дозировках – 100 мг / 10 мл и 500 мг / 50 мл. Соответственно, реальная одноразовая доза, которая может быть введена пациенту, составляет 500-600-700 мг. С учетом этого не всегда возможно ввести дозу, необходимую конкретному пациенту в соответствии с его индивидуальными антропометрическими данными. Мабтера® для п/к введения вводится в фиксированной дозе – 1400 мг [2], что является одним из преимуществ данной лекарственной формы. Результаты расчетов, представленные в таблице 1, убедительно свидетельствуют об экономических преимуществах п/к лекарственной формы. Эти преимущества становятся еще более очевидными, если учитывать затраты на медицинские услуги, связанные с процедурой введения препарата (табл. 2). Замена в/в формы ЛП Мабтера® на п/к позволяет уменьшить затраты при проведении одного цикла ПХТ почти на 7 тыс. грн. В зависимости от клинической ситуации количество циклов ПХТ пациентов с лимфомами может варьировать от 1 до 8 (при первом введении используется только в/в форма препарата Мабтера®), при этом с увеличением количества циклов экономия затрат на ПХТ будет возрастать (рис.).
На заключительном этапе исследования для проведения анализа влияния на бюджет использовались данные о применении ритуксимаба (препарат Мабтера®) у пациентов с В-клеточными неходжкинскими лимфомами, прошедших курс ПХТ в Национальном институте рака (г. Киев) в 2000-2010 гг. [8]. Всего таких больных было 110 человек. Они получили от 1 до 8 курсов ПХТ с использованием ритуксимаба (медиана – 4,2 курса). Для этой когорты пациентов экономия денежных средств при замене в/в формы препарата Мабтера® на п/к составит 3 186 368 грн. На основании полученных данных был рассчитан показатель упущенных возможностей, который позволяет оценить, на сколько больше пациентов можно обеспечить лечением при одних и тех же затратах в случае применения менее затратной технологии. При расчете использовалась формула:
Q = CMR/DC2,
где Q – показатель упущенных возможностей, CMR – разница затрат при применении альтернативных технологий, DC2 – затраты при применении более бюджетной медицинской технологии [7].
Показатель упущенных возможностей составил 97. Это означает, что при переводе анализируемой когорты пациентов с в/в на п/к лекарственную форму ЛП Мабтера® в рамках выделенных средств можно провести 97 дополнительных циклов ПХТ.
Важно отметить, что п/к лекарственная форма применяется в фиксированной дозе, а при использовании препарата Мабтера® для в/в введения доза зависит от площади поверхности тела больного. В связи с этим зачастую некоторое количество препарата остается не использованным ввиду нарушения стерильности лекарственной формы, либо, наоборот, доза, которая вводится пациенту, несколько меньше необходимой, что может влиять на эффективность.
При использовании ЛП Мабтера® для п/к введения заметно сокращается время, которое медицинский сотрудник должен уделить пациенту, так как процедура п/к введения по инструкции предполагает 5 мин, а в/в введение препарата рассчитано на 3-4 ч. Также значительно снижается время пребывания пациента в лечебно-профилактическом учреждении (ЛПУ), что влияет на качество его жизни и величину затрат на проведение ПХТ. Результаты международного исследования (5 стран) показали, что при переводе с в/в на п/к форму препарата Мабтера® время, проведенное пациентом в ЛПУ, сокращается на 65-95%, что можно использовать для увеличения числа пролеченных в ЛПУ пациентов. Время, затрачиваемое медперсоналом на введение ритуксимаба (препарата Мабтера®), уменьшается на 37-65%. Это время может быть использовано для медицинского ухода за другими пациентами или другой работы [14, 15].
Фармацевтический рынок находится в постоянной динамике, и цены на препараты могут существенно изменяться. Для оценки устойчивости полученных результатов об экономической целесообразности п/к формы препарата Мабтера® был проведен анализ чувствительности, в котором оценивались затраты на эквивалентные дозы лекарственных форм для в/в и п/к введения при разнонаправленном изменении цен препарата Мабтера® (удешевлении более дорогого и подорожании более дешевого). Анализ чувствительности показал, что полученный результат является устойчивым к колебаниям стоимости препарата Мабтера® – удешевлению лекарственных форм для в/в введения и удорожанию формы для п/к введения в пределах 3-5-8%.
Таким образом, проведенный фармакоэкономический анализ показал следующее.
1. Ритуксимаб (Мабтера®) в лекарственной форме для п/к введения обладает равными клиническими эффективностью и переносимостью с лекарственной формой для в/в введения.
2. Применение ритуксимаба (препарата Мабтера®) в лекарственной форме для п/к введения позволяет упростить процедуру ПХТ, избежать потери препарата вследствие индивидуального подбора дозы с учетом ППТ (нет необходимости утилизировать неиспользованный препарат, оставшийся во флаконе), существенно сократить время пребывания больного в специализированном стационаре при проведении химиотерапии, сэкономить рабочее время врача и медсестры.
3. Наряду с клиническими преимуществами в современных условиях фармацевтического рынка Украины применение ритуксимаба (препарат Мабтера®) в лекарственной форме для п/к введения является экономически целесообразным, позволяя сэкономить до 19% от затрат при каждом введении.
Литература
1. Еженедельник «Аптека» [Электронный ресурс] – режим доступа к сайту: http://www.apteka.ua/cenyna-lekarstvennye-sredstva-i-izdeliya-mednaznacheniya
2. Інструкція для медичного застосування препа- рату Мабтера®. Реєстраційне посвідчення № ИА/14231/01/01.
3. Новак В. Лімфома: успішне лікування мож- ливе при своєчасному виявленні // Укр. мед. часопис. – 2013, 17 вересня [Електронна публі- кація] www.umj.com.ua
4. Прейскурант на медицинские услуги. Сестринские процедуры. [Электронный ресурс] – режим доступа к сайту: http://zds.com.ua/medicine/prices
5. Тумян Г.С. Ритуксимаб (Мабтера®) для подкожного введения – новые возможности хорошо изученного препарата // Клиническая онкогематология. – 2014. – № 1. – С. 67-70.
6. Уніфікований клінічний протокол первинної, вторинної (спеціалізованої), третинної (високо- спеціалізованої) медичної допомоги. Неходжкінські лімфоми та лімфома Ходжкіна. Наказ Міністерства охорони здоров’я України від 8 жовтня 2013 р. № 866.
7. Фармакоекономіка / Л.В. Яковлєва, Н.В. Бездітко, О.Я. Міщенко та ін. – Вінниця: Нова Книга, 2009. – 208 с.
8. Эффективность терапии пациентов с неходжкин- скими лимфомами с использованием препарата ритуксимаб / И.А. Крячок, К.С. Филоненко, А.А. Губарева и др. // Клиническая онкология. – 2011. – № 3. – С. 81-84.
9. A Two-Stage Phase Ib Study to Investigate the Pharmacokinetics, Safety and Tolerability of Subcutaneous Rituximab In Patients with Follicular Lymphoma as Part of Maintenance Treatment / A. Salar, R. Bouabdallah, C. McIntyre et al. // Blood. – 2010. – Vol. 116. – P. 2858.
10. Comparison of Subcutaneous Versus Intravenous Administration of Rituximab As Maintenance Treatment for Follicular Lymphoma: Results From a Two-Stage, Phase IB Study / A. Salar, R. Bouabdallah, C. McIntyre et al. // Journal of Clinical Oncology. – 2014. – Vol. 32, № 17. – P. 1782-1791.
11. Davies A., Merli F., Mihaljevik B. et al. Pharmacokinetics and safety of subcutaneous Rituximab in follicular lymphoma (SABRINA): stage 1 analysis of a randomised phase 3 study // Lancet Oncol. Published Online February 10, 2014.
12. Pharmacokinetics (PK), Safety and Overall Response Rate (ORR) Achieved with Subcutaneous (SC) Administration of Rituximab in Combination with Chemotherapy Were Comparable to Those Achieved with Intravenous (IV) Administration in Patients (pts) with Follicular Lymphoma (FL) in the First-Line Setting: Stage 1 Results of the Phase III SABRINA Study (BO22334) / A. Davies, F. Merli, B. Mihaljevik et al. // Blood Nov. – 2012. – Vol. 120(21). – P. 1629.
13. Rascati К. Essentials of Pharmacoeconomics – Lippincott Williams & Wilkins. – 2013. – 310 р.
14. Rituximab for subcutaneous delivery: Clinical management principles from a nursing perspective / J. Carlson, K. Bedwell, K. Cox, M. Ku // International Journal of Nursing Practice. – 2015. – Vol. 21(S3). – P. 1-13.
15. Time Savings with Rituximab Subcutaneous Injection versus Rituximab Intravenous Infusion: A Time and Motion Study in Eight Countries / E. De Cock, P. Kritikou, M. Sandoval et al. // PLOS ONE. – 2016. – Vol. 11(6).