2 липня, 2017
Влияние вортиоксетина на когнитивные функции пациентов с большим депрессивным расстройством: метаанализ трех рандомизированных контролированных исследований
Введение
Лица с большим депрессивным расстройством (БДР) часто испытывают затруднения в реализации исполнительных функций, обработке информации, концентрации внимания, обучении, отмечают ухудшение памяти. Когнитивный дефицит становится основной причиной их социальной, функциональной и трудовой дезадаптации, даже после того как симптомы депрессии убывают. Среди работающих взрослых с БДР признаки когнитивной дисфункции могут в большей степени определять количество дней нетрудоспособности, чем общая оценка тяжести депрессии. В сфере общественного здравоохранения снижение исполнительности и внимания, замедление обработки информации и принятия решений отражаются в повышении риска дорожно-транспортных происшествий, падений, ошибок при приеме лекарств. Разработка вмешательств, направленных на улучшение когнитивного функционирования лиц с БДР, может улучшить психосоциальные исходы и, возможно, повысить трудоспособность и общественную безопасность, а также сократить расходы на здравоохранение и непрямые убытки.
Несмотря на обширный и пополняющийся арсенал антидепрессантов, средства фармакотерапии, которые улучшали бы дефицит когнитивных функций, остаются неудовлетворенной клинической потребностью. В последние годы инновационный мультимодальный антидепрессант вортиоксетин показал способность улучшать когнитивные функции в экспериментальных исследованиях и у пациентов с БДР. Предполагается, что этот эффект связан со множественными рецепторными взаимодействиями вортиоксетина. In vitro вортиоксетин ингибирует транспортер серотонина (5-HT), действует как агонист серотониновых рецепторов подтипа 5-HT1A, частичный агонист 5-HT1B и антагонист рецепторов 5-HT3, 5-HT7 и 5-HT1D. Фармакодинамические механизмы, посредством которых вортиоксетин влияет на когнитивную дисфункцию у пациентов с БДР, предположительно заключаются в усилении глутаматной нейротрансмиссии (через ингибирование ГАМК-эргических интернейронов, экспрессирующих на своей поверхности гетерорецепторы 5-HT3) и регуляции процессов нейропластичности в областях мозга, ответственных за когнитивные функции, таких как гиппокамп и префронтальная кора. Другие механизмы, гипотетически причастные к прокогнитивным эффектам вортиоксетина на животных моделях, включают прямые и/или непрямые влияния через серотонинергическую, норадренергическую, холинергическую, дофаминергичекую и гистаминергическую системы.
Уникальный фармакологический профиль вортиоксетина позволил предположить, что лечение пациентов с БДР этим препаратом принесет существенную пользу в отношении когнитивной дисфункции. Поскольку такая дисфункция в большей мере выражена у пожилых пациентов с БДР, чем у молодых, эта гипотеза изначально была проверена в контролированном исследовании с участием пациентов ≥65 лет и с дулоксетином в качестве препарата сравнения. В этом исследовании когнитивное функционирование оценивали в качестве вторичной конечной точки (первичной служили симптомы депрессии) с использованием двух объективных нейропсихологических тестов. Тест замены цифровых символов (Digit Symbol Substitution Test – DSST) требует интегрирования исполнительной функции, скорости обработки, внимания, пространственного восприятия и визуального сканирования. Слуховой вербальный тест обучения Рея (Rey Auditory Verbal Learning Test – RAVLT) позволяет оценить краткосрочную слуховую вербальную память, различные аспекты научения и воспроизведения информации. Исследование с пожилыми пациентами показало, что и вортиоксетин, и дулоксетин улучшают депрессивные симптомы и результаты RAVLT, однако только вортиоксетин улучшал результаты DSST. С учетом этих данных были спланированы два больших, адекватно контролированных исследования со схожими дизайнами, в которых использовали батарею объективных когнитивных тестов, а в одном из исследований – активный контроль, с участием взрослых пациентов моложе 65 лет с БДР. Оба исследования продемонстрировали достоверное улучшение когнитивного функционирования по результатам DSST (количество правильных символов), который служил первичной конечной точкой в одном исследовании и компонентом комбинированной конечной точки – в другом.
В настоящий момент проведено много исследований по изучению эффектов различных антидепрессантов в отношении когнитивного функционирования, однако не во всех применялись поправки на другие аспекты БДР, которые могли повлиять на когнитивные функции, такие как психиатрическая и/или соматическая коморбидность.
Данный метаанализ основывается на результатах трех рандомизированных двойных слепых плацебо-контролированных исследований адекватной мощности со схожими дизайнами, в которых изучали эффекты вортиоксетина у пациентов с БДР.
Материалы и методы
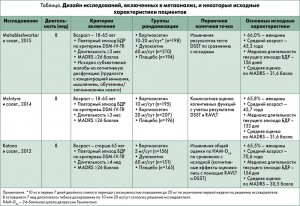
В исследования включали пациентов, которые отвечали критериям постановки диагноза повторного эпизода БДР согласно Руководству по диагностике и статистическому учету психических расстройств Американской психиатрической ассоциации (DSM-IV-TR – четвертое пересмотренное издание, 2000) и получили общую оценку ≥26 баллов по шкале депрессии Монтгомери-Асберг (MADRS) на скрининговом и исходном визитах.
Вортиоксетин применяли в дозах 5-20 мг/сут. В двух исследованиях для активного сравнения набирали группу пациентов, которым назначали дулоксетин в дозе 60 мг/сут. Во всех исследованиях было запланировано оценивание когнитивных функций с применением DSST. Этот тест считается подходящим, поскольку требует участия когнитивных доменов, которые в наибольшей мере страдают при БДР (таких как исполнительность, скорость обработки и внимание), и позволяет обнаружить изменения, если лечение эффективно.
Кроме DSST, применялись и другие когнитивные тесты для составления более полной картины влияния вортиоксетина на различные домены когнитивных функций при БДР, хотя эти данные не включались в метаанализ.
Изменения по DSST через 8 нед терапии по сравнению с исходными данными анализировали как первичный критерий эффективности вортиоксетина в отношении когнитивной дисфункции. Применялся метод пат-анализа (path analysis) для учета влияния сопутствующих изменений симптомов депрессии по шкале MADRS на результаты когнитивных тестов, так как известно, что улучшение некоторых симптомов (например, энергичность, концентрация внимания) в результате терапии антидепрессантами косвенно улучшает и когнитивное функционирование, затрудняя оценку прямого эффекта фармакотерапии.
Результаты
Характеристики 1657 рандомизированных пациентов с повторным эпизодом БДР представлены в таблице. Большинство составляли женщины, средний возраст – 45 лет в двух исследованиях и 70 лет в третьем исследовании.
Эффекты вортиоксетина в отношении когнитивных функций: данные без поправки на изменения по шкале MADRS
Результаты DSST у пациентов, которые принимали вортиоксетин, отличались в лучшую сторону от результатов в группах плацебо для всех применявшихся дозировок препарата (5, 10, 20 мг) и во всех трех исследованиях. Стандартизованный размер эффекта (SES) варьировал от 0,25 до 0,48 с номинальными р-значениями <0,05.
Вортиоксетин улучшал результаты практически всех остальных когнитивных тестов по сравнению с плацебо согласно данным двух исследований:
– приобретение навыков и отсроченное воспроизведение в тесте RAVLT в исследованиях Katona и соавт. и McIntyre и соавт.;
– результаты тестов последовательных соединений Trail Making Test, части A и B (TMT-A, TMT-B), оценивающих скорость обработки информации и исполнительную функцию, в исследовании McIntyre и соавт.;
– результаты цветного теста Струпа, простого теста на время реакции (SRT), теста на время выбора (CRT) в исследовании McIntyre и соавт.
В исследовании Mahableshwarkar и соавт. также наблюдалось улучшение результатов TMT-A, TMT-B и теста Струпа (RAVLT не применялся).
Метаанализ данных трех исследований показал, что вортиоксетин достоверно улучшает выполнение теста DSST по сравнению с плацебо: SES 0,35; 95% доверительный интервал (ДИ) от 0,19 до 0,50; p<0,0001. Отдельный метаанализ данных двух исследований с группами дулоксетина также показал статистически достоверное отличие результатов DSST на фоне приема вортиоксетина по сравнению с плацебо: SES 0,26; 95% ДИ от 0,10 до 0,41; р=0,001.
В то же время терапия дулоксетином не улучшала результаты DSST по сравнению с плацебо ни в каждом из исследований, ни в метаанализе (SES 0,13; 95% ДИ от 0,03 до 0,28; p=0,10).
Эффекты вортиоксетина в отношении когнитивных функций: данные с поправкой на изменения по шкале MADRS
Среднее уменьшение тяжести депрессивных симптомов, оцениваемой как средний балл по шкале MADRS на 8-й неделе лечения (вортиоксетин – 14,8-17,6 балла; дулоксетин – 15,8-19,2 балла), было достоверно больше в обеих группах активной терапии по сравнению с группой плацебо во всех трех исследованиях (разница на вортиоксетине по сравнению с плацебо – 2,3-6,7 балла; разница на дулоксетине по сравнению с плацебо – 3,3-7,6 балла; все р<0,05).
После введения поправки на изменения средних общих оценок MADRS улучшение результатов DSST в группе вортиоксетина по сравнению с плацебо оставалось достоверным согласно данным одного исследования. В двух других исследованиях наблюдали похожую, хотя и не достоверную, тенденцию. Как и ожидалось, в группах дулоксетина улучшение DSST утратило достоверность после введения поправки на изменения по MADRS.
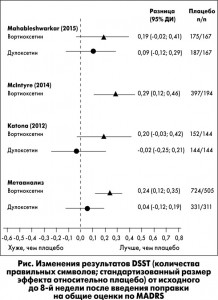
Метаанализ трех исследований показал, что различия между вортиоксетином и плацебо в отношении влияния на выполнение DSST остались достоверными, после того как результаты DSST скорректировали по изменениям MADRS: SES 0,24; 95% ДИ от 0,12 до 0,35; р<0,0001 (рис.). Подобным образом, метаанализ двух исследований с дулоксетином в качестве контроля подтвердил статистически достоверную разницу между результатами в группах вортиоксетина и плацебо после введения поправки на оценки по MADRS: SES 0,19; 95% ДИ от 0,04 до 0,35; р=0,01). При этом результаты в группах дулоксетина и плацебо не различались: SES 0,04; 95% ДИ от 0,12 до 0,19; р=0,62 (рис.).
Сравнение вортиоксетина с дулоксетином выявило статистически достоверную разницу результатов DSST в пользу вортиоксетина после введения поправки на изменения по MADRS: SES вортиоксетина по сравнению с дулоксетином = 0,16; 95% ДИ от 0,004 до 0,310; р=0,04.
Обсуждение
В этом метаанализе по данным трех рандомизированных двойных слепых плацебо-контролированных 8-недельных исследований адекватной мощности со схожими дизайнами терапия вортиоксетином в дозах 5-20 мг/сут ассоциировалась с достоверными улучшениями когнитивных функций по сравнению с плацебо, на что указывало улучшение результатов тестирования по DSST. Эти эффекты не зависели от благоприятного влияния вортиоксетина на симптомы депрессии; различия с группами плацебо оставались достоверными после поправки на изменения по шкале MADRS.
Подобным образом, метаанализ данных двух исследований с группами вортиоксетина и дулоксетина до и после коррекции на убывание симптомов депрессии обнаружил статистически достоверное улучшение результатов DSST по сравнению с плацебо на фоне приема вортиоксетина, но не дулоксетина. Более того, получены статистически достоверные различия результатов DSST в пользу вортиоксетина при сравнении с дулоксетином, даже после введения поправки на изменения по шкале MADRS.
Это первый метаанализ с достаточной статистической мощностью и строгой методологией, который убедительно доказал независимые эффекты вортиоксетина в отношении когнитивных функций у пациентов с БДР, и вортиоксетин – единственный антидепрессант с доказательствами таких эффектов.
При оценке основного исхода обращают на себя внимание постоянство и магнитуда стандартизованного размера эффекта вортиоксетина по сравнению с плацебо в отношении результатов когнитивных тестов как в отдельных исследованиях (SES 0,25-0,48), так и по данным метаанализа (SES 0,35). Это указывает на то, что клиническая значимость свойства вортиоксетина улучшать когнитивные функции выражена в степени от малой до умеренной. Практическая ценность результатов становится более ясной, если учесть, что размер эффекта вортиоксетина примерно соответствует размеру когнитивного дефицита (измеренному с помощью DSST и других тестов) у пациентов с БДР по сравнению со здоровыми добровольцами, для которого получены SES в пределах 0,2-0,7 согласно данным ранее опубликованных метаанализов. Предполагается, что полученная магнитуда когнитивного снижения оказывает выраженное негативное влияние на трудовую и учебную деятельность пациентов.
Необходимы дальнейшие исследования, чтобы детально охарактеризовать когнитивные эффекты вортиоксетина и выделить подгруппы пациентов (по возрасту, полу, генотипу), которые могут получить наибольшую пользу от этих эффектов. Кроме того, понадобится более длительное наблюдение за пациентами, чтобы лучше понять, как лечение когнитивной дисфункции влияет на долгосрочные исходы БДР, такие как функциональное восстановление, развитие деменции или других когнитивных расстройств. Дополнительные исследования также нужны для прояснения молекулярных механизмов, лежащих в основе когнитивных эффектов вортиоксетина при БДР, которые в настоящее время раскрыты лишь частично, но могут быть связаны с мультимодальными механизмами действия этого препарата. В исследованиях на животных моделях обнаружено увеличение активности пирамидных нейронов в медиальной префронтальной коре и усиление долговременной потенциации в гиппокампе.
В заключение следует отметить, что согласно данным метаанализа трех рандомизированных контролированных исследований у пациентов с БДР вортиоксетин отчетливо и достоверно улучшал когнитивные функции, которые оценивались в тесте DSST, как до, так и после введения поправки на убывание симптомов депрессии под влиянием терапии. Улучшения результатов когнитивного тестирования, полученные на терапии вортиоксетином, не наблюдались на терапии дулоксетином. Эти результаты подкрепляются рядом дополнительных когнитивных тестов, которые применялись в исследованиях, и подтверждают прямое положительное влияние вортиоксетина на когнитивное функционирование пациентов с БДР, не зависящее от его антидепрессивного эффекта. Таким образом, вортиоксетин может стать важной терапевтической опцией для пациентов с БДР и когнитивной дисфункцией.
Список литературы находится в редакции.
Сокращенный перевод с англ. Дмитрия Молчанова