6 серпня, 2017
Новий фенотипспецифічний підхід до ведення бронхіальної астми

Бронхіальна астма (БА) є одним з найпоширеніших хронічних захворювань людини, яке характеризується гетерогенністю клінічних форм і варіабельністю перебігу. На сучасному етапі ведення БА потребує глибокого аналізу факторів, відповідальних за прогресування захворювання і розвиток загострень, а також вибору терапії БА на основі клінічних і біологічних фенотипів хвороби. На сьогодні в більшості пацієнтів з БА є можливість проводити терапію з врахуванням фенотипу захворювання, біологічних маркерів запалення дихальних шляхів, визначення яких є важливим завданням лікаря-спеціаліста.
Зазвичай пацієнти з БА в першу чергу звертаються до сімейного лікаря чи терапевта. Останнім обрати правильний та успішний шлях діагностичних і терапевтичних процедур у багатьох випадках складно, незважаючи на настанови, протоколи та рекомендації. Наказ МОЗ України від 29.12.2016 № 1422 забезпечує можливість використання не лише вітчизняних протоколів, а й документів, розроблених національними
та/або фаховими медичними асоціаціями країн – членів Європейського Союзу (членство визначається станом на 1 січня 2017 р.), США, Канади та Австралійського Союзу. Метою такого кроку є пришвидшене впровадження принципів доказової медицини в сучасну медичну практику та використання світового досвіду у сфері охорони здоров’я.
Згадуючи історію впровадження практичних рекомендацій щодо ведення БА, слід зазначити, що Глобальна ініціатива боротьби з астмою (Global Strategy for Asthma Management and Prevention, GINA), яка вперше опублікована як спільна доповідь Всесвітньої організації охорони здоров’я та Інституту серця, легенів та крові (США) у 1995 р., і сьогодні залишається основним стратегічним документом, присвяченим даній патології. За рекомендаціями GINA слідкують лікарі та вчені всього світу. Починаючи з 2006 р. настанови щорічно оновлюються. У лютому 2017 р. опублікована їх оновлена версія. Цей документ створено науковою групою міжнародних експертів GINA на підставі останніх публікацій та результатів досліджень. До настанов внесена низка змін, найважливішими серед яких є:
- виокремлення терміну «БА-ХОЗЛ-оверлап» (видалено слово «синдром» з поняття «БА-ХОЗЛ-оверлап-синдром» (asthma-COPD overlap syndrome, ACOS) з метою привернути увагу дослідників до проблеми коморбідності БА та ХОЗЛ (хронічне обструктивне захворювання легень) з подальшим уточненням механізмів такого поєднання та удосконаленням методів лікування);
- оптимізація частоти досліджень легеневої функції залежно від категорій пацієнтів (враховується вік, ризик прискореного погіршення функціональних показників);
- переоцінка значення фракції оксиду азоту в повітрі, що видихається (FeNO);
- доповнення покрокового лікування БА: на кроці 5 шляхом додавання до терапії середніми/високими дозами інгаляційних кортикостероїдів (ІКС) в поєднанні з тривалодіючими ββ2-агоністами (ТДБА) не лише тіотропію чи анти-IgE препарату, а й меполізумабу чи реслізумабу (антитіла до інтерлейкіну-5); доцільність застосування антагоністів лейкотрієнових рецепторів (АЛТР) при step-down терапії від низьких доз ІКС;
- відсутність достовірних даних щодо покращення контролю над БА чи зниження числа загострень при використанні вітаміну D;
- застосування топічних кортикостероїдів у пацієнтів із супутнім хронічним риносинуситом достовірно поліпшує назальні симптоми, але не перебіг БА.
У GINA 2017 підкреслено гетерогенність БА з виділенням найчастіших фенотипів БА.
- Алергічна БА: фенотип, який найлегше розпізнати. Часто вперше проявляється в дитинстві та асоціюється з наявністю алергічного захворювання, такого як екзема, алергічний риніт або харчова чи медикаментозна алергія в особистому і/або сімейному анамнезі. При дослідженні мокротиння до лікування часто виявляють еозинофільний тип запалення дихальних шляхів. Пацієнти з цим фенотипом БА добре реагують на лікування ІКС.
- Неалергічна БА: зустрічається в деяких дорослих осіб, не пов’язана з алергією. Цитологічний профіль мокротиння таких пацієнтів може бути нейтрофільним, еозинофільним чи малогранулоцитарним (містить мало клітин запалення). Часто пацієнти з цим фенотипом БА гірше відповідають на лікування ІКС.
- БА з пізнім початком: у деяких осіб, частіше жінок, БА розвивається в дорослому віці. Зазвичай ці пацієнти не схильні до алергії. Часто такі хворі потребують високих доз ІКС або відносно рефрактерні до терапії ІКС.
- БА з фіксованим обмеженням швидкості потоку повітря: у деяких пацієнтів з тривалим перебігом БА виникає фіксоване обмеження швидкості потоку повітря, що зумовлено ремоделюванням стінок дихальних шляхів.
- БА на тлі ожиріння: у таких пацієнтів спостерігаються виражені симптоми з боку органів дихання і незначне еозинофільне запалення дихальних шляхів.
Результати багатьох досліджень, виконаних протягом останнього десятиріччя, свідчать, що ступінь тяжкості БА не є оптимальним показником для оцінки стану хворих у повсякденній практиці, оскільки може змінюватися з часом (навіть упродовж короткого періоду), залежить не лише від клінічних проявів, але й від відповіді на терапію, не дає змоги оцінювати та прогнозувати ризик розвитку середньотяжких або тяжких (у тому числі небезпечних для життя) загострень астми. З метою визначення, як саме пацієнт може реагувати на призначену терапію, доцільно максимально точно окреслити фенотип БА. Деякі з вищевказаних фенотипів досить просто визначити в реальній клінічній практиці, але трапляються випадки, коли БА погано відповідає на класичне лікування, існує потреба в додаткових, часто високовартісних дослідженнях й особливому терапевтичному підході. Тому практичні рекомендації, запропоновані GINA, є актуальними і корисними як для лікарів первинної ланки, так і для спеціалістів вузького профілю.
Стратегії GINA ретельно вивчаються експертами та лікарями у світі, адаптуються до локальних умов країни з урахуванням особливостей її системи охорони здоров’я, економічного та освітнього рівня. Вважаємо доцільним ознайомити вітчизняних фахівців і з рекомендаціями, запропонованими нещодавно, зокрема, у Чехії.
У зв’язку зі значною гетерогенністю БА два чеських медичних товариства (Чеська спілка пульмонологів та фтизіатрів і Чеське товариство алергологів та клінічних імунологів) запросили 10 експертів для вивчення літератури та розробки рекомендацій щодо ведення БА, які б віддзеркалювали неоднорідність захворювання. Мета полягала в тому, щоб створити просту у використанні діагностичну стратегію як раціональний підхід до розширення можливостей застосування таргетної терапії БА на основі фенотипу захворювання.
Основною ознакою діагностичного підходу є прагматична концепція, яка оцінює наявність алергії та еозинофілії в кожного пацієнта з БА. Запропоновано визначати 3 клінічно значущих фенотипи БА: еозинофільну алергічну астму, еозинофільну неалергічну астму та нееозинофільну неалергічну. У підсумку отримано багатофункціональну класифікацію, яка описує ступінь тяжкості перебігу, рівень контролю та фенотип і є відправною точкою для комплексної стратегії лікування. Рівень контролю над астмою постійно зіставляється з об’ємом та інтенсивністю загальної ступеневої фармакотерапії, тому одночасне визначення фенотипу астми є дуже цінним та необхідним кроком для оптимізації лікування, що формує фенотипспецифічний персоналізований підхід до терапії.
Епідеміологія
Поширеність БА у різних регіонах світу варіює від 1 до 16%, а в країнах Європейського Союзу – від 5 до 16%. Глобальний тягар астми поступово збільшується, при цьому відмінності між регіонами і країнами скорочуються. У Чехії з населенням 10 млн поширеність БА становить 7-8% (700-800 тис. осіб). У 2014 р. приблизно 360 тис. пацієнтів (майже половина з популяції хворих на БА) спостерігалися в алергологів та пульмонологів.
Діагностика БА
Для підтвердження діагнозу БА та визначення терапії необхідні дослідження, які б відображали основні характеристики астми, – бронхіальне запалення, бронхіальну гіперреактивність (БГР) та ремоделювання дихальних шляхів. Деякі методи, що використовуються для діагностики і моніторингу астми в рутинній клінічній практиці, не оцінюють ці важливі критерії безпосередньо, а лише аналізують симптоми та характеристики, зокрема задишку, свист у грудях, зворотність та мінливість бронхіальної обструкції. Проте в складних випадках БА важливо більш точно дослідити такі патофізіологічні процеси, як запалення та БГР.
Використання декількох діагностичних методів та інтерпретація отриманих даних відрізняються в нових пацієнтів без призначеного протизапального лікування та хворих, які вже розпочали протизапальну терапію.
На фоні використання ефективного протизапального лікування еозинофільної астми найшвидше (від декількох днів до 2 тижнів) нормалізуються показники FeNO та еозинофілії мокротиння, потім спостерігається зменшення вираженості основних симптомів захворювання та нормалізація функції легень (від декількох тижнів або місяців). Залишкові ознаки запалення зникають значно пізніше (через кілька місяців), а для ослаблення БГР потрібно ще більше часу. Доказів впливу ІКС на кількість еозинофілів та концентрацію еозинофільного катіонного протеїну (EКП) в крові небагато; такі ефекти можна очікувати через 2 тижні після початку лікування.
Метою діагностичних процедур є:
- підтвердження діагнозу БА наявністю варіабельної та зворотної бронхіальної обструкції і/або БГР. Еозинофільне запалення стінки бронха може спростити встановлення діагнозу, хоча існує нееозинофільна БА;
- точніше визначення інших характеристик захворювання (класифікація за ступенем тяжкості перебігу, рівнем контролю, фенотипування (ендотипування); оцінка супутніх захворювань, що можуть ускладнити перебіг БА та її лікування. Для фенотипування астми, окрім оцінки еозинофілії, необхідно провести алергологічне й імунологічне дослідження.
Бронхіальна обструкція має три компоненти: констриктивний (відповідає на дію бронходилататорів), запальний (реагує на протизапальне лікування) та ремоделювання (персистує навіть на фоні бронходилатаційної і протизапальної терапії). Як тільки тяжкість астми зростає, пропорція та роль двох останніх компонентів суттєво збільшується. Фундаментальними при встановленні діагнозу астми є визначення вентиляційних порушень обструктивного типу, їх важкості, зворотності та варіабельності (підтвердження БГР). Ці критерії мають бути належним чином задокументовані для кожного пацієнта. Збільшення об’єму форсованого видиху за першу секунду (ОФВ1) на ≥12% і ≥200 мл при постбронходилатаційній спірометрії порівняно з початковим значенням зазвичай використовують для підтвердження діагнозу астми. Збільшення ОФВ1 на 400 мл чи 15% є ще більш вагомим. Проте багато пацієнтів з БА не відповідають цим критеріям при одному обстеженні. У таких ситуаціях рекомендовані багаторазові вимірювання в різні дні, застосування у фармакологічних тестах вищих доз чи інших бронходилататорів (стандартно використовують 400 мкг сальбутамолу через спейсер) та оцінка форми кривої потік/об’єм. Якщо все ж обструктивне вентиляційне порушення не вдається підтвердити, необхідно провести провокаційний (бронхоконстрикторний) тест (непрямий тест з манітолом чи прямий тест з метахоліном, який є менш специфічним). Якщо неможливо продемонструвати зворотність бронхообструкції, рекомендована тест-терапія (тест-«удар») кортикостероїдом. Діагноз БА є пожиттєвим.
Підтвердження еозинофільного запалення дихальних шляхів значною мірою допомагає у виявленні БА, особливо коли воно визначено перед стартом превентивного протизапального лікування. Наявність еозинофілії є маркером Th2-залежного запалення та хорошої відповіді на лікування кортикостероїдами. Якщо запалення є нееозинофільним (нейтрофільне чи «малогранулоцитарне»), то діагноз БА і відповідь на кортикостероїдне лікування є менш імовірними.
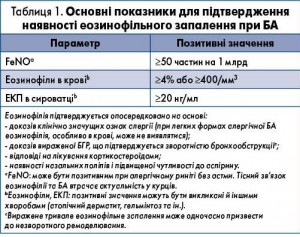 Спроба продемонструвати наявність еозинофілії дихальних шляхів повинна бути зроблена під час діагностичного процесу в кожного пацієнта з БА. Якщо це можливо, рекомендовано використання усіх трьох маркерів еозинофілії, або принаймні двох з перерахованих у таблиці 1 (переважно FeNO і один маркер, визначений у крові). При менш важкій формі БА системні ознаки еозинофілії можуть і не виявлятися (диференційний аналіз крові та ЕКП). У Чехії лікарі в клінічній практиці орієнтуються на FeNO-тестування або наявність непрямих ознак еозинофільного запалення (табл. 1). Навіть якщо актуальність, інтерпретація FeNO та бронхоконстрикторні тести не можуть вважатися рівноцінними, визначення FeNO є досить інформативним для діагностики БА. У деяких ситуаціях, коли ознаки астми є типовими і в стероїднаївного пацієнта спостерігається високе значення FeNO (>80 частин на 1 млрд), бронхоконстрикторний тест можна не проводити, навіть якщо результати оцінки функції легень не підтверджують обструктивні респіраторні порушення та зворотність бронхообструкції. FeNO також відіграє важливу діагностичну роль: його негативні та низькі значення (<25 частин на 1 млрд у нелікованих пацієнтів з негативним результатом бронхоконстрикторного тесту майже завжди виключають діагноз БА.
Спроба продемонструвати наявність еозинофілії дихальних шляхів повинна бути зроблена під час діагностичного процесу в кожного пацієнта з БА. Якщо це можливо, рекомендовано використання усіх трьох маркерів еозинофілії, або принаймні двох з перерахованих у таблиці 1 (переважно FeNO і один маркер, визначений у крові). При менш важкій формі БА системні ознаки еозинофілії можуть і не виявлятися (диференційний аналіз крові та ЕКП). У Чехії лікарі в клінічній практиці орієнтуються на FeNO-тестування або наявність непрямих ознак еозинофільного запалення (табл. 1). Навіть якщо актуальність, інтерпретація FeNO та бронхоконстрикторні тести не можуть вважатися рівноцінними, визначення FeNO є досить інформативним для діагностики БА. У деяких ситуаціях, коли ознаки астми є типовими і в стероїднаївного пацієнта спостерігається високе значення FeNO (>80 частин на 1 млрд), бронхоконстрикторний тест можна не проводити, навіть якщо результати оцінки функції легень не підтверджують обструктивні респіраторні порушення та зворотність бронхообструкції. FeNO також відіграє важливу діагностичну роль: його негативні та низькі значення (<25 частин на 1 млрд у нелікованих пацієнтів з негативним результатом бронхоконстрикторного тесту майже завжди виключають діагноз БА.
У пацієнтів, які вже отримують протизапальну терапію, необхідно докласти зусиль для оцінки FеNO та еозинофілії периферичної крові. Якщо немає змоги отримати ці результати, рекомендовано орієнтуватися на непрямі ознаки еозинофільного запалення: клінічно значущі прояви алергії, поліпоз носа, підвищена чутливість до аспірину. Якщо еозинофілія відсутня і зворотність обструкції бронхів/БГР не може бути доведена, діагноз БА сумнівний. У таких пацієнтів бажано зменшити або відмінити протизапальну терапію з повторним обстеженням на наявність еозинофілії (FеNO, кров) не швидше, ніж через 2-5 тижнів, дотримуючись інтервалу вимивання.
Тільки у випадку БА, стійкої до лікування, та за умови поганого контролю захворювання рекомендують використовувати більш специфічні тести: визначення еозинофілів у мокротинні, біопсія бронха і бронхоальвеолярний лаваж. У чеській системі охорони здоров’я ці дослідження виконуються здебільшого спеціалістами клінік Національних центрів тяжкої астми (www.tezke-astma.cz), де доступна також фенотипспецифічна терапія.
Класифікація БА
Особливістю чеських національних рекомендацій є запропонована мультифункціональна класифікація БА. Досягнутий рівень контролю постійно порівнюють з оцінкою тяжкості захворювання і його фенотипом/ендотипом. Такий підхід дозволяє розробити комплексну стратегію лікування, застосовуючи загальний поетапний алгоритм, а також розширити можливості індивідуальної фенотипспецифічної терапії. Якщо вдалося досягти повного контролю БА, доцільно прагнути до деескалації фармакотерапії (т. зв. крок униз – step down). Крім того, немає необхідності розглядати фенотипспецифічне лікування, за винятком специфічної імунотерапії (СІТ), зокрема при легких формах захворювання. І навпаки, при зростанні тяжкості астми і виникненні труднощів щодо досягнення контролю доцільно розглянути варіанти лікування, що враховують фенотип захворювання.
При забезпеченні контролю БА необхідно брати до уваги причину захворювання і такі параметри, як бронхіальне запалення, ремоделювання та БГР, а не лише вираженість клінічних проявів. Першочергове очікування хворих – контроль над симптомами, проте обов’язком фахівців є профілактика несприятливих наслідків БА, пов’язаних із залишковою активністю захворювання.
Термін «добре контрольована астма» передбачає відповідність таким критеріям:
- відсутні клінічні прояви або наявні мінімально виражені денні симптоми;
- потреба в застосуванні препаратів швидкої дії ≤2 р/ тиж;
- не спостерігається обмеження фізичної активності;
- постійна відсутність нічних порушень минулого місяця;
- у довгостроковій перспективі – тривала нормальна функція легень, відсутність загострень, побічних ефектів та несприятливих наслідків, зумовлених лікуванням.
 Терміни «добре контрольована астма», «частково контрольована» або «неконтрольована астма» не забезпечують достатнього розуміння тяжкості захворювання. Добре керована астма може бути як легкою формою захворювання, при якій необхідні лише низькі дози ІКС, так і тяжкою патологією, що потребує комбінованої терапії (ТДБА / високі дози IКС + АЛТР).
Терміни «добре контрольована астма», «частково контрольована» або «неконтрольована астма» не забезпечують достатнього розуміння тяжкості захворювання. Добре керована астма може бути як легкою формою захворювання, при якій необхідні лише низькі дози ІКС, так і тяжкою патологією, що потребує комбінованої терапії (ТДБА / високі дози IКС + АЛТР).
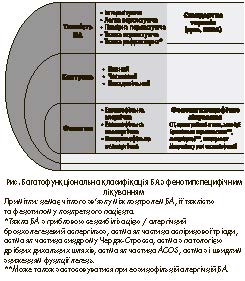
Тому чеські експерти рекомендують відповідно до п’яти етапів фармакотерапії БА зберегти п’ять ступенів тяжкості БА: інтермітуюча (І), легка персистуюча (ІІ), помірна персистуюча (ІІІ), тяжка персистуюча (ІV), тяжка рефрактерна астма (V), що відображено на рисунку.
Хоча вищезазначена оцінка тяжкості БА в клінічній практиці не є точною (реальність часто обтяжується надмірним чи недостатнім лікуванням), класифікацію за тяжкістю БА можна вважати раціональною. З огляду на збільшення можливостей специфічного лікування рекомендована фенотипічна класифікація, яка відображає наявність клінічно значущої еозинофілії та алергії (табл. 2).
Алергологічне й імунологічне обстеження рекомендовано кожному пацієнту з БА при:
- першому встановленні діагнозу;
- втраті контролю через невідомі причини.
Відправною точкою для діагностики алергії є збір анамнезу (поточні симптоми, причини алергії та аналіз аналогічних подій у минулому, оцінка позалегеневих ознак алергії, зокрема наявності атопічного маршу: харчова алергія, атопічний дерматит, сінна лихоманка, позалегеневі симптоми алергії на алергени домашніх тварин тощо). Визначення загального рівня імуноглобуліну E (IgE) має обмежене інформаційне значення, як і докази сенсибілізації (позитивні prick-тести, специфічні IgE), що не обов’язково підтверджують клінічно значущу алергію. У тяжких випадках БА необхідно проводити тестування на плісняві гриби (особливо на Alternarіа та Aspergillus). Принципи оцінки наявності еозинофілії та алергії і пов’язані з цим клінічні показники також включені до чеських національних рекомендацій з ХОЗЛ як частини великих та малих критеріїв, що використовують для діагностики ACOS. Наявність ACOS є вірогідною в пацієнтів з БА з домінуючою вираженою задишкою, хронічним відкашлюванням мокротиння, анамнезом куріння, стійкою персистуючою обструкцією після лікування із застосуванням стероїдів. Пацієнтам з ACOS рекомендовано провести комп’ютерну томографію з високою роздільною здатністю.
Еозинофільна алергічна БА
Домінуючою ознакою еозинофільної алергічної БА є наявність клінічно значущої алергії/атопії. Маніфестує захворювання, як правило, в дитинстві. Часто спостерігається коморбідність з атопічним дерматитом та іншими алергічними/атопічними захворюваннями або вони передують БА (атопічний марш). Еозинофілію в стінці бронха важко виявити, особливо після початку лікування ІКС. У випадку очевидного діагнозу БА разом з клінічно значущою алергією немає необхідності доводити бронхіальну еозинофілію. Еозинофільна алергічна БА – найпоширеніший і, як правило, найбільш сприятливий для лікування тип захворювання. Найбільш серйозні випадки спричинені грибковою сенсибілізацією: тяжка астма з грибковою сенсибілізацією (SAFS – Severe Asthma with Fungal Sensitization) або алергічний бронхолегеневий аспергільоз.
Еозинофільна неалергічна БА
Домінуючою ознакою еозинофільної неалергічної БА є наявність вираженої еозинофілії. Маніфестує захворювання, як правило, після досягнення середнього віку. Тестування на алергію зазвичай є негативним (якщо позитивне, це не має істотного клінічного значення). Еозинофілія бронхів супроводжується вираженою БГР та ризиком незворотного ремоделювання. Найтяжчі форми еозинофільної неалергічної БА часто асоціюються з назальним поліпозом та непереносимістю нестероїдних протизапальних препаратів або аутоімунними еозинофільними васкулітами (аспіринова тріада та синдром Чердж-Стросса).
Нееозинофільна неалергічна БА
При нееозинофільній неалергічній БА відсутня еозинофілія та клінічні прояви алергії, проте мають місце БГР, варіабельна бронхообструкція та типові симптоми БА. Маніфестує захворювання переважно в дорослому віці; на його тяжкість впливають ожиріння та інші коморбідні стани. Є більш поширеним варіантом серед жінок.
Лікування
Метою лікування БА є не лише елімінація поточних симптомів, а й мінімізація запалення, БГР, попередження загострення та формування незворотного ремоделювання. При цьому бажано мінімізувати фармакотерапію, враховуючи, що довготривале лікування із застосуванням препаратів у високих дозах, особливо кортикостероїдів, пов’язане зі значним ризиком системних побічних ефектів. Мають місце суперечливі погляди щодо комплексної стратегії терапії з урахуванням цих чинників. Запропонована багатофункціональна класифікація, в якій рівень досягнутого контролю постійно зіставляється з визначенням тяжкості перебігу та фенотипуванням БА.
Загальний покроковий підхід до лікування БА
Загальна поетапна стратегія лікування визнана в усьому світі. Принципи GINA включають п’ять кроків терапії. Згідно з рекомендаціями Чеської спілки пульмонологів та фтизіатрів і Чеського товариства алергологів та клінічних імунологів, вони відповідають п’яти ступеням тяжкості БА. Основним завданням є досягнення повного контролю над БА. Якщо цього не вдається забезпечити шляхом застосування низьких чи середніх доз ІКС, рекомендована комбінація з іншим протиастматичним препаратом замість збільшення дози IКС (через низьку терапевтичну користь та підвищений ризик несприятливих ефектів). Найчастіше використовують комбінацію ІКС з ТДБА. Крок 4 включає застосування тіотропію за допомогою пристрою Respimat®.
Інтенсивність мінімальної терапії, необхідної для повного контролю, визначає нинішню тяжкість захворювання. Зазвичай низькі дози ІКС використовуються на початку лікування пацієнтів, які ще не отримували контролюючу терапію. На практиці найчастіше розпочинають терапію із застосуванням ІКС (від помірних до високих доз) або комбіновану терапію, у т. ч. призначають фіксовані комбінації IКС + ТДБА. Такий підхід може бути прийнятним, особливо в пацієнтів з вираженими симптомами. Якщо досягнуто повного контролю і він підтримується щонайменше 3 місяці, потрібно докласти зусиль до поступового зменшення кількості та дози ліків. Після цього рекомендується ретельний моніторинг БА; необхідно враховувати навіть мінімальну залишкову активність захворювання. Для сезонної алергічної БА прийнятне лише сезонне превентивне лікування.
Якщо не вдається досягти контролю, перед початком посилення терапії необхідно виконати такі кроки:
- перевірити техніку інгаляцій;
- промоніторити умови побуту та праці, дотримання запобіжних заходів щодо впливу професійних алергенів та шкідливих речовин;
- забезпечити контроль супутніх захворювань (риносинусит, гастроезофагеальний рефлюкс, дисфункція голосових зв’язок та синдром обструктивного апное сну).
Останні два кроки співпадають з підходом до ведення БА, що базується на визначенні еозинофілії, оцінці алергії та використанні фенотипспецифічного лікування. Якщо повного контролю не вдається досягнути при застосуванні кроку 4, рекомендовано скерувати пацієнта до спеціалізованого центру для перегляду діагнозу, особливо в разі тривалого вживання системних кортикостероїдів.
Фенотипспецифічне лікування
Для еозинофільної алергічної БА запропоновано найбільше варіантів фенотипспецифічного лікування. Можливість СІТ слід розглядати в кожного пацієнта з БА з підтвердженою та клінічно значущою алергією, зумовленою пилковими алергенами, пиловими кліщами, алергенами котів та собак, деякими пліснявими грибами та іншими алергенами (рідко), переважно при легких формах БА. СIT не є альтернативою чи конкурентом фармакотерапії БА. Вона призначена для усунення гіперчутливості, що пов’язано з певними ризиками (виконується алергологом за умови повного контролю БА). Пацієнтів з еозинофільною БА, які не можуть досягти повного контролю навіть за допомогою лікування відповідно до кроку 4, та осіб, що мають докази/підозру щодо тяжкої рефрактерної, еозинофільної алергічної БА, рекомендовано скерувати до спеціалізованих центрів, де призначають та проводять біологічне лікування, використовуючи анти-IgE антитіла (омалізумаб) та, можливо, протигрибкову терапію (при SAFS чи алергічному бронхолегеневому аспергільозі).
У Національних центрах тяжкої астми в Чеській Республіці також здійснюють бронхіальну термопластику (БТ). Критерії включення для БT – неадекватний контроль БА при лікуванні відповідно до кроку 4, з підтвердженням значної БГР за останні 12 місяців (позитивний бронходилатаційний тест (>15% та/або >400 мл) або позитивний провокаційний тест з метахоліном на фоні превентивного лікування) як непрямих ознак гіпертрофії/гіперплазії непосмугованої мускулатури бронхів. Попередній досвід такого лікування в Чеській Республіці свідчить, що найчастіше відповідають цим критеріям пацієнти з еозинофільною неалергічною БА. У Національних центрах тяжкої астми приймається рішення щодо застосування метотрексату в пацієнтів, які щоденно потребують високих доз пероральних кортикостероїдів. Інші інноваційні продукти випробувані та продовжують вивчатися у фармакологічних дослідженнях. Меполізумаб схвалений для клінічного застосування в Чеській Республіці з 1 квітня 2016 р. У випадках нееозинофільної неалергічної БА велике значення має адекватне лікування супутніх захворювань (ожиріння, синдром обструктивного апное сну, гастроезофагеальна рефлюксна хвороба тощо). У випадку частих інфекційних загострень можна розглянути тривале лікування з використанням макролідів за інтермітуючою схемою.
Висновки
Зі зростанням рівня знань БА розглядається як захворювання гетерогенного характеру. Чеські рекомендації, що ґрунтуються на оцінці фактичного клінічного значення еозинофілії та алергії, є раціональним способом використання обох варіантів терапевтичного підходу: стандартної фармакотерапії та персоналізованої фенотипспецифічної терапії. Ознайомлення вітчизняних фахівців з останніми чеськими настановами щодо ведення БА має велике пізнавальне значення, є корисним як для сімейних лікарів, так і для спеціалістів вузького профілю.
ІКС залишаються найефективнішими препаратами для тривалого контролю БА, вони показані для лікування персистуючих симптомів захворювання. Максимальний ефект ІКС демонструють у пацієнтів з еозинофільною алергічною БА. У багатьох випадках доцільно застосовувати ІКС у низьких дозах у режимі монотерапії. Серед препаратів ІКС, представлених на українському фармацевтичному ринку, Флутіксон (флутиказону пропіонат) у двох дозуваннях (125 та 250 мкг) довів високу ефективність, зручність і технічну простоту застосування за допомогою пристрою Циклохалер.
Використання фіксованих чи вільних комбінацій ІКС/ТДБА є пріоритетною стратегією в пацієнтів, у яких не вдається досягти контролю захворювання при використанні низьких/середніх доз ІКС. Окреме застосування ІКС, зокрема флутиказону пропіонату (Флутіксону) та формотеролу (Зафірону) в широкому діапазоні доз (12-72 мкг на добу), має низку переваг у хворих з нееозинофільною неалергічною БА, яка спостерігається переважно в курців:
- гнучка модифікація дози ІКС без збільшення ТДБА;
- можливість застосування в правильній послідовності (ТДБА – 10-хвилинна перерва – ІКС).
Використання вищих доз формотеролу (Зафірону) в поєднанні з невисокими дозами ІКС доцільне для досягнення та підтримки контролю нееозинофільної БА: БА у курців, пізньої менопаузальної БА в жінок з ожирінням, в яких часто розвивається резистентність до терапії ІКС.
Антагоністи лейкотрієнових рецепторів, зокрема Мілукант, підтвердили ефективність при аспіриновій БА, БА в поєднанні з алергічним ринітом, БА курців та БА, асоційованій з ожирінням. Доцільно застосовувати АЛТР при step-down терапії від низьких доз ІКС.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 13-14 (410-411), липень 2017 р.



