17 червня, 2017
Растительный препарат BNO 1016* – безопасное и эффективное средство для лечения острого вирусного риносинусита
Острый ринит является первой стадией развития риносинусита (РС). Грань между острым и хроническим РС (ОРС и ХРС) в основном определяется продолжительностью заболевания, а не специфическими симптомами. В соответствии с терминологией, предложенной в EPOS 2012, ОРС полностью вылечивается (без остаточных симптомов) через 12 нед, тогда как при ХРС один или несколько признаков сохраняются.
Острый вирусный РС длится <10 дней, а острый поствирусный – >10 дней. В последнем случае часто наблюдается картина двухфазного течения с сохранением или ухудшением симптомов к концу 10-дневного периода.
Причиной ОРС является ряд вирусов (риновирусы, вирусы парагриппа (типы 1 и 2), коронавирус и вирусы гриппа), которые повышают концентрацию провоспалительных цитокинов и нейтрофилов [2]. Подобный тип реакции встречается при бактериальной инфекции. Таким образом, ОРС можно ошибочно классифицировать как бактериальную инфекцию и, следовательно, лечить ее антибиотиками, что не способствует на этой стадии болезни излечению.
ОРС – наиболее распространенное инфекционное заболевание, провоцирующее индивидуальный дискомфорт, обусловленный сниженным качеством жизни, и имеющее огромное социально-экономическое значение [3]. Стратегия лечения направлена на снижение тяжести симптомов, сокращение продолжительности заболевания и предотвращение осложнений, а также хронизации воспалительного процесса.
В последние годы предложен новый способ лечения ОРС – фитотерапевтические препараты [4-6]. BNO 1016 («Бионорика СE», Германия) – новый препарат на основе сухого экстракта фиксированной комбинации пяти растительных препаратов, содержащей корень горечавки (Gentianae radix), цветки первоцвета (Primula flos), траву щавеля (Rumicis herba), цветки бузины черной (Sambuci f los) и траву вербены (Verbenae herba) в соотношении 1:3:3:3:3. Препарат является стандартизированным высокодозированным средством для лечения ОРС. Фармакологические исследования показали (in vitro и на животных моделях), что BNO 1016 обладает противомикробным и противовирусным эффектами, включая секретолитическую и противовоспалительную активности [6]. В исследовании фазы IIb/III – ARhiSi1 – документально зафиксирована эффективность и безопасность BNO 1016 при приеме в суточной дозе 160 мг 3 р/сут курсом 15 дней [7]. Это было подтверждено в исследовании фазы III – ARhiSi2 [8].
Чтобы подтвердить эффективность лечения на большей популяции пациентов, в ходе настоящей оценки были объединены данные исследований фазы IIb/III (ARhiSi1) и III (ARhiSi2). В испытаниях участвовали 589 пациентов, у которых сравнивали эффективность приема BNO 1016 в дозе 480 мг в день (160 мг 3 р/сут) с плацебо при лечении ОРС.
Материалы и методы
Пациенты
Для изучения объединенных данных применяли критерии включения в исследование ARhiSi2. Для анализа использовали данные взрослых амбулаторных пациентов (мужчин и женщин) в возрасте от 18 до 75 лет с клиническим диагнозом ОРС (МКБ10: J01.9), подтвержденным ультразвуковым исследованием (УЗИ) верхнечелюстных пазух. ОРС определялся как внезапное появление по крайней мере трех основных симптомов (насморк/ выделения из передних отделов носа, стекание слизи по задней стенке глотки, заложенность носа, головная боль, лицевая боль / ощущение тяжести). Для включения в исследование патологические признаки должны были сохраняться в течение ≤3 дней. К критериям включения относилось проверенное исследователем значение MSS ≥8 и ≤12 баллов (из возможных 15). Кроме того, должны были присутствовать заложенность носа и легкая/умеренная лицевая боль или ощущение тяжести (≥1 балл и ≤2 балла).
Из анализа исключались больные, принимавшие кортикостероиды или антибиотики (локально или системно) в течение 4 нед перед первым визитом к исследователю (т. н. визит включения); пациенты, использовавшие симптоматические противопростудные средства, иммуномодуляторы (за 7 дней до включения); беременные и кормящие грудью женщины; лица с тяжелыми заболеваниями почек или печени, выраженными соматическими, неврологическими и/или психическими нарушениями.
Дизайн
Анализ базировался на двух одинаковых проспективных рандомизированных двойных слепых плацебо-контроли руемых мультицентровых исследованиях с параллельными группами, проведенных в 2009-2010 гг. в 37 центрах Германии (16 специалистов по оториноларингологии, 21 специалист по внутренним болезням и врачи общего профиля).
В рамках визита 1 (день 0) амбулаторных пациентов с ОРС рандомизировали на группы (1:1) после получения письменного информированного согласия. Пациенты принимали BNO 1016 в дозе 160 мг или плацебо по 1 таблетке 3 р/сут в течение 15 дней.
В ходе лечения пациенты ежедневно фиксировали свои симптомы. Во время каждого визита в центр исследования (дни 3, 7, 10 и 14, что соответствовало визитам 2, 3, 4 и 5) оценивались тяжесть каждого из 5 симптомов по шкале MSS и ответ на лечение. Кроме того, во время визитов пациенты заполняли опросник SNOT20 GAV, позволяющий оценить качество жизни, обусловленное здоровьем [9].
УЗИ околоносовых пазух выполняли в ходе обоих исследований во время визита 1 с целью подтверждения диагноза. УЗИ в конце лечения (визит 5) проводили лишь во втором испытании.
Анализ эффективности
Критерии эффективности. Все анализы эффективности базируются на объединенных данных испытаний ARhiSi1 и ARhiSi2.
Первичной конечной точкой определено среднее значение MSS во время визита 5 (день 14, популяция для полного анализа – FAS, протокольная популяция – PP). Кроме того, анализировали одиночные симптомы по шкале MSS во время визита 5 (день 14; FAS и PP), а для FAS и PP осуществили оценку результатов согласно опроснику SNOT-20 во время визитов 3 (день 7) и 5 (день 14). Дополнительно ученые классифицировали (FAS и PP) пациентов с терапевтическим эффектом по 4-балльной шкале во время визитов 2, 3, 4, 5.
Оценка тяжести симптомов. Тяжесть каждого из 5 симптомов по MSS определялась во время всех визитов с помощью 4-балльной шкалы (0 – симптом отсутствует, 1 – незначительный, 2 – умеренный, 3 – тяжелый). Интенсивность боли и стекания слизи по задней стенке глотки оценивали в соответствии с описаниями пациентов.
Шкала выраженности основного симптома (MSS). Объединяет 5 наиболее важных симптомов РС, основанных на экспертных клинических рекомендациях (насморк/выделения из передних отделов носа, стекание слизи по задней стенке глотки, заложенность носа, головная боль, лицевая боль / ощущение тяжести). Эту шкалу использовали в качестве основного критерия эффективности в нескольких клинических испытаниях [1012]. Значения MSS рассчитывали как сумму пяти оценок каждого из симптомов.
Оценка пациентов с терапевтическим эффектом и без такового. Общий ответ на лечение определяли во время каждого визита с помощью 4-балльной шкалы (0–симптомы исчезли/излечены; 1 – выраженность симптома уменьшилась по сравнению с таковой в рамках визита 1; 2 – симптомы не изменились при сопоставлении с визитом 1; 3 – отмечено ухудшение по сравнению с визитом 1). Излечившихся и участников, сообщивших о купировании/уменьшении интенсивности симптомов (0-1 балл), классифицировали как пациентов с терапевтическим эффектом, тогда как при отсутствии положительной динамики и в случае ухудшения (2-3 балла) больных относили в категорию без терапевтического эффекта.
Статистические анализы
В комбинированный анализ были включены только группы плацебо и BNO 1016480 мг из испытания ARhiSi1: когда для такого анализа применили критерии включения/ исключения в ARhiSi2, пациенты с лицевой болью / тяжестью >2 или значением MSS >12 или <8 при включении вARhiSi1 были исключены изподлежащих анализу совокупностей в связи снарушением критерия включения вARhiSi2.
Анализы эффективности осуществляли в основном на FAS, которая включает данные для всех рандомизированных пациентов с ОРС, получивших как минимум 1 дозу препарата (используемого в исследовании) и как минимум 1 оценку эффективности.
PP включает всех рандомизированных пациентов из FAS, за исключением имеющих крупные протокольные нарушения. Для оценки безопасности объединения данных не проводили. Вместо этого для описания результатов по безопасности использовали выборку каждого испытания, подлежащую оценке безопасности (SEP).
Статистические методы
Значения p≤0,025 указывают на статистический уровень значимости. Если не указано иное, отклонения обозначены как стандартная ошибка среднего значения (SEM).
Результаты
Распределение пациентов
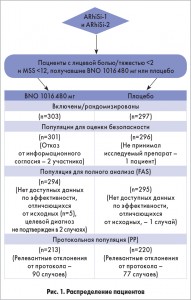
Распределение пациентов показано на рисунке 1. В группу терапии BNO 1016 вошли 303 пациента, в группу плацебо – 297 участников. Кроме того, 589 из 600 рандомизированных пациентов были рассмотрены в пределах FAS (294 (97%) пациента в группе BNO 1016 и 295 (98,2%) – в группе плацебо).
Критериям для включения в PP соответствовали 213 (70,3%) пациентов в группе BNO 1016 и 220 (74,1%) – в группе плацебо.
Результаты изучения эффективности
Продолжительность исследования и соблюдение режима лечения. Средняя длительность участия в исследовании составила 29 дней для обеих групп с диапазоном 3-57 дней для группы BNO 1016 и 3-86 – для группы плацебо. Судя по подсчету таблеток, процент соблюдения режима лечения составил 99,7% в группе BNO 1016 и 100,2% в группе плацебо.
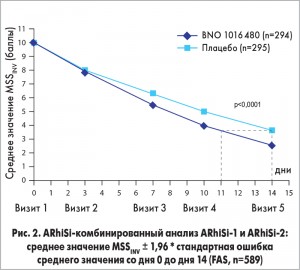
Шкала выраженности основного симптома (MSS). Исходные данные (среднее значение MSS) между двумя группами лечения статистически не различались (табл. 1). Значение MSS постепенно улучшалось в обеих группах в течение 15-дневного периода лечения в среднем на 10,02±1,61 до 2,47±2,55 для BNO 1016 и 9,87±1,52 до 3,63±3,63 – для плацебо (табл. 1, рис. 2). Разница между группами лечения во время визита 5 была статистически значимой в пользу BNO 1016 (FAS; p<0,0001).
Различия между двумя группами касательно значения по MSS были очевидны уже во время визита 4 (день 10), что свидетельствует о более быстром восстановлении в группе BNO 1016 (4,11 против 5,05 в группе плацебо). Во время визита 5 (день 14) указанные значения составляли 2,47±2,55 (BNO 1016) и 3,63±3,63 (плацебо).
Экстраполируя эти цифры на динамику состояния испытуемых, отмечено почти 3-дневное ускорение их восстановления на фоне приема BNO 1016 (дни 11 и 14 со ответственно). Разница между группами лечения на момент завершения терапии при анализе PP составила 1,70±3,13 ба лла (р<0,0001) – нормализации состояния пациентов, получавших BNO 1016, удалось достичь на 4 дня быстрее (день 10 и 14 соответственно).
В таблице 2 перечислены одиночные симптомы MSS во время визита 5 (день 14). В FAS каждый индивидуальный симптом демонстрирует статистический уровень значимости в пользу BNO 1016 (p<0,0001).
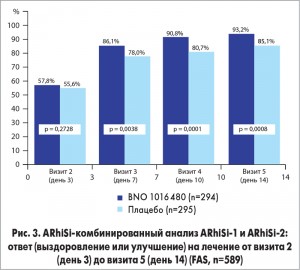
Ответ на лечение. Абсолютные и относительные результаты лечения приведены в таблице 3. Статистически значимое улучшение (и для FAS, и для PP) в пользу BNO 1016 было зарегистрировано уже на 7-й день (визит 3). На рисунке 3 показан комбинированный анализ ARhiSi1 и ARhiSi2: ответ (выздоровление или улучшение) на лечение в период с визита 2 (день 3) до визита 5 (день 14).
Определение качества жизни. Данные, полученные с помощью опросника SNOT20, содержатся в таблице 4. На момент завершения лечения отмечались очевидные преимущества BNO 1016 касательно данного параметра (р=0,0015).
Профиль безопасности. Не сообщалось о серьезных нежелательных явлениях (SAEs) в ходе испытаний ARhiSi1 или ARhiSi2.
В ARhiSi1 зафиксировано 42 нежелательных явления (AEs) у 33 пациентов из популяции для оценки безопасности (SEP; n=450): 33 AEs у 26 из 300 (8,7%) больных на фоне использования BNO 1016 (2 группы лечения BNO 1016: в дозе 240 мг/сут или 480 мг/сут) и 9 AEs у 7 из 150 (4,7%) участников при приеме плацебо.
В испытании ARhiSi2 зарегистрированы 53 нежелательные реакции – у 46 из 385 пациентов (21 – у 19 из 194 (9,8%) пациентов, получавших лечение BNO 1016 480 мг, 32 – у 27 из 191 (14,1%) участника, принимавшего плацебо). Сообщалось, что большинство нежелательных реакций в группе использования BNO 1016 имели небольшую/ умеренную интенсивность.
Обсуждение
Данный анализ свидетельствует об эффективности перорального приема 480 мг (160 мг 3 р/сут) растительного препарата BNO 1016. Эта новая стратегия лечения ОРС ускоряет нормализацию симптомов и улучшает качество жизни пациентов по сравнению с плацебо. Анализ PP превосходил результаты по FAS на протяжении всего исследования.
До сих пор наши знания о лечебных свойствах растительных лекарственных средств при лечении ОРС были ограниченными. Фармакологические исследования BNO 1011 показали его противовирусную активность [13], а также стимуляцию частоты движения ресничек респираторного эпителия in vitro путем активации форсколин стимулируемой секреции хлорида [14]. BNO 1011 – это сухой экстракт без вспомогательных веществ, тогда как в BNO 1016 их добавляют с целью прессования таблетки.
Недавно опубликован обзор о клинических свойствах Синупрета (препарат с теми же компонентами, что и BNO 1016, но в более низкой дозе), который демонстрирует благоприятный эффект при лечении ОРС [15]. Это растительное лекарственное средство оказывает выраженное противовоспалительное влияние, снижая экспрессию циклооксигеназы-2 и образование простагландина E2 [16].
Таким образом, механизм действия препарата оправдывает свое терапевтическое применение при лечении синусита и других вирусных/бактериальных респираторных инфекций, связанных с воспалением. Эксперимен тальные исследования Синупрета показывают снижение роста бактерий лишь после 4-дневного приема [6]. Другие растительные препараты, химический состав которых менее изучен, по-видимому, также обладают некоторым противовоспалительным эффектом, например при хроническом синусите [17].
Хотя интраназальные кортикостероиды (применяемые отдельно или в комбинации с антибиотиками) и рекомендованы для лечения ОРС, необходимо дальнейшее документальное обоснование их клинического применения [18]. Недавний метаанализ эффективности мометазона для лечения ОРС показал, что у 10 из 11 пациентов симптомы были облегчены или устранены [19]. Получены данные, что растительный препарат BNO 1016 так же полезен, как некоторые кортикостероиды, локально применяемые в терапии ОРС.
MSS в нашем анализе использовалась в соответствии с рекомендациями EPO S2012, которые объединяют 5 основных признаков ОРС и часто применяются в качестве стандарта для первичных критериев эффективности в клинических исследованиях [1].
Кроме того, УЗИ подтвердило терапевтическую результативность препарата [8]. Наш анализ и испытание ARhiSi2, посвященное клинической эффективности BNO 1016 [8], были первыми строго контролируемыми наблюдениями (для оценки эффекта комбинированного растительного препарата с фиксированной дозой), отвечающими всем современным стандартам качества для проспективного двойного слепого рандомизированного плацебо-контролируемого исследования.
Золотого стандарта лечения ОРС не существует. В терапии неосложненного ОРС антибиотики не показаны. Из-за большого количества различных вирусов, вызывающих ОРС, производство эффективной вакцины затруднено. Социально-экономические последствия этого заболевания весьма ощутимы – оно приводит к значительным расходам ресурсов здравоохранения и сопряжено с потерей производительности [3].
В среднем каждый взрослый ежегодно переносит 2-5 эпизодов заболеваний верхних дыхательных путей. С учетом данного факта невозможно переоценить важность каждого способа лечения, способного сократить длительность болезни и улучшить качество жизни пациентов.
Поскольку количество нежелательных явлений, а также их частота и интенсивность на фоне использования BNO 1016 и плацебо сопоставимы, можно сделать вывод о схожем профиле безопасности указанных стратегий. BNO 1016 имеет благоприятное соотношение польза/риск.
Данный анализ подтверждает результаты испытания III фазы препарата BNO 1016. Показано, что ежедневный прием 480 мг BNO 1016 в течение 2 нед является безопасным и эффективным методом лечения неосложненного ОРС. Препарат обеспечивает быструю и клинически значимую (в сравнении с плацебо) ремиссию симптомов и улучшает качество жизни больных.
Статья печатается в сокращении.
Список литературы находится в редакции.
ИНФОРМАЦИЯ
Источник: Оториноларингология. Восточная Европа, 1/2017