20 червня, 2017
Інфекція сечовивідних шляхів: сучасні напрями терапії
Інфекція сечовивідних шляхів (ІСШ) – це перший епізод клініко-лабораторних проявів їх інфекційного ураження без визначення топіки, тобто ІСШ є збірним поняттям, що включає цистити, пієліти, пієлоцистити, уретрити, простатити тощо.
Неускладнені ІСШ виникають в умовах відсутності в пацієнта структурних або функціональних порушень сечовидільних шляхів [7], переважно це епізоди гострого циститу в жінок.
Ускладненими вважають ІСШ, що виникають в осіб з анатомічними та/або функціональними аномаліями сечової системи, віком >65 років, вагітних, осіб з імуносупресивними станами, цукровим діабетом, хронічною хворобою нирок, після інструментальних втручань на органах сечової системи, попередньої антибіотикотерапії (АБТ) протягом кількох місяців, у разі виділення госпітальних штамів мікроорганізмів.
Якщо в пацієнта відзначалося ≥3 епізодів ІСШ за рік, це свідчить про її рецидивний характер [8].
Епідеміологія
Неускладнені ІСШ виявляються в 15% жінок віком 15-39 років та в 10% представниць вікової категорії 40-79 років. Клінічні прояви ІСШ турбують 70% жінок з бактеріурією.
У США щороку реєструється близько 6 млн звернень до лікаря з приводу ІСШ [5], з них понад 2 млн пов’язані з циститом [1].
Етіологія
Домінуючим збудником ІСШ є Escherichia сoli, яка ідентифікується в 70-95% хворих. Staphylococcus saprophyticus виділяють у 5-10% пацієнтів. Інші ентеробактерії, такі як Proteus mirabilis, Klebsiella spp., є причиною незначної кількості ІСШ [1].
Для більшості штамів E. coli та інших представників Enterobacteriaceae, що викликають цистит, характерна наявність бактеріальних ворсинок (т. зв. фімбрій), які відіграють вирішальну роль у бактеріальній адгезії до клітин промежини, піхви і крайньої плоті [18]. Фактори адгезії (ворсинки та ін.) дозволяють кишковим бактеріям прикріплятися до епітелію сечового міхура (СМ), що в подальшому призводить до його запалення.
Разом з тим зростає розповсюдженість грибкових ІСШ, що можна пояснити активним застосуванням антибіотиків (АБ) широкого спектра дії, глюкокортикоїдів, протипухлинних засобів, імуносупресивних препаратів і катетеризацією СМ. Супутні захворювання (наприклад, цукровий діабет) теж здатні спричиняти кандидоз.
Цистит може бути пов’язаний із запаленням піхви – бактеріальним вагінозом і статевими інфекціями.
Патогенез
Сприятливі умови для виникнення запального процесу в СМ виникають на фоні порушення уродинаміки нижніх відділів сечовивідних шляхів, бар’єрної функції епітелію слизової оболонки СМ, кровообігу в стінці СМ, зниження загальної реактивності організму. ІСШ часто поєднується із сечовим рефлюксом. Останній може бути на будь-якому рівні: від СМ до ниркової миски і навіть нирок (в останньому випадку класифікується не як ІСШ, а як рефлюкс-нефропатія).
Поширення інфекції сечовою системою можливе завдяки особливому механізму інтрамуральних тунелів, що мають спеціальні клапаноподобні утвори, розташовані в слизовій оболояці сечоводів. Серед причин – вагітність, будь-яка форма обструкції, дія бактеріального ендотоксину, що інгібує перистальтику.
Патогенез рецидивуючої ІCШ передбачає бактеріальну реінфекцію або бактеріальну стійкість. У разі персистенції ті ж бактерії визначаються у сечі через 2 тиж після початку відповідної АБТ. Реінфекція – повторне інфікування через 2 тиж після лікування.
Певну роль відіграє посткоїтальне інфікування. Відомо, що сперміциди, особливо ноноксінол-9, здатні впливати на нормальну флору і змінювати рН піхви, зменшуючи захист від бактеріальної колонізації СМ.
Клінічна картина
Клінічна картина ІСШ досить характерна: прискорене, іноді болісне сечовипускання, лихоманка, озноб; сечовий синдром (лейкоцитурія, бактеріурія); в аналізі крові – прискорена ШОЕ, нейтрофілія. Інструментальне дослідження підтверджує інтактність нирок.
Особливість ІСШ в осіб похилого віку – переважно безсимптомний перебіг, що є фактором ризику (особливо при виникненні обструкції) бактеріємії, септичного шоку, респіраторного дистрес-синдрому і викликає суттєві труднощі під час диференційної діагностики.
На наявність факторів ризику ускладненого перебігу ІСШ (наявність пієлонефриту і т. ін.) вказують наступні симптоми: тривалість >7 днів; лихоманка; інтенсивний біль у боці, що відновлюється з появою одного із цих симптомів. Велике значення має вивчення анамнезу. Про ускладнений перебіг ІСШ свідчать: цукровий діабет; вагітність; імуносупресія; структурні чи функціональні зміни сечової системи; сечокам’яна хвороба чи ниркова недостатність; катетеризація СМ чи інше лікування з використанням технічних засобів протягом останніх 2 тиж; рецидиви ІСШ; відсутність ефекту від лікування ІСШ в останні 4 тиж; виписка зі стаціонару в останні 2 тиж.
До ускладнюючих факторів відносяться:
• вік <18 або >65 років;
• чоловіча стать;
• лікування АБ в останні 4 тиж;
• пієлонефрит (гострий) в останні 3 міс;
• симптоми інших захворювань сечостатевої системи (уретриту, вагініту): поява чи зміна вагінальних виділень, неприємний запах, свербіння, диспауренія.
Фактори ризику розвитку хламідіозу: контакт з партнером, у якого наявне захворювання,що передається статевим шляхом; вік ≤25 років; пацієнтка незаміжня, не користується бар’єрною контрацепцією, новий сексуальний партнер упродовж останніх 3 міс. Лікування включає немедикаментозні та медикаментозні стратегії.
Немедикаментозні методи терапії
До них належать щадний режим; молочно-рослинна дієта; теплові процедури. Пацієнтам з ІСШ слід виключити з раціону каву та гостру їжу, консерви, м’ясні відвари. Рекомендується вживання достатньої кількості рідини (сечогінні трави, чай, мінеральна вода, ягідні морси, киселі, сік журавлини).
В усьому світі для профілактики і терапії циститу використовуються лікарські рослини [19]. Так, у народній медицині у разі ІСШ традиційно застосовується журавлина. Раніше її вважали ефективним засобом завдяки здатності підкислювати сечу, а також вмісту бензойної кислоти, що перетворюється в сечі на гіпурову кислоту, яка, у свою чергу, здійснює протимікробну дію. Проте, аби підтримувати рН сечі на рівні 5,5 для забезпечення антибактеріального ефекту, необхідно випивати не менше 1500 мл журавлинного соку на день [15]. Для більшості людей цей обсяг занадто великий для щоденного споживання. Існують дані, що журавлина володіє помірною прямою про тимікробною активністю [16].
Однак сьогодні на особливу увагу заслуговує здатність журавлини по переджувати прикріплення бактерій до епітелію СМ (за рахунок блокування адгезії ворсинок 1 типу). Основною антиадгезивною субстанцією журавлини вважається проантоціанідин типу А [4, 10]. Також він міститься в чорниці. У разі вживання журавлини бактерицидний вплив не є обов’язковим, оскільки бактерії, не здатні прикріпляться до епітелію сечових шляхів, видаляються із сечею. Це дозволяє запобігти порушенню нормальної сечової флори.
У великому подвійному сліпому дослідженні 153 жінки (середній вік 78 років) з бактеріурією та піурією отримували 300 мл підсолодженого соку журавлини на день або сік плацебо. У групі вживання соку журавлини у достовірно більшої кількості пацієнток порівняно з групою плацебо спостерігалася стерильність сечі [2]. Проте дослідження не продемонструвало захисної дії журавлини щодо нової бактеріальної колонізації. В іншому невеликому спостереженні за участю 12 жінок, у яких за фіксовано принаймні 6 епізодів ІСШ за попередній рік, встановлено, що прийом щодня 400 мг екстракту журавлини асоціюється з відсутністю ІСШ у всіх пацієнток протягом 12 тиж. Вісім жінок продовжували приймати екстракт після закінчення дослідження; протягом 2 років спостереження в них не відзначалося проявів ІСШ [3].
Систематичний огляд показав, що профілактичне застосування журавлини в пацієнтів з рецидивуючою ІСШ достовірно знижує частоту виникнення таких інфекцій протягом 12 міс [11].
За ефективністю сік журавлини поступається антибіотикам, проте не індукує бактеріальної резистентності [4].
Листя мучниці, що володіє антисептичними властивостями, вже багато століть використовується для лікування ІСШ. Рослина містить відносно високі рівні арбутозиду – глікозиду фенольного типу (також відомий як арбутин), який розщеплюється нормальною флорою кишечнику на глюкозу і гідрохінон. Гідрохінон поглинається і кон’югує в печінці з глюкуроновою кислотою (і, можливо, також приєднує сульфатні групи), завдяки чому набуває властивості розчинятися у воді. Гід рохінон-глюкуронідний комплекс потім виводиться з організму із сечею. У лужній сечі (рН≥8) він спонтанно дисоціює, вивільняється гідрохінон, який чинить протимікробну дію. Максимальна антибактеріальна активність виявляється через 3-4 години після прийому мучниці. Споживання фруктів і овочів посилює лужну реакцію сечі і збільшує ефективність мучниці [19].
Одночасно з мучницею не слід за стосовувати вітамін С, який збільшує кислотність сечі і, відповідно, пригнічує терапевтичну дію рослини. Прийом мучниці з журавлиною вва жається недоцільним, оскільки остання підкислює сечу [19].
Подвійне сліпе дослідження з оцінки ефективності використання протягом місяця екстракту мучниці, стандартизованого за рівнем арбутозиду, в жінок з рецидивуючим циститом показало, що засіб забезпечував профілактику епізодів циститу протягом року після дослідження. У той же час у 23% жінок у групі плацебо відзначався щонайменше 1 епізод циститу впродовж року після завершення спостереження. Різниця між групами була статистично і клінічно значущою [14].
Мучниця містить дубильні речовини, що здатні спричиняти нудоту, тому її треба приймати з їжею або у вигляді холодного настою трави, з якого таніни погано екстрагуються. Потрібно враховувати, що гідрохінон має низку потенційно небезпечних ефектів, включаючи пригнічення дозрівання В-лімфоцитів і нефротоксичність [13]. Тож засіб на основі мучниці не слід застосовувати впродовж тривалого часу.
В іншому клінічному дослідженні вивчали вплив комбінації екстракту кореня хрону і листя настурції при лікуванні неускладненої ІСШ. Встановлено, що дана схема була настільки ж ефективною, як і застосування АБ, але значно безпечнішою [9].
Трави, що містять берберин, використовуються для лікування багатьох типів інфекції. Цей алкалоїд виявляє антимікробну активність у високих концентраціях, а також, як і журавлина, є антиадгезивним агентом. Берберин запобігає адгезії ворсин E. coli до епітелію СМ і блокує прикріплення Streptococcus pyogenes.
Рослини, які традиційно вважа ються сечогінними, не впливають на іонний обмін, але збільшують потік крові до нирок і тим самим підвищують швидкість клубочкової фільтрації, що допомагає механічно видалити бактерії із СМ. Відомо, що листя кульбаби викликає сечогінний ефект у щурів. Доведено, що збір, до складу якого входили листя берези, глід, ягоди полуниці та суниці, кукурудзяні рильця, квітки ромашки, кінський хвіст, у щурів забезпечував на 47% більший сечогінний ефект, ніж використання лише кінського хвоста, і на 34% інтенсивнішу дію порівняно з такою гідрохлортіазиду [17].
Поширений рослинний флавоноїд кверцетин (міститься у великій кількості в зеленому чаї, яблуках і цибулі) зменшує симптоми інтерстиціального циститу [12].
Показані (крім випадків гемо рагічного циститу) теплові процедури – сидячі ванни, грілка, теплові мікроклізми та спринцю вання відварами трав, фізіотерапе втичні процедури. Інколи на певний час забороняється статева близькість, що дозволяє ліквідувати запалення.
Якщо ІСШ має легкий перебіг, медикаментозне лікування не є обов’язковим, слід забезпечити лише хороший відтік сечі.
Антибіотикотерапія
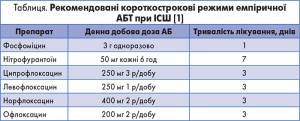
Основна стратегія лікування не ускладненої ІСШ – короткотривала АБТ (табл.). Препаратами першої лінії є фосфоміцину трометамол 3 г одноразово; нітрофурантоїн у макрокристалах (5-7 днів) 50-100 мг кожні 6 год. Короткі курси АБТ ефективніші за плацебо та асоціюються з низьким ризиком ускладнень [1].
Необхідно уникати застосовування нітрофурантоїну та фосфоміцину у разі загрози раннього пієлонефриту [5].
Друга лінія терапії – 3-денний курс фторхінолонів перорально: ципрофлоксацин 250 мг 2-3 р/добу; левофлоксацин 250 мг 1 р/добу, офлоксацин 200 мг кожні 12 годин.
Як альтернативні застосовують пероральні β-лактами курсом 3-7 діб: амоксициліну/клавуланат 500/125 мг, цефдинір 300 мг, цефаклор 500 мг, цефподоксим 100 мг, цефуроксим 250 мг [5].
У випадку циститу в жінок похилого віку, викликаного Staphylococcus saprophyticus, пропонується АБТ протягом 7 днів [5].
Тривалішу АБТ (норфлоксацин; офлоксацин мінімум 7 днів) слід проводити в разі відсутності ефекту від лікування протягом 3-5 днів, при наявності факторів ризику ускладненого перебігу ІСШ або виникненні рецидиву.
За відсутності ефекту від терапії слід призначити повторний курс з викорис танням іншого АБ протягом 7 днів [1].
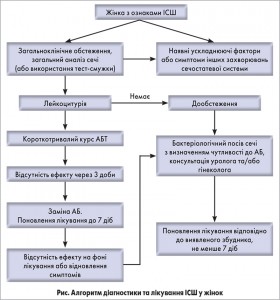
Жінкам, у яких симптоми після завершення лікування зберігаються або зникають, проте відновлюються впродовж 2 тиж, рекомендується провести бактеріологічне дослідження сечі з визначенням чутливості до АБ (рис.)
При лікуванні ускладненої ІСШ у жінок застосовується перша лінія терапії:
•перорально (ципрофлоксацин 500 мг 7-14 діб, левофлоксацин 750 мг 5 днів)
або
• в/в, коли пацієнт погано переносить пероральні АБ або є підозра на інфікування резистентною флорою:
♦ ципрофлоксацин 400 мг кожні 12 годин 7-14 діб;
♦ левофлоксацин 750 мг 5 діб;
♦ ампіцилін 1-2 г кожні 6 годин + гентаміцин 2 мг/кг кожні 8 год 7-14 днів;
♦ піперацилін/тазобактам 3,375 г кожні 6 год 7-14 діб;
♦ доріпенем 500 мг кожні 8 годин 7-14 діб;
♦ іміпенем/циластатин 500 мг кожні 6 годин 7-14 діб;
♦ меропенем 1 г кожні 8 годин 7-14 діб.
Тривалість курсу терапії залежить від динаміки (10-14 діб у госпіталі зованих пацієнтів із слабкою відповіддю на лікування) [5].
При лікуванні ІСШ у чоловіків в/в призначаються АБ цефалоспоринового ряду ІІІ покоління (цефтриаксон, цефтазидим), фторхінолони (ципрофлоксацин, левофлоксацин, офлоксацин, норфлоксацин) або аміноглікозиди (гентаміцин, тобраміцин) [6].
Схеми лікування грибкової ІСШ поки не розроблені. Найбільш поширене промивання СМ амфотерицином В. Застосовують й інші протигрибкові засоби, зокрема похідні імідазолу – кетоконазол і міконазол.
Тривале промивання СМ з використанням 50 мг міконазолу, розчиненого в 1 л ізотонічного розчину хлориду натрію, що про водиться щодня протягом 5 днів, сприяє пригніченню грибкової ІСШ. Можливе пероральне призначення флуцитозину по 200 мг/кг на день протягом 21-28 днів. Цей препарат ефективний при лікуванні системних грибкових інфекцій, що викликаються Candida і Torulopsis glabrata. Флуцитозин добре абсорбується при прийомі всередину, близько 90% дози препарату виводиться в незміненому вигляді із сечею.
При безсимптомній кандидурії і наявності таких факторів ризику, як цукровий діабет або обструктивна уропатія, а також у пацієнтів, які перенесли трансплантацію нирки, показана профілактична терапія.
За показаннями слід призначати знеболювальні (ненаркотичні аналгетики, нестероїдні протизапальні засоби) та спазмолітики [1].
ІСШ при цукровому діабеті погано піддаються лікуванню, що обумовлено підвищеним рівнем глікемії, переважанням E. coli в посівах сечі (зазвичай у поєднанні з іншого флорою).
За допомогою АБ не завжди вдається здійснити ерадикацію патогенних мікроорганізмів, ці засоби не здатні усунути колонізацію бактерій, можуть порушувати склад вагінальної і уретральної флори. Дисбіоз, у свою чергу, є фактором ризику повторної колонізації поверхні сечового тракту патогенами. Через здатність АБ спричиняти розвиток резистентної флори дуже важливо забезпечити пробіотичну підтримку.
Профілактика
Первинна профілактика полягає в інформуванні жінок щодо правил поведінки з попередження ІСШ: споживання достатньої кількості рідини, своєчасне спорожнення СМ, обов’язкове спорожнення СМ після статевого акту, дотримання правил гігієни зовнішніх статевих органів, уникнення переохолодження [1].
Прогноз
Істинна ІСШ не призводить до рубцювання ниркової тканини, що відмічається при обструктивній уропатії, нефролітіазі, пієлонефриті. У цілому ризик рубцювання нирок не перевищує 10%.
Список літератури знаходиться в редакції.