19 липня, 2017
Своевременный старт инсулинотерапии — ключ к предотвращению осложнений при сахарном диабете 2 типа
Известно, что сахарный диабет (СД) 2 типа не является неким стабильным состоянием, напротив, представляет собой динамический процесс с присущими ему этапами развития. На разных стадиях формирования данной патологии преобладают те или иные патогенетические механизмы и гормонально-метаболические нарушения, которые закономерно усугубляются с течением времени и приводят к возникновению новых симптомов и осложнений.
Так, на начальных стадиях (преддиабет) прогрессирующая инсулинорезистентность (ИР) периферических тканей преодолевается за счет компенсаторной гиперинсулинемии, позволяющей некоторое время сохранять нормогликемию, однако при этом происходит истощение инсулиносекреторных резервов b-клеток поджелудочной железы настолько, что их функция к моменту выявления заболевания уже снижена на 40-50% [4, 6, 8-10, 29]. После манифестации СД 2 типа, характеризующейся превышением физиологического уровня глюкозы в крови, проявляются цитотоксические эффекты гипергликемии, вызывая многообразные структурно-функциональные изменения на молекулярном, субклеточном и клеточном уровнях. Скорость прогрессирования дальнейших нарушений зависит как от внутренних (генетически запрограммированных) особенностей организма, так и от внешних условий – питания, физической активности, сопутствующих заболеваний, приема медицинских средств, психологических и социальных условий, стрессирующих воздействий окружающей среды.
Применение современных сахароснижающих препаратов позволяет определенное время поддерживать гормонально-метаболические показатели на надлежащем уровне. Однако вектор развития заболевания, к сожалению, таков, что в конечном итоге пероральная сахароснижающая терапия (нередко дорогостоящая ввиду назначения новейших средств) становится неэффективной.
Своевременное начало инсулинотерапии: эффективное противодействие глюкозотоксичности и апоптозу b-клеток
Установлено, что на ранних стадиях заболевания дисфункция b-клеток обратима. Так, в экспериментах in vitro было показано, что длительная гипергликемия приводит к снижению экспрессии гена инсулина в b-клетках, однако данный глюкозотоксический эффект нивелируется при достижении эугликемии, и чем менее длительно воздействие гипергликемии, тем больше степень восстановления b-клеток [19, 25].
Неоспоримым является тот факт, что среди всех доступных на сегодняшний день противодиабетических препаратов только инсулин обеспечивает быструю (в течение нескольких дней) и устойчивую нормализацию уровня глюкозы даже при выраженной декомпенсации (HbA1c>10%) [20]. Данные ряда крупных исследований (UKPDS, DCCT и др.) подтвердили, что использование интенсивной терапии инсулином на ранних стадиях заболевания может иметь положительное клиническое воздействие и замедлять прогрессирование осложнений. Кроме того, при условии частичного сохранения чувствительности периферических тканей к инсулину у больных на ранних стадиях СД 2 типа введение дополнительного количества экзогенного инсулина может стимулировать эффекты, опосредованные инсулиновыми рецепторами, а именно: повысить поглощение мышечными клетками глюкозы, уменьшить глюконеогенез в печени, а также снизить липолиз и поступление в кровь свободных жирных кислот, корректируя проявления дислипидемии и снижая липотоксичность [27].
В дополнение к метаболическим эффектам установлено, что раннее назначение интенсивной инсулинотерапии у пациентов с впервые выявленным СД 2 типа способствует снижению показателя маркера воспаления – фактора некроза опухоли альфа, улучшает функцию эндотелия, тромбоцитов и лейкоцитов. Влияние инсулина на дифференциацию Т-клеток способствует снижению интенсивности иммунного процесса, тем самым обусловливая дополнительные преимущества инсулинотерапии, поскольку хроническое воспаление выступает важным патогенетическим звеном сердечно-сосудистых заболеваний и одной из причин апоптоза панкреатических b-клеток [31]. Эти данные позволили предположить, что противовоспалительный и антиапоптический эффекты инсулина, помимо контроля гликемии и липидемии, создают предпосылки к предотвращению макрососудистых осложнений и повышению выживаемости b-клеток при СД 2 типа [13, 16, 30].
Таким образом, результаты целого ряда исследований и клинических наблюдений привели к переоценке роли инсулинотерапии при СД 2 типа.
Обновленные рекомендации АDA 2017 г. по инсулинотерапии
В январе нынешнего года стало доступным очередное обновленное клиническое руководство по диагностике и лечению СД Американской диабетической ассоциации (ADA) – «Стандарты оказания медицинской помощи при сахарном диабете – 2017», которые ежегодно пересматриваются на основе экспертного анализа результатов новейших научных и клинических исследований. Как и предыдущие рекомендации по коррекции гипергликемии у пациентов с СД 2 типа они базируются на принципе ориентации на пациента, то есть персонифицированном подходе к выбору терапии, а также максимальном привлечении больных к совместному принятию решений о лечении. При этом учитываются эффективность назначаемых средств, риск гипогликемии, влияние на массу тела, возможные побочные эффекты, стоимость лечения и предпочтения пациента [11].
В руководстве подчеркивается, что многие больные СД 2 типа в конечном итоге нуждаются в инсулинотерапии, в связи с чем им следует регулярно объяснять, что назначение последней объективно обусловлено прогрессирующим характером заболевания, а не является «наказанием» за неправильное лечение. Пациенты избегают назначения инсулина вследствие безосновательных опасений и сложившихся стереотипов относительно смысла инсулинотерапии, что приводит к длительному периоду декомпенсации и увеличению риска развития микрососудистых и макрососудистых осложнений. Кроме того, важным условием успешного начала инсулинотерапии является обучение пациентов алгоритмам самостоятельной титрации доз инсулина на основе самоконтроля уровня глюкозы в крови. Всестороннее образование в отношении самоконтроля гликемии, диеты, а также предотвращение и соответствующее лечение гипогликемии имеют решающее значение для любого пациента, использующего инсулин.
Согласно последнему варианту рекомендаций возможность начала терапии инсулином (в комбинации или без дополнительных пероральных препаратов) следует рассмотреть у пациентов с впервые диагностированным СД 2 типа, которые имеют высокие показатели НbА1с (>10%) и/или глюкозы в крови (>16,7 ммоль/л). А также, если с помощью таблетированной монотерапии в максимально переносимой дозе не удается достигнуть или поддерживать целевой уровень НbA1с в течение 3 мес, рекомендуется добавить второе пероральное средство, агонист рецептора глюкагоноподобного пептида 1 (аГПП-1) или базальный инсулин.
Следует отметить, что некоторым больным СД 2 типа показан временный перевод на инсулинотерапию. Абсолютными показаниями для временного назначения инсулина являются: крупные хирургические вмешательства, серьезные заболевания инфекционного и воспалительного характера, целый ряд острых состояний (инфаркт миокарда, острое нарушение мозгового кровообращения, тяжелые травмы и т.д.). Кратковременная инсулинотерапия используется при данных состояниях, так как в эти периоды потребность в экзогенном инсулине, как правило, связана с отменой пероральных сахароснижающих средств (ПСС). В острых ситуациях применение инсулина быстро устраняет симптомы гипергликемии и неблагоприятные последствия глюкозотоксичности. Временная долгосрочная инсулинотерапия (2-3 мес) назначается при наличии временных противопоказаний к приему ПСС, при гипергликемии во время длительных воспалительных заболеваний с целью восстановления секреторной функции b-клеток [7, 16].
На начальных этапах инсулинотерапии могут быть использованы препараты инсулинов с различной длительностью действия и их комбинации.
Базальный инсулин – базовый инсулин, который рекомендовано комбинировать с метформином и другими ПСС. Является наиболее удобным в контексте инициации инсулинотерапии в целом. Начальная доза – 10 единиц в день или 0,1-0,2 ЕД/кг/сут в зависимости от степени гипергликемии.
Болюсный инсулин. Во многих случаях больным с СД 2 типа может потребоваться болюсное введение инсулина во время приема пищи дополнительно к базальному инсулину. Рекомендуемая начальная доза приема болюсного инсулина составляет 4 единицы или 0,1 ЕД/кг или 10% от основной дозы. Если концентрация HbA1c при назначении болюсного инсулина составляет 8%, то следует рассмотреть возможность уменьшения дозы базального инсулина.
Предварительно смешанный инсулин содержит как базальный, так и болюсный компонент (например, комбинированный инсулин 70/30 состоит из 70% инсулина средней продолжительности действия и 30% инсулина короткого действия), что позволяет эффективно контролировать как гликемию натощак, так и постпрандиальную гликемию с помощью двух инъекций утром и вечером.
Концентрированный инсулин. В настоящее время в Украине уже доступны препараты концентрированного инсулина (инсулин гларгин U‑300, деглюдек U‑200), особенностью которых является длительная продолжительность действия, а также подтвержденный результатами исследований меньший риск развития гипогликемий. Концентрированные препараты могут быть более удобными для пациента, а также, вероятнее всего, улучшат приверженность к лечению больных с выраженной резистентностью к инсулину, что, как известно, требует назначения больших доз последнего.
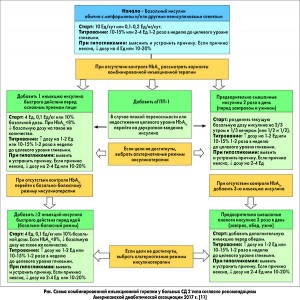
Комбинированная инъекционная терапия. В тех случаях, если путем титрования дозы базального инсулина у пациента достигнут приемлемый уровень глюкозы крови натощак (или если доза составляет 0,5 Ед/кг/сут), однако HbA1c сохраняется выше целевого уровня, рекомендовано перейти к комбинированной инъекционной терапии (рис.). При инициировании последней лечение метформином следует продолжать, в то время как прием других ПСС (производных сульфонилмочевины, ингибиторов ДПП‑4 и аГПП-1) может быть прекращен, чтобы избежать неоправданно сложных или дорогостоящих схем (то есть добавления четвертого гипогликемического агента).
В настоящее время на отечественном рынке представлен широкий ассортимент препаратов инсулина, особое место среди которых занимают высококачественные и доступные по цене препараты человеческого инсулина – Инсуман®. Их производство осуществляется в Германии (г. Франкфурт) на крупнейшем в мире заводе по производству инсулинов, а упаковка готовых флаконов и картриджей во вторичную упаковку производится в Украине в рамках партнерства ООО «Санофи-Авентис Украина» с ООО «Фарма Лайф», одним из ведущих производителей лекарственных препаратов в Украине. Инсуман® – это человеческий генно-инженерный инсулин, обеспечивающий постоянный и эффективный гликемический контроль у пациентов с СД 1 и 2 типа. Полный ассортимент препарата Инсуман®, который производится в Украине, включает: Инсуман® Базал (средней длительности действия), Инсуман® Комб 25 (25% инсулина короткого действия и 75% – продленного), Инсуман® Рапид короткого действия.
Представленные препараты инсулинов доступны в виде флаконов по 5 мл и картриджей, а для удобства пациентов представлена шприц-ручка многоразового использования AllStar®, безопасность, надежность и удобство которой позволяют повысить комплайенс при самостоятельном использовании пациентами. Следует упомянуть также, что в картридже препаратов Инсуман® Базал и Инсуман® Комб 25 имеется три тяжелых металлических шарика, которые эффективно ресуспендируют суспензию при меньшем количестве переворачиваний, обеспечивая точное дозирование вводимого препарата [3, 23].
Раннее применение инсулинотерапии: фокус на эффективность и безопасность в клинической практике
Большой интерес представляет изучение эффективности раннего назначения инсулина на начальных стадиях развития СД 2 типа. В Китайской Народной Республике проведено крупное мультицентровое рандомизированное исследование в параллельных группах, в которое были включены 382 пациента с впервые выявленным СД 2 типа со средним начальным уровнем HbA1с 9,7%. Рандомизированные группы пациентов, сопоставимые по своим клинико-демографическим характеристикам, в течение 12 мес получали инсулинотерапию или ПСС (контроль). Установлено, что группа пациентов, находившихся на ранней инсулинотерапии, характеризовалась значительно лучшим сохранением функции b-клеток, восстановлением первой фазы секреции инсулина и большей частотой достижения ремиссии в течение года по сравнению с контрольной группой (44,9 против 26,7%) [32].
В открытом мультицентровом проспективном обсервационном исследовании EARLY продемонстрирована эффективность и безопасность раннего использования базального инсулина гларгин у 1438 больных СД 2 типа, плохо контролируемых с помощью максимально переносимых доз метформина (HbA1c ≥7,5%). Инсулин гларгин титровали до целевого уровня гликемии натощак ≤5,6 ммоль/л, что привело к значительному снижению HbA1c – с 8,69±1,25 до 7,39±0,92% через 6 мес (p<0,001). Пациенты с более короткой продолжительностью диабета, более низким уровнем HbA1c в начале исследования и более низким индексом массы тела чаще достигали целевого диапазона HbA1c (<7 или <6,5%). Масса тела уменьшилась в среднем на 1 кг. Данные, полученные в реальных условиях, подтвердили, что раннее назначение инсулина гларгин является рациональным и практичным вариантом, в том числе с точки зрения нивелирования рисков прогрессирования заболевания [21].
В 2016 г. был опубликован обзор результатов клинических исследований, в котором на основе проведенного анализа данных продемонстрировано положительное влияние раннего начала интенсивной инсулинотерапии на функцию b-клеток, обусловленное тем, что быстрое достижение контроля гликемии, обеспечивая временный «отдых» и уменьшая гипергликемический стресс для панкреатических b-клеток, в итоге способствует восстановлению их инсулиносекреторной функции. Однако автор подчеркивает, что решение о введении базального инсулина дополнительно к метформину тем не менее должно быть индивидуализировано и базироваться на основе проведенного анализа отношения польза/риск [20].
Таким образом, результаты многочисленных исследований относительно прогрессирующего характера гормонально-метаболических нарушений при СД 2 типа стали основой переоценки значения инсулинотерапии в целом: на сегодняшний день ее рассматривают не как «последнее средство», а как наиболее физиологичный подход к лечению, позволяющий предупредить или быстро устранить высокие уровни глюкозы в крови, тем самым обеспечить защиту b-клеток от эффектов глюкозотоксичности, ведущей к их дисфункции и апоптозу. Использование современных препаратов человеческого инсулина и индивидуально подобранных схем комбинированной инсулинотерапии делает максимально эффективным и безопасным этот метод лечения, позволяя добиться оптимального гликемического контроля, снизить риск развития осложнений, а также повысить качество жизни пациентов.
Литература
1. Дедов И.И., Шестакова М.В., Абусуев С.А. и др. Оптимизация и интенсификация инсулинотерапии при сахарном диабете 2 типа (клинические рекомендации) // Сахарный диабет. – 2010. – № 5. – С. 9-16.
2. Занозина О.В., Боровков Н.Н., Щербатюк Т.Г. Свободно-радикальное окисление при сахарном диабете 2-го типа: источники образования, составляющие, патогенетические механизмы токсичности // Соврем. технол. мед. – 2010. – № 3. – С. 104-112.
3. Корпачева-Зиныч О.В., Гурина Н.М., Корпачев В.В. Инсуман® базал, инсуман® комб, инсуман® рапид в одноразовых шприц-ручках солостар® – единственные в украине человеческие инсулины в одноразовых шприц-ручках солостар® // Межд. Эндокр. Ж. – 2013. – № 2 (50).
4. Корпачев В.В. Инсулин и инсулинотерапия. – К.: РИА «Триумф», 2001. – 454 c.
5. Кушнарева Н.Н., Корпачев В.В., Ковальчук А.В. Опыт использования инсулина Инсуман® Базал и Инсуман® Комб 25 в лечении больных сахарным диабетом 2-го типа // Международный эндокринологический журнал. – 2012. – Т. 7 (47).
6. Маньковский Б.Н., Жердева Н.Н. Инсулинотерапия. Что нового? // МЭЖ. – 2013. – № 3 (51). – С. 43-46.
7. Мкртумян А.М., Бирюкова Е.В., Маркина Н.В. Выбор режима инсулинотерапии при сахарном диабете 2 типа // Лечащий врач. – 2005. – № 5.
8. Науменко В.Г. Инсулинотерапия в клинической практике // Межд. Эндокр. Ж. – 2012. – № 2 (42).
9. Полторак В.В., Красова Н.С., Горшунская М.Ю. Апоптоз панкреатических бета-клеток как новая мишень для инсулинотерапии больных сахарным диабетом 1 и 2 типа // Пробл. ендокр. патол. – 2015. – № 1. – С. 89-103.
10. Тронько М.Д. Основи клінічної фармакології цукрового діабету та його ускладнень: Посіб. для лікарів / М.Д. Тронько, В.В. Корпачев. – К.: Книга плюс, 2004. – 103 c.
11. American Diabetes Association. Glycemic targets. Sec. 6. Standards of Medical Care in Diabetes; Sec. 8. Pharmacologic Approaches to Glycemic Treatment – Diabetes Care. – 2017. – V. 40 (Suppl. 1). – P. S4-6; S67-74.
12. Bramlage P., Bluhmki T., Fleischmann H. Determinants of weight change in patients on basal insulin treatment: an analysis of the DIVE registry // BMJ Open Diab. Res. Care. – 2017. – V. 5. – P. e000301.
13. Chen H., Ren A., Hu S., Mo W., Xin X., Jia W. The significance of tumor necrosis factor-alpha in newly diagnosed type 2 diabetic patients by transient intensive insulin treatment // Diab. Res. Clin. Pract. – 2007. – V. 75. – P. 327-332.
14. Chon S., Oh S., Kim S. et al. The effect of early insulin therapy on pancreatic beta-cell function and long-term glycemic control in newly diagnosed type 2 diabetic patients // Korean J. Intern. Med. – 2010. – V. 25. – P. 273-281.
15. Dandona P., Aljada A., Mohanty P. The anti-inflammatory and potential anti-atherogenic effect of insulin: a new paradigm // Diabetologia. – 2002. – V. 45. – P. 924-930.
16. Dandona P., Chaudhuri A., Ghanim H. et al. Use of Insulin to Improve Glycemic Control in Diabetes Mellitus // Cardiovasc. Drugs Ther. – 2008. – V. 22. – P. 241.
17. Drzewoski J., Kasznicki J., Trojanowski Z. The role of «metabolic memory» in the natural history of diabetes mellitus // Pol. Arch. Med. Wewn. – 2009. – V. 119. – P. 493-500.
18. Evans J.L., Goldfine I.D., Maddux B.A., Grodsky G.M. Oxidative stress and stress-activated signaling pathways: a unifying hypothesis of type 2 diabetes // Endocr. Rev. – 2002. – V. 23 (5). – P. 599-622.
19. Gleason C.E., Gonzalez M., Harmon J.S., Robertson R.P. Determinants of glucose toxicity and its reversibility in the pancreatic islet beta-cell line, HIT-T15 // Am. J. Physiol. Endocrinol. Metab. – 2000. – V. 279. – P. E997-1002.
20. Hanefeld M., Monnier L., Schnell O., Owens D. Early Treatment with Basal Insulin Glargine in People with Type 2 Diabetes: Lessons from ORIGIN and Other Cardiovascular Trials // Diabetes Ther. – 2016. – V. 7. – P. 187-201.
21. Hanefeld M., Fleischmann H., Landgraf W., Pistrosch F. EARLY study: early basal insulin therapy under real-life conditions in type 2 diabetics // Diabetes Stoffw Herz. – 2012. – V. 21. – P. 91-97.
22. Holman R.R., Paul S.K., Bethel M.A., Neil H.A., Matthews D.R. Long-term follow-up after tight control of blood pressure in type 2 diabetes // N. Engl. J. Med. – 2008. – V. 359. – № 15. – P. 1565-1576.
23. Kaiser P., Maxeiner S. еt al. Assessment of the Mixing Efficiency of Neutral Protamine Hagedorn Cartridges // J. Diab. Sci. Technol. – 2010. – Vol. 4. – P. 652-657.
24. LeRoith D., Fonseca V., Vinik A. Metabolic memory in diabetes – focus on insulin // Diabetes Metab. Res. Rev. – 2005. – V. 21 (2). – P. 85-90.
25. Monnier L., Colette C., Mas E. et al. Regulation of oxidative stress by glycaemic control: evidence for an independent inhibitory effect of insulin therapy // Diabetologia. – 2010. – V. 3. – P. 562-571.
26. ORIGIN Trial Investigators., Gerstein H., Yusuf S., Riddle M.C., Ryden L., Bosch J. Rationale, design, and baseline characteristics for a large international trial of cardiovascular disease prevention in people with dysglycemia: the ORIGIN Trial (Outcome Reduction with an Initial Glargine Intervention) // Am. Heart J. – 2008. – V. 155 (1). – P. 26-32, 32. e1-6.
27. Poitout V., Robertson R.P. Glucolipotoxicity: fuel excess and beta-cell dysfunction // Endocr. Rev. – 2008. – V. 29. – P. 351-366.
28. Sheetz M.J., King G.L. Molecular understanding of hyperglycemia’s adverse effects for diabetic complications // J. Amer. Med. Assoc. – 2002. – V. 288 (20). – P. 2579-2588.
29. Stumvoll M., Goldstein B.J., van Haeften T.W. Pathogenesis of type 2 diabetes // Endocr. Res. – 2007. – V. 32 (1-2). – P. 19-37.
30. Tian J., Wang J., Li Y. et al. Endothelial function in patients with newly diagnosed type 2 diabetes receiving early intensive insulin therapy // Am. J. Hypertens. – 2012. – V. 25. – P. 1242-1248.
31. Viardot A., Grey S., Mackay F., Chisholm D. Potential Antiinflammatory Role of Insulin via the Preferential Polarization of Effector T Cells toward a T Helper 2 Phenotype // Endocrinology. – 2007. – V. 148. – P. 346-353.
32. Weng J., Li Y., Xu W. et al. Effect of intensive insulin therapy on — cell function and glycaemic control in patients with newly diagnosed type 2 diabetes: a multicentre randomised parallel-group trial // Lancet. – 2008. – V. 371 (9626). – P. 1753-1760.