Статья в формате PDF.
Гормон-рецептор-позитивный рак молочной железы (РМЖ) – самый распространенный тип РМЖ, составляющий около 60-65% всех случаев. Более 50 лет лечение гормон-рецептор-позитивного РМЖ было направлено на эстроген-рецепторный сигнальный путь. Тем не менее в большинстве случаев развивается как первичная, так и вторичная резистентность к гормональной терапии, что требует новых подходов к лечению. Палбоциклиб – таргетный препарат, избирательно ингибирующий циклин-зависимые киназы CDK4 и CDK6, что приводит к восстановлению контроля клеточного цикла и подавлению роста злокачественных клеток у больных с эстроген-рецептор-позитивным/HER2‑негативным РМЖ (ER+/HER2‑ РМЖ).
Циклинзависимые киназы (CDK) представляют собой большое семейство серин-треониновых киназ, которые играют важную роль в регуляции прогрессирования клеточного цикла. Взаимодействие циклина D с CDK4 и CDK6 облегчает гиперфосфорилирование продукта гена ретинобластомы (Rb), что приводит к клеточному прогрессированию от фазы G1 к S-фазе клеточного цикла. Альтерация в сигнальном пути циклин-D-CDK4/6-Rb, которая встречается при многих злокачественных образованиях и ассоциирована с эндокринной резистентностью при РМЖ, приводит к утрате регуляции контрольной точки Rb. Альтерации включают в себя циклин-D амплификацию, потерю или мутацию Rb, утрату негативных регуляторов, таких как p16.
Палбоциклиб является таргетным препаратом, который ингибирует CDK4 и CDK6. Данные доклинических исследований показали способность палбоциклиба ингибировать рост эстроген-позитивных злокачественных клеток при РМЖ, действуя синергически с антиэстрогенами и нивелируя эндокринную резистентность.
Эти данные послужили основанием для проведения рандомизированного исследования II фазы PALOMA‑1, в котором эффективность палбоциклиба в комбинации с летрозолом сравнивалась с монотерапией летрозолом в первой линии терапии у женщин в постменопаузе с распространенным РМЖ, с экспрессией рецепторов эстрогенов в отсутствие экспрессии рецепторов эпидермального фактора роста РМЖ.
По результатам исследования PALOMA‑1 палбоциклиб в комбинации с летрозолом показал значимое увеличение выживаемости без прогрессирования (ВБП) по сравнению с монотерапией летрозолом, что дало основания Управлению по контролю качества пищевых продуктов и лекарственных препаратов (FDA) США одобрить эту комбинацию к применению у пациенток с распространенным ER+/HER2- РМЖ.
PALOMA‑2 – более крупное исследование – было разработано для подтверждения результатов PALOMA‑1 и дальнейшей оценки безопасности и эффективности комбинации палбоциклиба и летрозола в качестве первой линии терапии у женщин в постменопаузе с распространенным ER+/HER2- РМЖ.
Дизайн исследования
В двойном слепом исследовании III фазы пациентки были рандомизированы в соотношении 2:1 на 2 группы, одна из которых получала палбоциклиб (125 мг/день перорально в течение 3 недель, 1 неделя перерыв) и летрозол (2,5 мг/день перорально постоянно), вторая – плацебо + летрозол. Пациентки были стратифицированы с учетом расположения опухоли, времени без прогрессирования от момента окончания неоадъювантой или адъювантной терапии, предшествующей гормонотерапии.
Лечение продолжалось до прогрессирования заболевания в соответствии с критериями RECIST (версия 1.1), развития неприемлемых токсических эффектов или отказа от дальнейшего лечения.
Пациентки
В исследование были включены женщины с распространенным ER+/HER2- РМЖ, ранее не получавшие системную терапию. По возможности были получены свежие образцы биопсии рецидивирующих или метастатических опухолей. Статус HER2 определяли с использованием анализа, одобренного FDA. Критерием включения был период постменопаузы, а именно: предварительная двусторонняя овариэктомия, спонтанное прекращение менструаций в течение последних 12 мес и более, уровень фолликулостимулирующего гормона и эстрадиола в постменопаузальных диапазонах. Были включены пациентки, получавшие адъювантную или неоадъювантную терапию нестероидными ингибиторами ароматазы, если болезнь не рецидивировала на фоне или в течение 12 мес после завершения лечения. Критериями включения также были адекватная функция органа, функциональный статус 0-2, возможность измерять очаги заболевания согласно критериям RECIST или только костные поражения.
Конечные точки исследования
Первичной конечной точкой исследования был показатель ВБП, т.е. время от рандомизации до рентгенологически подтвержденного прогрессирования заболевания или смерти пациентки. Кроме того, оценивались общая выживаемость (ОВ), частота объективного ответа (ЧОО), объективный ответ, длительность ответа, уровень клинического ответа (полный ответ, частичный ответ, стабилизация болезни в течение ≥24 недель), фармакокинетика, биомаркеры, а также профиль безопасности препаратов.
Результаты
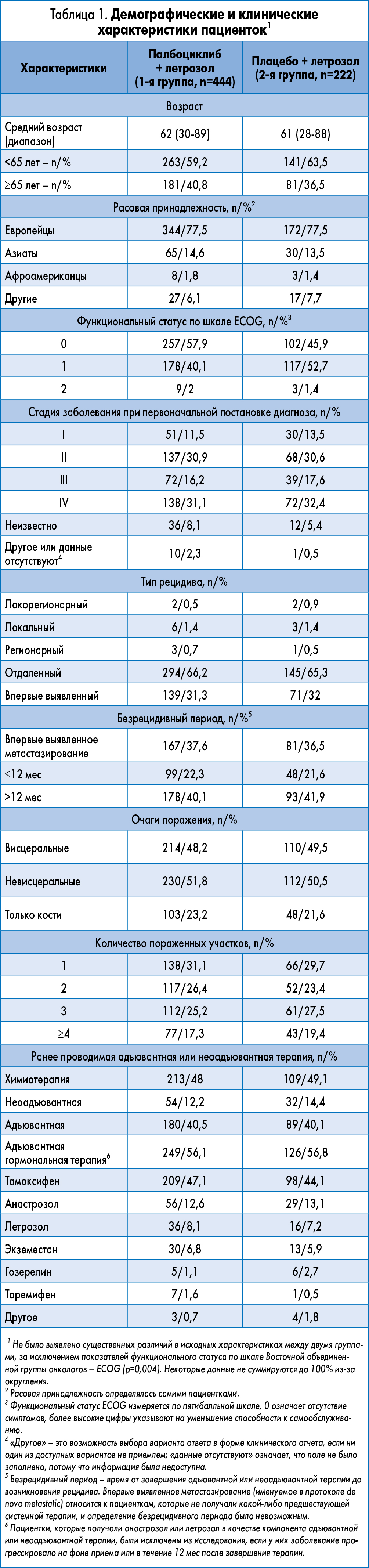
С февраля 2013 по июль 2014 г. 666 женщин из 17 стран были отобраны для исследования и рандомизированы в соотношении 2:1 на группу палбоциклиб + летрозол (1-я группа, 444 пациентки) и группу плацебо + летрозол (2-я группа, 222 пациентки). На этапе рандомизации исследовательские группы были хорошо сбалансированы относительно базовых характеристик пациенток (табл. 1). Средний возраст составлял 62 года в 1-й группе и 61 – во 2-й. У 48,6% всех пациенток диагностировано висцеральное поражение, 62,8% получали системную терапию, у 37,2% недавно диагностировано прогрессирование заболевания, у 40,7% безрецидивный период составил >12 мес, а у 22,1% – <12 мес. Чуть меньше половины пациенток получили химиотерапию в качестве адъювантной или неоадъювантной терапии, а 56,3% из них ранее получали адъювантную гормональную терапию.
На момент проведения окончательного анализа (26 февраля 2016 г.) прогрессирование заболевания или смерть произошли в 331 случае, из них 43,7% – в 1-й группе и 61,7% – во 2-й. Продолжали терапию 44,8% пациенток в группе палбоциклиба и 27,5% – в группе плацебо. Доза палбоциклиба была снижена в соответствии с протоколом в 36% случаев в 1-й группе, тогда как во 2-й снижение дозы плацебо требовалось в 1,4% случаев. Основной причиной прекращения лечения было прогрессирование заболевания, которое произошло у 38,7 и 56,3% в 1-й и 2-й группах соответственно. Полное прекращение лечения в результате неблагоприятных явлений на фоне приема палбоциклиба или плацебо произошло у 7,4 и 4,5% пациенток в 1-й и 2-й группах соответственно.
Нежелательные явления
Наиболее частыми нежелательными явлениями в 1-й группе были нейтропения, лейкопения, утомляемость, тошнота, артралгия и алопеция (табл. 2). За исключением случаев нейтропении и лейкопении, у 57% пациенток наблюдались неблагоприятные события с максимальной степенью тяжести 1 или 2 и 39,2% сообщили о событиях 3 или выше степени. Гематологические побочные эффекты включали в себя нейтропению (79,5 и 6,3% пациенток в 1-й и 2-й группе соответственно), лейкопению (39 и 2,3%), анемию (24,1 и 9%) и тромбоцитопению (15,5 и 1,4%). Гематологические нежелательные явления 3-й или 4-й степени тяжести: нейтропения (66,5 против 1,4%), лейкопения (24,8 против 0%), анемия (5,4 против 1,8%) и тромбоцитопения (1,6 против 0%).
![]() Фебрильная нейтропения 3 или 4 степени тяжести наблюдалась у 1,8% в 1-й группе, тогда как во 2-й не было отмечено ни одного случая. Наиболее частыми негематологическими побочными эффектами были утомляемость (37,4 против 27,5%), тошнота (35,1 против 26,1%) и артралгия (33,3 против 33,8%). У пациенток 1-й группы отмечалась более высокая, чем во 2-й, частота возникновения алопеции 1 степени (30,2 против 14,9%). Другие неблагоприятные события, частота которых также была выше в 1-й группе, – диарея (26,1 против 19,4%), кашель (25 против 18,9%) и стоматит (15,3 против 5,9%). Частота возникновения головной боли, так же, как и частота приливов, в 1-й группе были ниже, чем во 2-й (21,4 против 26,1% и 20,9 против 30,6% соответственно). Более чем у 2,5% пациенток 1-й группы не наблюдалось негематологических событий 3 или 4 степени.
Фебрильная нейтропения 3 или 4 степени тяжести наблюдалась у 1,8% в 1-й группе, тогда как во 2-й не было отмечено ни одного случая. Наиболее частыми негематологическими побочными эффектами были утомляемость (37,4 против 27,5%), тошнота (35,1 против 26,1%) и артралгия (33,3 против 33,8%). У пациенток 1-й группы отмечалась более высокая, чем во 2-й, частота возникновения алопеции 1 степени (30,2 против 14,9%). Другие неблагоприятные события, частота которых также была выше в 1-й группе, – диарея (26,1 против 19,4%), кашель (25 против 18,9%) и стоматит (15,3 против 5,9%). Частота возникновения головной боли, так же, как и частота приливов, в 1-й группе были ниже, чем во 2-й (21,4 против 26,1% и 20,9 против 30,6% соответственно). Более чем у 2,5% пациенток 1-й группы не наблюдалось негематологических событий 3 или 4 степени.
В целом серьезные побочные эффекты наблюдались у 19,6% пациенток 1-й группы и у 12,6% – 2-й. Тяжелая фебрильная нейтропения была зарегистрирована только у больных, получавших палбоциклиб + летрозол (1,6%). Легочная эмболия произошла у 0,9% пациенток 1-й группы и у 1,4% – 2-й. Смертельный исход наступил в 10 случаях в группе палбоциклиб + летрозол (2,3%) и в 4 случаях – в группе плацебо + летрозол (1,8%). Одна смерть во 2-й группе была связана с режимом исследования.
Эффективность комбинации палбоциклиба и летрозола
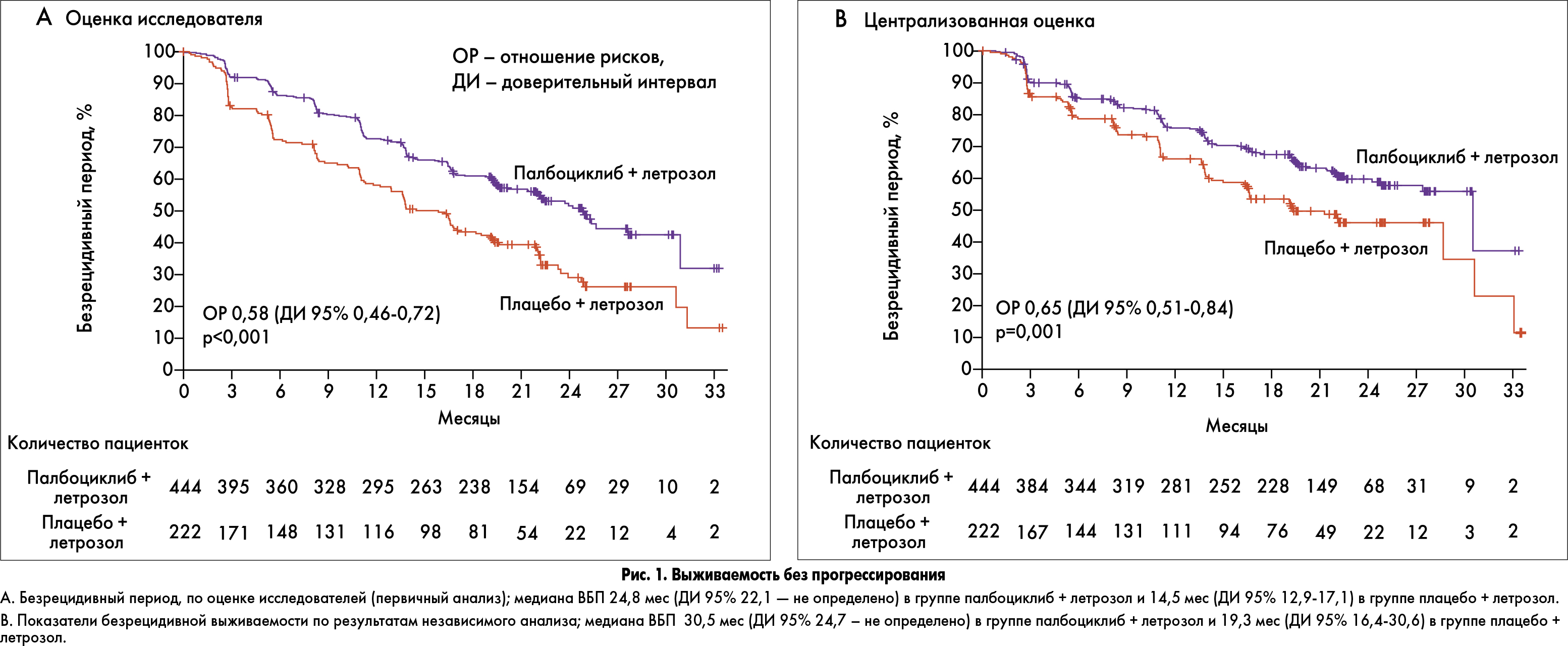
В исследовании PALOMA‑2 была достигнута первичная конечная точка, по результатам исследования медиана ВБП составила 24,8 мес (палбоциклиб + летрозол) и 14,5 мес (плацебо + летрозол), что также подтвердилось результатами независимого наблюдения. Медиана продолжительности наблюдения составила 23 мес (рис. 1.)
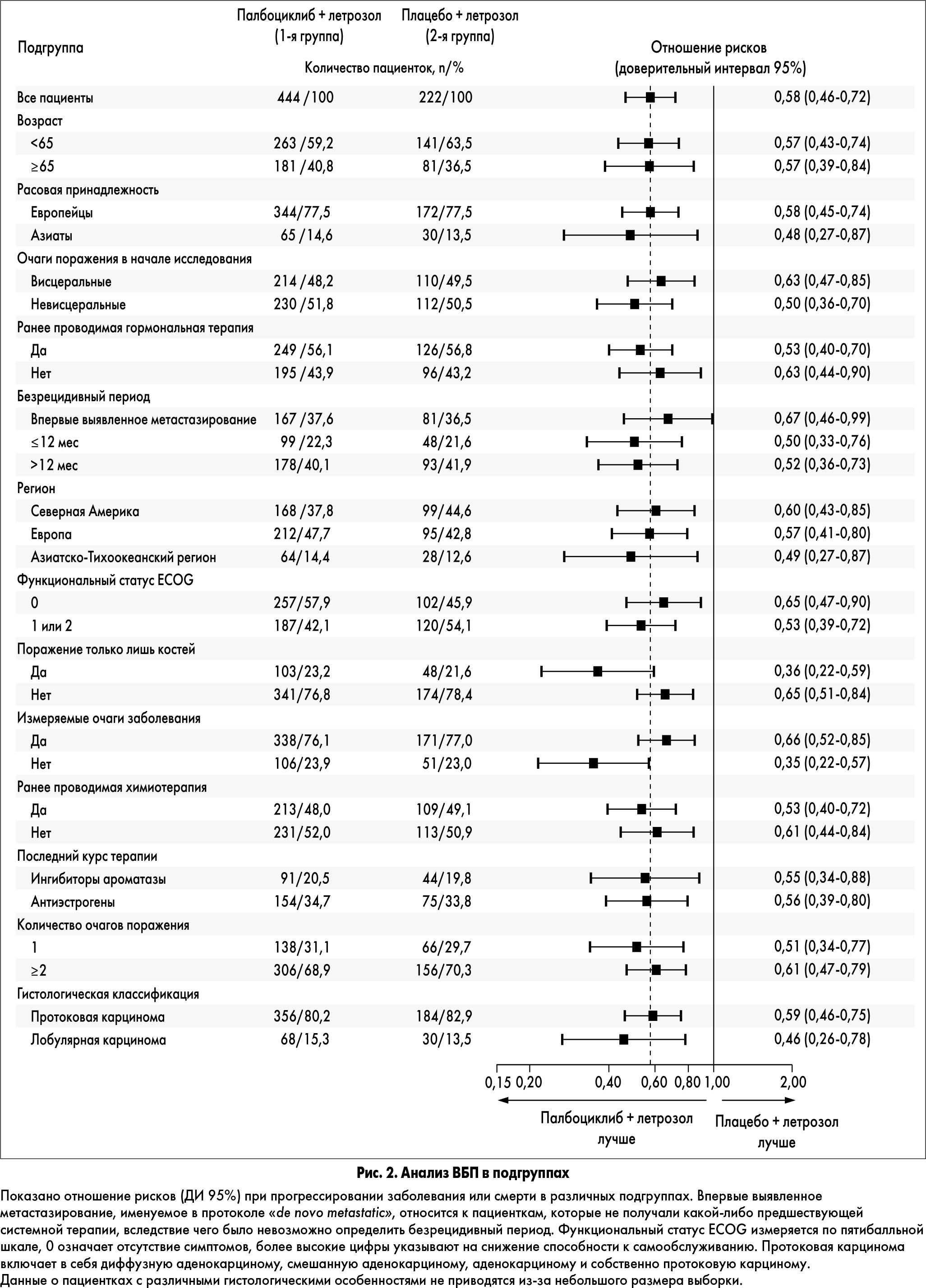
Анализ ВБП в подгруппах по факторам стратификации и другим исходным характеристикам подтвердил эффективность комбинации палбоциклиба и летрозола во всех подгруппах.
В анализ были включены пациентки с поражением (48,2% в 1-й группе против 49,5% во 2-й) и без поражения висцеральных органов (51,8 против 50,5%); пациентки, ранее получавшие гормональную терапию (56,1 против 56,8%), и те, которые ранее ее не получали (43,9 против 43,2%). Риск прогрессирования заболевания или смерти был также ниже в 1-й группе среди пациенток, у которых безрецидивный период составлял <12 мес (22,3 против 21,6%) и при безрецидивном периоде >12 мес (40,1 против 41,9%). В подгруппе пациенток с недавним метастазированием риск прогрессирования заболевания или смерти был ниже в 1-й группе: 37,6 против 36,5% (рис. 2).
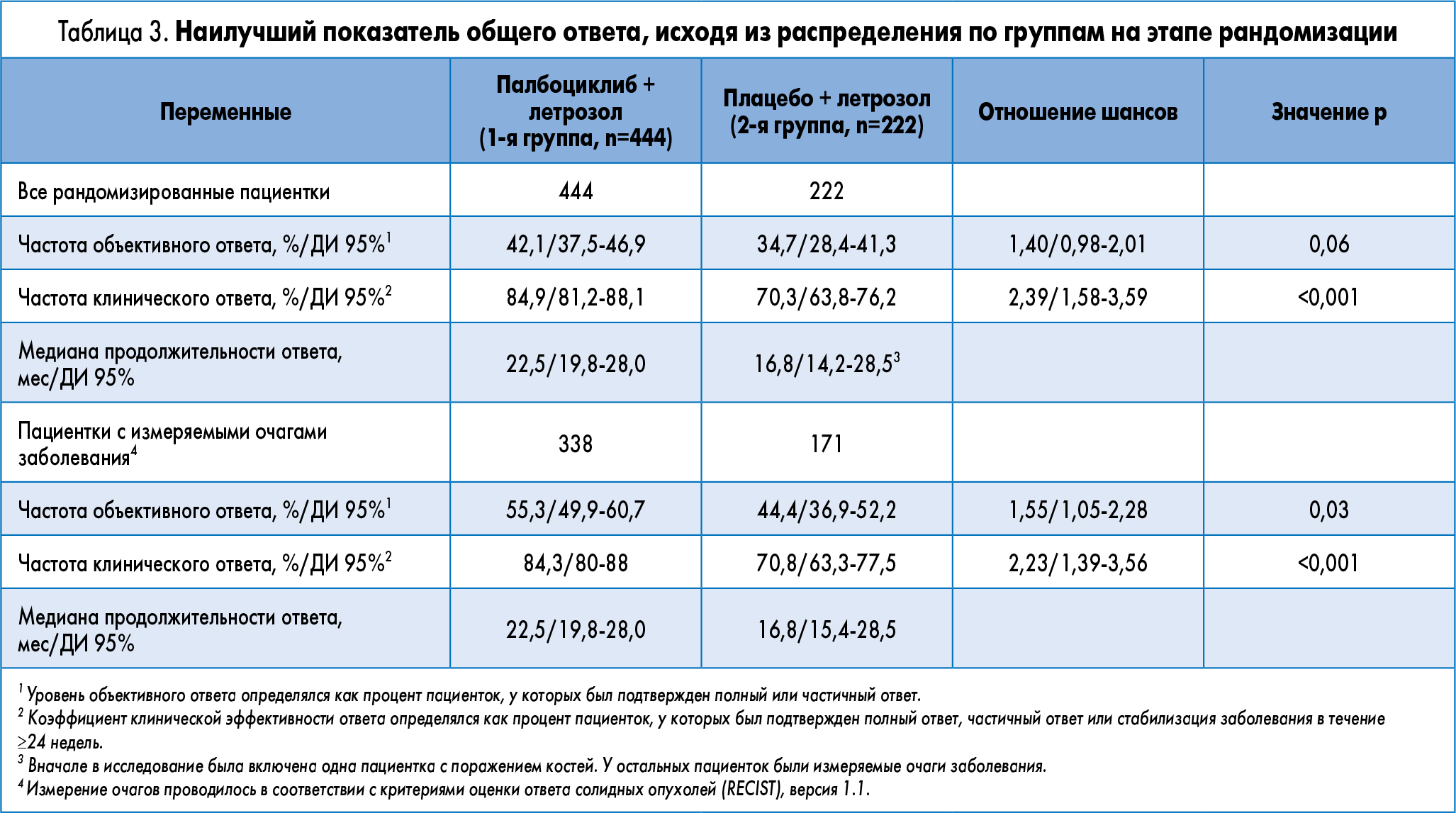
Показатель ЧОО был также выше в группе больных, получавших палбоциклиб + летрозол (42,1 против 34,7%), и среди пациенток с измеряемыми очагами заболевания согласно критериям RECIST (55,3 против 44,4% соответственно). Показатель частоты клинического ответа составил 84,9 и 70,3% в 1-й и 2-й группах соответственно (табл. 3).
Это подтверждает эффективность и безопасность комбинации палбоциклиба и летрозола в качестве первой линии терапии у женщин в постменопаузе с распространенным ER-позитивным РМЖ. Установлено также, что эффективность данной комбинации не зависит от возраста, общего состояния, распространенности заболевания, предшествующей химио- или гормональной терапии, длительности безрецидивного периода после адъювантной терапии или гистологического подтипа.
Таким образом, исследование PALOMA‑2 подтверждает полученные ранее данные о том, что палбоциклиб в сочетании с летрозолом приводит к значительному увеличению ВБП в сравнении с монотерапией летрозолом у женщин в постменопаузальном периоде с ER+/HER2- РМЖ, а ингибирование CDK4 и CDK6 эффективно в терапии первой линии. Применение этой комбинации в схемах клинических исследований может способствовать значительному улучшению результатов лечения пациенток с РМЖ.
Перевела с англ. Екатерина Марушко
Статья печатается в сокращении.
Finn R. S., Martin M., Rugo H.S. et al. Palbociclib and Letrozole in Advanced Breast Cancer, The New England Journal
of Medicine, 2016.
WUKIBR0317010
Напечатано при поддержке Pfizer. H.C.P Corporation
Тематичний номер «Онкологія» № 2 (48), квітень 2017 р.

Фебрильная нейтропения 3 или 4 степени тяжести наблюдалась у 1,8% в 1-й группе, тогда как во 2-й не было отмечено ни одного случая. Наиболее частыми негематологическими побочными эффектами были утомляемость (37,4 против 27,5%), тошнота (35,1 против 26,1%) и артралгия (33,3 против 33,8%). У пациенток 1-й группы отмечалась более высокая, чем во 2-й, частота возникновения алопеции 1 степени (30,2 против 14,9%). Другие неблагоприятные события, частота которых также была выше в 1-й группе, – диарея (26,1 против 19,4%), кашель (25 против 18,9%) и стоматит (15,3 против 5,9%). Частота возникновения головной боли, так же, как и частота приливов, в 1-й группе были ниже, чем во 2-й (21,4 против 26,1% и 20,9 против 30,6% соответственно). Более чем у 2,5% пациенток 1-й группы не наблюдалось негематологических событий 3 или 4 степени.