Стаття у форматі PDF.
Сучасна анестезіологічна практика поширилася на такі напрями, як ведення післяопераційного болю і хірургічна
анестезія поза операційною. Післяопераційна аналгезія може істотно полегшувати гострий біль, викликаний
хірургічною травмою, зменшувати дискомфорт і стрес, підвищувати задоволеність пацієнтів і знижувати витрати на їх
реабілітацію. Високої ефективності післяопераційної аналгезії за мінімальних побічних ефектів можна досягти завдяки
застосуванню збалансованої мультимодальної аналгезії.
Збалансована мультимодальна аналгезія передбачає одночасне використання двох і більше аналгетиків, що мають різні механізми дії і дозволяють досягти адекватного знеболення за мінімальних побічних ефектів, пов’язаних із призначенням великих доз аналгетика в монотерапії. У сучасній онкологічній практиці мультимодальна аналгезія є методом вибору для знеболювання тих пацієнтів, яким проводиться хірургічне втручання.
Парекоксиб натрію – перший специфічний інгібітор циклооксигенази 2 типу (ЦОГ‑2), доступний в ін’єкційній формі. Після введення в організм людини парекоксиб зазнає ферментативного гідролізу в печінці з утворенням активного метаболіту вальдекоксибу. Останній діє як селективний інгібітор ЦОГ‑2 щодо простагландинів як на периферичному, так і на центральному рівнях.
Парекоксиб за ефективністю перевершує неселективні нестероїдні протизапальні препарати і, на відміну від них, практично не впливає на агрегацію тромбоцитів і функцію гастроінтестинального тракту. Важливо, що парекоксиб забезпечує контроль болю не лише в спокої, а й під час рухів, що створює передумови для ранньої мобілізації пацієнтів і швидкого відновлення їх фізіологічних функцій в післяопераційному періоді. Крім того, останніми роками отримано обнадійливі дані, що свідчать про його протипухлинну активність.
У клінічних дослідженнях парекоксиб застосовували як у монотерапії, так і в комбінації з опіоїдами або іншими аналгетиками для контролю легкого і помірного болю у пацієнтів при мініінвазивних хірургічних втручаннях. Результати цих досліджень свідчать про те, що комбінування парекоксибу з парентеральними опіоїдами підвищує ефективність знеболення і знижує сумарні дози препаратів при веденні та профілактиці післяопераційного болю. Загалом завдяки своїм характеристикам парекоксиб можна вважати оптимальним вибором відповідно до принципів збалансованої мультимодальної аналгезії.
Мета дослідження, проведеного L. Nong і співавт. (2013), – вивчення ефективності та безпеки парекоксибу при його застосуванні в комбінації з морфіном та оцінка його опіоїдзберігаючого ефекту в пацієнток, яким проводяться хірургічні втручання з приводу пухлин жіночих статевих органів.
Критеріями включення в дослідження були вік пацієнток – від 18 до 60 років – і соматичний статус I-II за класифікацією Американського товариства анестезіологів (ASA). Показаннями до хірургічного втручання були міома матки, рак тіла або шийки матки, карцинома фалопієвої труби або пухлина яєчника.
Жінок (n=79) було рандомізовано на дві групи. Пацієнткам основної групи призначили парекоксиб натрію 40 мг (2 мл) внутрішньовенно за 30 хв до індукції анестезії з подальшим введенням 40 мг кожні 12 год протягом 48 год після операції. Хворі контрольної групи отримували фізіологічний розчин 2 мл внутрішньовенно як плацебо з такою самою періодичністю введення.
За день до хірургічного втручання пацієнткам пояснили принципи використання пристрою ПКА (пацієнт-контрольованої аналгезії) і видали опитувальники, призначені для оцінки післяопераційного болю і несприятливих подій за візуально-аналоговою шкалою (ВАШ).
В операційній залі всі пацієнтки отримували пенехіклідин 0,5 мг внутрішньовенно. Анестезію індукували фентанілом (4 мкг/кг), мідазоламом (0,1 мг/кг), пропофолом (2 мг/кг) і рокуронієм (0,6 мг/кг). Після оротрахеальної інтубації анестезію підтримували севофлураном 2-3% (концентрація в кінці видиху), фентанілом (1-2 мкг/кг/год) і цизатракурієм (1-2 мкг/кг/год). Дози препаратів автоматично коригував апарат MT Monitor Technik для досягнення рівня Narcotrend D2-E0.
Внутрішньовенну ПКА морфіном починали відразу після того, як пацієнтка була здатна контролювати помпу, і припиняли через 48 год після операції. Апарат ПКА було запрограмовано на болюсне введення 1 мл морфіну (1 мг/мл) на вимогу з мінімальними інтервалами 5 хв і лімітом 10 мг/год. Анестетики та інші потенційні коаналгетики інтраопераційно і протягом 48 год після операції не призначали. Однак пацієнтки з дуже інтенсивним болем, який неадекватно контролювався ПКА морфіном, мали можливість вийти з дослідження і отримати додаткову аналгезію.
Через 2, 6, 12, 24 і 48 год після операції здійснювали оцінку болю за ВАШ (0 – біль відсутній; 10 – найбільш інтенсивний біль), кумулятивного споживання морфіну, седації і несприятливих подій. Крім того, визначали ступінь задоволеності пацієнток знеболенням (0 – незадовільно; 10 – найбільша задоволеність) і тяжкість побічних ефектів (нудоти/блювання, свербежу, тремору і седації). Побічні ефекти коригували на вимогу пацієнток. При нудоті та блюванні призначали ондансетрон 4 мг внутрішньовенно.
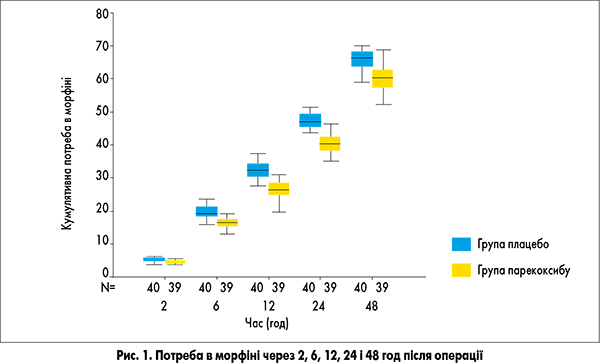
Аналіз споживання морфіну показав, що пацієнтки, які отримували парекоксиб натрію 40 мг кожні 12 год, потребували значно менше морфіну, ніж ті хворі, яким вводили плацебо, через 2, 6, 12, 24 і 48 год після операції (р<0,05) (рис. 1). Порівняно з групою плацебо, у групі парекоксибу сумарні потреби в морфіні були нижчими приблизно на 9%.
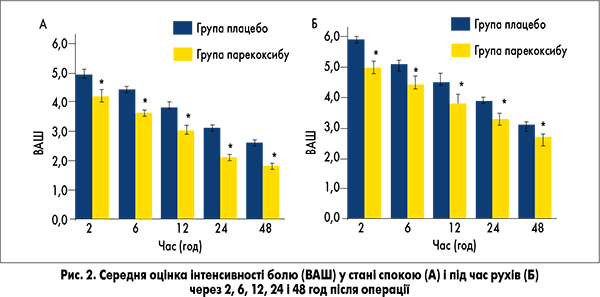
Інтенсивність болю у пацієнтів у стані спокою і під час рухів була значно нижчою в групі парекоксибу порівняно з групою плацебо у всіх точках часу після операції (р<0,05) (рис. 2). Отже, парекоксиб натрію, який призначається в комбінації з морфіном, забезпечує більш ефективне полегшення післяопераційного болю порівняно із застосуванням тільки морфіну.
Загальна задоволеність пацієнток післяопераційним веденням болю в основній і контрольній групах становить 8,6 vs 6,8 відповідно, різниця між групами є статистично значущою (р<0,001).
Несприятливі події моніторували протягом 48 год після операції. У групі парекоксибу спостерігалася тенденція до зниження частоти таких опіоїд-індукованих побічних ефектів, як нудота (8 vs 15% у групі плацебо), блювання (5 vs 10%), свербіж (3 vs 5%) і седація (13 vs 20%). Інших серйозних побічних ефектів протягом проведення дослідження не зареєстровано.
Таким чином, результати дослідження підтвердили те, що Династат® (парекоксиб) має характеристики, необхідні для мультимодальної аналгезії. У пацієнток онкогінекологічного профілю, котрим проводять великі хірургічні втручання, періопераційна аналгезія з включенням парекоксибу покращує контроль післяопераційного болю і зменшує потребу в опіоїдах із тенденцією до зниження частоти післяопераційних несприятливих подій.
За матеріалами статті: Nong L., Sun Y., Tian Y. et al. Effects of parecoxib on morphine analgesia after gynecology tumor operation: a randomized trial of parecoxib used in postsurgical pain management. J Surg Res. 2013 Aug; 183 (2): 821-6.
Підготував Олександр Гладкий
Статтю надруковано за підтримки Представництва «Файзер Ейч.Сі.Пі. Корпорейшн» в Україні.
WUKDYN0317032