25 вересня, 2017
Хроническая мезентериальная ишемия: нюансы диагностики и консервативной терапии
 Хроническая мезентериальная ишемия (ХМИ) является достаточно редким сосудистым заболеванием, характеризующимся медленным, постепенным началом и неспецифичностью клинической симптоматики, что обусловливает несвоевременную диагностику этой патологии. В отличие от острой мезентериальной ишемии, развивающейся вследствие эмболии, тромбоза или неокклюзионной ишемии, ХМИ возникает в результате прогрессирующей атеросклеротической обструкции или окклюзии сосудов. Несмотря на значительную распространенность случаев атеросклеротического поражения мезентериальных сосудов в общей популяции, клинические признаки ХМИ могут не проявляться вплоть до терминальной стадии заболевания, что обусловлено формированием экстенсивного коллатерального кровотока (М. Mathur и соавт., 2016).
Хроническая мезентериальная ишемия (ХМИ) является достаточно редким сосудистым заболеванием, характеризующимся медленным, постепенным началом и неспецифичностью клинической симптоматики, что обусловливает несвоевременную диагностику этой патологии. В отличие от острой мезентериальной ишемии, развивающейся вследствие эмболии, тромбоза или неокклюзионной ишемии, ХМИ возникает в результате прогрессирующей атеросклеротической обструкции или окклюзии сосудов. Несмотря на значительную распространенность случаев атеросклеротического поражения мезентериальных сосудов в общей популяции, клинические признаки ХМИ могут не проявляться вплоть до терминальной стадии заболевания, что обусловлено формированием экстенсивного коллатерального кровотока (М. Mathur и соавт., 2016).
Распространенность ХМИ в общей популяции относительно невелика, но она значительно возрастает с 6% у 40-летних пациентов до 14% у 60-летних больных, достигая максимума у лиц старше 75 лет – у 18-67% (J. Kolkman и соавт., 2017).
Особенности мезентериального кровообращения
Мезентериальное кровообращение осуществляется посредством трех основных артерий, отходящих от абдоминального отдела аорты: чревного ствола (ЧС), верхней мезентериальной артерии (ВМА) и нижней мезентериальной артерии (НМА). Как правило, ЧС отходит от аорты на высоте Th12-L1 и делится на левую желудочную, селезеночную и общую печеночную артерии. Таким образом ЧС обеспечивает кровоснабжение печени, селезенки, желудка, двенадцатиперстной кишки, поджелудочной железы. ВМА отходит от аорты на 1-2 см ниже ЧС и разделяется на ветви, отходящие к поджелудочной железе, органам желудочно-кишечного тракта (ЖКТ) от двенадцатиперстной кишки до селезеночного изгиба ободочной кишки.
НМА отходит от аорты на уровне L3, возле места бифуркации подвздошной артерии, и разделяется на ветви, обеспечивающие кровоснабжение толстого кишечника от селезеночного изгиба ободочной кишки до прямой кишки (рис. 1). Вызывают интерес особенности мезентериального кровообращения, описанные в работе Someya и соавт. (2008). Исследователи установили, что натощак скорость кровотока в ЧС составляет 450 мл/мин, а после приема пищи увеличивается до 700 мл/мин (пиковые значения наблюдаются спустя 10 мин после еды).
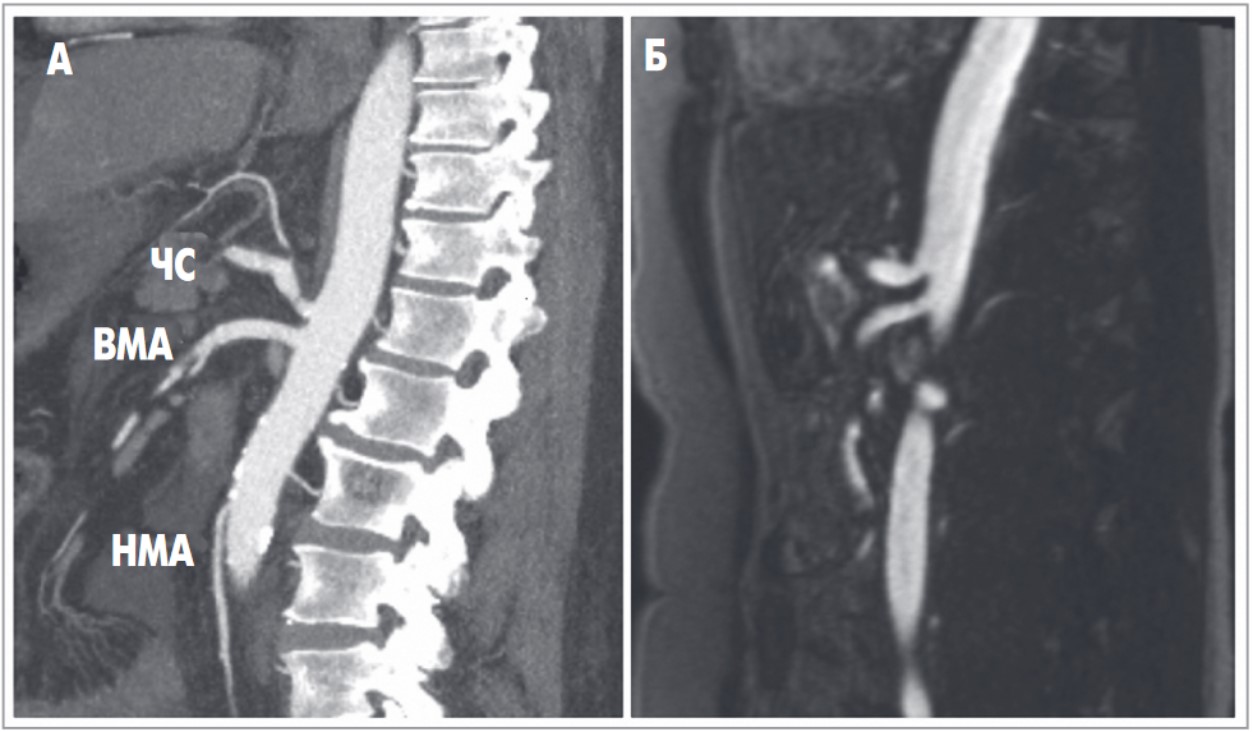
Рис. 1. Мезентериальные ветви аорты
А – на абдоминальном КТ-скане, выполненном с внутривенным (в/в) контрастированием, визуализируется незначительное сужение ЧС, ВМА и НМА; Б – на МРТ живота после в/в введения контраста, содержащего гадолиний, визуализируются неизменные ЧС и ВМА, а НМА не визуализирована (М. Mathus et al., 2016).
В ВМА кровоток возрастает в среднем с 400 до 800 мл/мин (пиковые показатели регистрируются через 40 мин) и может сохраняться на таком уровне в течение 3 ч. Ученые утверждают, что увеличение скорости кровотока зависит от объема и характера съеденной пищи: максимальные постпрандиальные пики зафиксированы после приема жирной пищи (белки по сравнению с жирами и углеводами вызывают менее значимые изменения этого показателя). ЧС, ВМА и НМА обеспечивают адекватное кровоснабжение органов брюшной полости (ОБП), а при возникновении обструкции они способны компенсировать сосудистый дефицит посредством формирования коллатералей.
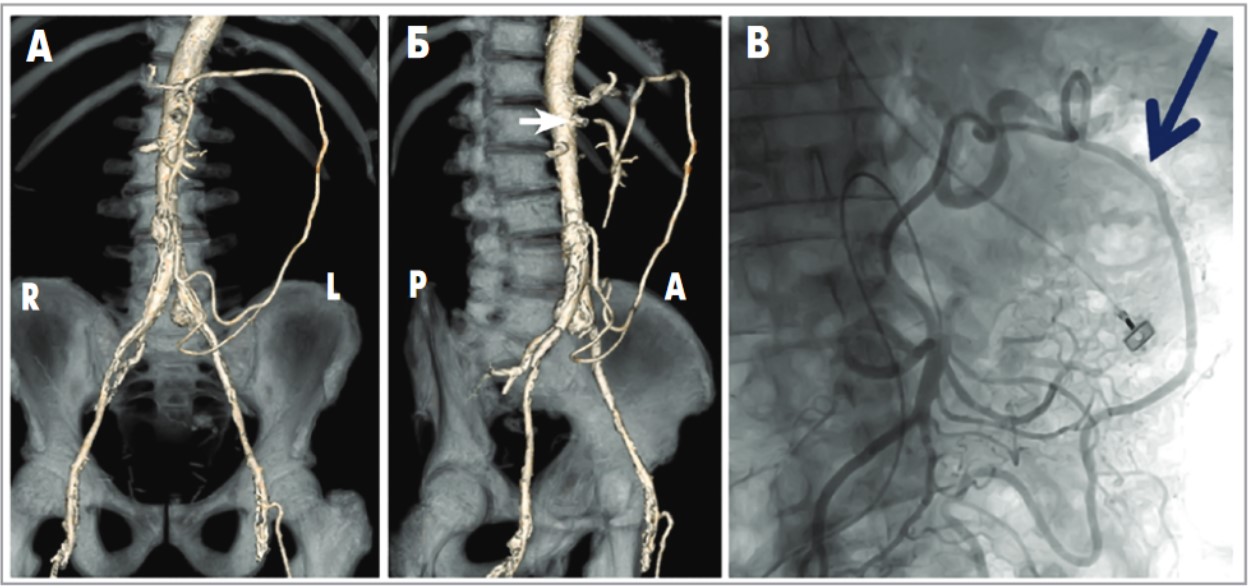
Рис. 2. Коллатеральный кровоток (арка Риолана)
А – на абдоминальном КТ-скане после в/в контрастирования (3D-реконструкция) визуализируется арка Риолана; Б – тот же пациент, те же анатомические образования, под другим углом видна окклюзия ВМА (белая стрелка); В – селективная абдоминальная ангиография ВМА у другого пациента. Видна арка Риолана (синяя стрелка) (М. Mathus et al., 2016).
Наиболее часто коллатерали формируются между ВМА и НМА, при этом образуются так называемые арка Риолана (рис. 2) и маргинальная (пристеночная) артерия Драммонда (рис. 3). Визуализация указанных сосудов по данным ангиогра- фии может свидетельствовать об окклюзии ВМА или НМА. Панкреатико-дуоденальная дуга является еще одной системой коллатералей, возникающей между ЧС и ВМА (рис. 4).
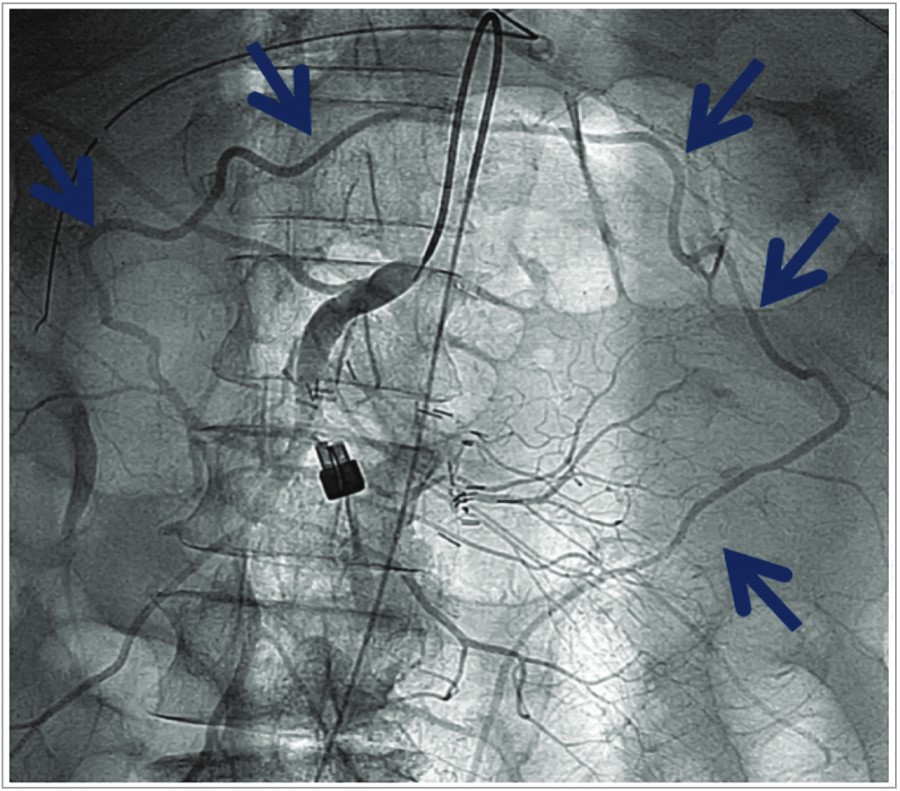
Рис. 3. Коллатеральный кровоток – маргинальная артерия Драммонда. При селективном введении контраста в ВМА визуализируется маргинальная артерия Драммонда, что свидетельствует о высокой степени стеноза НМА
(М. Mathus et al., 2016)
У пациентов, перенесших абдоминальное хирургическое вмешательство или эндоваскулярное лечение аневризмы аорты, источники образования коллатерального кровотока могут изменяться: в таких случаях компенсация кровотока осуществляется посредством альтернативных сосудов.
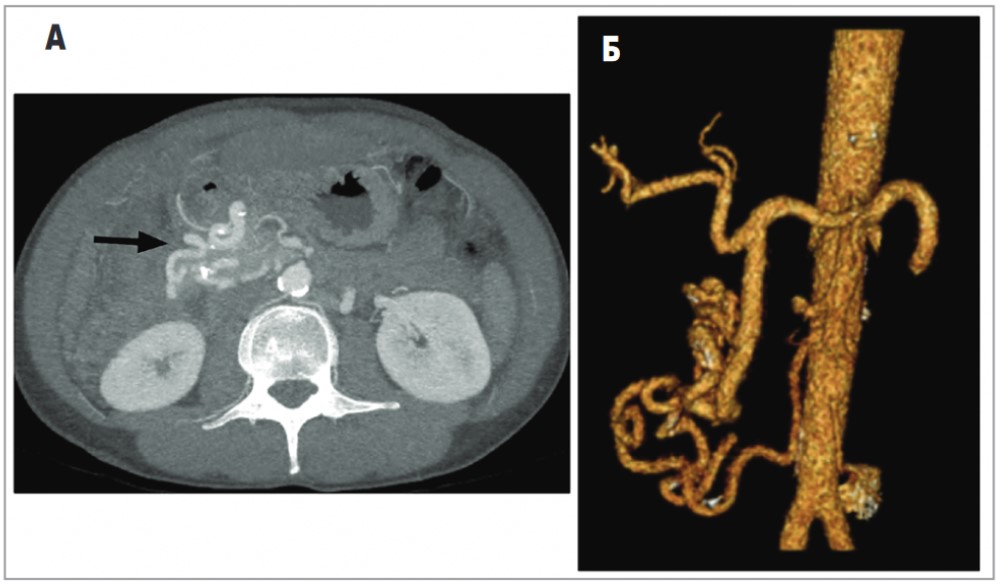
Рис. 4. Коллатеральный кровоток – панкреатико-дуоденальная дуга
А – на абдоминальном КТ-скане после в/в введения контраста визуализируется выраженный коллатеральный кровоток в области панкреатико-дуоденальных артерий у пациента с окклюзией ЧС;
Б – КТ-скан (3D-реконструкция) того же пациента с выраженным коллатеральным кровотоком в области панкреатико-дуоденальной дуги (М. Mathus et al, 2016).
Этиология
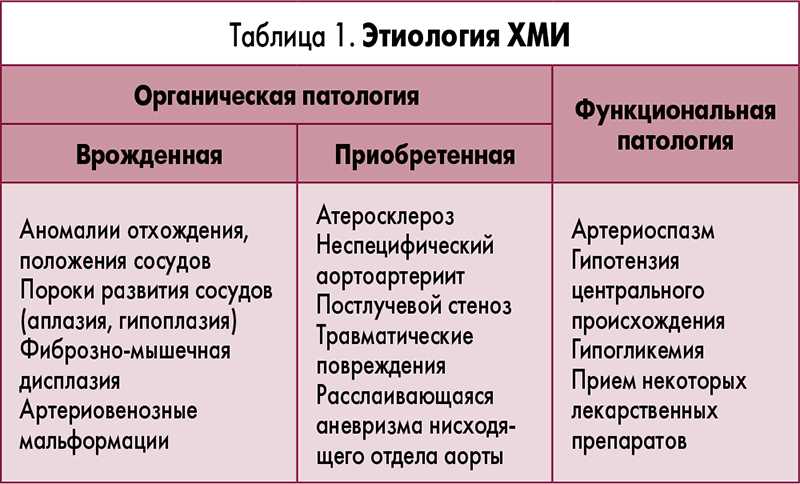 Наиболее распространенной причиной стеноза мезентериальных артерий является атеросклеротическое поражение сосудов, менее частой – васкулиты и фибро-мышечная дисплазия (А.В. Азаров, 2017) (табл. 1).
Наиболее распространенной причиной стеноза мезентериальных артерий является атеросклеротическое поражение сосудов, менее частой – васкулиты и фибро-мышечная дисплазия (А.В. Азаров, 2017) (табл. 1).
Необходимо упомянуть о синдроме срединной дугообразной связки, при котором это важное анатомическое образование, являющееся частью диафрагмы, во время вдоха или выдоха сдавливает ЧС, уменьшая тем самым приток крови к мезентериальным сосудам и провоцируя развитие ХМИ. Факторы риска атеросклеротического поражения мезентериальных сосудов хорошо известны: артериальная гипертония, гиперлипидемия, избыточная масса тела, курение.
Клиническая картина
Пациенты с ХМИ – это, как правило, пожилые люди, старше 50 лет, имеющие такую сопутствующую патологию, как ишемическая болезнь сердца, сахарный диабет (СД), артериальная гипертония, заболевания почек и/или ассоциированные с ними факторы риска (гиперлипидемия, курение, ожирение, малоподвижный образ жизни).
Наиболее типичной жалобой больных с ХМИ является спастическая постпрандиальная боль (90% случаев), которая возникает, как правило, сразу после приема пищи и продолжается от 30 мин до 2 ч (уменьшение или увеличение (4-6 ч) продолжительности болевого синдрома нехарактерно для ХМИ). В ряде случаев появление боли провоцируют стресс или физические нагрузки. Интенсивный болевой синдром вынуждает пациентов принимать пищу небольшими порциями, отказаться от жиров, пропускать приемы пищи, что, в конечном итоге, приводит к появлению ситофобии (страха перед едой) и снижению массы тела, мальнутриции.
Некоторые пациенты (7-35%) предъявляют жалобы на появление необъяснимой диареи или постпрандиальное вздутие живота, что менее типично для ХМИ и может быть признаком функциональной диспепсии, синдрома раздраженного кишечника, гастропареза. Клиническая картина заболевания при вовлечении в патологический процесс одного сосуда или поражении нескольких артерий существенно не отличается, за некоторым исключением: при тяжелом многососудистом поражении абдоминальный болевой синдром становится более продолжительным (5-6 ч), нарастает слабость и усиливается диарея. Такие пациенты входят в группу риска по развитию острого инфаркта толстого кишечника. J. Kolkman и соавт. (2017) рекомендуют рассматривать их как больных с неотвратимой острой мезентериальной ишемией (так называемой острой-хронической мезентериальной ишемией).
В ряде случаев ХМИ может протекать «под маской» рецидивирующих гастродуоденальных язв неопределенного генеза или правостороннего колита. У таких пациентов не обнаруживаются признаки инфицирования Helicobacer pylori, в анамнезе отсутствуют упоминания о приеме нестероидных противовоспалительных препаратов. Проявления хронической ишемии правых отделов толстого кишечника, вызванных стенозом ВМА, иногда очень трудно отличить от таковых при болезни Крона. ХМИ следует заподозрить у пациентов старческого возраста с первые выявленной болезнью Крона.
Указанная клиническая симптоматика не является строго специфичной для ХМИ и может наблюдаться при различных гастроэнтерологических заболеваниях (язвенной болезни, функциональной диспепсии, синдроме раздраженного кишечника, хроническом панкреатите, воспалительных заболеваниях кишечника, неопластическом синдроме). Неспецифичная клиническая картина приводит к поздней диагностике заболевания. По данным J. Kolkman и соавт. (2017), многие пациенты на протяжении 20-25 мес предъявляют «типичные» для ХМИ жалобы, но получают лечение по поводу другой патологии.
Диагностика
Диагностика ХМИ основывается на детализации жалоб пациента, тщательном анализе анамнеза болезни, данных, полученных с использованием современных инструментальных методов исследования.
При сборе жалоб у пациента следует уточнить:
– является ли болевой синдром постпрандиальным или боль возникает сразу после приема пищи;
– снизилась ли масса тела (если да, то обусловлено ли это ситофобией);
– изменилось ли привычное пищевое поведение (уменьшился объем потребляемой пищи, участились приемы пищи, снизилось содержание жиров и т.п.);
– появилась ли диарея неустановленной этиологии. Наличие жалоб на протяжении длительного периода, а также сопутствующей кардиологической патологии увеличивает вероятность развития ХМИ.
Тем не менее изолированное использование анамнеза болезни не позволяет с высокой точностью спрогнозировать наличие у пациента ХМИ.
При аускультации живота примерно у половины больных с ХМИ может быть выявлен систолический шум, определяемый в точке, расположенной посередине линии, условно проведенной от мечевидного отростка до пупка, что соответствует локализации верхней брыжеечной артерии, у них также могут усиливаться кишечные шумы после еды. Следующим этапом при подозрении на ХМИ является инструментальная оценка анатомии мезентериальных сосудов, в том числе определение степени и природы стеноза (атеросклероз, внешняя компрессия), а также наличия и степени выраженности коллатералей. С этой целью используются дуплексная ультрасонография, компьютерная томография (КТ), магнито-резонансная томография (МРТ), ангиография.
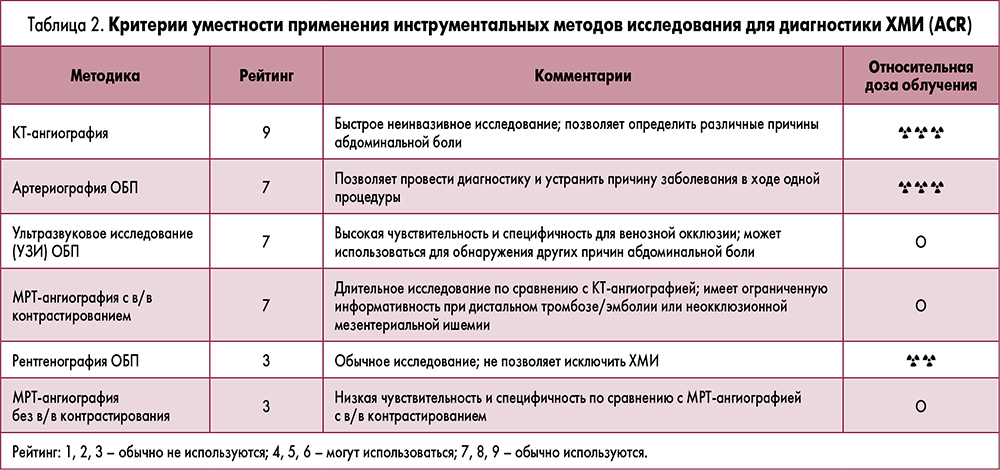
Эксперты Американской коллегии радиологов под руководством I. Oliva (ACR) сформулировали критерии уместности применения инструментальных методов исследования для диагностики ХМИ (табл. 2). Как правило, обследование больного с подозрением на ХМИ начинается с УЗИ ОБП и дополняется дуплексной ультрасонографией, КТ-ангиографией, МРТ-ангиографией. Современная цифровая обработка и возможность 3D-реконструкции изображения делают КТ чрезвычайно информативным методом исследования, единственным недостатком которого является высокая лучевая нагрузка. МРТ-ангиография также может использоваться при диагностике ХМИ, однако эффективность данной методики зависит от применения контрастных веществ; их использование (желательно использование гадолиний- содержащих препаратов) позволяет повысить чувствительность и специфичность исследования в обнаружении патологии проксимальных мезентериальных сосудов почти до >90%.
Селективная мезентериальная ангиография остается золотым стандартом диагностики ХМИ, особенно при поражении дистальных сосудов или планировании одновременного эндоваскулярного вмешательства. Ранее широко использовались алиментарные провокационные пробы, основанные на тесной взаимосвязи болевого синдрома и приема пищи, а также провокационные пробы с физической нагрузкой или лекарственными средствами (вазоспастическими препаратами), провоцировавшими развитие абдоминального ишемического синдрома. В настоящее время эти функциональные пробы используются достаточно редко.
Лечение
Консервативная терапия
Один из наиболее простых способов улучшения самочувствия больных с ХМИ заключается в уменьшении притока крови в пораженные мезентериальные сосуды после еды, что достигается уменьшением количества потребляемой пищи, сокращением доли жиров и увеличением частоты приема пищи. Как правило, больные самостоятельно изменяют свое привычное пищевое поведение подобным образом, чтобы облегчить абдоминальную боль. При ХМИ следует воздержаться от увеличения калорийности рациона, так как это может повлечь за собой усиление ишемии и даже спровоцировать развитие эпизода острой мезентериальной ишемии.
J. Kolkman и соавт. (2017) рекомендуют больным c ХМИ назначать ингибиторы протонной помпы с целью уменьшения интенсивности болевого синдрома. Для этого же могут использоваться периферические вазодилататоры – пероральные нитраты, обладающие свойством незначительно увеличивать просвет сосуда и уменьшать выраженность абдоминальной боли.
Следующим шагом в лечении пациента c ХМИ должен стать его отказ от курения, так как доказано, что никотин способствует прогрессированию атеросклероза и усилению мезентериальной ишемии. Консервативная терапия ХМИ должна быть направлена на контролирование факторов риска развития и прогрессирования атеросклероза (гипертонии, гиперхолестеринемии, гипергликемии) и модификацию образа жизни пациента. Увеличение физической активности, умеренное употребление алкоголя и поваренной соли, насыщение рациона здоровой пищей (фруктами, овощами), сокращение доли углеводов и красного мяса позволяют предотвратить появление избыточной массы тела и снизить вероятность развития ХМИ.
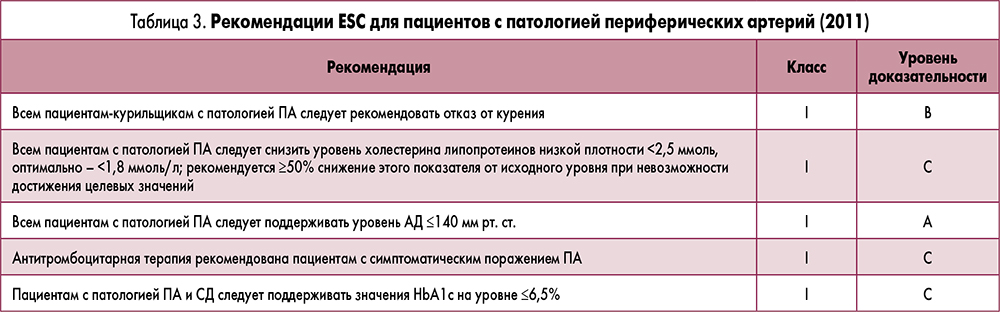
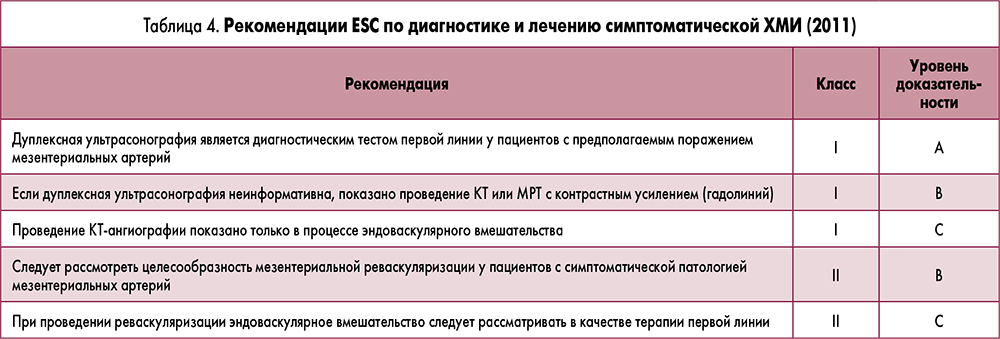
Дальнейшая тактика ведения пациентов с ХМИ частично регламентируется общими положениями практического руководства Европейского общества кардиологов (ESC) по диагностике и лечению атеросклероза периферических артерий (ПА), которые представлены в таблицах 3-4. При тяжелом течении заболевания и выраженной нутритивной недостаточности в качестве поддерживающей терапии может использоваться тотальное парентеральное питание, проводиться коррекция дефицита витаминов и минералов.
Несмотря на то что рекомендации экспертов ESC не предусматривают коррекцию нутривной недостаточности, больным с ХМИ показана симптоматическая терапия, направленная на улучшение функционального состояния органов пищеварения и компенсацию мальабсорбции в тонком кишечнике. С этой целью могут применяться панкреатические ферментные препараты в форме минимикросфер, репаранты и антиоксиданты. Проведение консервативного лечения ХМИ оправдано только при условии компенсации мезентериального кровообращения, при отсутствии перитонеальной симптоматики или невозможности проведения оперативного вмешательства (нежелание пациента, высокий риск развития послеоперационных осложнений/летальности у больных с тяжелой сопутствующей соматической патологией). Неэффективность медикаментозной терапии, прогрессирующее сужение просвета сосудов, несостоятельность коллатерального кровообращения являются показаниями к проведению оперативного вмешательства.
Оперативное лечение
Хирургическое вмешательство при ХМИ рекомендуется выполнять при наличии выраженной клинической симптоматики, свидетельствующей о суб- или декомпенсации мезентериального кровообращения.
Как правило, используются несколько видов оперативного лечения:
– условно-реконструктивные (декомпрессионные) техники;
– реконструктивные операции (шунтирование, реимплантация, протезирование, эндартерэктомия);
– эндоваскулярные вмешательства (реканализация, стентирование).
Нарушения кровотока, вызванные органическим сужением сосудов, могут быть устранены только в специализированных отделениях сосудистой хирургии оперативным путем с помощью наложения обходных анастомозов из сосудистых протезов и трансплантатов. Прогноз у пациентов с ХМИ всегда серьезный, поскольку прогрессирование нарушения проходимости мезентериальных артерий может привести к инфаркту кишечника, перитониту и стать причиной летального исхода. Своевременно выполненное оперативное вмешательство в большинстве случаев позволяет достичь выздоровления больного и восстановления его трудоспособности.
Литература
1. Jeroen J. Kolkman Diagnosis and treatment of chronic mesenteric ischemia: An update. Best Practice & Research Clinical Gastroenterology 31 (2017); 49e57.
2. Mathur М. Role of Endovascular Therapies in Chronic Mesenteric Ischemia: Current Status and Technical Considerations. http://www.acc.org/latest-incardiology/articles/20...
3. Someya N., Endo M.Y., Fukuba Y. and Hayashi N. Blood flow responses in celiac and superior mesenteric arteries in the initial phase of digestion. Am J Physiol Regul Integr Comp Physiol. 2008; 294: R1790-R1796.
4. Азаров А.В. Абдоминальная ишемия (angina abdominalis): патогенез, клиника, диагностика и лечение // Курс «Основы интервенционной радиологии»; 23-25 марта 2017 г. – Суздаль.
5. Oliva I.B. American College of Radiology. ACR Appropriateness Criteria Imaging of Mesenteric Ischemia.
6. ESC Guidelines on the diagnosis and treatment of peripheral artery diseases. Michal Tendera. European Heart Journal, 2011; 32: 2851-2906.
Тематичний номер "Гастроентерологія, Гепатологія, Колопроктологія" № 3 (45) вересень 2017 р.