Статья в формате PDF
Храни премного печень – от нее всех органов зависит бытие.
Запомни: в ней основа всех основ, здоров дух печени – и организм здоров
Абу Али ибн Сина (Авицена)
Хронические заболевания печени (ХЗП) являются весьма распространенной патологией. Кроме достаточно известных факторов риска развития ХЗП, таких как вирусы, генетические, иммунные, метаболические нарушения, все большее внимание уделяется взаимосвязи между патологией печени и факторами окружающей среды.
Наряду с химическими веществами, оказывающими токсическое действие на ткань печени, особе место занимают алкоголь и лекарственные средства, с которыми человек контактирует чаще, чем с химическими агентами, а также курение (сигаретный дым).
Алкогольная болезнь печени является одним из наиболее серьезных последствий хронического злоупотребления алкоголем. Цирроз печени как кульминация болезни – одна из ведущих причин смерти в западных странах. В США до 48% случаев летального исхода при циррозе печени обусловлены алкогольной этиологией заболевания. Ежегодно от заболеваний печени, вызванных алкоголем, в развитых странах Запада умирает около 2 млн человек.
Основным токсическим продуктом метаболизма этанола является ацетальдегид, который играет ключевую роль в повреждении печени. Вступая напрямую в химическую связь с целым рядом внутриклеточных компонентов, прежде всего белками, нарушая их функции и образуя новые молекулы с антигенными свойствами (малоновый диальдегид, 4-гидроксиноненал и др.), он способствует иммуно-опосредованному поражению печени. В процессе образования и утилизации ацетальдегида происходит восстановление никотинамиддинуклеотида (NAD в NADН), что приводит к выраженному нарушению метаболизма жиров и углеводов, накоплению в клетках печени триглицеридов и развитию стеатоза. Кроме того, ацетальдегид является одним из факторов, активирующих звездчатые клетки, которые играют основную роль в процессе фиброгенеза в печени.
Важнейший фактор токсичности этанола – развитие окислительного стресса, который обусловлен повышенным образованием в печени свободнорадикальных молекул и снижением ее антиоксидантного потенциала. Активация микросомальной этанолокислительной системы, преимущественно цитохрома Р450-2Е 1, приводит к синтезу большого количества различных активных форм кислорода (супероксида кислорода, перекиси водорода и др.). Свободные радикалы вызывают перекисное окисление полиненасыщенных жирных кислот и липопротеидов, составляющих основу мембраны клеток, повреждают митохондрии клеток, нарушая перенос электронов в дыхательной цепи. Это, в свою очередь, приводит к гибели клеток печени или их повышенной чувствительности к повреждению, индуцированному цитокинами. Значительная утилизация глутатиона в условиях окислительного стресса, а также подавление алкоголем его синтеза существенно снижают антиоксидантный потенциал печени.
Таким образом, метаболизм этанола в печени генерирует реактивные виды кислорода и вызывает перекисное окисление липидов, истощение митохондриального глутатиона и S-аденозилметионина, приводящие к повреждению гепатоцитов, активирует метаболизм некоторых лекарств и химических веществ, повышая их гепатотоксичность.
Как упоминалось выше, ацетальдегид является реакционно способным соединением, очень токсичным для гепатоцитов, поскольку образует множество аддуктов белка и ДНК, обусловливающих истощение глутатиона, перекисное окисление липидов и повреждение митохондрий.
Митохондрии являются главной мишенью при интоксикации этанолом из-за токсического воздействия ацетальдегида, побочного продукта метаболизма этанола. Морфологические и функциональные изменения в митохондриях являются одним из ключевых признаков хронического воздействия этанола. Функциональные изменения в митохондриях проявляются общим снижением уровня аденозинтрифосфата (АТФ) в результате более низкой скорости синтеза АТФ вследствие нарушения ферментов окислительного фосфорилирования, кодируемых геномом митохондриальной ДНК.
Глутатион в митохондриях происходит из цитозоля, при помощи специальной транспортной системы он транслоцируется в матрицу. При хроническом употреблении этанола эта транспортная система повреждена, что приводит к селективному и значительному истощению содержания глутатиона митохондрий, а также к развитию повышенной восприимчивости к окислительному стрессу.
Митохондриальный глутатион играет решающую роль в функционировании и поддержании жизнеспособности гепатоцитов, а также в процессах детоксикации экзогенных ксенобиотиков и эндогенных метаболитов. Поэтому при алкогольном поражении печени не вызывает сомнений патогенетическая обоснованность введения глутатиона в форме его лекарственных препаратов.
Существует более 900 препаратов, которые могут обусловить лекарственные поражения печени. Применение наркотических веществ является причиной 5% всех случаев госпитализации и 50% всех острых печеночных событий. По этой причине лица, принимавшие лекарства в течение длительного периода, подвергаются более высокому риску развития гепатотоксичности при воздействии экзогенных токсинов.
В последние годы наблюдается четкая тенденция к увеличению частоты возникновения лекарственных поражений печени, что обусловено постоянным расширением ассортимента медикаментов, представленных на фармацевтическом рынке.
Медикаментозные гепатиты в 1-28% случаев осложняют проводимую фармакотерапию и в 12-25% случаев приводят к развитию цирроза печени и печеночной недостаточности.
Медикаментозное поражение печени включает прямое токсическое действие препарата на гепатоциты, токсическое действие метаболитов лекарственных средств и иммуноаллергические поражения печени. При наличии генетического дефекта в печени лекарство превращается в токсический метаболит, ковалентно связывается с клеточным глутатионом, приводя к некрозу гепатоцитов, стимулирует образование антигена и сенсибилизирует Т-лимфоциты, которые запускают иммунную гепатотоксичность.
Приоритетная антиоксидантная роль эндогенного глутатиона заключается в защите иммунных клеток (в первую очередь – лимфоцитов) от токсичных лекарственных метаболитов и свободных радикалов. При истощении запасов глутатиона в организме могут нарушаться механизмы иммунной защиты.
В последние годы активно обсуждается роль курения (воздействия на организм сигаретного дыма) как весомого этиологического фактора в развитии хронических заболеваний печени.
Курение является основным фактором риска не только сердечно-сосудистых заболеваний, но и неалкогольной жировой болезни печени (НАЖБП), первичного билиарного цирроза (ПБЦ) и других заболеваний печени. Курение снижает чувствительность к инсулину или индуцирует к нему резистентность, ингибируя киназы в печени. Пассивное и активное воздействие сигаретного дыма являются сильными независимыми предикторами наличия метаболического синдрома [4, 13, 14]. Курение усиливает отрицательное воздействие ряда других факторов риска развития заболеваний печени, таких как повышение уровня триглицеридов плазмы крови, снижение содержания холестерина липопротеинов высокой плотности, а также усугубляет гипергликемию.
Влияние курения сигарет на патогенез поражения печени долгое время оставалось недостаточно изученным. Первоначальные данные были получены из двух ретроспективных исследований, в которых предполагалось, что курение сигарет может увеличить распространенность и/или тяжесть алкогольного и связанного с вирусным гепатитом В цирроза. В двух недавних исследованиях с участием пациентов с ПБЦ выявлено, что независимым предиктором развития фиброза являлось табакокурение. Наконец, в ряде исследований показано, что из-за канцерогенных свойств табака курение сигарет связано с повышением частоты гепатоцеллюлярной карциномы у пациентов с циррозом печени.
Существуют данные о том, что пассивное или активное воздействие табака может относиться к стрессовым факторам окружающей среды, способствующим прогрессированию повреждения печени. H. Uang и соавт. [15] включают в их число и НАЖБП и дают убедительные доказательства того, что табачный дым может изменить регуляторный эффект активируемой протеинкиназы (AMР) на липидный обмен. Прекращение табакокурения может считаться необходимым условием при лечении пациентов с НАЖБП.
Курение повышает уровень аланинаминотрансферазы (АЛТ) сыворотки крови и степень поражения печени, увеличивает агрессивность окислительного стресса и гепатоцеллюлярного апоптоза, печеночную экспрессию тканевого ингибитора металлопротеиназы‑1 и проколлагена альфа-2, регулирует фосфорилирование внеклеточной регулируемой киназы (ERK) и протеинкиназы альфа (AKT).
У курящих (а также у злоупотребляющих алкоголем) людей значительное количество эндогенного глутатиона расходуется на обезвреживание продуктов табачного дыма. Курение приводит к снижению уровня глутатиона, на фоне чего все токсичные вещества табачного дыма, в особенности свободные радикалы, оказывают еще более интенсивное отрицательное воздействие на клетки человеческого организма и повышают его уязвимость к заболеваниям.
Ключевая роль в противодействии вредным эффектам курения принадлежит именно глутатиону, который активно поглощает свободные радикалы как попавшие в организм с табачным дымом, так и образованные в самом организме вследствие воздействия сигаретного дыма. В клетках печени глутатион вступает во взаимодействие с токсическими веществами, проникшими из табачного дыма в кровь. Благодаря его действию организм может обезвредить многие из этих токсинов и вывести их из организма с желчью.
На современном этапе приоритетную этиологическую роль в развитии заболеваний печени играют экологические токсины – ядовитые вещества (ксенобиотики), что подтверждается эпидемиологическими исследованиями, экспериментальными моделями на животных и анализом географической кластеризации (районы с необычайно высокой распространенностью заболеваний, связанных с местами скопления известных токсичных отходов).
Факторы окружающей среды играют роль в этиологии и патогенезе заболеваний, опосредованных иммунной системой (в том числе первичного склерозирующего холангита, аутоиммунного гепатита, ПБЦ), а также НАЖБП, неалкогольного стеатогепатита, на которые ежегодно приходится значительная доля трансплантаций печени и смертей от цирроза. Проводимые клинические исследования доказывают, что на частоту распространенности аутоиммунных заболеваний печени влияют сочетание генетических факторов, ультрафиолетового излучения (избыток витамина D) и соответствующего экзотоксина (трихлорэтилена).
Ксенобиотики – это чужеродные химические токсины, которые обычно не содержатся в организме. Они могут накапливаться в различных тканях, как правило, из-за воздействия загрязняющих веществ. Профессиональное воздействие ксенобиотиков повышает распространенность НАЖБП.
Доказано увеличение распространенности НАЖБП в большой группе рабочих, хронически подвергающихся воздействию нескольких летучих нефтехимических продуктов [4]. Среди нефтехимических продуктов, наиболее часто выявляемых в промышленной зоне – бензол, толуол, четыреххлористый углерод и хлорированные углеводороды. После оценки других известных факторов риска развития НАЖБП воздействие профессионального токсина оказалось независимым фактором риска возникновения данного заболевания. При биопсии печени у людей с НАЖБП, ассоциированной с токсином, наряду с токсическим гепатитом отмечалось повышение холестатических маркеров. Хотя многие из этих токсинов накапливаются и депонируются в основном в жировых тканях, экскреция этих липофильных токсинов осуществляется с желчью, что вызывает или усугубляет ранее существовавший холестаз. Эти токсины обнаруживаются в тканях организма и могут использоваться в качестве будущих биомаркеров для выявления общего воздействия ксенобиотиков на печень.
Токсические гепатиты могут быть вызваны следующими экзогенными промышленными и бытовыми токсинами: хлорированными углеводородами, нафталинами и дифенилами, бензолом, металлами и другими неорганическими элементами, мономерами, используемыми для получения полимерных материалов, пластмасс, гидразином и его производными, диоксинами и диоксинподобными веществами, радионуклидами.
Все перечисленные экзогенные токсины оказывают кумулятивный повреждающий эффект на печень, поэтому они должны быть трансформированы в нетоксичные для организма соединения и элиминированы.
К основным механизмам токсического поражения печени относятся перекисное окисление липидов, денатурация белков, истощение запасов АТФ, нарушение функции митохондрий, разрушение клеточного скелета и блокада мембранных рецепторов. Митохондрии и цитохром Р450 являются основными точками приложения экзогенных токсинов.
В печени метаболизируются примерно 2/3 от общего количества ксенобиотиков, попадающих в организм. Серные, глутатионовые и глюкуронидные конъюгаты ксенобиотиков из печени могут выводиться с желчью в кишечник, подвергаться там дальнейшей биотрансформации, реабсорбироваться в кровь и вновь поступать в печень. Далее эти соединения выделяются с мочой или повторно поступают с желчью в кишечник и выводятся с калом.
Детоксикация ксенобиотиков происходит в две фазы. Десинхронизация этих процессов ведет к быстрому отравлению организма в результате накопления продуктов перекисного окисления, различных канцерогенов, мутагенов и тератогенов. При этом особенно неблагоприятно сочетание высокой активности ферментов фазы I (ферменты цитохрома Р450) и низкой активности ферментов фазы II (глутатионтрансферазы; рис. 1).
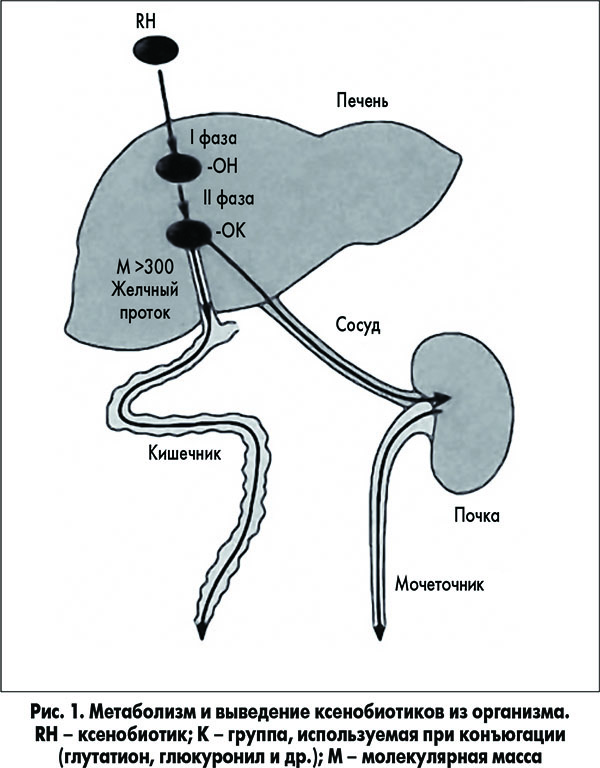
Из множества цитохром Р450-зависимых реакций на рисунке приведена только одна – схема гидроксилирования ксенобиотика. В ходе первой фазы в структуру вещества RH вводится полярная группа ОН–. Далее происходит реакция конъюгации; конъюгат в зависимости от растворимости и молекулярной массы удаляется либо через почки, либо с фекалиями.
Хлорированные углеводороды, в частности трихлорэтилен (ТХЭ), являются одними из наиболее изученных экзотоксинов, взывающих иммунно-воспалительные реакции в печени с развитием аутоиммунных заболеваний.
Хроническая (32-недельная) низкоуровневая экспозиция TХЭ способствует развитию аутоиммунного гепатита в связи с активацией Т-клеток CD4+, секретирующих повышенные уровни провоспалительного интерферона гамма, которые могут регулировать экспрессию в печени воспалительных генов с развитием в дальнейшем аутоиммунного воспаления и аутоиммунных опухолей.
Результаты исследований показали, что аутоиммунный гепатит, индуцированный TХЭ, может быть обнаружен всего после 26 недель воздействия. Экспрессия гена коррелирует с результатами анализа уровней метаболитов, доказывающих, что TХЭ активирует метионин/гомоцистеин в печени после 26 недель воздействия. Результаты также показали, что воздействие TХЭ меняет экспрессию селективных печеночных генов, связанных с иммунитетом и воспалением, в частности участвующих в метаболизме/детоксикации, включая ферменты, метаболизирующие фазу I (CYP2A12 и CYP2C39) и фазу II (S-трансфераза глутатиона). ТХЭ-воздействие индуцирует в печени несколько маркеров окислительного стресса, включая изменения в супероксиддисмутазе (SOD) и глутатионе [5].
Полиморфизм CYP450 может помочь объяснить межличностные изменения восприимчивости к токсичности, вызванной лекарственными средствами и другими ксенобиотиками. Так, у китайских рабочих полиморфизм CYP2E1 коррелировал с увеличением вероятности токсического поражения печени винилхлоридом.
Железо является одним из наиболее важных, но и наиболее токсичных элементов, выявленных в человеческом теле. Неконтролируемое повышение уровня каталитически активных форм железа в крови и в паренхиматозных органах приводит к окислительному стрессу и повреждению печени. Кроме того, генетические (HFE и не-HFE-гемохроматические генные мутации) и негенетические факторы (алкоголь, вирус гепатита С и др.) приводят к избыточному накоплению железа в печени и низкой экспрессии гепсидина – основного гормона, регулирующего обмен железа в организме.
Основные мишени токсичности железа и генотоксичность обусловлены снижением синтеза или инактивацией ферментов дыхательной цепи с помощью аддуктов LP-белка (липопротеина), пероксидативным повреждением фосфолипидов внутренней мембраны гепатоцитов, особенно кардиолипина, индуцированным высвобождением Ca2+ за счет открытия канала Ca2+ во внутренних мембранах, отеком и лизисом гепатоцитов.
Гепатотоксичность железа приводит к гепатоцеллюлярному некрозу (так называемый sideronecrosis). На этом этапе клетки Купфера становятся фагоцитолизирующими сидеронекротическими гепатоцитами. На фоне этого происходит активация печеночных звездчатых клеток, портальных фибробластов и/или живых и инфильтрирующих воспалительных клеток, что способствует фиброгенезу. Кроме того, железосодержащие активные формы кислорода (ROS) и их побочные продукты, вероятно, индуцируют продукцию коллагена посредством «паракринного» эффекта. Избыток железа способствует выработке ROS, при этом происходит стимуляция цитокинов и других фиброгенных или гепатотоксических медиаторов, что приводит к портальному и перипортальному фиброзу, портопортальному мостовидному фиброзу, микронодулярному циррозу и гепатоцеллюлярной карциноме. Последняя также может развиваться и при отсутствии цирроза из-за ряда механизмов. Они могут включать в себя: прямое мутагенное действие железа, вмешательство в иммунологическое наблюдение за опухолью, удаление трансформированных клеток, а также стимулирование железом роста опухоли.
Более выраженные, хотя и менее очевидные патогенные эффекты железа, возникают в случае поражения печени этим элементом в сочетании с другими гепатотоксинами. Это относится к ряду заболеваний печени, включая алкогольный и неалкогольный стеатогепатит или вирусный гепатит. В этих условиях прооксидантный ингибитор карбоксипептидазы (LCI), связанный с избытком железа в печени, значительно усиливает окислительный стресс. Это явление либо вызвано только одним гепатотоксином (например, при алкогольных, вирусных или метаболических заболеваниях печени), либо комбинацией (например, при порфирии).
В настоящее время среди экзогенных ксенобиотиков большое значение придается цианотоксинам, или токсинам сине-зеленых водорослей, которые приобретают агрессивные свойства в условиях аномальной жары и образуют яд.
Люди подвергаются воздействию токсинов цианобактерий при употреблении зараженной воды и купании в водоемах со стоячей зеленой водой. Другими источниками токсинов являются пищевые таблетки из водорослей.
Токсины цианобактерий классифицируются по их воздействию на организм человека. Среди них выделяются гепатотоксины, производимые некоторыми штаммами цианобактерий – Microcystis, Anabaena, Oscillatoria, Nodularia, Nostoc, Cylindrospermopsis и Umezakia.
Цианобактерии Microcystis продуцируют токсин микроцистин, который устойчив к перевариванию в желудочно-кишечном тракте и обычно накапливается в клетках печени с помощью активной транспортной системы. Отравления микроцистином приводят к разрушению печеночной архитектуры, что сопровождается потерей органом крови и геморрагическим шоком, а в дальнейшем приводит к раку печени, вызываемому мощным гепатокарциногеном микроцистина AFB1.
В настоящее время в пищевой промышленности применяют универсальный подсластитель из кукурузного крахмала и консервант для пищевых продуктов, который изготавливается с использованием агента, содержащего токсичную ртуть и имеющего прямую связь с развитием НАЖБП.
За последние несколько десятилетий марганец заменил свинец как антидетонационный агент в бензине, что приводит к загрязнению воздуха и дорожного покрытия этим элементом.
Патологическое действие марганца как гепатотоксина происходит посредством генерации свободных радикалов в митохондриях. Он уменьшает энергетический метаболизм клетки, включая снижение активности митохондриальных ферментов, мембранного потенциала и производства АТФ. Накопление марганца в митохондриях, включая митохондрии печени, также ингибирует окислительное фосфорилирование, увеличивая производство гидроксильных радикалов (OH). Перегрузка марганцем обычно встречается у пациентов с хронической печеночной недостаточностью.
Избыток марганца в печени может способствовать фиброзу с развитием в дальнейшем цирроза печени. Поскольку марганец разделяет абсорбционные и экскреторные механизмы с железом, то как перегрузка железом, так и его дефицит обусловливают восприимчивость печени к марганцевой токсичности.
Специфических морфологических критериев определения токсического агента нет. Во всех случаях обнаруживают различной степени выраженности стеатоз, фиброз, очаги некроза, тельца Маллори, холестаз, зависящие от длительности действия токсического вещества, его количества и физико-химических свойств (рис. 2).
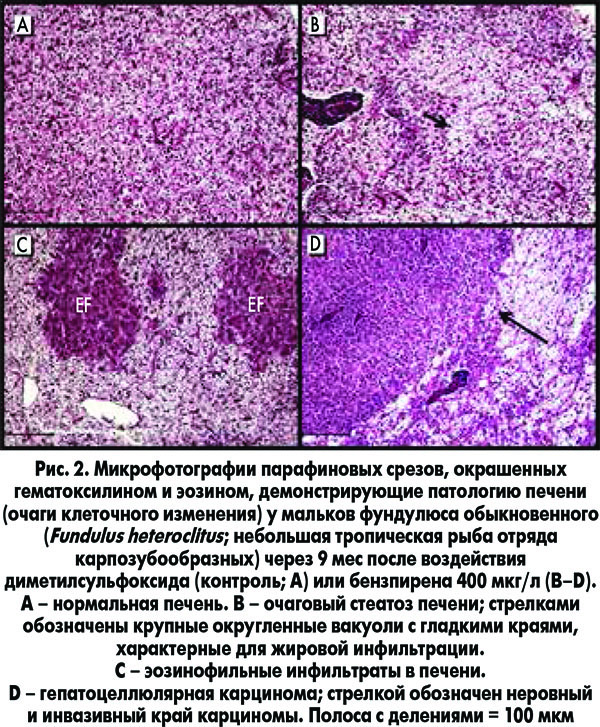
Таким образом, выявление факторов (алкоголь, курение, прием гепатотоксичных лекарственных средств, воздействие экзогенных ксенобиотиков и др.), указывающих на этиологию заболеваний печени, должно способствовать улучшению профилактики и лечения ХЗП, а также расширению нашего понимания патогенетической роли экологических токсинов в развитии аутоиммунных, метаболических и генетических заболеваний печени. В дальнейшем необходимо внедрение в диагностику специфических экологических маркеров с целью определения наличия ксенобиотика и его связи с патологией печени.
Основной подход в лечении – прекращение контакта с токсичным веществом, гепатотоксичными лекарственными средствами, алкоголем, сигаретным дымом и элиминация токсина.
В настоящее время доказано, что механизмы инициации окислительного стресса при алкогольной болезни печени, лекарственно-индуцированном, любом токсическом поражении печени связаны с митохондриальной и эндотелиальной дисфункцией, нарушением обмена глутатиона, поэтому патогенетической терапией является использование гепатопротекторов-антиоксидантов, содержащих глутатион.
Оксидативный стресс сопровождает практически любую патологию печени, в том числе НАЖБП. При усилении процессов пероксидного окисления липидов повреждаются мембраны гепатоцитов. Их прогрессирующая гибель в свою очередь запускает воспалительную реакцию и создает предпосылки для активации фибро- и канцерогенеза [1].
В Украине на фармацевтическом рынке появился препарат Гепавал® для внутривенного введения, один флакон которого содержит 643 мг глутатиона натрия, что эквивалентно 600 мг глутатиона. Препарат обладает мощным антиоксидантным, детоксикационным, противовоспалительным, иммуномодулирующим потенциалом.
Гепавал® – единственный в Украине препарат восстановленного (активного) глутатиона, имеющего в своем составе активные SH-группы, которые являются донорами водорода для других нестабильных молекул и отвечают за детоксикацию. Это лекарственное средство является приоритетным гепатопротектором-антиоксидантом, рекомендованным при токсических, алкогольных, лекарственных, метаболических поражениях печени.
Терапию препаратом Гепавал® следует начинать с введения 1-2 флаконов (600-1200 мг) в сутки внутримышечно или внутривенно в течение 10-30 дней, затем 2-4 капсулы (250-1000 мг) в сутки перорально в течение 1-6 мес. При тяжелых токсических поражениях печени дозу глутатиона для внутривенного введения можно повышать до 2400 мг/сут (согласно данным рандомизированных клинических исследований).
Глутатион, входящий в состав препарата, представляет собой трипептид, состоящий из глицина, глутамина и цистеина. Он обладает тиольной SH-группой и участвует в реакциях восстановления/окисления, выступая в качестве основного клеточного акцептора свободных радикалов. Обезвреживание ксенобиотиков глутатионом может осуществляться тремя различными способами: путем конъюгации субстрата с глутатионом, в результате нуклеофильного замещения и в результате восстановления органических пероксидов до спиртов.
Система обезвреживания с участием глутатиона играет уникальную роль в формировании резистентности организма к самым различным воздействиям и является наиболее важным защитным механизмом клетки. В ходе биотрансформации некоторых ксенобиотиков при участии глутатиона образуются тиоэфиры, затем превращающиеся в меркаптаны, среди которых обнаружены токсичные продукты. Конъюгаты глутатиона с большинством ксенобиотиков менее способны к реакциям и более гидрофильны, чем исходные вещества, а поэтому менее токсичны и легче выводятся из организма.
Глутатион связывает огромное количество липофильных соединений, предотвращая их внедрение в липидный слой мембран и нарушение функций клетки, улучшает стабильность клеточной мембраны, защищает мембрану клеток печени, повышает активность ферментов и печени и способствует детоксикации и восстановительной активности органа путем уничтожения свободных радикалов.
Проведенные рандомизированные клинические исследования показали достоверный выраженный антиоксидантный эффект глутатиона и его высокую терапевтическую активность при токсических поражениях печени различными токсинами (алкоголь, лекарственные средства, наркотические вещества, соли тяжелых металлов и другие экзогенные токсины).
Huqi-Jiang и соавт. [19] изучали эффективность глутатиона при лечении алкогольных заболеваний печени. 60 пациентов с алкогольными заболеваниями печени были случайным образом разделены на группы A и B. Пациенты в группе A получали глутатион в течение 4 недель, а в группе B – калия аспартат в течение такого же времени. В группе А в конце периода общий показатель эффективности терапии составил 96,7% – значительно выше, чем в группе B (р<0,01). Время достижения отмеченного эффекта составляло 9,8±6,5 дня – то есть, он наступал значительно раньше, чем в группе B (P<0,01). Снижение уровней AЛT, аспартатаминотрансферазы (AСT) и γ–глутамилтрансферазы (ГГТ) после лечения было более значительным в группе А (глутатиона), чем в группе B (P<0,01). Частота нормализации содержания AЛT, AСT и ГГТ у пациентов группы A составляла 96,7, 93,3 и 90% соответственно; все эти показатели были значительно лучше, чем в группе B (P<0,01). Авторы сделали вывод о высокой активности глутатиона при алкогольных заболеваниях печени [19]. Глутатион обладает большей эффективностью, чем калия и магния аспартат, при лечении пациентов с алкогольными заболеваниями печени.
Zhang и соавт. [17] выполнили многоцентровое двойное слепое рандомизированное контролируемое исследованиие, в ходе которого оценили влияние внутривенного введения глутатиона на уровни AЛT и АСТ в сыворотке крови при алкогольной болезни печени, а также безопасность такой терапии. В исследование было включено 120 пациентов с алкогольной болезнью печени, 60 из них получали длительную инфузию глутатиона в дозе 1200 мг/сут в течение 30 дней. Авторы сделали выводы о том, что терапевтические эффекты, связанные с уменьшением выраженности клинических проявлений алкогольной болезни печени и улучшением функции органа, могут быть достигнуты в случае внутривенного введения глутатиона; при этом такое лечение характеризуется высоким профилем безопасности [17].
L.V. Dong и X.U. You-qing [10] исследовали терапевтическую эффективность глутатиона у 66 пациентов с алкогольным циррозом печени. Пациенты были случайным образом разделены на 2 группы по 33 человека. Пациенты контрольной группы получали только стандартное лечение, а пациентам группы исследуемого лечения в дополнение к стандартной терапии внутривенно вводили глутатион в дозе 2400 мг/сут в течение 4 недель. У больных обеих групп были оценены изменения симптомов, параметров функции печени и гемореологии до и после лечения. Авторы отметили, что уменьшение выраженности симптомов, улучшение параметров функции печени и гемореологии в группе исследуемого лечения были более значительными, чем в контрольной. Глутатион обладает выраженной терапевтической эффективностью в лечении алкогольного цирроза печени; механизм его действия может быть связан с антиоксидантным эффектом и улучшением микроциркуляции в печени [10].
Tamphasana Wairokpam и соавт. [14] сообщают о проведенном рандомизированном контролируемом исследовании с участием 100 пациентов (96 мужчин и 4 женщины, средний возраст составил 46,43 года) с алкогольным гепатитом. Пациенты были разделены на 2 группы по 50 человек. Больные основной группы получали внутривенно капельно глутатион в дозе 1200 мг 1 раз/сут в течение 15 дней, контрольной – стандартное лечение без глутатиона. Введение глутатиона не вызывало серьезных побочных эффектов. Авторы отмечают, что уменьшение выраженности симптомов было зарегистрировано у 45% пациентов; достоверное снижение показателей АЛТ, АСТ, ГГТ, билирубина, щелочной фосфатазы и повышение альбуминов у больных основной группы происходило в 2 раза быстрее, чем контрольной, – уже на 10-15-й день лечения, что свидетельствует о выраженном и быстром дезинтоксикационном действии внутривенной формы препарата [14].
В мультицентровое исследование эффективности и безопасности внутривенного введения глутатиона, проведенное в Китае в 2000 г., были включены 245 пациентов с хроническими вирусными гепатитами, активным циррозом печени, стеатогепатитом, лекарственно-индуцированным и алкогольным гепатитом. Все пациенты получали глутатион в дозе 1200 мг 1 раз/сут внутривенно капельно в течение 3 недель. В результате наиболее высокая эффективность глутатиона выявлена при токсических поражениях печени: у 100% пациентов с лекарственными гепатитами и у 86% больных алкогольными гепатитами определялся отличный и хороший терапевтический эффект после 3 недель лечения.
У 57% пациентов с лекарственно-индуцированным поражением печени зафиксировано исчезновение субъективных симптомов, уменьшение гепатоспленомегалии, нормализация АЛТ, АСТ и/или билирубина. У 43% пациентов отмечалось уменьшение или отсутствие прогрессирования субъективных симптомов, отсутствие прогрессирования гепатоспленомегалии, снижение более чем на 50% уровня АЛТ, АСТ и/или билирубина, что свидетельствует о выраженном дезинтоксикационном и антиоксидантном эффектах глутатиона.
Следовательно, в лечении заболеваний печени, обусловленных отрицательными экологическими факторами, целесообразно применение гепатопротекторов-антиоксидантов, устраняющих все проявления оксидативного стресса и восстанавливающих эндогенный запас глутатиона.
Назначение внутривенной формы препарата Гепавал® патогенетически обосновано и способствует своевременной активной терапии хронических заболеваний печени, обусловленных развитием агрессивного оксидативного стресса под воздействием токсических факторов – алкоголя, курения, лекарственных средств и различных экзогенных ксенобиотиков.
Список литературы находится в редакции.





