4 жовтня, 2017
Терапия глюкокортикоидами в вопросах и ответах
 Вопрос о применении глюкокортикоидов (ГК) давно привлекает пристальное внимание врачей-ревматологов и вызывает многочисленные дискуссии. Назначая гормоны, врач берет на себя большую ответственность. В конце прошлого века после периода увлечения ГК-терапией и осознания количества побочных явлений, с ней связанных, академик В.А. Насонова, желая предостеречь от необоснованного назначения ГК, в одной из публикаций написала, что квалификация врача-ревматолога обратно пропорциональна частоте назначения им кортикостероидов [11].
Вопрос о применении глюкокортикоидов (ГК) давно привлекает пристальное внимание врачей-ревматологов и вызывает многочисленные дискуссии. Назначая гормоны, врач берет на себя большую ответственность. В конце прошлого века после периода увлечения ГК-терапией и осознания количества побочных явлений, с ней связанных, академик В.А. Насонова, желая предостеречь от необоснованного назначения ГК, в одной из публикаций написала, что квалификация врача-ревматолога обратно пропорциональна частоте назначения им кортикостероидов [11].
По данным Hart, прием даже низких доз ГК (до 10 мг преднизолона) через несколько недель или месяцев приводит к развитию побочных явлений, в частности признаков гиперкортицизма. Hart образно пишет: «Стремительное улучшение состояния и глубокая признательность больного («медовый месяц» кортикостероидной терапии) постепенно сменяются стойким обострением и присо&единением ятрогенной болезни Кушинга («период несчастливого супружества»)» [12].
В то же время другие авторы подчеркивают высокую эффективность правильно подобранной ГК-терапии. «Немного глюко&кортикоидов, как стакан вина, могут быть полезными многим (пациентам), много глюкокортикоидов, как бутылка вина, вредны всем» (Т. Пинкус).
Поэтому для практикующего врача всегда остаются актуальными следующие вопросы назначения ГК.
- Кому назначать?
- Когда назначать?
- Как долго продолжать терапию?
- Какова стартовая доза?
- Какова поддерживающая доза?
- Какой режим терапии?
- В каких комбинациях?
- Когда и как отменять?
- Нежелательные реакции (НР) – страхи больных или реальность?
- Как предупредить НР?
- Влияют ли данные препараты на симптомы заболевания, рентгенологическое прогрессирование, летальность?
При ряде ревматологических заболеваний, таких как системные болезни соединительной ткани, васкулиты, данные доказательной медицины свидетельствуют о том, что ГК являются препаратами первого ряда, без которых невозможно достижение клинико-&лабораторной ремиссии. В то же время при таком распространенном заболевании, как подагра, длительное назначение ГК может привести к усугублению патологии и развитию порочного круга НР (гиперурикемия – избыточная масса тела – гипертензия – прием комбинированных препаратов, содержащих тиазидные диуретики, – усугубление гиперурикемии), один из таких случаев изложен в нашей работе [13].
А какова тактика использования ГК при ревматоидном арт&рите (РА)? Быть или не быть ГК в схеме лечения РА? Дискуссии по этому вопросу привлекают внимание многих экспертов, рекомендации международных организаций, занимающихся лечением РА (Европейская противоревматическая лига – EULAR, Американская коллегия ревматологов – ACR), трактуют эти вопросы по-разному. Допускается несколько вариантов применения ГК: системная терапия, в том числе пульс-терапия высокими дозами, местная инъекционная терапия и локальная терапия (капли, мази). Начиная с 50-х годов прошлого века для ревматологов стало аксиомой, что назначение высоких доз ГК при РА оправдано только по очень строгим показаниям, таким как потенциально смертельные осложнения ревматоидного васкулита, высокая активность аутоиммунного процесса, тяжелые осложнения терапии базисными противовоспалительными препаратами (БПВП). А вот вопрос со средними и малыми дозами ГК и длительностью их приема до последнего времени остается предметом дискуссий.
Эра применения генно-инженерных биологических препаратов (ГИБП) для лечения РА и проведение большого количества рандомизированных клинических исследований (РКИ) позволили обобщить и суммировать выводы и по влиянию ГК на исходы РА. По данным РКИ, около 40-80% пациентов с РА принимали ГК, в том числе около 50% больных одновременно принимали ГИБП. То есть актуальность этих препаратов, несмотря на появление высокотехнологичных методов лечения, не утрачена. В этой связи представляются интересными данные Andre и соавт. [1], продемонстрировавшие, что процент больных, получавших наряду с ГИБП и ГК, составлял от 34 до 93% (в среднем 58±13%) в целом и отличался по биологическим агентам следующим образом: абатацепт – 74,4%; голимумаб – 67,9%; инфликсимаб – 60,6%; цертолизумаб – 57,5%; ритуксимаб – 57,5%; этанерцепт – 54,4%; тоцилизумаб – 52,8%; адалимумаб – 50,4%. Эти проценты не менялись в период между 1997 и 2010 годами. То есть частота использования таких высокотехнологичных методов лечения не умаляет значимости использования ГК.
Для лечения ревматических заболеваний используют исключительно синтетические молекулы, которые проявляют длительное противовоспалительное и иммуносупрессивное действие при относительно слабой или даже нулевой минералокортикоидной активности. К препаратам средней длительности действия относят преднизолон, метилпреднизолон (МП) и триамцинолон, к длительно действующим – дексаметазон и бетаметазон. Для длительной терапии ГК с длительным периодом полураспада (дексаметазон, бетаметазон) применять не рекомендуется. Наилучшей переносимостью обладает МП, который является препаратом выбора у больных с нестабильной психикой, артериальной гипертензией, избыточной массой тела, предрасположенностью к язвенной болезни желудка [13].
Что говорят международные рекомендации по поводу назначения ГК при РА и как они изменились за последние годы? До 2002 года в ревматологии и других медицинских специальностях существовало несоответствие между широким использованием и неточным обозначением схем лечения ГК. Словесные описания схем лечения ГК, используемых в различных фазах заболеваний, различались между странами и учреждениями. Поэтому в 2002 году в г. Берлине под эгидой постоянного комитета EULAR по международным клиническим исследованиям был проведен семинар и выработан консенсус по номенклатуре для ГК-терапии. Была внесена терминологическая определенность для обозначения доз ГК. В настоящее время принято считать, что низкая доза ГК составляет <7,5 мг/сут (в пересчете на преднизолон), средняя доза – >7,5-30 мг/сут, высокая – >30 мг/сут. Также принято определение, что ранний РА – это РА с продолжительностью заболевания не более 12 мес.
Еще в 1999 году появились работы [3], показывающие, что при раннем РА у условно здоровых людей с доклиническим РА имеет место скрытая недостаточность оси «гипоталамус-гипофиз-&надпочечник», а также неадекватный синтез эндогенного кортизола в ответ на стрессорные стимулы, и назначение ГК может рассматриваться как своего рода заместительная терапия.
В 2002 году в рекомендациях ACR по лечению РА впервые упоминается назначение ГК: «ГК в низких дозах высокоэффективны в отношении облегчения симптомов у пациентов с активным РА». С накоплением данных РКИ в 2009 году в рекомендациях Национального института здоровья и совершенствования клинической практики Великобритании (NICE) уже более определенно говорится: «У пациентов с ранним и развернутым РА следует использовать короткий курс ГК для подавления обострения заболевания». Рекомендации EULAR (2010) освещают комбинацию ГК и БПВП: «Добавление ГК в низких и умеренных дозах может быть полезным в комбинации с БПВП». Однако дискуссии ведущих экспертов не утихают. В 2012 году ACR не освещала вопросы применения ГК при РА в связи с отсутствием достижения консенсуса экспертов по этому вопросу.
В 2012 году появился новый сетевой метаанализ РКИ [4], проведенный Graudal и соавт., который суммировал данные о влиянии комбинированной терапии на прогрессирование изменений суставов при РА за длительный период времени, начиная с 1989 года. Были сделаны следующие выводы.
ГК в дозе <15 мг/сут эффективнее плацебо и нестероидных противовоспалительных препаратов (НПВП) относительно подавления боли и воспаления, уменьшения утренней скованности, недомогания, СОЭ, уровня С-реактивного белка, в сочетании с БПВП эффективнее монотерапии БПВП при раннем РА, структурно-модифицирующий эффект ГК сохраняется длительно и после отмены.
Актуальным и наиболее обсуждаемым остается вопрос побочных явлений – соотношение риска и пользы назначения ГК для системной терапии РА. Но с появлением новых молекул ГК (в частности, МП) и анализов данных современных исследований ряд мифов, касающихся побочных эффектов ГК, также развеян.
Увеличение массы тела, характерное для высоких доз ГК, минимизировано при использовании низких доз с&овременных молекул ГК и может быть связано не столько с метаболическими эффектами ГК, сколько со снижением активности воспаления и уменьшением явлений ревматоидной кахексии. Похожая прибавка массы тела [5] отмечена также у пациентов, получающих ингибиторы фактора некроза опухоли, особенно тоцилизумаб.
Согласно данным Piper и соавт. [6] ГК реже вызывают тяжелое поражение желудочно-кишечного тракта, чем НПВП. Двукратное увеличение риска развития язв желудка, описанное на фоне лечения ГК, возможно, связано с сочетанным приемом НПВП.
Противоречивы данные, касающиеся роли ГК в развитии атеро&склеротического поражения сосудов. Поскольку воспалительная активность РА является важным проатерогенным фактором, подавление воспаления, в том числе с помощью ГК, потенциально может снижать риск развития атеросклероза. В недавних исследованиях было показано, что ГК могут способствовать нормализации липидных нарушений, связанных с высокой воспалительной активностью РА.
Имеются данные о том, что при РА развитие резистентности к инсулину коррелирует с активностью воспаления, противо&воспалительная терапия, включая ГК, приводит к восстановлению чувствительности к инсулину [7].
Dixon и соавт. [14] обобщили материалы 21 рандомизированного проспективного клинического исследования (РПКИ) и 42 наблюдательных исследований: по данным РПКИ, риск инфекционных осложнений в группе ГК не отличался от плацебо; по данным наблюдательных исследований, имеет место 67% риск развития инфекций, но результаты очень гетерогенны и связаны с суточной и кумулятивной дозой ГК, коморбидностью и сопутствующей терапией. Риск развития инфекций больше у тех пациентов, которым необходимо принимать более высокие дозы более длительное время, но вместе с тем это наиболее тяжелые и по РА пациенты, поэтому в этой ситуации трудно определить, что привело к инфекционным осложнениям – прием ГК или аутоиммунный процесс высокой степени активности.
Риск остеопоротических переломов у пациентов с РА (доза ГК – в среднем 8,6 мг/сут) составляет 33% в течение 5 лет. Однако воспалительная активность РА и нарушение физической активности являются не менее важными факторами риска развития остеопороза, чем лечение ГК. Таким образом, у некоторых пациентов с РА ГК оказывают опосредованный антиостеопоротический эффект [15].
В связи с вышеизложенным в рассуждениях о побочных явлениях ГК иногда имеет место преувеличение токсичности терапии ГК, автоматический перенос данных о плохом профиле переносимости высоких доз ГК на пациентов, получающих низкие. Включается систематическая ошибка channeling bias – ГК назначают пациентам с наиболее тяжелым течением РА. Трудно разделить НР, связанные с самим РА, и НР терапии. Эти вопросы достаточно полно изложены в работе [8], где показано, что прогрессирование остеопороза, резис&тентность к инсулину, риск инфекционных осложнений, риск кардиоваскулярных катастроф могут являться признаками как класс-неспецифических НР терапии ГК, так и высокой активности РА.
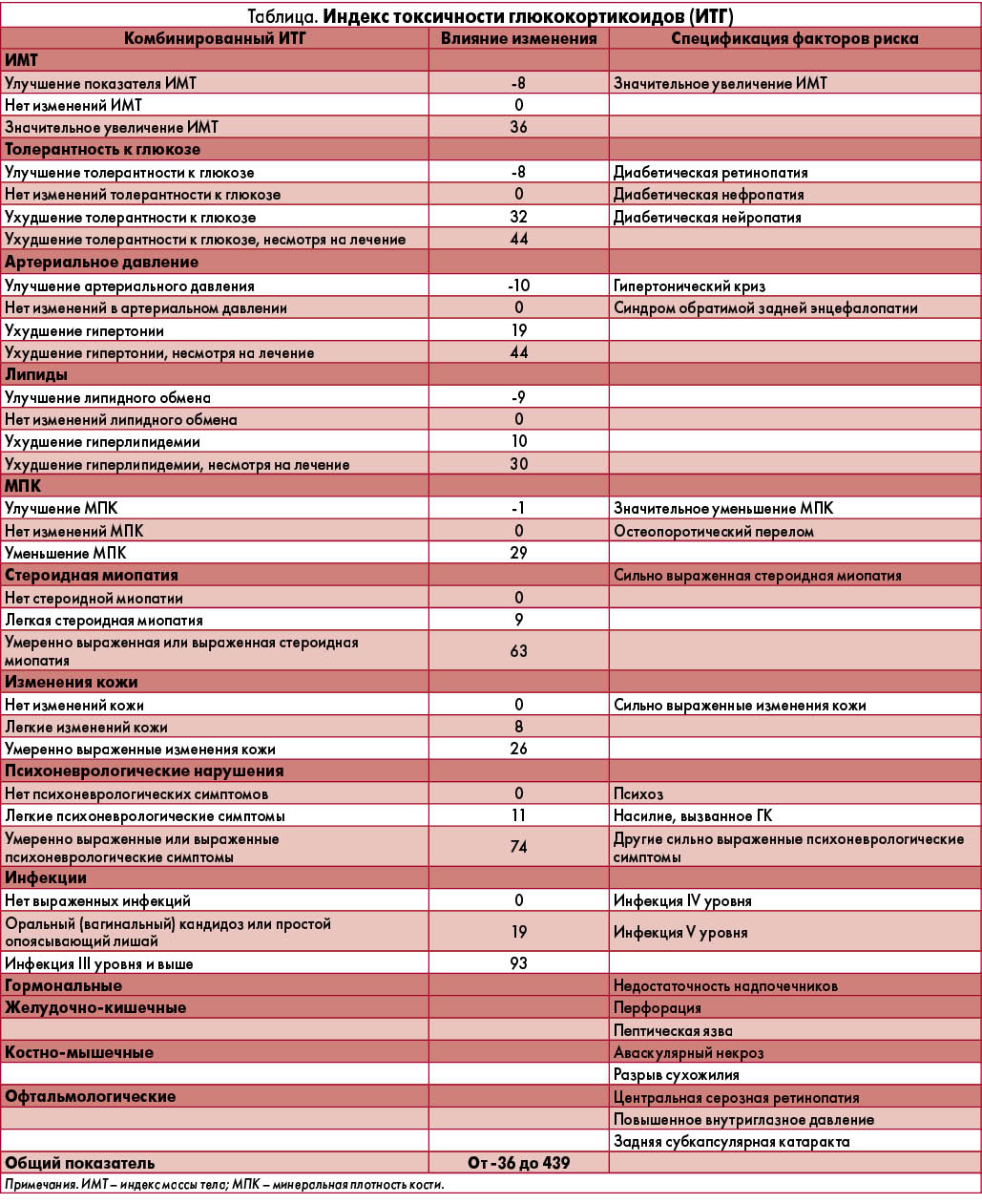
Для оценки побочных явлений терапии ГК представляется интересным анонсированный на конгрессе EULAR (2016) новый индекс GTI – индекс токсичности ГК, который представляет из себя суммированный показатель действия ГК на разные органы и системы [9]. 19 экспертов 11 специальностей по вопросам использования ГК (США, Канада, Европа, Австралия) в течение 10 мес взаимодействия (телефонные звонки, митинги, работа в группах, интернет-дискуссии) посредством методов консенсуса в группах и мультикритериального анализа решений (1000 Mind) разработали и предложили оценивать токсичность ГК по 31 показателю. Составляющими этого математического показателя являются оценки индекса массы тела, толерантности к глюкозе, артериальная гипертензия, данные липидного обмена, показатели минеральной плотности костной ткани, выраженность стероидной миопатии, кожных изменений, нейропсихиатрические изменения и инфекции. Изменения в каждой из этих систем с помощью математических коэффициентов градуированы как улучшение, отсутствие изменений, средней степени нарушения, тяжелые нарушения. Более подробный расчет этого индекса представлен в таблице. Авторами предполагается создание на этой основе web-интерфейса для использования данного показателя как в клинических исследованиях, так и в реальной клинической практике.
Также много новых данных по побочным явлениям терапии ГК получено в результате последних РКИ, например исследования COBRA (2008-2012), которое продемонстрировало отсутствие различий в количестве НР при использовании схем лечения РА с метотрексатом (МТ) и МТ + ГК. Через 11 лет лечения сравнили группы пациентов, принимающих и не принимающих ГК, и получили уменьшение летальности, дислипидемии, злокачественных новообразований, инфекционных осложнений в группе приема ГК, частота кардиоваскулярной патологии и остеопоротических переломов была одинаковой в обеих группах, а также имело место достоверное увеличение частоты артериальной гипертензии в группе приема ГК и недостоверное увеличение частоты развития катаракты и остеопороза. Сходные данные были продемонстрированы и в исследовании BEST: не отмечено различий относительно выживаемости в зависимости от стратегии лечения РА, в том числе и высокими дозами. Увеличение смертности было связано с возрастом, мужским полом, курением и плохим состоянием здоровья (индекс HAQ). А исследование BAFROT длительностью 10 лет было одним из первых исследований, в котором была показана более высокая эффективность длительной (2 года) комбинированной терапии БПВП и низкими дозами ГК (преднизолон 7,5 мг/сут) по сравнению с монотерапией БПВП, не отмечено различий в час&тоте развития кардиоваскулярных осложнений. Поэтому в целом о НР при терапии ГК можно сформулировать следующие выводы: большинство из них достаточно тяжелые и являются неизбежным последствием ГК-терапии, но некоторые развиваются реже, чем при лечении другими БПВП. Само неконтролируемое ревматоидное воспаление может приводить к развитию ряда тяжелых осложнений, напоминающих побочные эффекты ГК. Некоторые осложнения РА, которые рассматриваются как следствие лечения ГК, на самом деле связаны с неадекватной ГК-терапией. Неадекватной ГК-терапией считается применение слишком высоких или слишком низких доз, неоправданная длительность, монотерапия ГК без сочетанного применения эффективных БПВП, обладающих «стероидосберегающей» активностью.
Влияют ли ГК на рентгенологическое прогрессирование РА, которое является не только важной конечной точкой РКИ, но и используется для оценки отдаленного прогноза болезни? Более того, замедление рентгенологического прогрессирования включено в официальные показания для назначения новых БПВП. В работе Hafstrom и соавт. [10] показано положительное действие приема 7,5 мг преднизолона на замедление скорости развития рентгенологических изменений у пациентов с ранним РА.
Как долго нужно продолжать терапию ГК у больных РА? Обратимся к рекомендациям EULAR. Главной концепцией рекомендаций EULAR (2016) остается концепция «treat to target» – лечение до достижения длительной ремиссии или низкой активности заболевания. В то же время необходимо помнить, что ГК следует отменять «как можно быстрее, насколько это возможно с клинической точки зрения». Монотерапия ГК не рекомендуется и может использоваться только как исключение при наличии противо&показаний к БПВП и ГИБП.
Как назначать ГК и какие схемы лечения наиболее оптимальны для лечения РА? Наиболее оптимальной схемой применения ГК при РА была и остается так называемая bridge-терапия – назначение ГК в комбинации с МТ и другими БПВП в течение времени, необходимого до развития эффекта БПВП, при обострении заболевания или как исключение в виде монотерапии при невозможности назначения БПВП и ГИБП. ГК следует отменять как можно быстрее (не позже 6 мес от начала терапии). В последних рекомендациях EULAR (2016) более четко прописаны следующие стратегии назначения ГК: применение пероральной низкой дозы, одной внутримышечной инъекции или однократное внутривенное введение. Последние два подхода обычно обеспечивают более низкую кумулятивную дозу и могут быть использованы при небольшой исходной активности заболевания. Непосредственным руководством по дозам и режимам терапии могут служить наиболее известные протоколы РКИ, в результате которых были получены убедительные данные по преимуществу использования именно этих схем назначения ГК. А именно:
- Однократная внутривенная инфузия высокой дозы МП (125 мг) внутривенно струйно (протокол IDEA).
- Однократное внутримышечное введение 40 мг МП (протокол tREACH).
- Пероральный прием ГК в стартовой дозе 24 мг МП (эквивалентно 30 мг преднизолона) с быстрым снижением до полной отмены (протокол COBRA-light).
Все эти схемы применения ГК реализуются на фоне активной терапии МТ в дозе 15-25 мг/сут, оптимальный эффект которого развивается через 3-6 мес.
В некоторых случаях возможно длительное назначение ГК – так называемая long-bridge-терапия, которая позволяет реализовать структурно-модифицирующий эффект ГК.
Таким образом, резюмируя вышеизложенное, необходимо подчеркнуть, что ГК назначаются пациентам с высокой активностью болезни, имеющим факторы неблагоприятного прогноза, при отсутствии факторов риска развития НР и противопоказаний. Применение таких современных высокотехнологичных методов лечения, как ГИБП, даже в дебюте РА не решает всех проблем фармакотерапии. Более широкое применение комбинации МТ + ГК позволит улучшить прог&ноз и снизить «стоимость» болезни, что, в свою очередь, уменьшит риск инвалидности, потребности в ГИБП и протезировании суставов.
Литература
- Andre V., le Goff B., Leux C., Pot-Vaucel M., Maugars Y., Berthelot J.M. Information on glucocorticoid therapy in the main studies of biological agents. Joint Bone Spine. 2011 Oct; 78 (5): 478-83. doi: 10.1016/j.jbspin.2011.01.001. Epub 2011 Feb 22.
- Buttgereit F., da Silva J.A., Boers M., Burmester G.R., Cutolo M., Jacobs J., Kirwan J., Kohler L., Van Riel P., Vischer T., Bijlsma J.W. Standardised nomenclature for glucocorticoid dosages and glucocorticoid treatment regimens: current questions and tentative answers in rheumatology. Ann. Rheum. Dis. 2002 Aug; 61 (8): 718-22.
- Cutolo M., Foppiani L., Prete C., Ballarino P., Sulli A., Villaggio B., Seriolo B., Giusti M., Accardo S. Hypothalamic-pituitary-adrenocortical axis function in premenopausal women with rheumatoid arthritis not treated with glucocorticoids. J. Rheumatol. 1999 Feb; 26 (2): 282-8.
- Graudal N., Hubeck-Graudal T., Tarp S., et al. Effect of combination therapy on joint destruction in rheumatoid arthritis: a network meta-analysis of randomized controlled trials. PLoS ONE, 2014; 9: e106408. doi: 10.1371.
- Jurgens M.S., Jacobs J.W., Geenen R., Bossema E.R., Bakker M.F., Bijlsma J.W., van Albada-Kuipers I.A., Ehrlich J.C., Lafeber F.P., Welsing P.M.; Utrecht Arthritis Cohort Study Group. Increase of body mass index in a tight controlled methotrexate-based strategy with prednisone in early rheumatoid arthritis: side effect of the prednisone or better control of disease activity? Arthritis Care Res (Hoboken), 2013 Jan; 65 (1): 88-93. doi: 10.1002/acr.21797.
- Piper J.M., Ray W.A., Daugherty J.R., Griffin M.R. Corticosteroid use and peptic ulcer: role non-steroidal anti-inflammatory drugs. Ann. Intern. Med. 1991; 114: 735-740.
- Halgren R., Berne C. Glucose intolerance in patients with chronic inflammatory diseases is normalized by glucocorticoids. Acta. Med. Scand. 1983; 213: 351-355.
- Skeoch S., Bruce I.N. Atherosclerosis in rheumatoid arthritis: is it all about inflammation? Nat. Rev. Rheumatol. 2015 Jul; 11 (7): 390-400. doi: 10.1038/nrrheum.2015.40. Epub 2015 Mar 31.
- Miloslavsky E.M., Naden R.P., Bijlsma J.W., Brogan P.A., Brown E.S., Brunetta P., Buttgereit F., Choi H.K., DiCaire J.F., Gelfand J.M., Heaney L.G., Lightstone L., Lu N., Murrell D.F., Petri M., Rosenbaum J.T., Saag K.S., Urowitz M.B., Winthrop K.L., Stone J.H. Development of a Glucocorticoid Toxicity Index (GTI) using multicriteria decision analysis. Ann. Rheum. Dis. 2017 Mar; 76 (3): 543-546. doi: 10.1136/annrheumdis-2016-210002. Epub 2016 Jul 29.
- Hafstrom I., Albertsson K., Boonen A., van der Heijde D., Landewe R., Svensson B.; BARFOT Study Group. Remission achieved after 2 years treatment with low-dose prednisolone in addition to disease-modifying anti-rheumatic drugs in early rheumatoid arthritis is associated with reduced joint destruction still present after 4 years: an open 2-year continuation study. Ann. Rheum. Dis. 2009 Apr; 68 (4): 508-13. doi: 10.1136/ard.2008.087833. Epub 2008 Apr 17.
- Насонова В.А., Сигидин Я.А. Патогенетическая терапия ревматических заболеваний. АМН СССР. – М.: Медицина, 1985. – 288 с., илл.
- Насонов Е.Л., Чичасова Н.В., Ковалев В.Ю. Глюкокортикоиды в ревматологии. – М., 1998. – 160 с.
- Триполка С.А., Головач И.Ю. Ошибки ведения пациента с подагрой в практике семейного врача: описание клинического случая // Ліки України. – 2017. – № 1. – С. 24-29.
- Dixon W.G., Suissa S., Hudson M. The association between systemic glucocorticoid therapy and the risk of infection in patients with rheumatoid arthritis: systemic review and metaanalysis. Arthritis. Res. Ther. 2011; 13: R139. doi: 10.1186/ar3453.
- Van der Goes M.C., Jacobs J.W.G., Jurgens M.S., et al. Are changes in bone mineral density different between groups of early rheumatoid arthritis patients treated according to a tight control strategy with or without prednisone if osteoporosis prophylaxis is applied? Osteop. Int. 2013; 24: 1429-36. doi: 10.1007/s00198-012-2073-z.
Статья напечатана при поддержке Представительства
«Файзер Эйч. Си. Пи. Корпорейшн» в Украине.


