11 жовтня, 2017
Тактика врача при редких пароксизмах фибрилляции предсердий
 В рамках VII Научно-практической конференции Ассоциации аритмологов Украины (18-19 мая, г. Киев) сотрудники отдела нарушений ритма и проводимости сердца ННЦ «Институт кардиологии им. Н.Д. Стражеско» – кандидаты медицинских наук Елена Николаевна Романова и Ольга Владимировна Срибная провели интересный мастер-класс по ведению пациентов с редкими эпизодами фибрилляции предсердий (ФП).
В рамках VII Научно-практической конференции Ассоциации аритмологов Украины (18-19 мая, г. Киев) сотрудники отдела нарушений ритма и проводимости сердца ННЦ «Институт кардиологии им. Н.Д. Стражеско» – кандидаты медицинских наук Елена Николаевна Романова и Ольга Владимировна Срибная провели интересный мастер-класс по ведению пациентов с редкими эпизодами фибрилляции предсердий (ФП).
По определению, данному Европейским обществом кардиологов (ЕОК) в 2012 году, нечастыми называются пароксизмы ФП, которые возникают с частотой от одного раза в месяц до одного раза в год.

Актуальность проблемы прежде всего определяется тем, что такие редкие события трудно зафиксировать: вероятность уловить пароксизм при записи рутинной электрокардиограммы (ЭКГ) крайне низкая и даже 24-часовое мониторирование не всегда помогает обнаружить аритмию. Вместе с тем хорошо известно, что даже редкие пароксизмы ФП повышают риск развития кардиоэмболического инсульта, поэтому своевременная диагностика влияет не только на качество жизни пациента, но и на его жизненный прогноз.
В последних рекомендациях ЕОК по ведению пациентов с ФП (2016) внеплановый скрининг ФП любым удобным способом (определение пульса, регистрация ЭКГ) рекомендуется всем пациентам старше 65 лет. У пациентов с инсультом или транзиторной ишемической атакой в анамнезе скрининг ФП рекомендован путем анализа ЭКГ длительностью не менее 72 ч.
Тактика ведения пациента определяется тем, как он переносит пароксизмы, их влиянием на гемодинамику, длительностью текущего пароксизма (больше или меньше 48 ч), а также характеристиками основного или сопутствующего заболевания, которое послужило субстратом для развития аритмии. Полное кардиоваскулярное обследование и анализ истории болезни рекомендованы всем пациентам с ФП. Например, в состоянии гипертиреоза первичной задачей становится не подбор антиаритмической терапии ФП, а контроль частоты сокращений желудочков (ЧСЖ) и нормализация функции щитовидной железы.
Ведущие мастер-класса разобрали важный практический аспект: какие вопросы необходимо задать пациенту и какие параметры оценить для принятия решения о тактике в отношении мерцательной аритмии?
Прежде всего следует расспросить пациента о частоте, длительности пароксизмов и их влиянии на жизнедеятельность. Переносимость пароксизмов оценивается по шкале симптомов EHRA, которая в обновленных рекомендациях ЕОК претерпела изменения: класс 2 разделен на 2а (легкие симптомы, нормальная жизнедеятельность пациента не нарушается) и 2b (умеренные симптомы, нормальная жизнедеятельность пациента не нарушается, но пациент обеспокоен симптомами). Таким образом, необходимо выяснить, нуждается ли пациент в терапии для прерывания текущего и последующих эпизодов аритмии.
При пароксизме ФП, сопровождающемся нарушениями гемодинамики, показана ургентная электрическая кардиоверсия. В остальных случаях первое, что делает врач после сбора анамнеза и физикального обследования, – назначает рутинную ЭКГ. На ЭКГ необходимо оценить следующие параметры: частоту мерцания предсердий, ЧСЖ, признаки активной ишемии, гипертрофии миокарда, рубцовых изменений, нарушений внутрижелудочковой проводимости (ширина комплексов QRS, наличие полных и неполных блокад ножек пучка Гиса).
Возможность применения антиаритмических препаратов (ААП) для восстановления синусового ритма зависит от наличия или отсутствия структурной патологии сердца. При ее наличии противопоказаны ААП I класса. Для отнесения пациента к категории «без структурной патологии сердца» необходимо учитывать следующие факторы:
- отсутствие Q-инфаркта миокарда в анамнезе;
- отсутствие гипертрофической или дилатационной кардиомиопатии;
- фракция выброса левого желудочка (ЛЖ) >45%;
- отсутствие застойной или прогрессирующей сердечной недостаточности (СН) и СН более II А стадии;
- отсутствие врожденных или ревматических пороков сердца;
- отсутствие выраженной гипертрофии ЛЖ (толщина одной из стенок ЛЖ ≥14 мм).
Артериальная гипертензия, хронические формы ишемической болезни сердца не являются противопоказаниями к применению ААП I класса, если не приводят к перечисленным выше изменениям.
Итак, в результате анализа совокупности рассмотренных выше данных принимается решение о восстановлении синусового ритма (электрическая или медикаментозная кардиоверсия) или переходе к тактике контроля ЧСЖ бета-адреноблокаторами и оптимизации лечения основного заболевания.
В соответствии с рекомендациями ЕОК у пациентов без ишемического или структурного поражения сердца флекаинид, пропафенон или вернакалант рекомендованы для фармакологической кардиоверсии новых эпизодов ФП длительностью не более 48 ч. У пациентов со структурной патологией сердца или активной ишемией единственным ААП для кардиоверсии остается амиодарон.
У пациентов с нечастыми симптомными пароксизмами ФП может использоваться тактика «таблетка в кармане» – прием единичной дозы флекаинида (200-300 мг) или пропафенона (450-600 мг) в амбулаторных условиях, когда пациент ощущает начало очередного эпизода аритмии. Это быстрый, эффективный и безопасный способ восстановления синусового ритма. Но перед тем как рекомендовать его пациенту, необходимо обязательно оценить показания и противопоказания, исключить структурную патологию сердца, а также проверить безопасность подхода «таблетка в кармане» в условиях стационара под наблюдением врача.
Кроме того, предварительная терапия флекаинидом, амиодароном, пропафеноном или ибутилидом может применяться для повышения эффективности плановой электрической кардиоверсии и профилактики рецидивов аритмии.
На украинский рынок компания «Сандоз» недавно вывела таблетированный флекаинид. Он применяется в Европе с 1982 года, но в Украине был доступен только в качестве гуманитарной помощи до 1996 года. В связи с тем что для многих врачей этот препарат новый, ведущие мастер-класса напомнили участникам его характеристики и особенности применения.
Флекаинид относится к ААП ІС класса. По механизму действия является ингибитором быстрых натриевых каналов клеточных мембран, благодаря чему резко угнетает фазу 0 потенциала действия, что на ЭКГ проявляется удлинением комплекса QRS, но практически не влияет на реполяризацию, поэтому не увеличивает интервал QT.
Биодоступность флекаинида – около 90%, пиковая концентрация в крови достигается через 3-4 ч после перорального приема. Период полувыведения в среднем 20 ч, что определяет двукратный прием. Биотрансформация происходит в печени с участием ферментов системы цитохрома Р450.
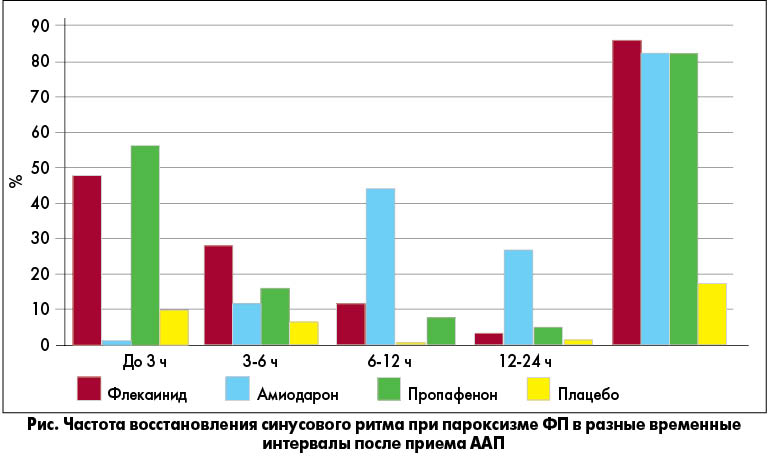
Параметры фармакокинетики определяют фармакодинамический профиль флекаинида. В пределах 3 ч после перорального приема в дозе 200 мг у пациентов с пароксизмом ФП синусовый ритм восстанавливается у 45% пациентов, до 6 ч – еще у 27%. Таким образом, окно максимального эффекта флекаинида – от 3 до 6 ч. В первые 6 ч флекаинид лидирует по эффективности в сравнении с амиодароном и пропафеноном (рис.). Частота восстановления ритма в этом промежутке времени достигала 73%. В пределах 24 ч ритм восстанавливался у 87,5% пациентов.
Побочные эффекты при приеме флекаинида возникают с частотой от 1 до 3%. Их перечень достаточно обширный, но большинство очень редкие (менее 1%). К дозозависимым побочным эффектам, которые непосредственно связаны с механизмом действия препарата, относятся учащение или урежение ритма, атриовентрикулярная блокада, симптомы нарушения гемодинамики (гипотония, головокружение, синкопе). Для профилактики побочных эффектов необходимо строго соблюдать рекомендованные дозы.
Однократная доза для восстановления ритма – 200 мг; при недостаточной эффективности через 3 ч можно принять еще 100 мг. Максимальная доза флекаинида – 400 мг/сут. Не рекомендуется ее применять, если пациент не отвечает на дозу 300 мг.
Поскольку флекаинид относится к I классу ААП, его можно применять только у пациентов без структурной патологии сердца. Все ААП обладают проаритмогенным потенциалом, и флекаинид не исключение, поэтому после назначения необходимо контролировать ЭКГ, особенно в первые дни терапии.
Критерии проаритмогенных эффектов:
- при терапии ФП – рецидив аритмии в виде трепетания предсердий с проведением на желудочки в соотношении 1:1;
- двунаправленная тахикардия torsade de pointes;
- появление или усугубление имеющейся дисфункции синусового узла;
- развитие или усугубление атриовентрикулярной блокады;
- развитие внутрижелудочковых блокад;
- увеличение частоты пароксизмов наджелудочковой тахикардии, ФП, предсердной экстрасистолии.
Последний вопрос, рассмотренный в рамках мастер-класса: когда и как использовать противорецидивный прием ААП у пациентов с редкими пароксизмами ФП? Предложить пациенту поддерживающую антиаритмическую терапию следует в случаях, когда пароксизмы становятся чаще, удлиняются, становятся гемодинамически нестабильными или появляются новые провоцирующие факторы. Но главное, на что следует обращать внимание, – это течение основного заболевания, послужившего причиной возникновения аритмии. Если пароксизмы становятся более частыми, то обязательно необходимо выяснить, что произошло с пациентом и его сердцем между визитами к врачу. Принцип здесь такой же, как при первичном обращении: начинать не с антиаритмической терапии, а с уточнения причины ФП и оптимизации лечения основного и коморбидных заболеваний (контроль артериального давления, функции щитовидной железы, менеджмент стресса, нормализация массы тела, уменьшение интенсивности или отказ от курения). Важные факторы, влияющие на течение и заболевания сердца, и ФП, – курение и прием алкоголя.
Для удержания синусового ритма после успешной кардиоверсии при пароксизмальной ФП начальная доза флекаинида должна составлять 50 мг 2 р/сут. Титровать дозу под контролем ЭКГ следует через 2-3 дня до достижения целевой – 100 мг 2 р/сут. При увеличении продолжительности комплекса QRS на 25% от исходного препарат следует отменить.
Также необходимо помнить о других противопоказаниях, не связанных со структурной патологией сердца. Флекаинид противопоказан пациентам с клиренсом креатинина <50/мин и при тяжелых заболеваниях печени. Это означает, что функцию почек и печени также следует периодически контролировать на фоне длительного приема препарата. Момент отмены может наступить не по кардиальным противопоказаниям, даже если ритм успешно контролируется.
По данным разных исследований, при длительном применении для профилактики рецидивирования ФП эффективность флекаинида сопоставима с эффективностью пропафенона и составляет около 75%. Есть данные о том, что комбинация флекаинида с бета-блокатором более эффективно предотвращает рецидивы ФП. В исследовании Capucci и соавт. (2016) частота рецидивирования у пациентов, которые принимали флекаинид в комбинации с метопрололом, в течение года составила 46,8% по сравнению с 66,7% в группе монотерапии флекаинидом.
Обобщая информацию, полученную в ходе мастер-класса, следует отметить, что Флекаинид Сандоз стал существенным пополнением арсенала ААП, рекомендованных ЕОК для восстановления и удержания синусового ритма у пациентов с пароксизмальной ФП. Флекаинид может применяться для фармакологической кардиоверсии в стационаре, в качестве стратегии «таблетка в кармане» амбулаторно, для повышения эффективности электрической кардиоверсии, а также для поддерживающей противорецидивной терапии у пациентов с симптомными пароксизмами ФП. Исследования и практика подтверждают, что это эффективный и безопасный препарат при условии соблюдения дозировок, исключения структурной патологии сердца и тщательного мониторирования ЭКГ.
Подготовил Дмитрий Молчанов
3-06-ФЛК-РЕЦ-0917


