12 жовтня, 2017
Сучасні методи терапії алергічних захворювань глоткового мигдалика
Незважаючи на доволі широку поширеність такого захворювання, як аденоїдит, питання про оперативне й консервативне лікування цієї хвороби на вітчизняних науково-практичних конференціях обговорюється нечасто. Ще рідше розглядається проблема алергічних аденоїдитів.

Саме цю складну дискутабельну й, безумовно, актуальну тему обрав для своєї доповіді в рамках науково-практичної конференції «Міждисциплінарний підхід до діагностики та лікування тонзиліту з позицій доказової медицини», що відбулася 21 квітня в Харкові, завідувач кафедри оториноларингології Одеського національного медичного університету, доктор медичних наук, професор Сергій Михайлович Пухлік.
– Алергічний аденоїдит (АА) – це хронічне захворювання глоткового мигдалика, яке розвивається внаслідок контакту з алергенами й проявляється утрудненням носового дихання, ринореєю, відчуттям свербіння в носі, хропінням і гугнявістю. Основою патогенезу АА є продукція антитіл, що агресивно поводяться стосовно потенційного алергену, намагаючись відторгнути його. Відтак алергія являє собою своєрідну «ведмежу послугу» імунної системи, яка проявляється виробленням антитіл на у принципі нешкідливі речовини. Продукція антитіл, а також їхня зустріч з алергенами провокують алергічну реакцію, одним із проявів якої і є АА з формуванням характерних назальних і позаназальних симптомів.
Глотковий мигдалик розташований у «критичній зоні», у якій реєструють найбільш інтенсивний антигенний вплив – як інфекційної, так і неінфекційної природи. При алергічному риніті (АР) аденоїди стають своєрідним шоковим органом, на поверхні якого затримуються інгаляційні алергени. Вітчизняні й зарубіжні дослідники докладно описали патогенез формування симптомів АА. Основними його етапами є такі:
1. Утруднення назального дихання (через будь-яку причину).
2. Порушення мукоциліарного транспорту й виникнення застою слизу в порожнині носа та носоглотці.
3. Фіксовані в порожнині носа й носоглотці алергени стають тригерами алергічного запалення, на цьому тлі розмноження вірусів та бактерій призводить до виникнення інфекційного запалення.
Взагалі аденоїдит і гіпертрофія глоткового мигдалика (ГГМ) – доволі поширені у дитячому віці. Проте доведено, що ГГМ частіше трапляються саме в дітей з атопією. У дослідженні M. Modrzynski і E. Zavisza (2007) зазначається, що найчастіше ГГМ зустрічається у дітей з АР чи з АР у поєднанні з бронхіальною астмою (БА). При цьому частота ГГМ у дітей з АР у віці 6 років сягає 90%. Найбільш значуща стосовно ГГМ сенсибілізація спостерігається на пилок дерев, рослин та плісняві грибки.
Тож який механізм розвитку ГГМ при АР? У хворих на АР синтез IgE відбувається переважно в ділянці лімфоепітеліального кільця Пирогова-Вальдейєра та в лімфатичних вузлах, а не на слизовій оболонці порожнини носа, на якій опасисті клітини з’являються уже вкриті антитілами. Тобто в глотковому мигдалику відбувається переключення синтезу антитіл на IgE, що призводить до розвитку IgE-залежного алергічного запалення. При цьому еозинофільний катіонний протеїн і численні прозапальні цитокіни тривалий час стимулюють тканину глоткового мигдалика, що й спричиняє його гіпертрофію.
Дуже важливим питанням є своєчасна діагностика АА, що сприяє профілактиці розширення спектра алергенів та розвитку БА. Сучасний діагностичний алгоритм АА має передбачати:
• збір скарг і поглиблення вивчення анамнезу;
• об’єктивне обстеження хворого;
• алерготестування;
• консультування у лікарів-спеціалістів.
На жаль, наразі склалася ситуація, коли лікарі суміжних спеціальностей у дитини з АА можуть побачити симптоми різних захворювань: оториноларинголог – аденоїдит і ГГМ, алерголог – АР, невролог – затримку психорозумового розвитку, а педіатр узагалі бачить пацієнта, що хворіє часто й тривалий час. Незалежно від спеціальності лікарі, на прийом до яких приходять такі діти, мають розуміти, що назальні симптоми в поєднанні з поганим сном, хропінням, відставанням у розвитку, сонливістю тощо з високою ймовірністю можуть бути проявами алергії. Ендоскопічними ознаками АА є блідо-рожевий колір лімфоїдної тканини, виражена набряклість, згладжена поверхня і рясний секрет слизового характеру. На відміну від АА неалергічний аденоїдит проявляється гіперемією лімфоїдної тканини, незначним набряком, згладженою поверхнею та слизово-гнійним секретом. Безумовно, основою діагностики АА є алерготестування.
Тим часом не лише діагностика АА є складним питанням – лікування також викликає безліч суперечок. Проте у разі встановлення правильного діагнозу алгоритм лікування доволі простий. Утім, слід зауважити, що алергія не виліковується у повному розумінні цього слова, адже «забути» алерген імунна система може тільки у разі тотального імунодефіциту. Отже, завданням лікування АА має бути усунення симптомів та індукція тривалої ремісії. Відповідно до сучасної концепції основою медикаментозного лікування АА є ступінчасте застосування патогенетично зумовленої фармакотерапії, що ґрунтується на розумінні основних механізмів розвитку алергії. Принципи лікування АА відповідно до ступеня тяжкості захворювання наведені в таблиці 1.
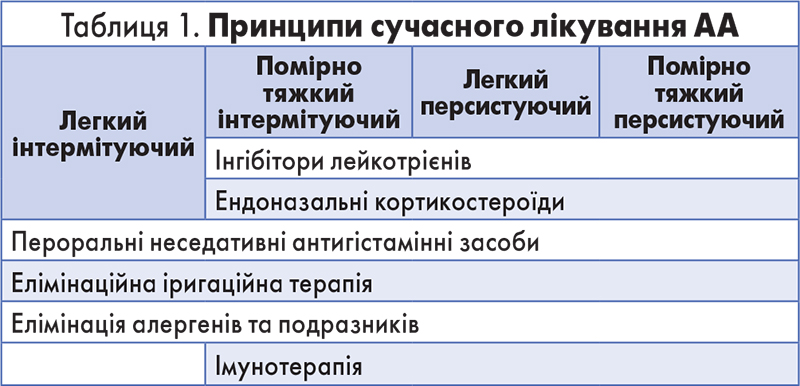
Призначення елімінаційної іригаційної терапії необхідне для очищення слизової оболонки від патогенів та алергенів, пилових іригантів, продуктів клітинного розпаду й запальних субстанцій, а також від густого секрету. Іригаційну терапію проводять із використанням ізотонічних розчинів морської солі. Подальші призначення потрібно робити з огляду на дані щодо дії основних груп лікарських засобів на симптоми АА, а також на тяжкість захворювання. Ефективність різних груп препаратів, що використовують для усунення проявів алергії, стосовно різних симптомів АА і АР наведено в таблиці 2.
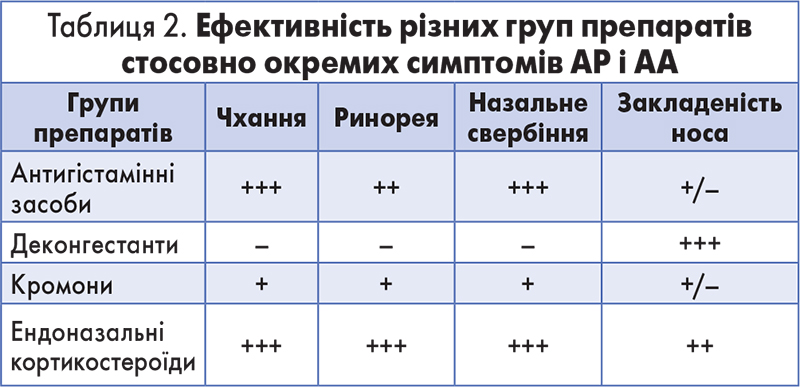
Як бачимо, антигістамінні засоби (АГС) тією чи іншою мірою здатні подолати всі симптоми алергії. АГС являють собою групу лікарських засобів, дія яких реалізується через зв’язування на конкурентних принципах із рецепторами гістаміну на клітинах різних тканин організму. Таким чином нівелюються ефекти гістаміну на органи-мішені. Як відомо, саме гістамін є основним медіатором алергічного запалення, що відіграє провідну роль у виникненні таких симптомів, як порушення носового дихання, ринорея, чхання, свербіж.
АГС традиційно поділяють на дві групи-покоління. Залежно від приналежності конкретного АГС до одного з поколінь можна говорити про рівень побічних ефектів під час використання цього засобу. АГС першого покоління (димедрол, супрастин, діазолін, тавегіл, піпольфен тощо) мають суттєві недоліки, до яких, зокрема, належать:
• короткочасність антигістамінної дії (1-3 год);
• неповне зв’язування з Н1-гістаміновим рецептором;
• проникнення через гематоенцефалічний бар’єр (снодійна дія, седація);
• швидке звикання (7-12 діб);
• неселективність дії (зв’язування з іншими рецепторами: М-холінорецепторами, α-адренорецепторами).
Натомість АГС другого покоління (наприклад, лоратадин, цетиризин) мають такі переваги:
• відсутність седативної дії у терапевтичних дозах;
• швидкий початок дії (1-3 год);
• тривалість дії 12-24 год;
• відсутність тахіфілаксії при тривалому застосуванні.
Проте й серед АГС другого покоління існують певні відмінності. Наприклад, лоратадин, акривастин метаболізуються в печінці через систему цитохрому Р450 і перетворюються в активні метаболіти, які й блокують Н1-рецептори гістаміну. Натомість цетиризин (Цетрин©) – активний метаболіт, лише 8-10% активної речовини метаболізується в печінці. Завдяки цьому цетиризин не конкурує за ферментні системи печінки й не впливає на метаболізм інших лікарських засобів. Узагалі цетиризин має сприятливі фармакокінетичні характеристики. Так, цетиризин має низький обсяг розподілення, що забезпечує створення високих концентрацій препарату в ділянці основного розташування Н1-рецепторів – міжклітинному просторі. Майже повна відсутність проникнення в клітину забезпечує нівелювання ризику токсичної дії засобу на клітини органів. Висока ефективність цетиризину доведена в ході багатьох клінічних досліджень. Так, Lee і співавт. (2009) довели, що протизапальна активність цетиризину є вищою за таку в левоцетиризину. Окрім того, цетиризин наразі є найбільш вивченим АГС другого покоління, що забезпечує безпечність лікування будь-яких алергічних захворювань.

Ще однією групою препаратів, які суттєво впливають на прояви АА, є топічні кортикостероїди (ТКС). Необхідно нагадати, що цю групу препаратів не слід використовувати при легких інтермітуючих симптомах АА і АР. Проте ТКС – сучасні засоби контролю за алергією. Маємо пам’ятати, що не всі ТКС однакові й відрізняються ступенем біодоступності, що й зумовлює профіль безпеки кожного окремого препарату. Перед призначенням ТКС варто звернути увагу на вікові обмеження, зазначені в інструкції.
Терапію АГС і ТКС можуть використовувати у своїй практиці лікарі будь-яких спеціальностей, натомість імунотерапія – поле діяльності лікарів-алергологів. Імунотерапія вважається сучасним засобом індукції тривалої ремісії алергічних захворювань, профілактикою розширення спектра алергенів й розвитку БА.
Доповідь професора С.М. Пухліка викликала великий резонанс серед президії та гостей конференції, адже АА досі залишається захворюванням, яке не завжди вчасно розпізнають, діагностують і призначають правильне лікування. Лікарі-практики мають пам’ятати: щороку захворюваність на алергію зростає і треба бути особливо пильними у разі наявності симптомів тривалої хвороби респіраторного тракту, особливо якщо йдеться про дітей.
Підготувала Олександра Мєркулова
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 2 (39), травень 2017 р.


