12 жовтня, 2017
Лимфогенный карциноматоз легких: клинические наблюдения

 Лимфогенный карциноматоз легких (ЛКЛ) представляет собой вторичный неопластический процесс с распространением опухолевых клеток по лимфатическим сосудам. В большинстве случаев ЛКЛ является результатом первично гематогенного метастазирования, проявляющегося на рентгенограммах и компьютерных томограммах в виде уплотнений – узелков, образований и консолидаций. Приблизительно в 6-8% случаев ЛКЛ характеризуется распространением опухолевого процесса исключительно в интерстиции легкого [1] без нарушения нормальной архитектоники легочной паренхимы, что обусловливает трудности в диагностике процесса.
Лимфогенный карциноматоз легких (ЛКЛ) представляет собой вторичный неопластический процесс с распространением опухолевых клеток по лимфатическим сосудам. В большинстве случаев ЛКЛ является результатом первично гематогенного метастазирования, проявляющегося на рентгенограммах и компьютерных томограммах в виде уплотнений – узелков, образований и консолидаций. Приблизительно в 6-8% случаев ЛКЛ характеризуется распространением опухолевого процесса исключительно в интерстиции легкого [1] без нарушения нормальной архитектоники легочной паренхимы, что обусловливает трудности в диагностике процесса.
В большинстве случаев ЛКЛ возникает при новообразованиях молочной железы, легкого, желудка, толстого кишечника, почек и предстательной железы [1-4].
Основные клинические проявления ЛКЛ – это прогрессирующая одышка, непродуктивный кашель и общая слабость.
Ведущим методом диагностики ЛКЛ является компьютерная томография высокого разрешения (КТВР).
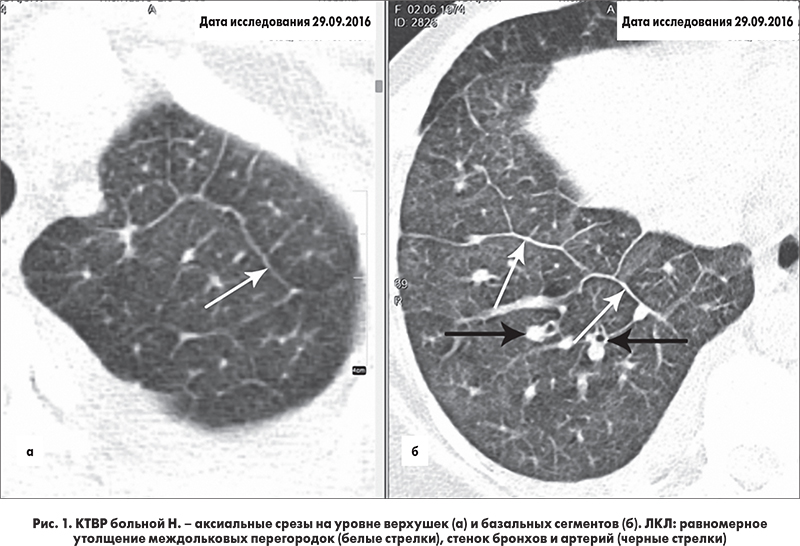
ЛКЛ характеризуется преобладанием интерстициальных (ретикулярных) изменений. Наибольшее диагностическое значение имеет равномерное утолщение междольковых перегородок без нарушения архитектоники легочной ткани в сочетании с перибронхиальными и периваскулярными муфтами (рис. 1) [5].
У части больных одновременно наблюдается увеличение лимфатических узлов средостения и накопление жидкости в плевральных полостях. Изменения в легких чаще носят двусторонний характер и более выражены в базальных отделах. Одностороннее поражение, в том числе в пределах одной доли легкого, характерно для лимфогенных метастазов рака легкого и молочной железы [6].
КТ-картина ЛКЛ в ранних стадиях процесса существенно зависит от механизма распространения опухоли. При антеградном распространении процесса от плевры к корню преобладают изменения периферического (междолькового) и внутридолькового интерстиция, часто с плевральным выпотом. Ретроградное распространение опухоли из лимфатических узлов корня легкого характеризуется преобладанием изменений центрального (перибронховаскулярного) интерстиция и более частым увеличением лимфатических узлов [6].
При ЛКЛ могут выявляться узелки, которые имеют различное происхождение. Это отчетливо видно только при КТ-исследовании. Часть узелков представляют собой разрастания опухолевой ткани вдоль лимфатических сосудов. Такие узелки размерами 1-2 мм располагаются перилимфатически, то есть в утолщенных стенках вторичных легочных долек, вдоль сосудов и бронхов, в междолевой плевре. Реже узелки видны вне связи с интерстициальными структурами, непосредственно в легочной ткани. Их происхождение связывают с одновременным гематогенным метастазированием [5, 7].
Утолщение стенок крупных долевых и сегментарных артерий и бронхов, составляющих так называемый центральный интерстиций, является важнейшим отличительным признаком ЛКЛ. Эти изменения наиболее выражены при ретроградном распространении опухолевых клеток из лимфатических узлов средостения в легочную ткань. При этом стенки крупных бронхов оказываются значительно толще, чем в норме, просвет бронхов уменьшается, а наружный контур их становится нечетким, часто лучистым. Диаметр расположенных рядом с бронхами артерий также увеличен, контуры их могут быть нечеткими. Часто эти изменения сочетаются с уплотнением перибронхиальной легочной ткани за счет лимфостаза [5, 6].
Выявление ЛКЛ даже в ранних стадиях процесса практически не влияет на исход заболевания. Более половины больных с такими изменениями умирают в течение ближайших трех месяцев. Поэтому основное значение лучевого исследования заключается в предотвращении ненужного оперативного вмешательства в случае выявления признаков ЛКЛ [6].
Ниже представлено описание двух клинических случаев ЛКЛ с локализацией процесса исключительно в интерстиции без признаков гематогенного метастазирования в виде уплотнений паренхимы, что представляет наибольшие трудности для диагностики.
Клинический случай № 1
Пациентка Н., 1974 года рождения, поступила 03.10.2016 в пульмонологическое отделение Волынской областной клинической больницы (ВОКБ) с жалобами на одышку и сердцебиение при умеренной физической нагрузке, непродуктивный кашель, общую слабость.
Считает себя больной с апреля 2016 года, когда без очевидных причин появился сухой кашель, который имел непостоянный характер и не ограничивал повседневную активность пациентки. К врачу не обращалась.
В сентябре на фоне непродуктивного кашля появилась одышка, которая быстро нарастала. Пациентке проведена КТ органов грудной полости (КТ ОГП) 29.09.2016, а 03.10.2016 она была направлена в ВОКБ для консультации и в этот же день госпитализирована.
Работает учителем в средней школе. Не курит, аллергических заболеваний в анамнезе нет. Сопутствующие болезни – киста правой доли щитовидной железы, фибромиома матки.
Объективно: состояние удовлетворительное, цианоза кожи и слизистых оболочек нет. Периферические лимфатические узлы не увеличены, пальпируется узел в правой доле щитовидной железы.
Частота дыханий (ЧД) в покое – 19/мин, дыхание в легких с жестким оттенком, хрипов нет. Насыщение крови кислородом при пульсоксиметрии – 96% в покое. Частота сердечных сокращений (ЧСС) – 108 уд/мин, артериальное давление (АД) – 130/90 мм рт. ст. Тоны сердца ритмичны, выслушивается акцент II тона над легочной артерией.
Живот мягкий, безболезненный; печень не увеличена. Периферических отеков нет.
КТ ОГП от 29.09.2016: двусторонняя прикорневая лимфаденопатия, диффузное снижение прозрачности паренхимы легких по типу матового стекла.
Анализ крови: гемоглобин – 141 г/л, эритроциты – 5,6×1012/л, лейкоциты – 6,6×109/л, эозинофилы – 6%, палочкоядерные – 1%, сегментоядерные – 64%, моноциты – 9%, лимфоциты – 20%, тромбоциты – 316×109/л, СОЭ – 26 мм/ч.
Анализ мочи: удельный вес – 1017, белок не обнаружен, сахар не обнаружен, лейкоциты – 0-1 в поле зрения.
Биохимическое исследование крови: билирубин общий – 8,5 мкмоль/л, общий белок – 66,0 г/л, креатинин – 46,0 мкмоль/л, глюкоза крови – 6,4 ммоль/л, АЛТ – 9 Ед/л.
Спирометрия: умеренные нарушения вентиляционной функции легких рестриктивного типа.
Электрокардиография (ЭКГ): неполная блокада правой ножки пучка Гиса.
Эхокардиографическое исследование (ЭхоКГ): признаки легочной гипертензии I степени.
УЗИ органов брюшной полости и почек: печень не изменена, пристеночные множественные полипы желчного пузыря размерами 3-5 мм; эхогенность ткани поджелудочной железы повышена за счет мелкоочаговых фиброзных изменений; селезенка не увеличена, правосторонний нефроптоз, паренхима почек не изменена.
УЗИ органов малого таза: признаки миомы матки.
Цитология пунктата правой доли щитовидной железы: цитограмма соответствует узловому зобу с кистозной дегенерацией.
Клинический диагноз: интерстициальное заболевание легких неуточненное (саркоидоз органов дыхания ІІ стадии (?) гиперсенситивный пневмонит(?)), синдром легочной гипертензии, легочная недостаточность (ЛН) І степени.
Назначено лечение метилпреднизолоном в дозе 32 мг/сут в сочетании с препаратами калия и кальция.
Для уточнения диагноза больная была направлена в Национальный институт фтизиатрии и пульмонологии им. Ф.Г. Яновского НАМН Украины (НИФП НАМН Украины).
25.10.2016 – консультация в НИФП НАМН Украины.
Субъективные проявления болезни прежние – одышка при выполнении привычной физической нагрузки, сухой кашель, общая слабость.
Состояние пациентки удовлетворительное, одышки и цианоза в покое и при разговоре нет. ЧД – 20/мин, аускультативное дыхание в легких с жестким оттенком, хрипов нет. ЧСС – 96 уд/мин, АД – 125/90 мм рт. ст. Тоны сердца ритмичны, акцент II тона над легочной артерией.
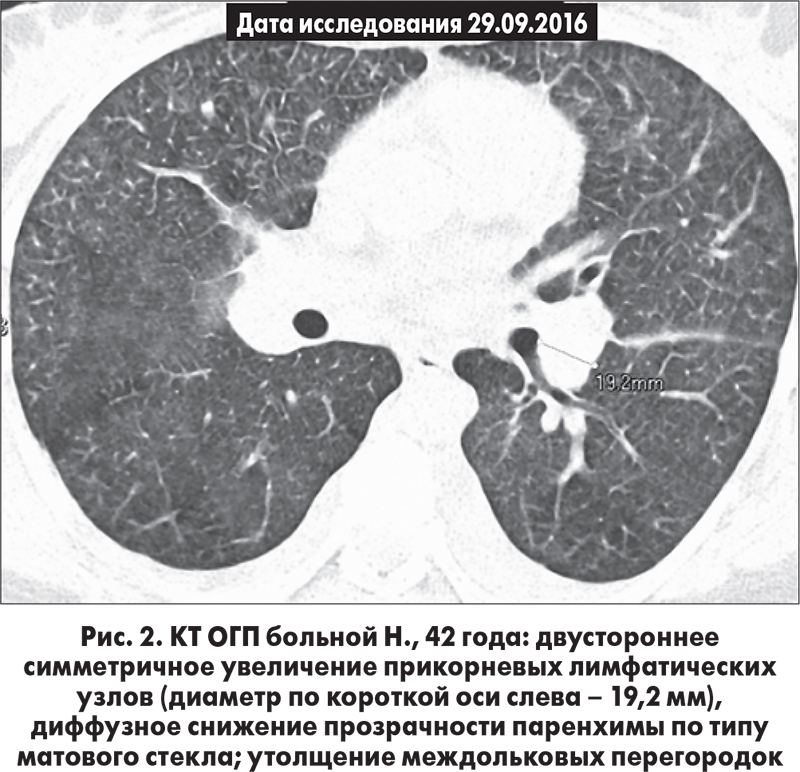
КТ ОГП от 29.09.2016: двустороннее симметричное увеличение прикорневых лимфатических узлов (диаметр по короткой оси – 18-20 мм), края узлов ровные без признаков периаденита в паренхиме (рис. 2); увеличение медиастинальных узлов паратрахеальной группы и области аортопульмонального окна (рис. 3); диффузное снижение прозрачности паренхимы по типу матового стекла; утолщение междольковых перегородок.
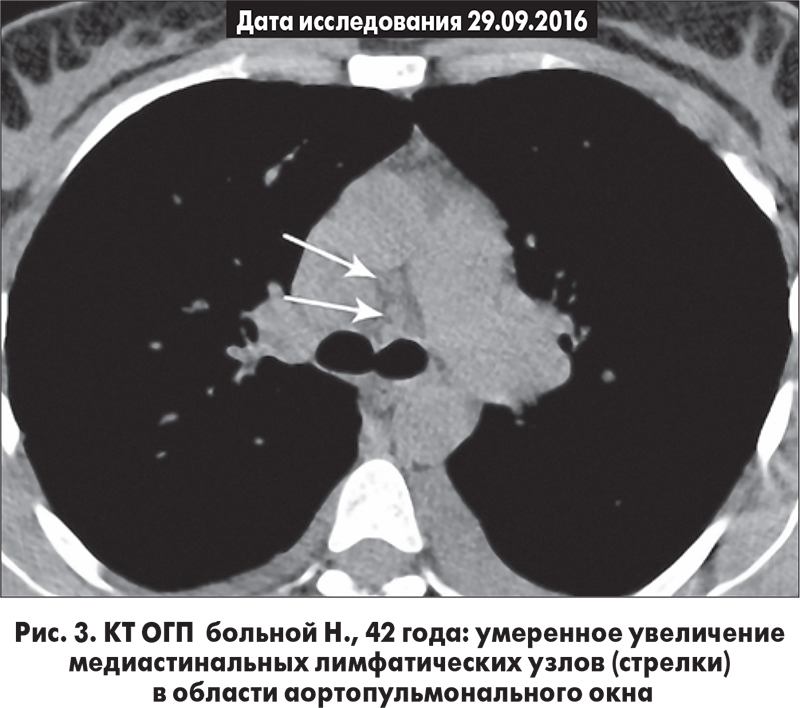
Атипичными, но не противоречащими диагнозу саркоидоза КТ-симптомами были диффузное распределение зон «матового стекла» и равномерное утолщение междольковых перегородок без характерных для саркоидоза четкообразных утолщений. Учитывая наличие высокоспецифичного для саркоидоза симптома билатеральной симметричной прикорневой лимфаденопатии, умеренное увеличение медиастинальных лимфатических узлов характерной локализации, а также принимая во внимание совместимую клиническую семиотику, больной был установлен диагноз: саркоидоз органов дыхания ІІ стадии, впервые выявленный, ЛН І степени. Рекомендовано уменьшить дозу метилпреднизолона до 24 мг/сут.
30.10.2016 больная отметила резкое ухудшение самочувствия: усилилась одышка при незначительной физической нагрузке и общая слабость. 31.10.2016 в порядке cкорой помощи повторно госпитализирована в пульмонологическое отделение ВОКБ.
На момент госпитализации общее состояние средней тяжести. Дыхание в покое – 23-25/мин, при минимальной нагрузке увеличивается до 30-35/мин. Насыщение крови кислородом в покое – 90%, при нагрузке снижается до 80%. Дыхание везикулярное, хрипов нет. Тахикардия до 102 уд/мин, АД – 110/60 мм рт. ст. Тоны сердца ослаблены, выслушивается акцент ІІ тона над легочной артерией. Живот при пальпации мягкий, безболезненный. Периферических отеков нет.
КТ ОГП от 31.09.2016: признаки двустороннего диффузного снижения пневматизации паренхимы по типу матового стекла, утолщение интерстиция в сочетании с двусторонней прикорневой лимфаденопатией; по сравнению с данными от 29.09.2016 существенной динамики КТ-данных не отмечается за исключением увеличения поперечных размеров сердца. Заключение: КТ-картина может соответствовать гранулематозу (наиболее вероятно – саркоидоз), дифференцировать с васкулитами, гиперсенситивным пневмонитом (менее вероятно).
Анализ крови: гемоглобин – 140 г/л, эритроциты – 5,9×1012/л, лейкоциты – 14,6×109/л, сегментоядерные – 95%, моноциты – 2%, лимфоциты – 3%, тромбоциты – 218×109/л, СОЭ – 3 мм/ч.
Анализ мочи: без особенностей.
Биохимическое исследование крови: креатинин – 58,0 мкмоль/л, глюкоза крови – 6,8 ммоль/л, АЛТ – 9 Ед/л. СРП – 28,3 (норма – до 5,0 в ед. СИ).
ЭКГ: ритм синусовый, правильный; ЧСС – 119 уд/мин, неполная блокада правой ножки пучка Гиса; отрицательный Т в ІІІ и AVF, V1, V4 отведениях.
ЭхоКГ: увеличение полости правого желудочка, регургитация на митральном и трикуспидальном клапанах, признаки легочной гипертензии.
Консилиум врачей в составе заместителя главного врача, заведующего пульмонологическим отделением, кардиолога, завотделением кардиохирургии, ревматолога, завотделением интервенционной радиологии, завотделением реанимации: саркоидоз ІІ стадии с преимущественным поражением паренхимы легких, вторичная легочная гипертензия. Лечение: оксигенотерапия в режиме 5 л/мин, эноксапарин, илопрост, метилпреднизолон (52 мг/сут), фуросемид, бисопролол.
С 06 на 07.11.2016 общее состояние больной резко ухудшилось: усилилась одышка в покое, тахикардия – 120 уд/мин, АД – 90/60 мм рт. ст. 07.11.2016 в 14:30 – внезапная потеря сознания, остановка дыхания и сердечной деятельности. После безрезультатных реанимационных мероприятий констатирована смерть.
Клинический диагноз: саркоидоз органов дыхания ІІ стадии, диффузное альвеолярное поражение легких, тромбоэмболия легочной артерии (?), острая дыхательная недостаточность, острая сердечно-сосудистая недостаточность.
При аутопсийном исследовании легкие мраморного вида, бледно-розового и серо-оранжевого цвета, пальпаторно на всем протяжении умеренно плотные, на разрезе однородные, без патологических включений. Паратрахеальные и трахеобронхиальные лимфоузлы увеличены в размерах (от 0,8 до 3 см в диаметре), спаяны между собой, на разрезе серо-коричневого цвета с мелкими включениями бело-серого цвета.
Микроскопическое описание тканей легких и лимфатических узлов: во всех биоптатах легких и практически во всех забранных при аутопсии лимфоузлах (кроме одного) множественные, различных размеров метастазы – округлой формы разрастания опухолевых клеток эпителиальной природы. В крупных метастазах – признаки центрального некроза. Клетки опухоли средне-крупных размеров, относительно мономорфные, со светлой цитоплазмой и мелким темным ядром, часто эксцентрически расположенным. В некоторых полях зрения опухолевые клетки формируют примитивные железистые структуры (рис. 4).
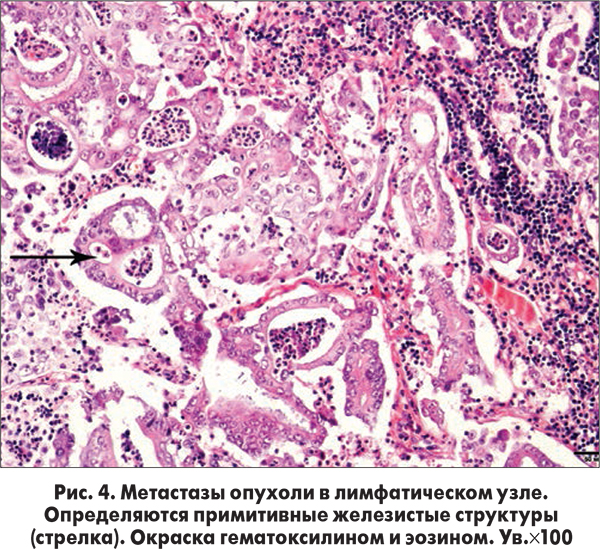
В легких обращает внимание исключительно периваскулярное и перибронхальное расположение опухолевых пролифератов, что является важным диагностическим признаком лимфогенного метастазирования (рис. 5).
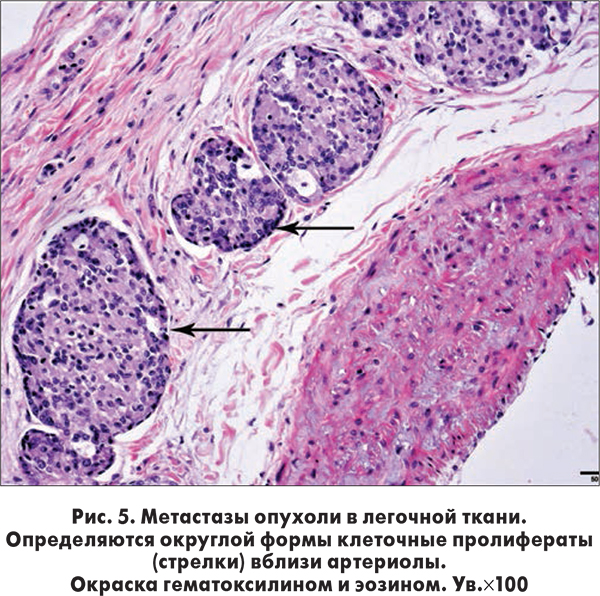
Заключение: лимфогенные метастазы аденокарциномы в легких и лимфатических узлах грудной полости с анонимной первичной опухолью.
Выполнено иммуногистохимическое исследование для верификации не первичного характера опухолевого поражения легких с использованием следующей панели маркеров: TTF‑1, Napsin A, CK7 (лаборатория патоморфологии CSD Health сare, г. Киев, зав. – Е.А. Кошик).
Результаты исследования опухолевых клеточных разрастаний в легочной ткани: TTF‑1 – негативная реакция клеток опухоли, Napsin A – негативная реакция клеток опухоли, СК7 – выраженная позитивная реакция клеток опухоли. Таким образом, можно заключить, что ЛКЛ развился из анонимной первичной опухоли нелегочного происхождения.
Клинический случай № 2
Больной П., 34 года, был госпитализирован в отделение интерстициальных заболеваний легких НИФП НАМН Украины по направлению Днепропетровской областной больницы с целью уточнения диагноза.
Поступил с жалобами на одышку при незначительной физической нагрузке, сухой кашель, потерю массы тела около 10 кг за 3 месяца, выраженную общую слабость.
Из анамнеза известно, что около 3 месяцев назад (в начале декабря 2016 года) появился сухой приступообразный кашель, стали беспокоить одышка при нагрузке и общая слабость. После проведения рентгенографии органов грудной полости был госпитализирован в центральную районную больницу с диагнозом негоспитальной пневмонии. После безуспешной антибактериальной терапии направлен в Днепропетровскую областную больницу, где был установлен диагноз: неспецифическая интерстициальная пневмония неуточненного генеза, по поводу чего с 06.01.2017 по 25.01.2017 проводилось лечение глюкокортикостероидами. Вместе с тем состояние больного прогрессивно ухудшалось: усилилась одышка, нарастала общая слабость.
Заболеваний легких в анамнезе нет. Курил на протяжении 10 лет, бросил в декабре 2016 г. Работает кассиром на автозаправочной станции, контакта с токсичными веществами не имел. Сведений в анамнезе о хронических заболеваниях органов дыхания у родственников нет. На протяжении последних 5 лет периодически беспокоят боли в эпигастральной области, однако к врачу не обращался.
Объективно: состояние относительно удовлетворительное – одышки, цианоза в покое нет.
Периферические лимфатические узлы не увеличены. ЧД – 24/мин. Притупление перкуторного тона в подлопаточных областях. Аускультативно над легкими дыхание везикулярное, в базальных отделах резко ослабленное. ЧСС – 108 уд/мин. АД – 122/80 мм рт. ст. При аускультации тоны сердца ясные, шумов нет. Живот при пальпации мягкий, печень не увеличена. Периферических отеков нет.
КТВР от 10.01.2017 (выполнена в Днепропетровской областной больнице): во всех легочных зонах определяется значительное равномерное утолщение междольковых перегородок (рис. 6); уплотнений легочной паренхимы не определяется; двустороннее увеличение прикорневых лимфатических узлов (до 20 мм по короткой оси) и медиастинальных – в области бифуркации трахеи. КТ-картина соответствует ЛКЛ.
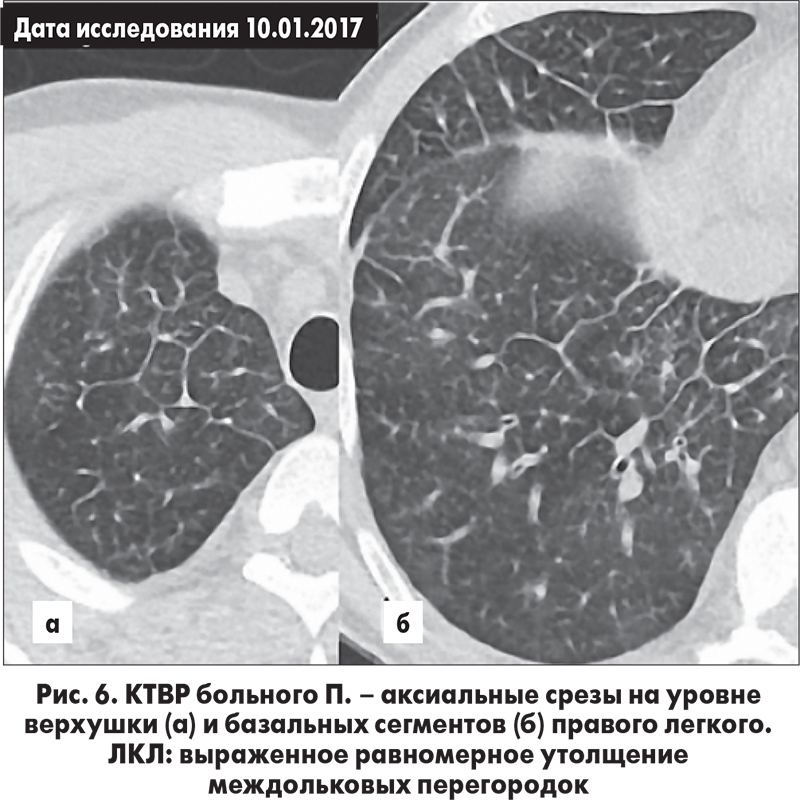
Спирометрия от 31.01.2017: VC – 54,3% должной величины, FVC – 52,5%, FEV1 – 46,3%, FEV1/FVC – 73,0% (умеренно выраженные рестриктивные нарушения).
Диффузионная способность легких: DLCO – 38% должной величины (умеренно выраженные нарушения).
Общий анализ крови: лейкоциты – 13,9×109л, СОЭ – 13 мм/ч, в остальном – без особенностей.
Физикальные признаки двустороннего плеврального выпота были подтверждены при УЗИ. Во время пункции левой плевральной полости было эвакуировано около 700 мл серозной жидкости, при цитоморфологическом исследовании пунктата были обнаружены элементы железистого рака (рис. 7).
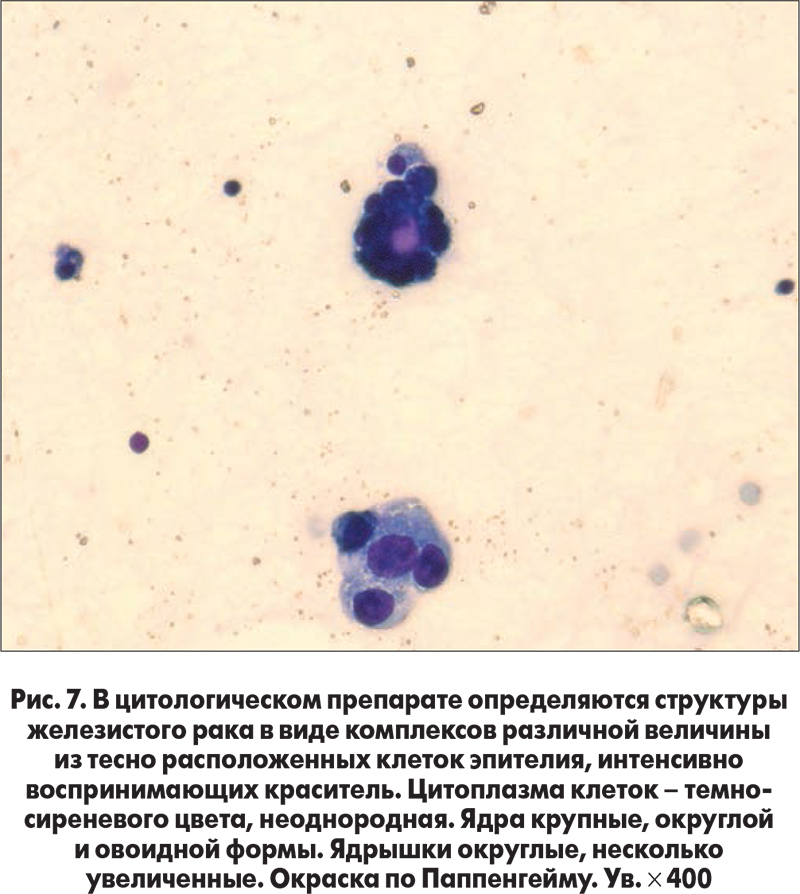
Пациент был направлен на консультацию в Национальный институт рака, где дополнительно была проведена КТ органов грудной и брюшной полости с контрастированием: помимо ЛКЛ выявлены множественные метастазы в забрюшинные и брюшные лимфоузлы, а также в кости позвоночника, лопатки, рукоятки и тела грудины, тазовых костей.
Как и в первом случае, первичный источник метастазирования не был идентифицирован.
Пациент был выписан для симптоматического лечения под наблюдение онколога по месту жительства. По информации родственников, больной умер через две недели после выписки.
Литература
1. Bruce D.M. Limphangitis carcinomatosa: a literature review / D.M. Bruce, S.D. Heys, O. Eremin // J.R. Coll. Surg. Edinb. – 1996. – Vol. 41. – P. 7-13.
2. Gudatti A.K. Pulmonary Limphangitic Carcinomatosis due to renal cell carcinoma / A.K. Gudatti, C.P. Marak // Case Rep. Oncol. – 2012. – Vol. 5. – P. 246-252.
3. Witczak A. Pulmonary limphangitic Carcinomatosis in the course of gastric cancer – Case report / A. Witczak, A. Prystupa, M. O. Zamecka, et al. // Pre-Clin. Clin. Res. – 2014. – Vol. 8. – H. 116-119.
4. Albhaisi S. Pulmonary Limphangitic Carcinomatosis due to Metastatic Adenocarcinoma of the Lung / S. Albhaisi, N. Luqman // Clin. Med. Rev. Case Rep. – 2016. – Vol. 3. – P. 99.
5. Gotway M.B. High-Resolution CT of the Lung: Patterns of Disease and Differential Diagnoses / M.B. Gotway, G.P. Reddy, W.R. Webb, et al. // Radiol. Clin. N. Am. – 2005. – Vol. 43. – P. 513-542.
6. Johkoh T. CT Findings in Limphangitic Carcinomatosis in the Lung: Correlation with Histologic Findings and Pulmonary Tests / T. Johkoh, J. Tomiyama, N. Nagareda, et al. // AJR. – 1992. – Vol. 158. – P. 1217- 1222.
7. Elicker B. High-resolution computed tomography patterns of diffuse interstitial lung disease with clinical and pathological correlation / B. Elicker, C.A. Pereira, R. Webb, et al. // J. Bras. Pneumol. – 2008. – Vol. 34. – P. 715-744.
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 2 (39), травень 2017 р.


