16 жовтня, 2017
Сучасні клінічні рекомендації з лікування тонзилофарингіту та профілактика його ускладнень у дітей

20-22 вересня 2017 р. у м. Полтава відбулася XIX Всеукраїнська науково-практична конференція «Актуальні питання педіатрії», присвячена пам’яті видатного вітчизняного вченого, члена-кореспондента НАН, НАМН України, професора Віктора Михайловича Сідельникова. Наукова програма цього щорічного заходу включала обговорення широкого кола питань сучасної клінічної педіатрії, а участь у ньому взяли відомі вітчизняні клініцисти й експерти з питань організації охорони здоров’я дітей. Традиційно значний інтерес аудиторії викликали доповіді, у яких знані українські вчені розглядали практичні підходи до діагностики, лікування та профілактики найбільш поширених дитячих захворювань, адже саме ці завдання щоденно доводиться вирішувати кожному педіатру та сімейному лікарю. Однією з таких «вічних» проблем педіатрії та дитячої оториноларингології є гострий тонзилофарингіт – дуже поширене у дитячій популяції інфекційно-запальне захворювання. Здавалося б, зараз про цю патологію вже відомо майже все, проте в реальній клінічній практиці під час вибору засобів його емпіричного лікування у лікарів дійсно виникає багато запитань і сумнівів. З сучасними науковими даними про етіологічну структуру збудників гострого тонзилофарингіту, а також з клінічними рекомендаціями щодо його терапії та профілактики ускладнень учасників конференції докладно ознайомив авторитетний вітчизняний вчений-педіатр, академік НАМН України, завідувач кафедри педіатрії № 4 Національного медичного університету ім. О.О. Богомольця, доктор медичних наук, професор Віталій Григорович Майданник. Пропонуємо увазі читачів огляд цієї цікавої доповіді.
– Етіологічні фактори, що викликають розвиток гострого тонзилофарингіту у дітей, досить неоднорідні – до них належать віруси, бактерії та ціла низка неінфекційних чинників (R. Gereige, B. Cunill-De Sautu, 2011). Вважається, що у 30-50% випадків тонзилофарингіт спричинюють різноманітні віруси: зокрема рино-, аденовіруси, респіраторно-синцитіальний вірус, вірус Епштейна–Барр, віруси грипу та парагрипу, корона-, ентеровіруси, вірус простого герпесу. Бактеріальними збудниками тонзилофарингіту можуть стати стрептококи різних груп (А, С, G), хламідії, мікоплазми, коринебактерії, анаеробні бактерії та ін. Проте найбільш поширеними серед них, «класичними» збудниками бактеріального тонзилофарингіту та основними етіологічними чинниками розвитку його серйозних ускладнень є, як відомо, стрептококи групи А. Встановлено, що у дітей віком до 5 років стрептококи групи А (Streptococcus pyogenes) обумовлюють близько 24% випадків (95% довірчий інтервал (ДІ) 21-26%) гострого тонзилофарингіту, а у дітей старших 5 років – вже близько 37% випадків (95% ДІ 32-42%) цього захворювання (N. Shalkh et al., 2010; M.E. Wessels, 2011). Саме тонзилофарингітам стрептококової етіології традиційно надається велике значення у педіатричній практиці, адже їх своєчасна діагностика й адекватна антибактеріальна терапія є запорукою попередження як місцевих гнійно-запальних ускладнень, так і тяжких ускладнень з боку інших органів і систем, таких як гостра ревматична лихоманка (ГРЛ) та гострий постстрептококовий гломерулонефрит (ГПГН). Дослідженнями останніх років було встановлено, що стрептококи групи А мають багато різних факторів патогенності, які беруть активну участь в етіопатогенезі захворювання. Зокрема серед властивих стрептококам групи А факторів патогенності сьогодні найбільше значення надається так званому білку М – типоспецифічному основному поверхневому антигену, який визначає їх вірулентність. Молекули білка М містяться в клітинній стінці стрептококів і утворюють на ній ниткоподібні вирости. Зараз відомо більше 80 варіантів цього білка, кожен із яких властивий певному серотипу бактерії. Саме білок М забезпечує стійкість стрептококів групи А до фагоцитозу та зв’язує фібриноген, перешкоджаючи активації системи комплементу та реалізації процесу опсонізації.
З позиції визначення підходу до терапії гострого тонзилофарингіту вирішальне значення має проведення диференційної діагностики між стрептококовою та вірусною етіологією захворювання. Існує ціла низка епідеміологічних ознак, які характерні саме для інфекції, викликаної стрептококами групи А (GAS-інфекції), та дозволяють її вчасно припустити. До них насамперед належать (D.M. Langlois, M. Andreae, 2011; R. Gereige, B. Cunill-De Sautu, 2011):
• вік дитини – частіше хворіють діти віком 5-10 років;
• інгаляційний характер зараження або анамнестичні відомості про прямий контакт із хворим на гострий тонзилофарингіт;
• сезон розвитку захворювання – частіше виникає взимку або ранньою весною;
• раптова поява симптомів;
• симптоми найбільш виражені протягом перших 3-5 днів захворювання.
На ймовірну вірусну етіологію гострого тонзилофарингіту вказують такі епідеміологічні ознаки, як розвиток захворювання у немовлят і дітей раннього дошкільного віку, анамнестичні відомості про прямий контакт із хворим на гостру респіраторну вірусну інфекцію, можливість розвитку захворювання у будь-яку пору року, поступова поява симптомів та їх виражений характер протягом більше ніж 4-5 днів.
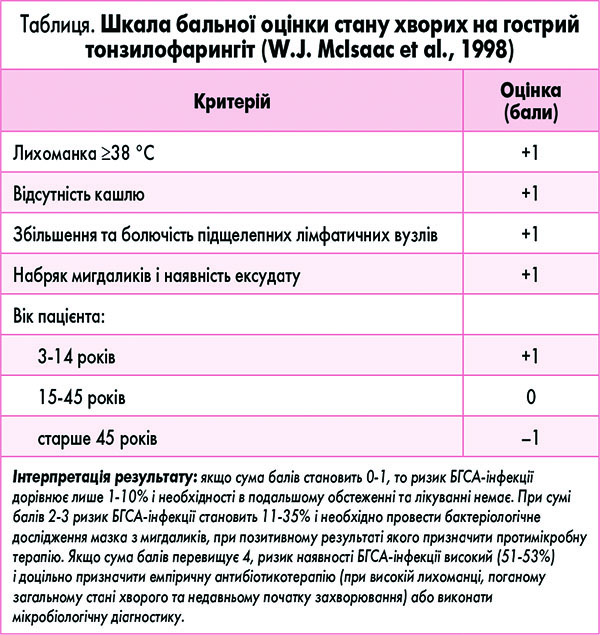
У сучасній клінічній практиці широко застосовується проста бальна шкала, що була розроблена W.J. McIsaac та співавт. (1998) із метою полегшення підтвердження клінічного діагнозу гострого тонзилофарингіту, спричиненого β-гемолітичним стрептококом групи А (БГСА), та прийняття відповідних клінічних рішень (табл.).
Крім того, зараз все більшої значущості набуває оцінювання симптомів ймовірного стрептококового тонзилофарингіту з позиції діагностичної чутливості та специфічності (B.A. Choby, 2009). Наприклад, найвища чутливість характерна для таких ознак, як відсутність у пацієнта кашлю (51-79%) та збільшення передніх шийних лімфатичних вузлів (55-82%), а найвища специфічність – для петехій на піднебінні (95%) та виявлення фарингеального та тонзилярного ексудату (85-88%).
Важливим аспектом вибору тактики антибактеріальної терапії гострого тонзилофарингіту, викликаного стрептококами групи А, є аналіз сучасних даних щодо їх антибіотикорезистентності. Дані міжнародних досліджень останніх років демонструють подальше підвищення частоти виявлення стійкості стрептококів групи А до таких «класичних» антибіотиків, як еритроміцин, кліндаміцин, тетрациклін, ко-тримоксазол та ін. Водночас резистентність стрептококів групи А до цефалоспорину III покоління цефтріаксону навпаки демонструє тенденцію до зниження: 1,3% штамів у 2013 р. порівняно з 1,7% у 2012 р. та 3,2% у 2011 р.
Різні підходи до антибіотикотерапії при тонзилофарингітах, викликаних стрептококами групи А, в останні роки були оцінені зарубіжними вченими з позицій доказової медицини шляхом виконання метааналізів відповідних клінічних досліджень. Їх результати засвідчили, що пеніциліни та цефалоспорини при цьому захворюванні характеризуються найвищою та порівнянною ефективністю. Однак цефалоспорини виявилися значно ефективнішими за пеніциліни у дітей віком до 12 років, а також у пацієнтів із хронічним рецидивуючим тонзилітом. Крім того, застосування цефалоспоринів дозволило забезпечити ерадикацію більшої кількості штамів стрептококів (К. Steller, 2014; M.L. van Driel et al., 2016).
Дані декількох більш ранніх досліджень продемонстрували, що призначення короткого курсу (5 днів) терапії цефалоспоринами для перорального застосування (зокрема цефподоксиму проксетилом) забезпечувало високу ефективність ерадикації БГСА у дітей (90-98%), що навіть перевищувала таку при 10-денному лікуванні пеніциліном (M.E. Pichichero et al., 1994; A.S. Dajani et al., 1995). У дослідженні Y. Aujard та співавт. (1995) також була підтверджена висока ефективність ерадикації БГСА у дітей після 4-денної терапії цефуроксиму аксетилом, аналогічна бактеріологічній ефективності 10-денного лікування пеніциліном (88% порівняно з 87%). Пізніше дані щодо можливості застосування коротких курсів терапії цефуроксиму аксетилом при стрептококовому тонзилофарингіті були підтверджені у метааналізі (W.M. Gooch et al., 2000), який показав, що прийом цього препарату протягом 4-5 днів забезпечував ерадикацію патогенних бактерій у 90% пацієнтів, у той час як 10-денна терапія пеніциліном V – у 85% пацієнтів. Тому нині цефподоксиму проксетил і цефуроксиму аксетил поряд з антибіотиками пеніцилінового ряду визнані препаратами вибору у лікуванні дітей зі стрептококовим тонзилофарингітом (D.M. Langlois, M. Andreae, 2011).
В Україні ці цефалоспоринові антибіотики для перорального прийому представлені добре відомими вітчизняним педіатрам препаратами Цефодокс і Цефутил®. Як свідчать дані клінічних досліджень і досвід, призначення дітям з гострим стрептококовим тонзилофарингітом препарату Цефодокс у дозі 10 мг/кг маси тіла, розділеній на 2 прийоми, або 5 мг/кг 2 рази на добу (максимальна добова доза – 200 мг) протягом 5 днів забезпечує високу клінічну ефективність та успішну ерадикацію збудників. Цефуроксиму аксетил на території України представлений препаратом Цефутил®, який також можна призначати дітям старше 2 років згідно з інструкцією.
В узагальнених рекомендаціях з лікування GAS-тонзилофарингіту з позицій доказової медицини (M.G. Kalra et al., 2016) вказано, що лікарі мають діагностувати це захворювання, застосовуючи підхід, який поєднує верифіковані клінічні ознаки із селективним використанням швидкого тестування на наявність стрептококових антигенів. Що ж стосується призначення хворим на GAS-тонзилофарингіт антибактеріальної терапії, то антибіотиками першої лінії є пеніциліни і цефалоспорини. Слід зазначити, що обидві ці рекомендації характеризуються найвищим рівнем доказовості – А. Симптоматичне лікування GAS-тонзилофарингіту може включати пастилки, нестероїдні протизапальні препарати та топічні анестетики, застосування яких дозволяє покращити суб’єктивне самопочуття хворого (рівень доказовості В).
На жаль, у 10-15% хворих на GAS-тонзилофарингіт існує ризик виникнення такого серйозного ускладнення, як ГПГН. Показник захворюваності на ГПГН у дітей в країнах, що розвиваються, становить 2 на 100 000, а в розвинених країнах – 0,2 на 100 000 дитячого населення. За даними Всесвітньої організації охорони здоров’я, щорічно в світі реєструють близько 470 000 хворих на ГПГН і 5000 летальних випадків від ГПГН (J.R. Carapetis et al., 2005).
На сьогодні встановлено, що існує велика кількість нефритогенних штамів стрептокока, які мають на своїй поверхні М-протеїни: 1-4, 12, 25, 49. З нефритогенних штамів стрептокока були виділені два специфічні антигени – катіонна протеаза цистеїну (стрептококовий пірогенний екзотоксин B – speB) та гліцеральдегід‑3-фосфатдегідрогеназа (GAPDH, або HAPLr), які мають схожість з антигенною структурою гломерул і здатні викликати синтез антитіл, що виявляють у біоптатах паренхіми нирок у хворих на ГПГН (S.R. Bafsford et al., 2005). Саме вони, згідно з сучасними уявленнями, відповідальні за розвиток імунокомплексного ураження нирок і подальше формування хронічного гломерулонефриту. Слід зазначити, що патогенез такого відомого ускладнення стрептококового тонзилофарингіту, як ГРЛ, також пов’язаний з утворенням антитіл проти стрептококів і формуванням циркулюючих імунних комплексів, які, відкладаючись на базальних мембранах капілярів, артерій і синовіальної оболонки, викликають їх пошкодження (W.G. Couser, 2016). Але незважаючи на ці глибокі знання механізмів етіопатогенезу ГПГН та ревматизму, поки що не існує лікарських засобів, які могли б ефективно їх усувати. Саме тому питання адекватного лікування гострого стрептококового тонзилофарингіту та первинної профілактики розвитку його ускладнень (зокрема ГПГН і ревматизму) як і раніше мають пріоритетне значення у сучасній педіатричній практиці.
Підготували Олена Терещенко та Марина Тітомір
Тематичний номер «Педіатрія» №3 (42), вересень 2017 р.