19 жовтня, 2017
Апластична анемія в підлітків і дорослих молодого віку
Апластична анемія (АА) – діагноз, що може бути встановлений у будь-якій віковій групі. Підлітки і дорослі молодого віку (до 30 років) з тяжкою АА можуть мати унікальні прояви недостатності кісткового мозку порівняно з пацієнтами старшого віку. Молодій популяції властиве інше співвідношення вроджених і набутих станів, тому диференційний діагноз є ширшим і потребує глибшого обстеження. Встановлення точного діагнозу є надважливим, оскільки етіологія захворювання і вік пацієнта можуть впливати на вибір лікування.
Патофізіологія
Апластична анемія може бути вродженою або набутою. Вроджені форми розвиваються в результаті дефектів репарації ДНК (анемія Фанконі – АФ), аномальної фізіології теломер (вроджений дискератоз – ВДК) або аномалій біогенезу рибосом (синдром Швахмана-Даймонда). Причиною набутих форм АА вважають аутоімунну атаку, спрямовану на гемопоетичні клітини-попередники. Цією атакою керують цитотоксичні Т-лімфоцити, які викликають апоптоз гемопоетичних стовбурових клітин з подальшим розвитком недостатності кровотворення. Утім дотепер не з’ясовано, на які саме антигени націлені Т-лімфоцити.
Клінічна картина і діагностика
Апластична анемія визначається як клінічний синдром, що характеризується панцитопенією з гіпоклітинним кістковим мозком за відсутності його патологічної інфільтрації або збільшення кількості ретикуліну. Прояви захворювання безпосередньо пов’язані з тяжкістю й етіологією цитопенії – дефіциту всіх трьох типів клітин крові: еритроцитів (анемія), лейкоцитів (лейкопенія) і тромбоцитів (тромбоцитопенія). У цій фізично активній групі діагноз часто встановлюється із запізненням, оскільки загальна слабкість, інфекції й утворення синців можуть пов’язуватись з іншими причинами. Високий кардіальний резерв у молодих пацієнтів також може відтерміновувати системні прояви анемії. Крім того, у таких пацієнтів захворювання може діагностуватись несвоєчасно через менш часті контакти із системою охорони здоров’я, що обумовлено загальним добрим здоров’ям і соціальними аспектами, зокрема відсутністю страховки та підвищеною географічною мобільністю.
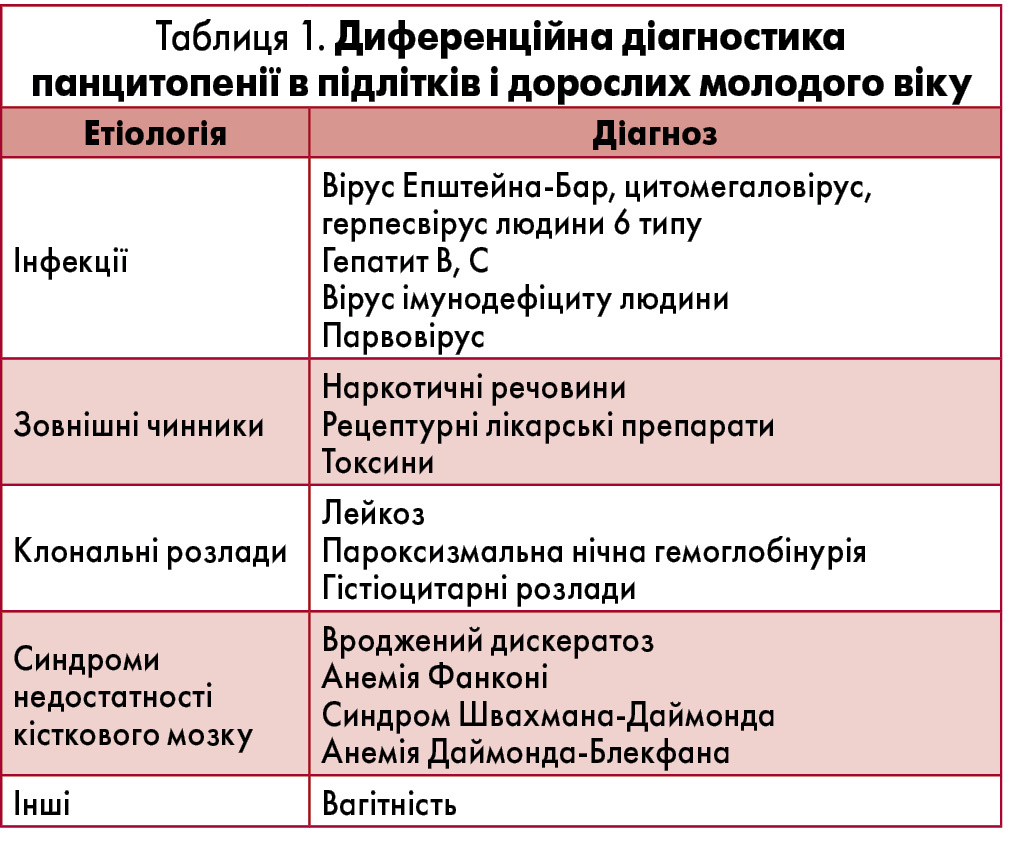
Апластичну анемію слід підозрювати в усіх пацієнтів з панцитопенією цієї вікової групи. Особливу увагу необхідно звертати на дані анамнезу, що вказують на синдром вродженої недостатності кісткового мозку (СВНКМ). Деякі пацієнти можуть мати явні прояви захворювання (наприклад, короткий зріст, гіперпігментація, трифалангові великі пальці рук), пропущені під час попередніх оглядів, при цьому симптоми певних захворювань (приміром, раннє посивіння волосся і ретикулярна пігментація при ВДК, передчасна менопауза при АФ) можуть посилюватися з віком. Диференційна діагностика панцитопенії в молодих пацієнтів представлена в таблиці 1. Також у цій віковій групі частіше зустрічаються інші, зазвичай рідкісні причини недостатності кісткового мозку, наприклад anorexia nervosa.
Фізикальний огляд, який є надважливим для встановлення діагнозу, у підлітків може ускладнюватись у разі присутності батьків. Про деякі деталі, зокрема наявність розладів харчування, вживання наркотичних речовин або незаплановану вагітність, краще дізнаватись, спілкуючись з пацієнтом віч-на-віч. Сімейний анамнез може суттєво допомогти в діагностиці СВНКМ (скажімо, короткий зріст, патологічна пігментація шкіри, легенева недостатність). Необхідно визначати походження всіх хірургічних шрамів, у т. ч. таких, що можуть залишатись після ортопедичних втручань, операцій на серці, нирках або шлунково-кишковому тракті. Особливу увагу слід звернути на моменти, наведені в таблиці 2.
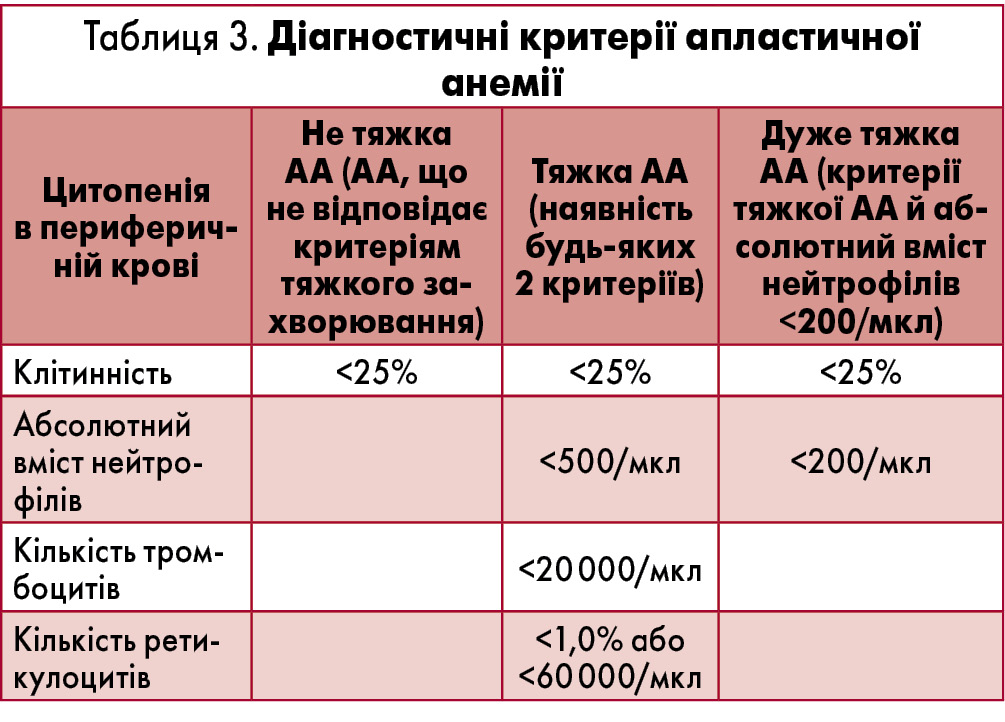
Аспіраційна біопсія кісткового мозку є обов’язковою. На відміну від пацієнтів старшої вікової групи в підлітків (так само як і в дітей) цю процедуру рекомендовано проводити під седацією. За наявності гіпоклітинності кісткового мозку визначають тяжкість АА (табл. 3). Природний перебіг тяжкої АА передбачає прогресування цитопенії з мінімальною вірогідністю спонтанної ремісії. Клінічний прогноз залежить від тяжкості на момент встановлення діагнозу, отже, найгірший він у разі дуже тяжкої АА. Помірна АА може зникати спонтанно і не потребувати лікування.
Цитогенетичні дослідження, зокрема флюоресцентна гібридизація in situ, показані всім пацієнтам з тяжкою АА незалежно від віку. Гіпоклітинну мієлодисплазію, яку часто важко відрізнити від тяжкої АА, допомагають діагностувати хромосомні дослідження. Клінічна (тобто така, що супроводжується гемолізом) пароксизмальна нічна гемоглобінурія (ПНГ) у молодих пацієнтів зустрічається рідко, але такі випадки можливі. Крім того, наявність клону ПНГ може свідчити про набуту АА і більшу чутливість до імуносупресивної терапії (ІСТ). Визначення ламкості хромосом є практично завжди необхідним для виключення АФ, тому що пацієнти з цією анемією можуть не мати будь-яких явних фізикальних ознак захворювання. Такі хворі майже не чутливі до ІСТ, можуть відповідати на андрогени і потребують менш інтенсивних кондиціонуючих режимів перед трансплантацією гемопоетичних стовбурових клітин (ТГСК). У пацієнтів із сімейним анамнезом (легеневий фіброз, раннє посивіння, хвороба печінки) або фізикальними ознаками (дистрофія нігтів, лейкоплакія слизових оболонок), що вказують на ВДК, доцільним є визначення довжини теломер і генних мутацій, оскільки такі хворі також відповідають на андрогени та є дуже чутливими до мієлоаблятивних кондиціонуючих режимів.
Лікування
Підлітки і дорослі віком до 30 років з тяжкою АА, що мають HLA-ідентичного брата або сестру, повинні отримувати ТГСК, адже ця процедура може повністю вилікувати хворобу. Останніми роками покращились результати ТГСК із застосуванням донорів – не родичів. Предикторами виживаності після ТГСК є HLA-ідентичний донор, вік реципієнта <16 років, рання ТГСК (час від встановлення діагнозу до трансплантації <83 днів) і кондиціонуючий режим без опромінення. Перевагами ТГСК порівняно з ІСТ є значне зниження вірогідності рецидиву та відсутність ризику віддалених клональних розладів, зокрема мієлодиспластичного синдрому й ПНГ. П’ятирічна виживаність є кращою при трансплантації гемопоетичних стовбурових клітин кісткового мозку порівняно з клітинами периферичної крові (85 vs 73% відповідно).
Ще однією високоефективною терапією в разі тяжкої АА є ІСТ антитимоцитарним глобуліном і циклоспорином (АТГ/ЦС). Частота гемопоетичної відповіді на цей режим становить 60-70%, 5-річна виживаність – 60-85%. Проте в 40% пацієнтів відбувається рецидив, що з огляду на очікувану тривалість життя є значною проблемою в цій віковій групі. Десятирічна виживаність після першої лінії терапії ТГСК та ІСТ становить 73 і 68% відповідно (р=0,002). Частота злоякісних новоутворень є майже в 10 разів вищою в разі ІСТ (1,2 vs 0,1%). Додавання до АЦТ/ЦС інших імуносупресивних препаратів, зокрема мофетилу мікофенолату, такролімусу чи алемтузумабу, не покращує клінічних результатів. Є повідомлення про успішне застосування високодозової терапії циклофосфамідом, проте цей режим є доволі токсичним.
Важливою складовою ведення пацієнтів з АА є підтримувальна терапія. З огляду на частоту флеботомії, гемотрансфузій та призначення лікарських препаратів усім хворим на АА рекомендовано встановлення центрального венозного катетера, тип якого необхідно обговорити з пацієнтом. Основною причиною смерті пацієнтів з АА є бактеріальні та грибкові інфекції, тож їх необхідно своєчасно діагностувати й лікувати. Дослідження свідчать про підвищений ризик інфекції грибами Aspergillus у пацієнтів, які курять. Стандартизованих протоколів антибіотикотерапії при АА немає. Рекомендовано проактивне призначення антибіотиків, противірусних і протигрибкових засобів, при цьому за можливості слід утримуватись від застосування препаратів, що пригнічують кістковий мозок.
Повторювальні гемотрансфузії можуть призвести до перевантаження залізом із потенційно незворотним ураженням печінки, серця та ендокринних органів. Для попередження цього ускладнення використовують більш низькі цільові рівні гемоглобіну та призначають комплексоутворювальні препарати, найчастіше дефероксамін при сироваткових рівнях феритину >1000-2000 мкг/л.
Для корекції цитопенії та профілактики ускладнень у пацієнтів з АА можуть використовуватись гемопоетичні фактори росту. Рекомбінантний тромбопоетин (рТПО) специфічно стимулює проліферацію і диференціацію мегакаріоцитів, сприяє утворенню і вивільненню тромбоцитів, а також відновленню загального вмісту лейкоцитів. Терапія із застосуванням рТПО зазвичай рекомендована пацієнтам з рівнем тромбоцитів <50×109/л або у випадках, коли необхідно збільшити кількість тромбоцитів (приміром, перед хірургічним втручанням).
Менструальна кровотеча може значно поглиблювати прояви АА, особливо тромбоцитопенію. Тому для попередження крововтрати та збереження фертильності необхідною є менструальна супресія з індукцією аменореї. Жінкам, які отримують ТГСК, найчастіше призначаються аналоги гонадотропін-рилізинг-гормону, наприклад лейпролід. Альтернативою можуть бути оральні контрацептиви; з підлітками їх застосування рекомендовано обговорювати за відсутності батьків.
У виняткових випадках АА може розвиватися під час вагітності. У 25-30% випадків відбувається спонтанна ремісія, зазвичай після пологів або переривання вагітності. У разі небажання або неможливості переривання вагітності можливе спостереження з підтримувальною терапією; циклоспорин може безпечно призначатись антенатально. Ускладнення частіше реєструються у вагітних з низькою кількістю тромбоцитів і ПНГ.
Підлітки та дорослі молодого віку з АА – унікальна популяція пацієнтів, що потребує особливої уваги під час діагностики та лікування. Терапією вибору в цій категорії хворих залишається ТГСК від HLA-ідентичного брата або сестри, а за відсутності такої можливості – імуносупресивна терапія. Незалежно від обраного методу лікування пацієнти потребують адекватної підтримувальної терапії та тривалого спостереження для своєчасного виявлення і корекції пізніх ускладнень.
За матеріалами статті: DeZern A.E., Guinan E. C. Aplastic anemia in adolescents and young adults. Acta Haematol. 2014; 132 (3-4): 331-9.
Підготував Олександр Гладкий
Медична газета «Здоров’я України 21 сторіччя» № 18 (415), вересень 2017 р.