20 жовтня, 2017
Рациональная терапия поствирусного риносинусита у детей с рекуррентными заболеваниями респираторного тракта и гиперплазией аденоидов
Наличие рекуррентных заболеваний носоглотки у детей на фоне гиперплазии лимфоидной ткани глотки (ГЛТГ) является актуальной проблемой современной педиатрии и детской оториноларингологии.
Учитывая то, что большинство острых респираторных заболеваний (ОРЗ) имеют вирусную этиологию и являются индуктивным фактором формирования ГЛТГ, сложно осуществлять эффективные этиопатогенетические терапевтические мероприятия. Установлено, что почти 73% детей с ГЛТГ, болеющих рекуррентными респираторными инфекциями, нуждаются в амбулаторно-реабилитационных мероприятиях, а 27% – в специализированной медицинской помощи [1].
Склонность к отечности слизистых оболочек при воспалении вследствие повышенной гидрофильности тканей – особенность детского организма. В такой клинической ситуации всегда возникает опасность развития осложнений, связанных с нарушением дренирования околоносовых пазух и полости среднего уха, что нередко приводит к формированию тяжелого рекуррентного или хронического течения синуситов и отитов. Учитывая особенности течения и лечения воспалительных заболеваний носоглотки у детей, в International Consensus Statement on Allergy and Rhinology (2016) выделяется отдельная нозологическая единица – педиатрический риносинусит, который имеет клинические проявления, распространяющиеся далеко за пределы синоназального региона, с дополнительными симптомами в виде ГЛТГ, астении, нарушений сна, физической боли, психоневрологических нарушений [2], и требует особых комплексных терапевтических подходов.
Многообразие клинических проявлений заболеваний носоглотки побуждает практических врачей к применению противомикробных, противоотечных, противовоспалительных, мукоактивных и иммунотропных средств, что сопряжено с высоким риском полипрагмазии. Серьезной проблемой является то, что активная медикаментозная терапия в детском возрасте может быть более опасной, чем само заболевание [3].
В связи с этим важно использовать максимально безопасные лекарственные средства. При лечении вирусно-бактериальных риносинуситов к таким методам относится применение медикаментозных препаратов, созданных на основе растительных компонентов. Крайне важно, чтобы используемые средства наряду с достаточной эффективностью обладали максимальной безопасностью, поскольку применяются у детей. Таким требованиям отвечает комплексный растительный препарат Синупрет® экстракт (Bionorica SE). Одна таблетка содержит 160 мг специального сухого экстракта (3-6:1) BNO 1016 из корня горечавки (Radix Gentianae), цветков первоцвета с чашечкой (Flores Primulae cum Calycibus), травы щавеля (Herba Rumicis), цветков бузины (Flores Sambuci), травы вербены (Herba Verbenae) (1:3:3:3:3). Благодаря комплексному составу и стандартизации по содержанию ключевых биологически активных веществ лекарственных растений Синупрет® экстракт обладает комплексом лечебных свойств, необходимых для эффективного лечения заболеваний верхних дыхательных путей (ВДП). Выраженное секретолитическое и мукокинетическое действие способствует устранению мукостаза, противовоспалительная активность – уменьшению отечности слизистой оболочки и лимфоидных образований ВДП. Противовирусное действие в отношении широкого спектра патогенов снижает вероятность повторных повреждений слизистой и лимфоидной ткани возбудителями острой респираторной вирусной инфекции. Кроме того, Синупрет® экстракт имеет солидную доказательную базу применения при вирусном риносинусите. Его высокая эффективность была доказана в ходе двух хорошо спланированных рандомизированных плацебо-контролируемых исследований, проведенных в Германии.
Цель работы – повышение эффективности терапии поствирусного риносинусита у детей с рекуррентными заболеваниями респираторного тракта и гиперплазией аденоидов путем использования препарата Синупрет® экстракт.
Разработка эффективных подходов очищения слизистых оболочек носоглотки от патогенных микроорганизмов при поствирусных риносинуситах способна снизить вероятность формирования патологических биопленок, уменьшить воспаление миндалин и, следовательно, снизить количество сигналов к пролиферации, поступающих на лимфоидную ткань, что приводит к уменьшению ее размеров и ограничению хронических очагов инфекции.
Материалы и методы
Под наблюдением находились 60 детей в возрасте от 12 до 15 лет c диагнозом острого поствирусного риносинусита и гиперплазии аденоидов. В зависимости от схемы лечения пациенты были случайным образом распределены на 2 группы (по 30 детей в каждой). Участники 1-й группы принимали Синупрет® экстракт в течение 14 дней для терапии поствирусного риносинусита, в то время как представители 2-й группы не использовали данное лекарственное средство.
Режим дозирования препарата Синупрет® экстракт: по 1 таблетке 3 р/сут после еды, не разжевывая, запивая достаточным количеством жидкости.
Дети в группах наблюдения были сопоставимы по возрасту, полу, длительности и тяжести болезни, сопутствующей патологии. Клинический осмотр включал оценку анамнеза, фенотипических характеристик ребенка, использование общеклинических методов обследования. Количественное определение секреторного иммуноглобулина A (sIgA) в слюне проводилось методом иммуноферментного анализа тест-систем.
Статистическая обработка полученных результатов для сопоставления двух выборок по частоте встречаемости эффекта производилась с применением углового критерия Фишера (φ). С целью прогнозирования динамики состояния ребенка использовалась оценка относительного риска (ОР) формирования изучавшихся нарушений. ОР показывал силу связи между наличием заболеваний и расстройствами со стороны органов и систем. Значение ОР трактовали следующим образом: 1 – различий между двумя группами не существует; <1 – в экспериментальной группе событие развивается реже, чем в группе сравнения; >1 – в экспериментальной группе событие возникает чаще, чем в группе сравнения.
Наблюдение было выполнено в соответствии с этическими принципами медицинского исследования, проводимого с участием людей, закрепленными Хельсинской декларацией и Надлежащей клинической практикой.
Результаты исследования
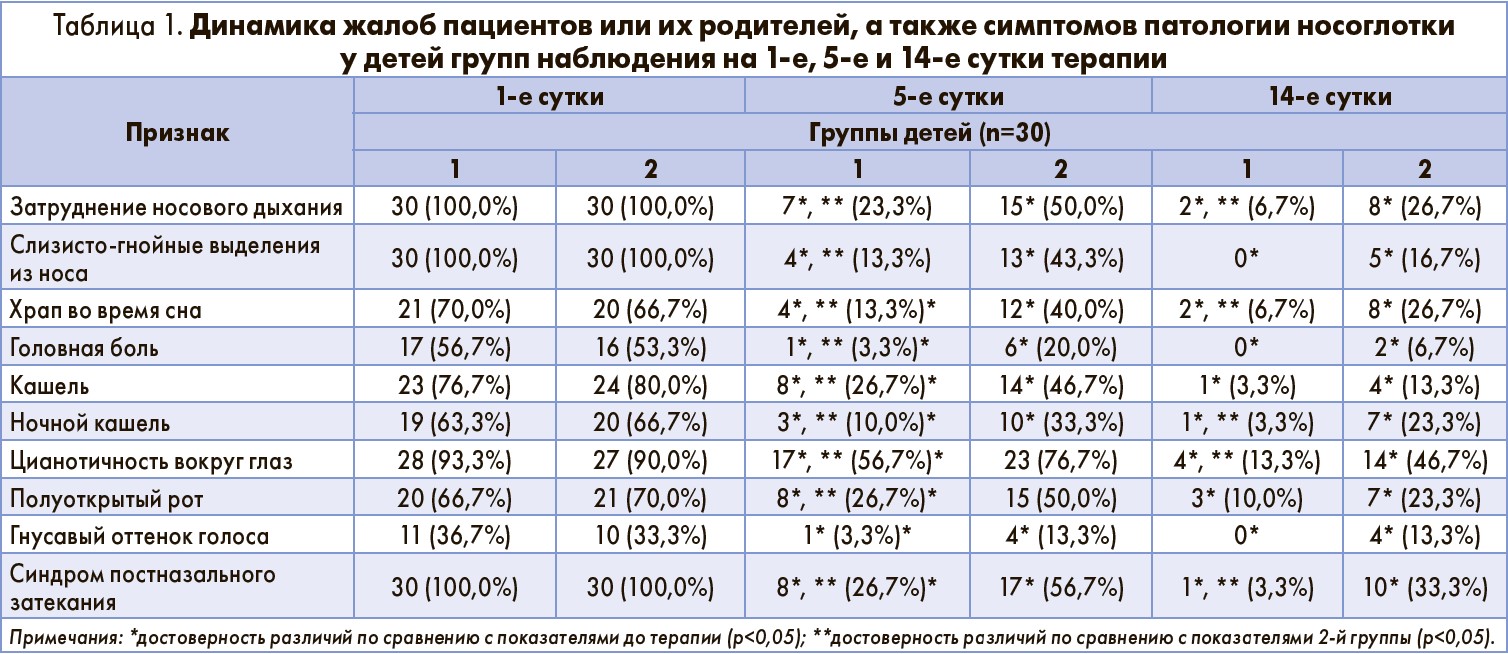
Динамика жалоб родителей пациентов, а также симптомов, характеризующих особенности течения патологии носоглотки у детей групп наблюдения на 1-е, 5-е и 14-е сутки терапии, представлена в таблице 1.
Как свидетельствуют данные этой таблицы, использование лекарственного средства Синупрет® экстракт у детей 1-й группы уже на 5-е сутки терапии позволило статистически значимо уменьшить (по сравнению с данными до лечения) количество эпизодов затруднения носового дыхания (на 76,7%; р<0,05), слизисто-гнойных выделений из носовых ходов (на 86,7%; р<0,05), храпа во время сна (на 56,7%; р<0,05), головной боли (на 53,4%; р<0,05), кашля (на 50,0%; р<0,05), ночного кашля (на 53,3%; р<0,05), периорбитального цианоза (на 36,6%; р<0,05), полуоткрытого рта (на 40,0%; р<0,05), гнусавого оттенка голоса (на 33,4%; р<0,05), синдрома постназального затекания (на 73,3%; р<0,05).
При сравнении полученных данных с результатами детей 2-й группы на 5-е сутки терапии было продемонстрировано, что при применении препарата Синупрет® экстракт достоверно быстрее купируются затруднение носового дыхания (на 26,7%; р<0,05), слизисто-гнойные выделения из носовых ходов (на 30,0%; р<0,05), храп во время сна (на 26,7%; р<0,05), головная боль (на 16,7%; р<0,05), кашель (на 20,0%; р<0,05), ночной кашель (на 23,3%; р<0,05), периорбитальный цианоз (на 20,0%; р<0,05), полуоткрытый рот (на 23,3%; р<0,05), синдром постназального затекания (на 30,0%; р<0,05).
После 14 дней терапии у детей обеих групп сохранялась наиболее трудно купируемая симптоматика. В таких случаях применение только лекарственного средства Синупрет® экстракт позволяло добиться клинического улучшения. Так, при сравнении полученных данных с результатами детей 2-й группы на 14-е сутки терапии наиболее трудно купируемых симптомов было обнаружено, что использование препарата Синупрет® экстракт позволяет эффективно купировать затруднение носового дыхания (на 20,0%; р<0,05), храп во время сна (на 23,3%; р<0,05), ночной кашель (на 20,0%; р<0,05), периорбитальный цианоз (на 33,4%; р<0,05), синдром постназального затекания (на 30,0%; р<0,05); различия статистически значимы.
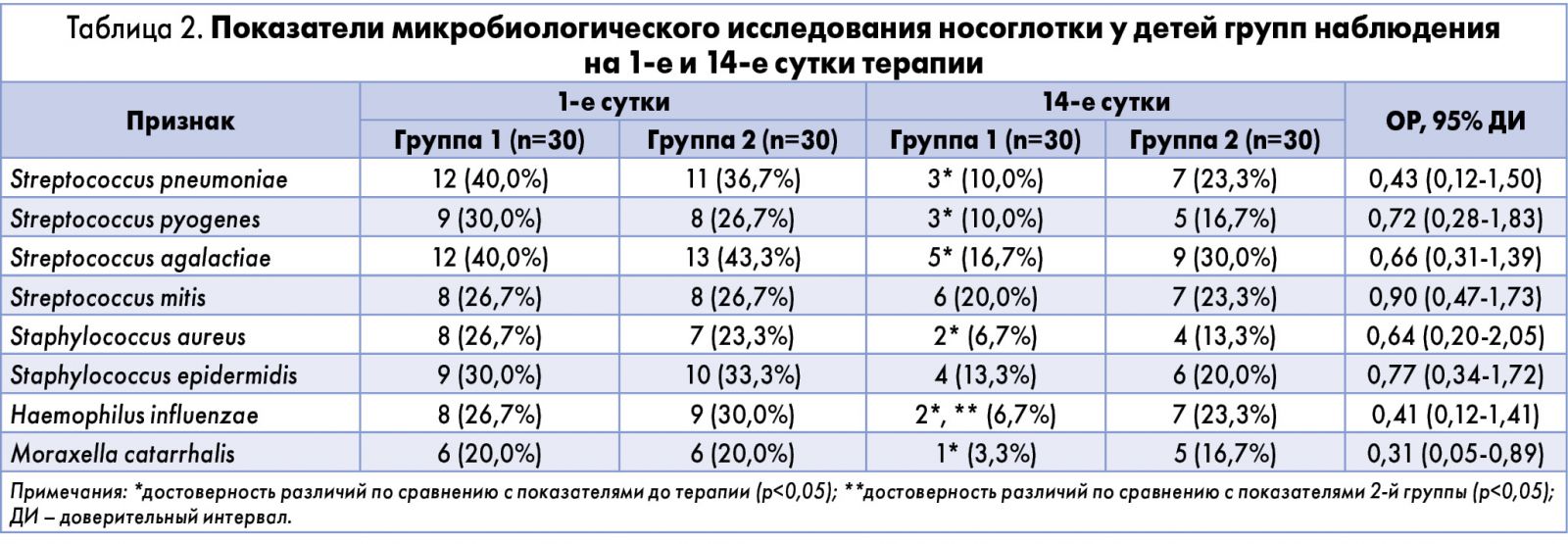
Динамика показателей микробиологического исследования носоглотки у детей групп наблюдения на 1-е и 14-е сутки терапии отражена в таблице 2.
Результаты микробиологического исследования носоглотки у детей групп наблюдения свидетельствуют о том, что применение лекарственного средства Синупрет® экстракт статистически значимо уменьшает количество детей, у которых слизистая оболочка носоглотки колонизирована патогенными и условно-патогенными микроорганизмами (S. pneumoniae, S. pyogenes, S. agalactiae, H. influenzae и M. catarrhalis). Терапия без применения препарата Синупрет® экстракт такого эффекта не имела, поскольку у детей 2-й группы на фоне лечения сохранялся высокий уровень патологической колонизации.
При оценке ОР колонизации данными микроорганизмами было установлено, что при включении лекарственного средства Синупрет® экстракт в схему терапии детей с риносинуситами на фоне ГЛТГ вероятность персистирования S. pneumoniae и H. influenzae в 2-3 раза, а M. catarrhalis – в ≥3 раза ниже.
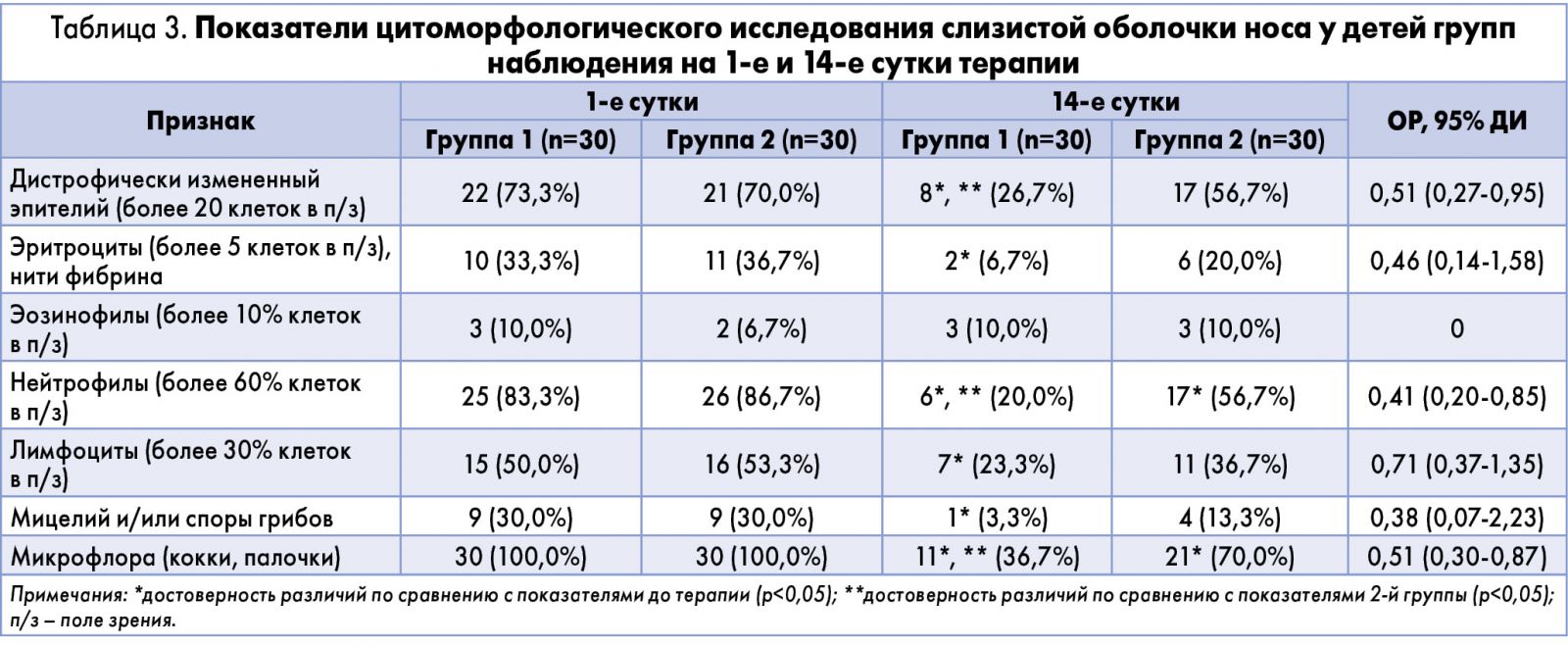
Для оценки состояния лимфоэпителиальных структур носоглотки и глоточного кольца у детей групп наблюдения использовались результаты цитоморфологического исследования слизистой оболочки носа; их динамика показана в таблице 3.
Анализ результатов цитоморфологического исследования слизистой оболочки носа показал, что в сравнении с исходными показателями применение препарата Синупрет® экстракт статистически значимо уменьшает количество детей с дистрофическими изменениями эпителия (на 46,6%; р<0,05), эритроцитами и нитями фибрина (на 26,7%; р<0,05), нейтрофилами (на 63,3%; р<0,05), лимфоцитами (на 23,3%; р<0,05), с мицелием и спорами грибов (на 26,7%; р<0,05), микрофлорой (на 66,3%; р<0,05) на назальной поверхности.
Сравнение с результатами обследования пациентов 1-й и 2-й группы показало, что использование лекарственного средства Синупрет® экстракт статистически значимо уменьшает количество детей с дистрофическими изменениями эпителия (на 30,0%; р<0,05), нейтрофилами (на 36,7%; р<0,05), лимфоцитами (на 26,7%; р<0,05), микрофлорой (на 23,3%; р<0,05) на поверхности слизистой оболочки полости носа.
При этом ОР цитоморфологических изменений слизистой оболочки носа в результате включения в схему терапии препарата Синупрет® экстракт снизился в 2-2,5 раза.
Динамика изменения концентрации sIgA в слюне детей групп наблюдения на 1-е и 14-е сутки терапии представлена в таблице 4.
Изменения концентрации sIgA в слюне пациентов групп наблюдения в процессе лечения свидетельствуют о том, что на 14-е сутки от начала использования лекарственного средства Синупрет® экстракт статистически значимо уменьшается количество детей с низким уровнем sIgA в слюне: на 53,3% (р<0,05) по сравнению с показателями до лечения и на 36,7% (р<0,05) при сопоставлении с контингентом 2-й группы. ОР развития локального дефицита sIgA при применении препарата Синупрет® экстракт на протяжении 14 суток снизился более чем в 2 раза.
На фоне терапии поствирусных риносинуситов во 2-й группе, не предполагавшей применения лекарственного средства Синупрет® экстракт, сохранялась исходно низкая концентрация sIgA в слюне на 14-е сутки наблюдения.
Интегральным показателем положительного эффекта добавления в схему терапии препарата Синупрет® экстракт у 1-й группы является уменьшение количества детей с бактериальными осложнениями поствирусного риносинусита (на 23,3%; р<0,05), требующими назначения антибиотиков (табл. 5).
У детей 1-й группы в 2,5 раза снизился ОР возникновения бактериальных осложнений и необходимости использования антибиотиков.
Таким образом, добавление в схему терапии поствирусного риносинусита препарата Синупрет® экстракт позволило улучшить клиническое состояние больных, восстановить микробиологический пейзаж и цитоморфологические характеристики слизистой оболочки носа, а также нормализовать уровень защитного sIgA в слюне.
Обсуждение результатов
Рекуррентные заболевания носоглотки у детей являются актуальной проблемой современной педиатрии, которая имеет несколько составляющих: медицинскую (существенный дефект состояния здоровья и качества жизни пациентов), социальную (в виде фармакоэкономической нагрузки на семью больного ребенка и государство в целом, увеличения количества дней нетрудоспособности родителей), а также этическую (активная медикаментозная терапия в детском возрасте иногда оказывается более опасной, чем само заболевание) [4].
Проблема значительно усложняется, когда в условиях частого повторного локального воспалительного процесса в носоглотке увеличивается инфекционная нагрузка на слизистые оболочки, что способствует компенсаторной гиперплазии лимфоидной ткани глоточного кольца, в частности аденоидов, с формированием механических препятствий для нормального оттока секрета из среднего уха и придаточных пазух носа, а также возникновением рекуррентных и хронических отитов, риносинуситов [5].
В период выздоровления после острого воспаления ВДП для полноценной регенерации слизистой оболочки происходят процессы ее инфильтрации разнообразными клеточными элементами. Такая перестройка слизистой оболочки носоглотки продолжается длительное время, в течение которого нарушение аэродинамики носоглотки приводит к постоянному прогрессивному иммунологическому ремоделированию с сопутствующей гиперплазией лимфоидных структур [6]. Так, у 58% детей с рекуррентными ОРЗ было обнаружено увеличение аденоидов [7]. Данное состояние сопровождается вторичным поражением мерцательного эпителия, что не только объясняет устойчивость этих заболеваний к лечению антибиотиками, но также создает условия для поддержания воспалительной реакции [8].
В этих условиях оптимальным решением терапевтических задач является применение стандартизированных препаратов комплексного действия, произведенных с использованием высококачественного растительного сырья. Лекарственное средство Синупрет® экстракт демонстрирует мукотропную и противомикробную активность, а также способность локально усиливать морфофункциональную регенерацию эпителиальных и лимфоидных структур глоточного кольца без иммуностимулирующей направленности.
Применение препарата Синупрет® экстракт у пациентов 1-й группы сопровождалось уменьшением количества детей с затруднением носового дыхания, слизисто-гнойными выделениями из носовых ходов, храпом во время сна, головной болью, кашлем, периорбитальным цианозом, синдромом постназального затекания (т. е. наблюдалось исчезновение клинической симптоматики назальной обструкции за счет уменьшения размеров глоточной миндалины).
В данных условиях большое значение приобретало исследование микрофлоры, колонизирующей поверхность гиперплазированных структур лимфоглоточного кольца. Результаты нашего исследования совпадали с данными литературы, согласно которым на поверхности аденоидов идентифицируются S. aureus (20% от общего объема микробиоты), S. haemolyticus (18%), S. epidermidis (15%); в меньших количествах присутствовали E. coli, E. faecium, P. aeruginosa, E. faecalis, P. morganii, P. mirabilis, S. saprophyticus, N. subflava. В 34% случаев были зарегистрированы ассоциации микроорганизмов, а в 30% культуральных образцов роста флоры не было обнаружено. Установлено, что 27,5-97,0% детей с гиперплазией аденоидов колонизированы различными типами/серотипами H. influenzae [9], а 62,5% – нетипируемыми штаммами данного возбудителя [10]. При исследовании распространенности S. pneumoniae в лимфоидной ткани носоглотки у 57 детей в возрасте 2-5 лет с гиперплазией аденоидов установлено, что колонизация пневмококками имела место в 70,2% детей, то есть аденоиды можно рассматривать как резервуар этих бактерий [11]. При бактериологическом исследовании носоглотки в группе больных хроническим гиперпластическим тонзиллитом в 78% случаев был выделен S. pyogenes, в 67% – S. aureus, что способствует возникновению гиперпластических процессов в ткани небных миндалин [12]. Бактериальные биопленки были обнаружены в 35,6% детей с увеличением аденоидов, что, по мнению авторов, приводит к дальнейшей лимфоидной гиперплазии, вентиляционным нарушениям и нарушениям локальной иммунореактивности [13].
Полученный нами выраженный клинический эффект во многом был обусловлен противомикробной активностью препарата Синупрет® экстракт, что выражалось в уменьшении количества детей 1-й группы, слизистая оболочка носоглотки которых была колонизирована патогенными микроорганизмами (S. pneumoniae, S. pyogenes, H. influenzae, M. catarrhalis), что ассоциировалось с ослаблением антигенной нагрузки, приводящей к гиперплазии лимфоидных образований глотки.
Для оценки состояния структур лимфоэпителиального глоточного кольца у детей после применения лекарственного средства Синупрет® экстракт мы использовали результаты цитоморфологического исследования носоглотки. В итоге было достигнуто уменьшение количества детей с дистрофическими изменениями эпителия, эритроцитами и нитями фибрина, нейтрофилами, лимфоцитами, с мицелием и спорами грибов, микрофлорой на назальной поверхности. Это указывало на уменьшение антигенной нагрузки на поверхности слизистых оболочек ВДП, уменьшение локальных провоспалительных проявлений и восстановление лимфоэпителиального симбиоза. При этом ОР цитоморфологических изменений слизистой оболочки носа в результате проведенных лечебно-профилактических мероприятий снизился в 2-2,5 раза.
Учитывая связь ГЛТГ у детей и повышения частоты/тяжести заболеваний респираторного тракта, важным является изучение функционирования мукозального иммунитета. В качестве неинвазивного метода оценки выраженности иммунологической реакции на бактериальную колонизацию гиперплазированных миндалин рекомендуется определение sIgA в слюне [14]. После использования препарата Синупрет® экстракт было установлено повышение концентрации sIgA в слюне, что способствовало усилению противомикробной защиты непосредственно на поверхности слизистых оболочек носоглотки со снижением вероятности повторного возникновения данных нарушений.
Еще одним немаловажным проявлением эффективности лекарственного средства Синупрет® экстракт было уменьшение количества бактериальных осложнений поствирусных риносинуситов, требующих использования антибиотиков.
Таким образом, наличие у ребенка ГЛТГ создает условия для более частых ОРЗ с тяжелым течением за счет длительной колонизации патогенных и условно-патогенных микроорганизмов на фоне морфофункциональной перестройки структур мукозального иммунитета с его транзиторной недостаточностью. Использование препарата Синупрет® экстракт у детей позволило улучшить показатели клинического состояния больных, восстановить цитоморфологические показатели слизистой оболочки носа и функционирование секреторного иммунитета, уменьшить частоту бактериальных осложнений.
Безопасность и переносимость препарата
На протяжении 14-дневного приема комплекса Синупрет® экстракт, а также в рамках последующего наблюдения нежелательных явлений и побочных реакций зарегистрировано не было. Аллергические реакции на фоне приема препарата не наблюдались.
Выводы
- Препарат Синупрет® экстракт является эффективным средством терапии рекуррентной инфекционной патологии носоглотки (поствирусного риносинусита) у детей старше 12 лет с гиперплазией аденоидов.
- Клиническая эффективность применения лекарственного средства Синупрет® экстракт проявилась в виде снижения общего количества, длительности и тяжести симптомов назальной обструкции, а также частоты развития бактериальных осложнений поствирусного риносинусита и необходимости применения системных антибактериальных средств.
- Использование препарата Синупрет® экстракт у детей старше 12 лет с гиперплазией аденоидов способствовало уменьшению колонизации слизистой оболочки носоглотки патогенными и условно-патогенными микроорганизмами (S. pneumoniae, S. pyogenes, H. influenzae и M. catarrhalis).
- Эпителио- и иммунотропное действие лекарственного средства Синупрет® экстракт снижает в 2-2,5 раза ОР формирования цитоморфологических изменений слизистой оболочки носа и локального дефицита sIgA.
- Хорошая переносимость и безопасность препарата Синупрет® экстракт на протяжении 14-дневного применения у пациентов старше 12 лет с рекуррентной инфекционной патологией носоглотки (поствирусный риносинусит) на фоне гиперплазии аденоидов позволяет рекомендовать его в качестве высокоэффективного средства терапии ОРЗ у детей.
Список литературы находится в редакции.
Медична газета «Здоров’я України 21 сторіччя» № 18 (415), вересень 2017 р.