12 листопада, 2017
Определение качества коррекции нейромедиаторной недостаточности с помощью метода количественной ЭЭГ
В рамках IX Международной конференции NeuroSymposium-2017 (12-14 сентября, г. Одесса) член-корреспондент НАМН Украины, профессор, главный научный сотрудник Государственного научного учреждения «Научно-практический центр профилактической и клинической медицины» Государственного управления делами (г. Киев) Владимир Ильич Черний представил результаты исследований, которые обосновывают применение препаратов нейрометаболического действия для восстановления уровня сознания и улучшения исходов у пациентов, находящихся в коматозном состоянии.
Актуальность проблемы нейротравмы как частой причины смерти и инвалидизации работоспособного населения не вызывает сомнений. При гематоме и размозжении мозга летальность достигает 55%, а инвалидами остаются 27% пострадавших. При ушибе-размозжении мозга эти показатели составляют 33 и 34% соответственно, а при диффузном аксональном повреждении летальность составляет 21%, но инвалидизация за счет отдаленных последствий травмы достигает 54%.
Первичное повреждение мозга создает условия для действия факторов вторичного повреждения, которые можно условно разделить на внутричерепные и внечерепные. К первой группе относятся ишемия и кровоизлияния, внутричерепная гипертензия и отек мозга, дислокационный синдром и компрессия сосудов мозга, церебральный вазоспазм, нейроинфекция. К внечерепным (системным) факторам вторичного повреждения мозга относятся артериальная гипотензия или гипертензия, гипертермия, гипо- и гипернатриемия, гипо- и гипергликемия, гипер- и гипокапния.
Механизмы вторичного повреждения мозга универсальны и не зависят от первичных повреждающих факторов. Они реализуются в соответствии с концепцией «ишемического каскада» и определяют единство подходов к интенсивной терапии больных с острыми церебральными поражениями.
Одним из наиболее перспективных направлений метаболической защиты мозга считается непосредственное воздействие на системы нейротрансмиттеров и рецепторов с целью нормализации соотношения процессов возбуждающей и тормозной нейротрансмиссии. В основе когнитивных нарушений и угнетения сознания при церебральной недостаточности лежит холинергическая недостаточность, обусловленная снижением выработки ацетилхолина и потерей холинергических нейронов. В связи с этим вызывает интерес применение препаратов, обладающих свойствами донаторов ацетилхолина или модуляторов холинергической передачи в центральной нервной системе (ЦНС).
На этом основан механизм нейропротекторного действия холина альфосцерата. Холина альфосцерат представляет собой соединение холина и глицерофосфата. Холин является предшественником ацетилхолина, а глицерофосфат служит субстратом для синтеза основного структурного компонента клеточных мембран – фосфатидилхолина. Введение холина альфосцерата способствует восстановлению холинергической нейротрансмиссии в ЦНС, что приводит к повышению уровня сознания и улучшению когнитивных функций. Мембраностабилизирующий эффект препарата предотвращает дальнейшую потерю нейронов и отек мозга.
Мы изучали эффекты холина альфосцерата (препарата Глиятон) и других нейропротекторов при поражениях ЦНС разной этиологии (черепно-мозговая травма, тяжелый инсульт), сопровождавшихся глубоким нарушением уровня сознания (Т.В. Островая, В.И. Черний, И.А. Андронова, 2007). Всего в отделении нейрохирургической реанимации под наблюдением находилось 10 пациентов в вегетативном состоянии. Оценка влияния нейрометаболической терапии на функции мозга проводилась методом интегрального количественного анализа электроэнцефалограммы (ЭЭГ). Обследование проводили в специально оборудованном реанимационном зале (лаборатория по исследованию функции мозга) с применением компьютерного цифрового энцефалографа NIHON KOHDEN EEG-1200.
Множественные публикации связывают активность определенных диапазонов ЭЭГ с функционированием различных медиаторных систем ЦНС. Медленные биоэлектрические процессы мозга частотой ниже 1 Гц рассматриваются как результат деятельности клеток нейроглии и служат индикатором энергетического метаболизма мозга. Активность с частотой 6-7,5 Гц связана с холинергической системой; 5-6 Гц – с серотонинергической системой; 4-5 Гц – с адренергической активацией; 11-12 Гц – с активацией дофаминергической системы; 24-25 Гц (бета-2) – с серотонинергической системой. Определение спектральной мощности сигнала в представленном диапазоне частот позволяет судить об угнетении или активации соответствующих нейромедиаторных систем, а анализ межполушарных различий ЭЭГ-паттернов дает представление о синхронизации билатеральных структур мозга.
Реактивность мозга исследовали как изменение спектральной мощности ЭЭГ (в %) во всех исследуемых диапазонах в ответ на введение нейротропных препаратов. Фармакологические пробы проводили с холина альфосцератом (Глиятон®), цитофлавином, амантадином, цитиколином, ипидакрином, диазепамом. Запись ЭЭГ производилась за 30 мин до и через 40 мин после введения полной дозы препарата.
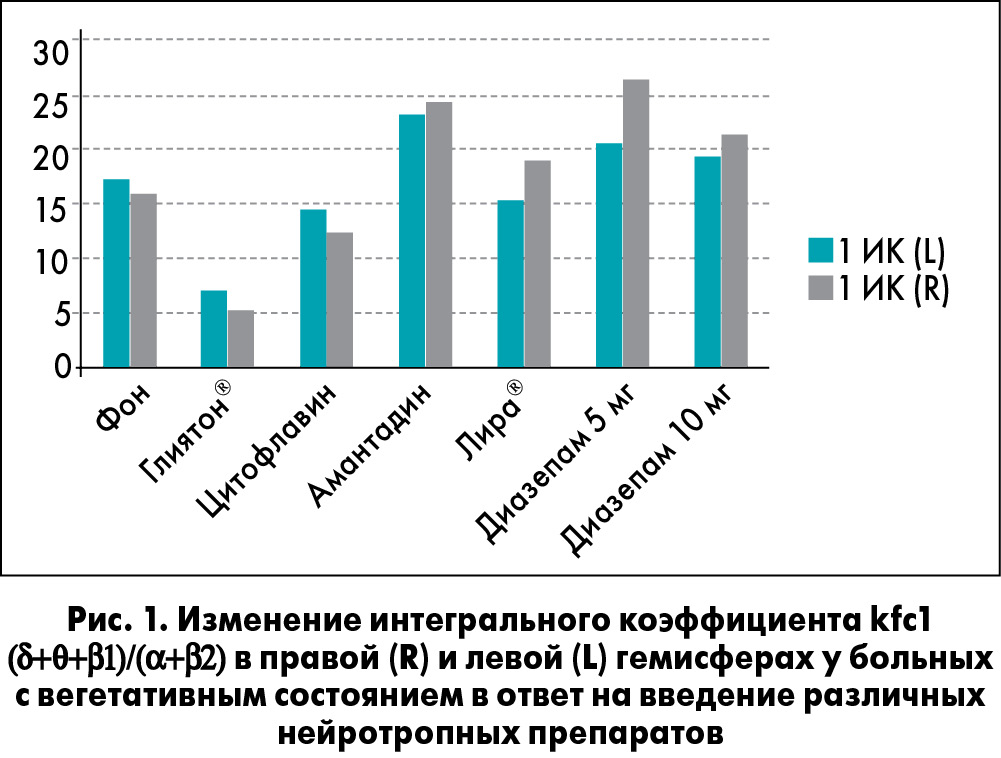
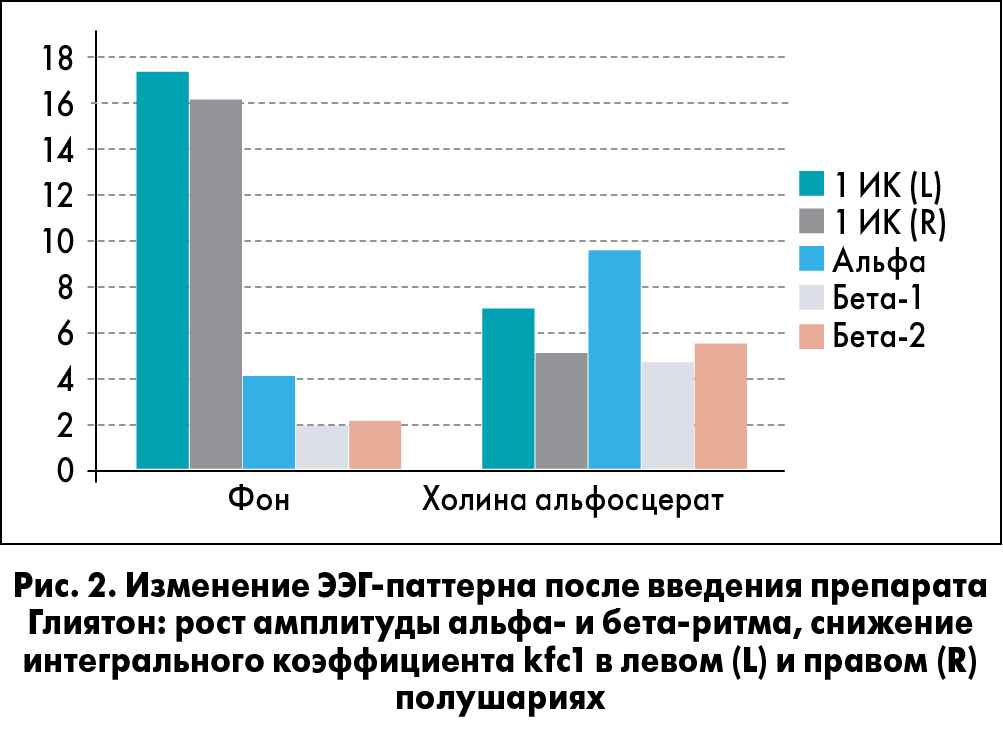
В процессе изучения реакции ЦНС на введение нейрометаболических препаратов наиболее эффективным по воздействию на интегральный показатель kfc1 (δ+θ+β1)/(α+β2) оказался холина альфосцерат (Глиятон®). В норме это соотношение близко к 1. После проведения фармакологических проб с препаратом Глиятон® зафиксировали наибольшее и статистически достоверное уменьшение (р≤0,05) уровня дезорганизации ЭЭГ-паттерна в правом и левом полушариях мозга (рис. 1), а также достоверный прирост биоэлектрической активности мозга в альфа- и бета-диапазонах (рис. 2).
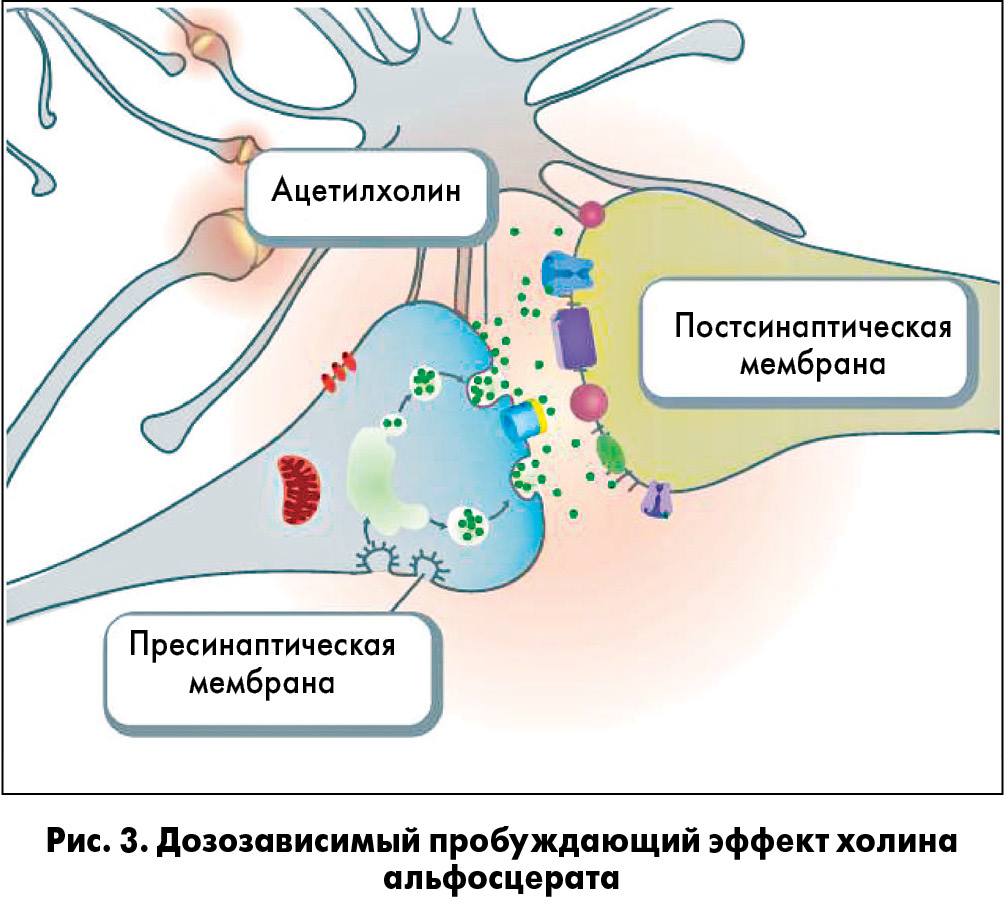
Применение холина альфосцерата в комплексной терапии больных с апаллическим синдромом способствует трансформации вегетативного состояния в «состояние малого сознания». В литературе этот феномен получил название «пробуждающий эффект». Он объясняется восстановлением физиологического уровня ацетилхолина в пресинаптических терминалях нейронов. При этом холина альфосцерат не связывается с постсинаптическими рецепторами ацетилхолина и не влияет на холинэстеразу, поэтому лишен побочных холинергических эффектов. Пробуждающий эффект описан при применении препарата в дозах 2000-4000 мг/сут внутривенно капельно (G. Bergamushi, 1994; М. Одинак, 2001).
Глиятон® применяется при состояниях с различной глубиной нарушения сознания (от оглушения до комы) в комплексной терапии пациентов с острыми нарушениями мозгового кровообращения, черепно-мозговой травмой, острым токсическим повреждением головного мозга, а также при хронической цереброваскулярной недостаточности (энцефалопатии, деменции различного генеза).
Еще одно важное направление нейропротекции при любом остром повреждении мозга – это повышение энергетической безопасности нейронов. Наиболее быстрым альтернативным путем коррекции тканевой гипоксии является сукцинатоксидазное окисление, которое достигается через повышение активности сукцинатдегидрогеназы и улучшение проникновения экзогенного сукцината в митохондрии. В этом направлении действует препарат Динар® – этилметилгидроксипиридина сукцинат. Он обладает способностью усиливать компенсаторную активацию аэробного гликолиза, снижать степень угнетения окислительных процессов в цикле Кребса в условиях гипоксии, активировать энергосинтезирующие функции митохондрий, что приводит к увеличению запасов АТФ и креатинфосфата.
Кроме того, Динар активирует эндогенную антиоксидантную систему супероксиддисмутазы и церулоплазмина, предупреждает снижение активности глутатионзависимых ферментов (глутатионпероксидазы, глутатионредуктазы), в результате чего эффективно подавляются процессы окислительного стресса клеточных мембран.
Модулируя активность мембраносвязанных ферментов (кальцийнезависимой фосфодиэстеразы, аденилатциклазы, ацетилхолинэстеразы), рецепторных комплексов (бензодиазепинового, ГАМК, ацетилхолинового) и усиливая их способность связывания с лигандами, Динар способствует сохранению структурно-функциональной организации биомембран, транспорту нейромедиаторов и улучшению синаптической передачи.
В исследовании с применением метода интегрального количественного анализа ЭЭГ в ответ на введение минимальной разовой дозы Динара (50 мг) преимущественно в пораженном полушарии была зафиксирована активация астроцитарной системы в зоне обратимого поражения тканей головного мозга (пенумбры), которая проявлялась в виде «мозаичного» роста абсолютной спектральной мощности в диапазоне 0,5-1 Гц (рис. 3).
Нейропротекторный эффект Динара объясняется не только нейрометаболическим действием, но и устранением вазоконстрикции интракраниальных сосудов, ликвидацией асимметрии кровотока, облегчением венозного оттока.
По нашему опыту, использование Динара в комплексе терапии при тяжелой черепно-мозговой травме сокращает сроки пребывания в отделении нейрохирургической интенсивной терапии до 8-10 суток. Эффективная доза препарата составила 8,5-13,5 мг/кг массы тела в сутки.
Таким образом, препарат Глиятон® устраняет центральную холинергическую недостаточность и обеспечивает прямую репарацию нейрональных мембран, что обеспечивает защиту мозга от каскада патологических реакций на ишемию и «пробуждающий эффект» у пациентов с тяжелой травматической болезнью головного мозга.
Динар® у пациентов с острой церебральной недостаточностью различного генеза даже в минимальных дозировках (разовая доза – 50 мг) активирует нейроглиальные структуры в зоне максимального поражения, в более высоких дозах (разовая доза – 100 более мг) обеспечивает восстановление локального кровотока, гематоэнцефалического барьера, глиальный синтез трофических факторов и модулирование синаптической передачи.
Подготовил Дмитрий Молчанов