25 грудня, 2017
Персонифицированный подход в хирургическом лечении злокачественных опухолей легких
 Радикальные хирургические вмешательства по поводу рака легкого включают пневмонэктомию и лоб(билоб)эктомию. Предпочтение отдается лоб(билоб)эктомии, поскольку при ее выполнении исключается инвалидизация и таким образом повышается качество жизни больного. Особую роль органосохраняющие операции приобретают у пациентов с низкими функциональными резервами при непереносимости пневмонэктомии. Но на момент выявления центрально расположенные опухоли легкого часто распространяются на устье долевого бронха и главный бронх. Выполнение лобэктомии возможно только с резекцией (клиновидной или циркулярной) главного бронха с последующей бронхопластикой. Инвазия опухолью легочной артерии является серьезным препятствием для органосохраняющей операции. При непереносимости пневмонэктомии бронхоангиопластическая лоб(билоб)эктомия является единственно возможным радикальным вмешательством. Особое место в структуре злокачественных опухолей легких занимает карциноид бронха – эта опухоль долгое время ведет себя, как доброкачественная, то есть растет в просвет бронха и перибронхиально с поздним метастазированием в регионарные лимфоузлы и редко дает отдаленные метастазы. Бронхопластическая операция при карциноиде крупного бронха позволяет сохранить легкое с хорошим отдаленным результатом.
Радикальные хирургические вмешательства по поводу рака легкого включают пневмонэктомию и лоб(билоб)эктомию. Предпочтение отдается лоб(билоб)эктомии, поскольку при ее выполнении исключается инвалидизация и таким образом повышается качество жизни больного. Особую роль органосохраняющие операции приобретают у пациентов с низкими функциональными резервами при непереносимости пневмонэктомии. Но на момент выявления центрально расположенные опухоли легкого часто распространяются на устье долевого бронха и главный бронх. Выполнение лобэктомии возможно только с резекцией (клиновидной или циркулярной) главного бронха с последующей бронхопластикой. Инвазия опухолью легочной артерии является серьезным препятствием для органосохраняющей операции. При непереносимости пневмонэктомии бронхоангиопластическая лоб(билоб)эктомия является единственно возможным радикальным вмешательством. Особое место в структуре злокачественных опухолей легких занимает карциноид бронха – эта опухоль долгое время ведет себя, как доброкачественная, то есть растет в просвет бронха и перибронхиально с поздним метастазированием в регионарные лимфоузлы и редко дает отдаленные метастазы. Бронхопластическая операция при карциноиде крупного бронха позволяет сохранить легкое с хорошим отдаленным результатом.
 Органосохраняющие операции являются более предпочтительными для хирургов, которые имеют дело со злокачественными опухолями различной локализации. Преимущества очевидны: радикальное вмешательство в сочетании с сохранением функции оперированного органа. Особое значение они приобретают в хирургии рака легкого. Во всем мире торакальные хирурги стремятся при выполнении операции по поводу рака легкого сохранить здоровую долю (или две доли при вмешательстве на правом легком) [1, 3-8]. Объясняется это двумя причинами: во-первых, тем, что пневмонэктомия – это инвалидизирующая операция, которая приводит к значительному снижению качества жизни пациента; во-вторых, непереносимостью пневмонэктомии у пациентов с низкими резервами дыхательной и сердечно-сосудистой систем. В некоторых случаях, например когда опухоль по главному бронху распространяется на бифуркацию трахеи, радикальное
Органосохраняющие операции являются более предпочтительными для хирургов, которые имеют дело со злокачественными опухолями различной локализации. Преимущества очевидны: радикальное вмешательство в сочетании с сохранением функции оперированного органа. Особое значение они приобретают в хирургии рака легкого. Во всем мире торакальные хирурги стремятся при выполнении операции по поводу рака легкого сохранить здоровую долю (или две доли при вмешательстве на правом легком) [1, 3-8]. Объясняется это двумя причинами: во-первых, тем, что пневмонэктомия – это инвалидизирующая операция, которая приводит к значительному снижению качества жизни пациента; во-вторых, непереносимостью пневмонэктомии у пациентов с низкими резервами дыхательной и сердечно-сосудистой систем. В некоторых случаях, например когда опухоль по главному бронху распространяется на бифуркацию трахеи, радикальное  вмешательство возможно только в объеме пневмонэктомии в сочетании с клиновидной или циркулярной резекцией бифуркации трахеи [2, 8]. При этом низкие функциональные резервы пациента могут стать непреодолимым препятствием на пути радикального лечения. В отдельных случаях (при раке верхнедолевого бронха справа) даже при распространении опухоли на бифуркацию трахеи можно избежать пневмонэктомии и выполнить верхнюю лобэктомию справа с краевой резекцией карины проксимальнее опухоли и формированием анастомоза между промежуточным бронхом и оставшейся частью бифуркации трахеи [5]. Сравнительный анализ пневмонэктомии и лобэктомии с бронхопластикой показал, что последняя не уступает в отношении возможности выполнения расширенной лимфодиссекции, при этом показатели послеоперационной летальности и количества осложнений более низкие по сравнению с пневмонэктомией. Пятилетняя выживаемость при обоих вмешательствах одинакова, а у группы больных с сердечно-сосудистой патологией она выше после выполнения бронхопластической лобэктомии [6]. Удельный вес бронхопластической лобэктомии при раке легкого остается низким в сравнении с пневмонэктомией в связи с более сложной хирургической техникой этого вмешательства и частым распространением опухоли с долевого бронха на правую (или левую) ветвь легочной артерии. В таких случаях при ограниченной инвазии легочной артерии возможно выполнение ее краевой или циркулярной резекции. Прямым показанием к выполнению бронхоангиопластических операций (лобэктомия с резекцией и пластикой бронхов и легочной артерии) является непереносимость пневмонэктомии. Немногочисленные сообщения об этих вмешательствах [3, 4, 7] могут свидетельствовать об их технической сложности.
вмешательство возможно только в объеме пневмонэктомии в сочетании с клиновидной или циркулярной резекцией бифуркации трахеи [2, 8]. При этом низкие функциональные резервы пациента могут стать непреодолимым препятствием на пути радикального лечения. В отдельных случаях (при раке верхнедолевого бронха справа) даже при распространении опухоли на бифуркацию трахеи можно избежать пневмонэктомии и выполнить верхнюю лобэктомию справа с краевой резекцией карины проксимальнее опухоли и формированием анастомоза между промежуточным бронхом и оставшейся частью бифуркации трахеи [5]. Сравнительный анализ пневмонэктомии и лобэктомии с бронхопластикой показал, что последняя не уступает в отношении возможности выполнения расширенной лимфодиссекции, при этом показатели послеоперационной летальности и количества осложнений более низкие по сравнению с пневмонэктомией. Пятилетняя выживаемость при обоих вмешательствах одинакова, а у группы больных с сердечно-сосудистой патологией она выше после выполнения бронхопластической лобэктомии [6]. Удельный вес бронхопластической лобэктомии при раке легкого остается низким в сравнении с пневмонэктомией в связи с более сложной хирургической техникой этого вмешательства и частым распространением опухоли с долевого бронха на правую (или левую) ветвь легочной артерии. В таких случаях при ограниченной инвазии легочной артерии возможно выполнение ее краевой или циркулярной резекции. Прямым показанием к выполнению бронхоангиопластических операций (лобэктомия с резекцией и пластикой бронхов и легочной артерии) является непереносимость пневмонэктомии. Немногочисленные сообщения об этих вмешательствах [3, 4, 7] могут свидетельствовать об их технической сложности.
Ниже представлено описание клинических наблюдений пациентов, которым были проведены бронхопластические вмешательства в сочетании с резекцией легочной артерии.
Клинические наблюдения
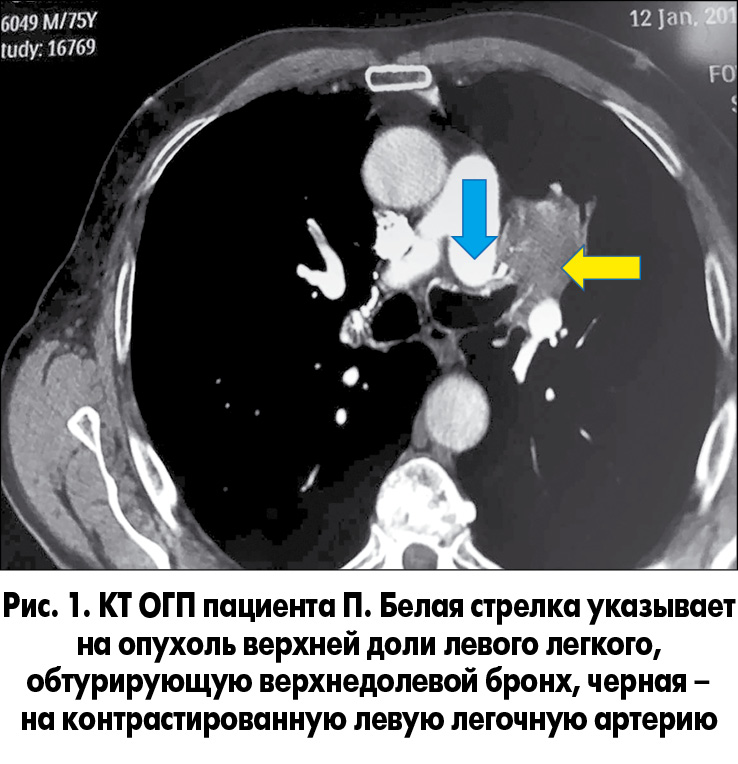
1. Пациент П., 75 лет, поступил 17.01.2016 в торакальное отделение Киевского городского клинического онкологического центра, которое является клинической базой кафедры онкологии НМУ имени А.А. Богомольца, с жалобами на сухой кашель, кровохарканье, одышку при физической нагрузке в течение последних 2 мес. До поступления пациент был проконсультирован и обследован в Национальном институте рака. При фибробронхоскопии (ФБС) выявлена карцинома верхнедолевого бронха левого легкого с обтурацией устья бронха. На компьютерной томограмме органов грудной полости (КТ ОГП) – картина опухоли верхней доли левого легкого с инвазией верхнедолевого бронха и интимным прилежанием опухоли к левой ветви легочной артерии с возможной инвазией (рис. 1).
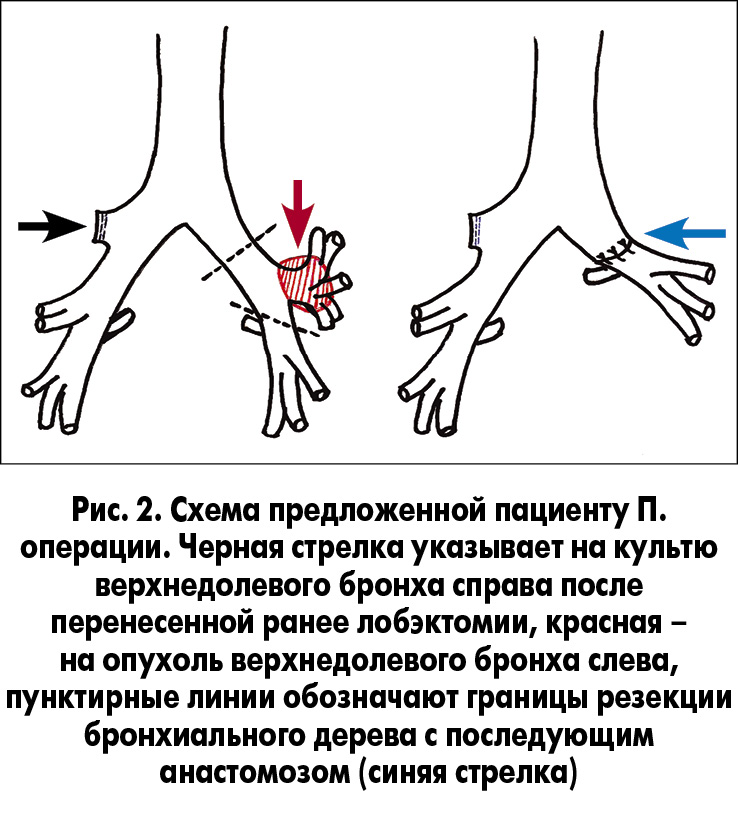
Из анамнеза: 20 лет назад пациенту была выполнена верхняя лобэктомия справа по поводу опухоли верхней доли правого легкого. Данные гистологического исследования опухоли получить не удалось, так как выписка из истории болезни пациентом утеряна. В Национальном институте рака ему предложили химиолучевую терапию, поскольку выполнить левостороннюю пневмонэктомию (необходимую при таком расположении опухоли) невозможно (справа отсутствует верхняя доля). Мы рекомендовали левостороннюю торакотомию с интраоперационной ревизией, по возможности – с выполнением реконструктивной органосохраняющей операции (рис. 2).
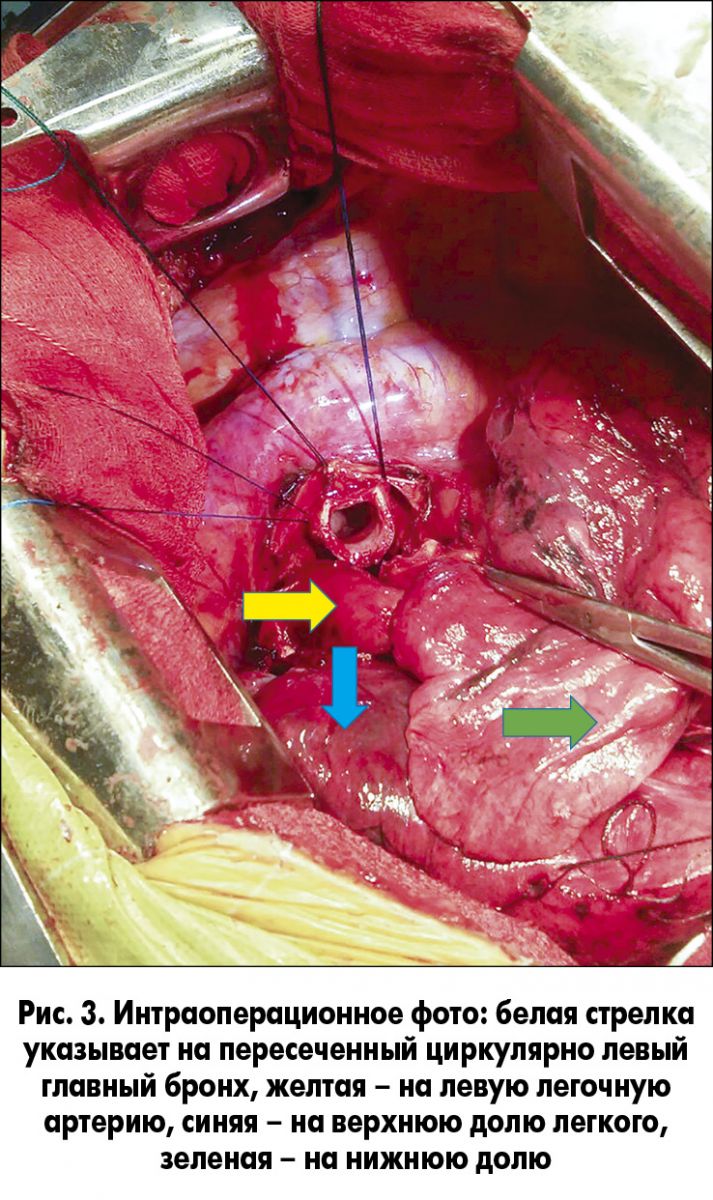
26.01.2016 пациенту выполнена левосторонняя боковая торакотомия. При ревизии выявлено, что опухоль локализована в корне верхней доли легкого, не переходит на нижнюю долю и отсутствует инвазия междолевой борозды. После разделения междолевой борозды, лигирования и пересечения артерий переднего и заднеапикального сегментов верхней доли выявлена инвазия устья артерии лингулярных сегментов верхней доли. Обработана вручную и пересечена верхняя легочная вена. После этого выполнена циркулярная резекция левого главного бронха и нижнедолевого бронха в зоне его деления на бронх шестого сегмента и ствол базальных сегментов (рис. 3).
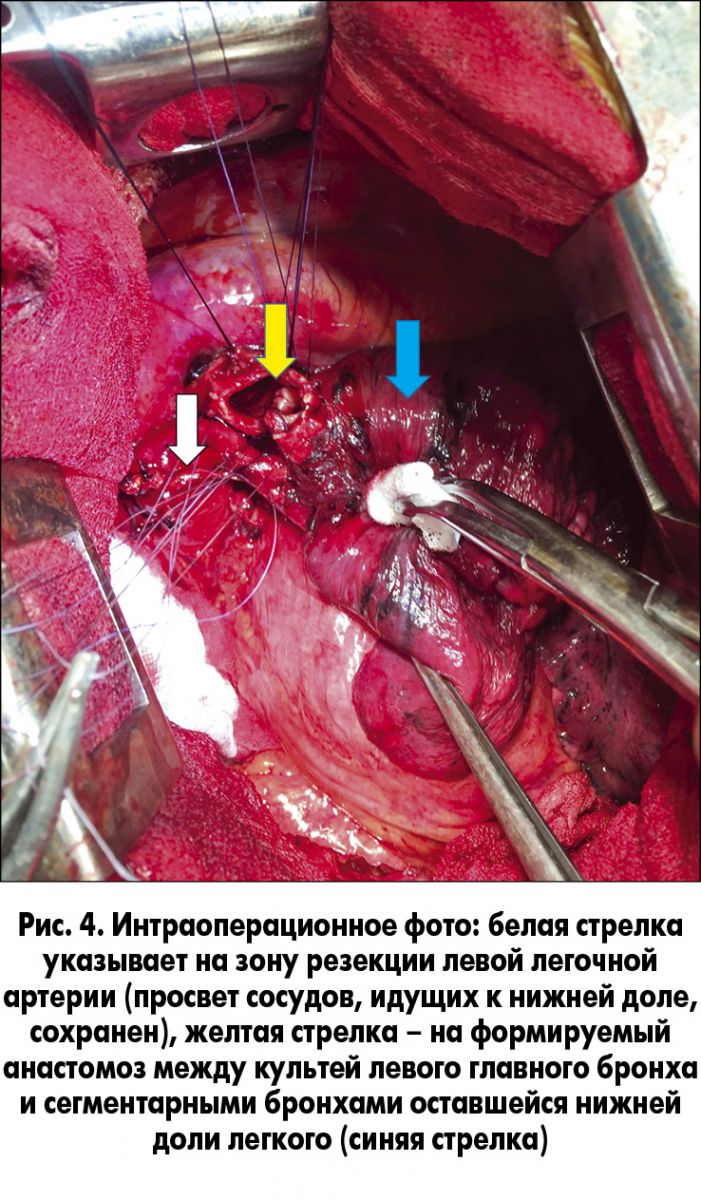
Это позволило, отведя бронхиальную манжету (из резецированного участка бронхов), выполнить краевую аппаратную резекцию легочной артерии в зоне опухолевой инвазии в пределах неизмененной стенки сосуда (макроскопически) (рис. 4).
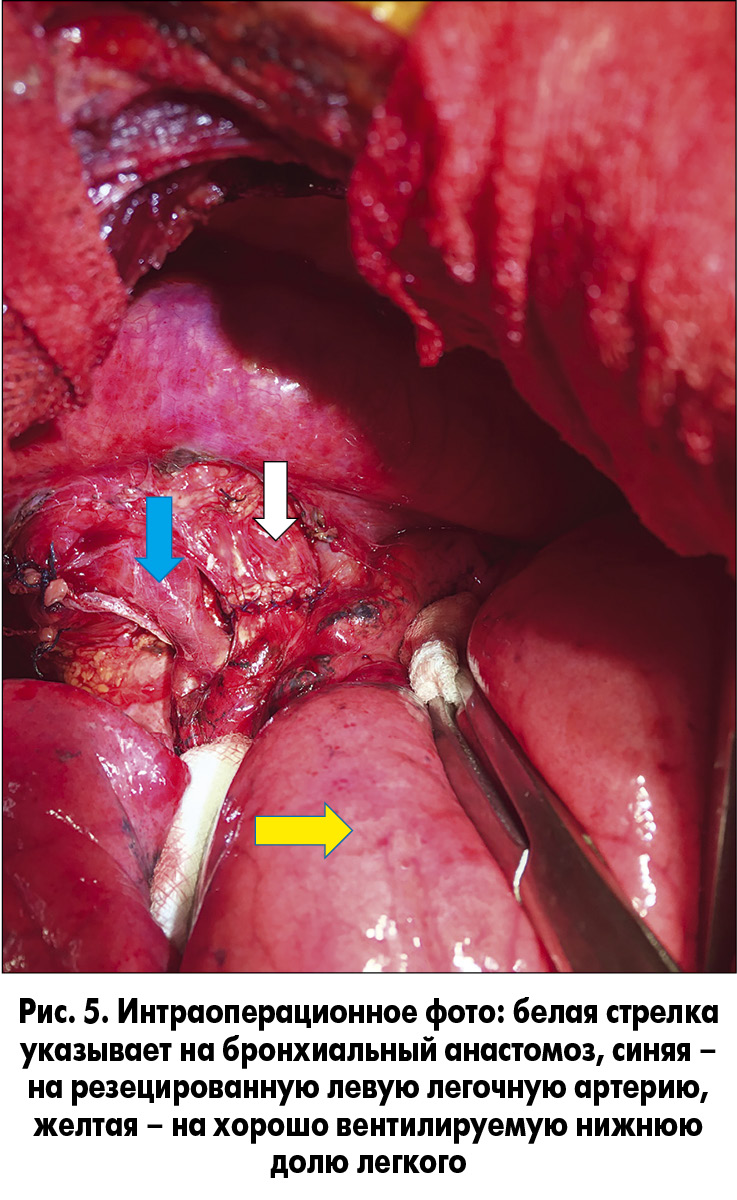
После завершения анастомоза последний был проверен на герметичность, и восстановлена вентиляция нижней доли левого легкого (рис. 5).
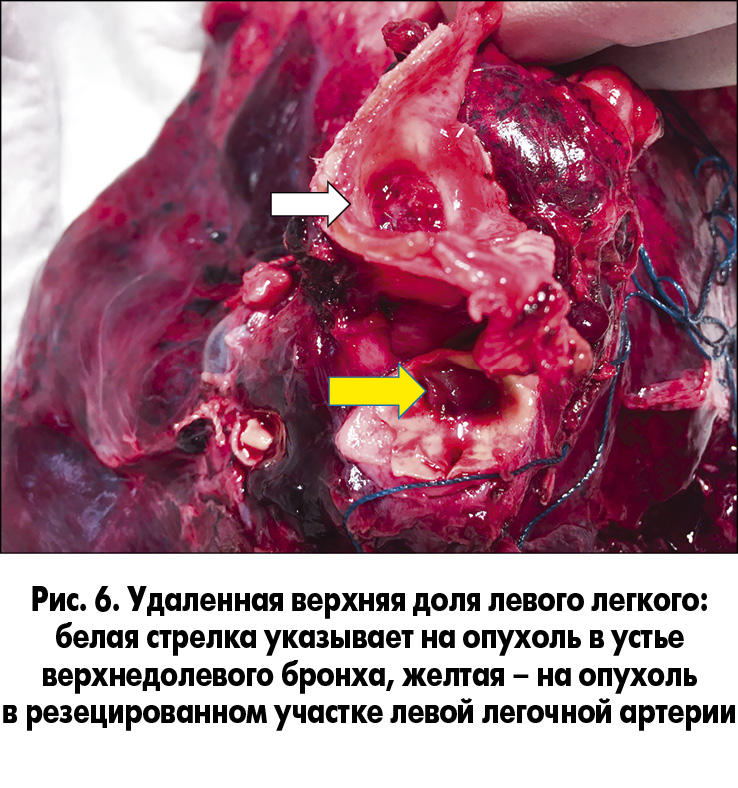
При осмотре удаленной верхней доли легкого хорошо видна опухоль в просвете резецированной легочной артерии и устье верхнедолевого бронха (рис. 6).
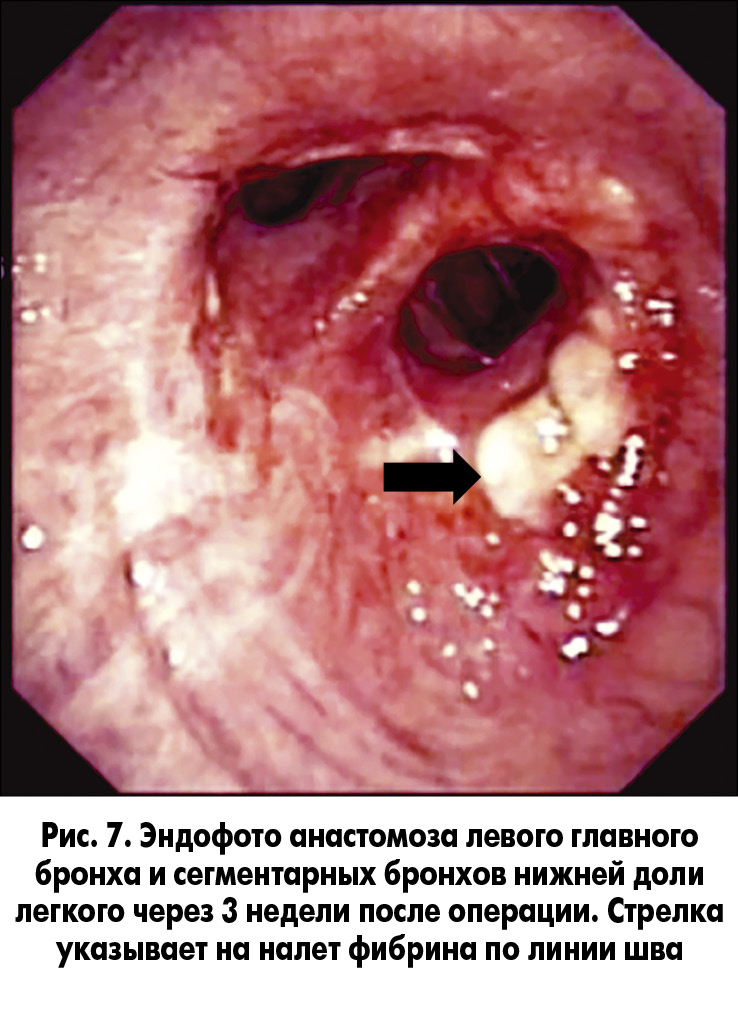
В послеоперационном периоде пациенту потребовалось регулярное проведение ФБС с санационной целью, так как он – курильщик со стажем, что явилось причиной обильного выделения мокроты, которую больной в первую неделю после операции не мог самостоятельно откашлять. Да и излишняя нагрузка на бронхиальный анастомоз, вызываемая кашлем, в первые две недели после операции нежелательна (рис. 7).
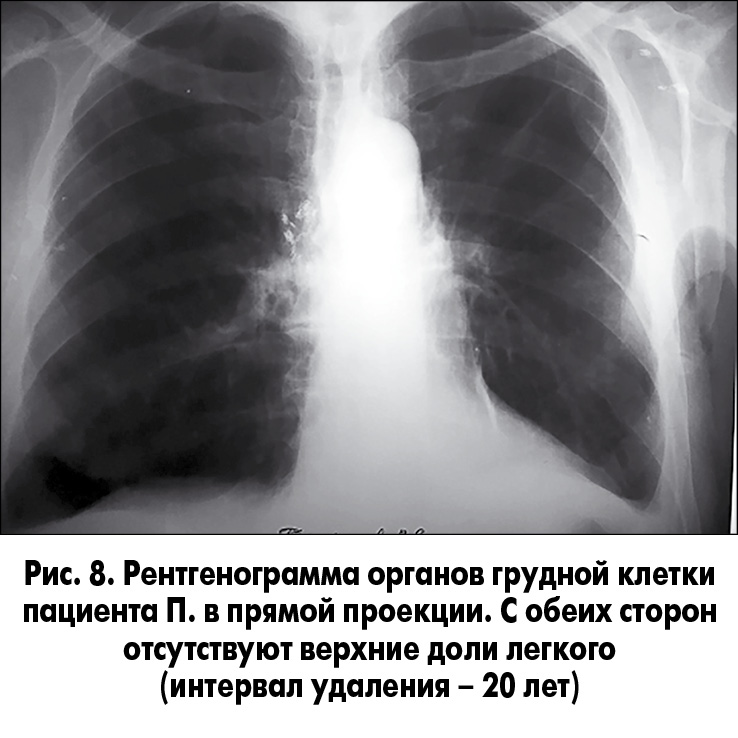
Послеоперационный период протекал без осложнений. Гистологическое заключение: плоскоклеточная карцинома легкого G2, метастазы в медиастинальных лимфоузлах и узлах корня легкого, а также в узлах, взятых из корня нижней доли, отсутствуют (pT2N1M0). Срезы бронхиального дерева и легочной артерии абластичны. На 22-е сутки после операции пациент в удовлетворительном состоянии выписан домой. Рентгенография органов грудной клетки проведена перед выпиской (рис. 8).
Послеоперационная химиотерапия больному не требовалась. Регулярно проходит обследование, данных о рецидиве заболевания нет.
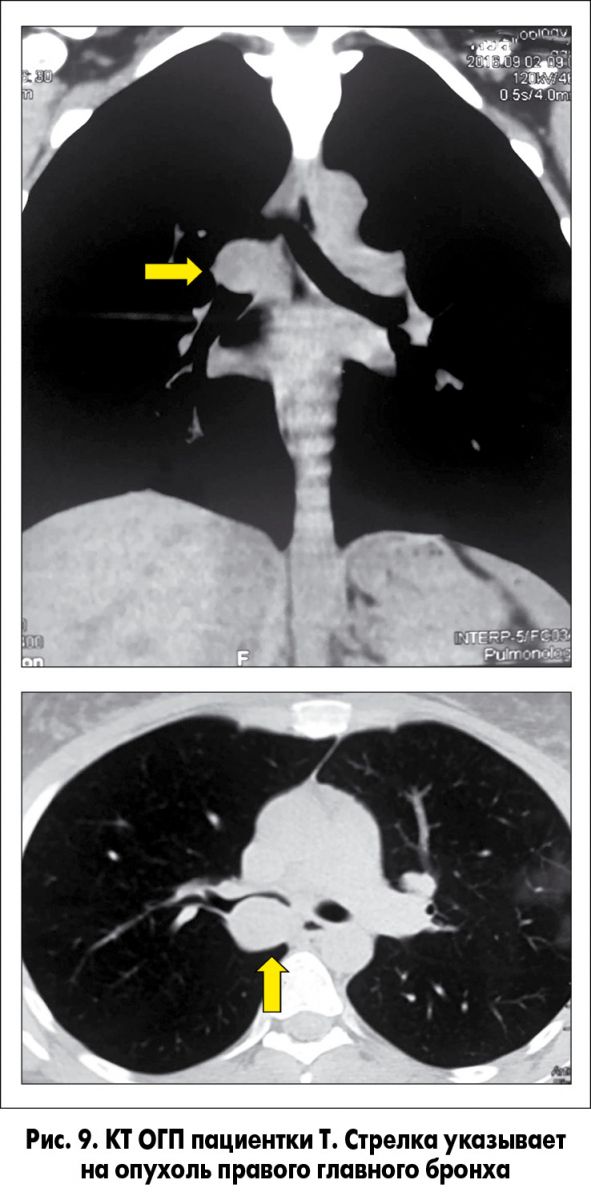
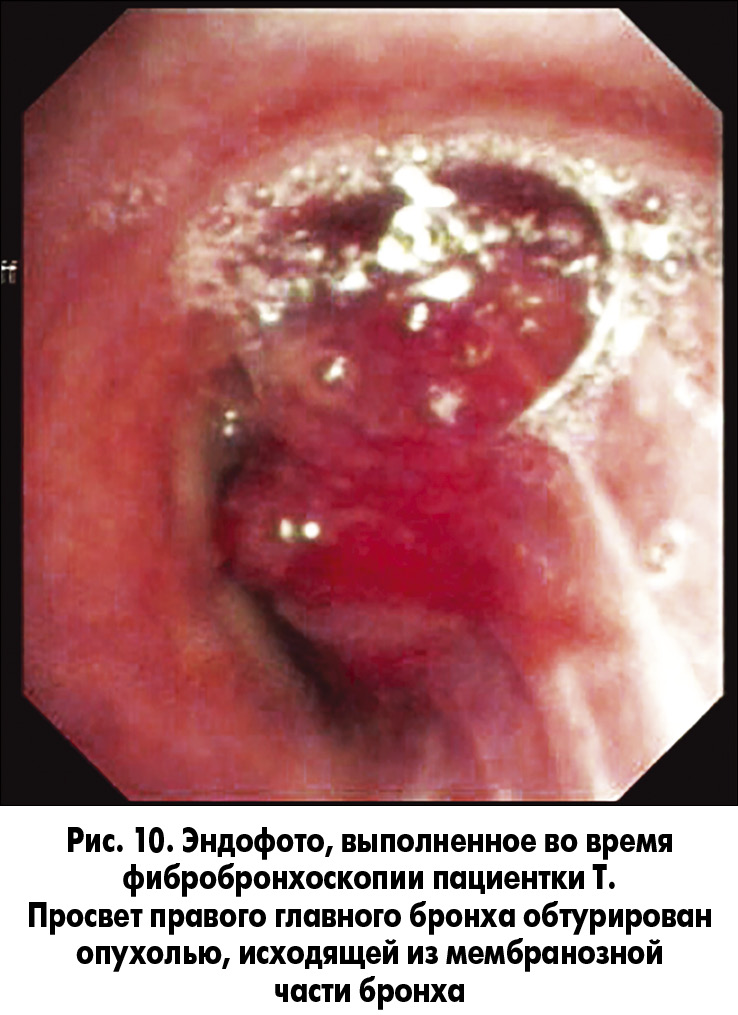
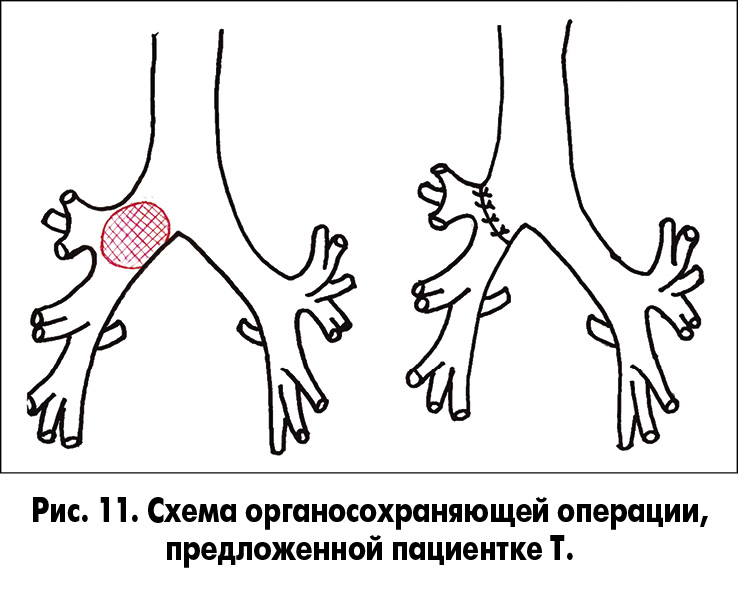
2. Пациентка Т., 30 лет, обратилась в клинику кафедры онкологии НМУ имени А.А. Богомольца на базе Киевской клинической больницы железнодорожного транспорта № 3 в сентябре 2016 г. Жалобы на кашель, периодически – с гнойной мокротой, одышку при умеренной физической нагрузке. До обращения была обследована (КТ ОГП, ФБС; рис. 9 и 10) в одном из лечебных учреждений г. Киева. У пациентки была диагностирована злокачественная опухоль (карциноид) правого главного бронха. Ей предложили операцию – пневмонэктомию справа. От этого варианта лечения пациентка отказалась. Мы рекомендовали органосохраняющую операцию (рис. 11).
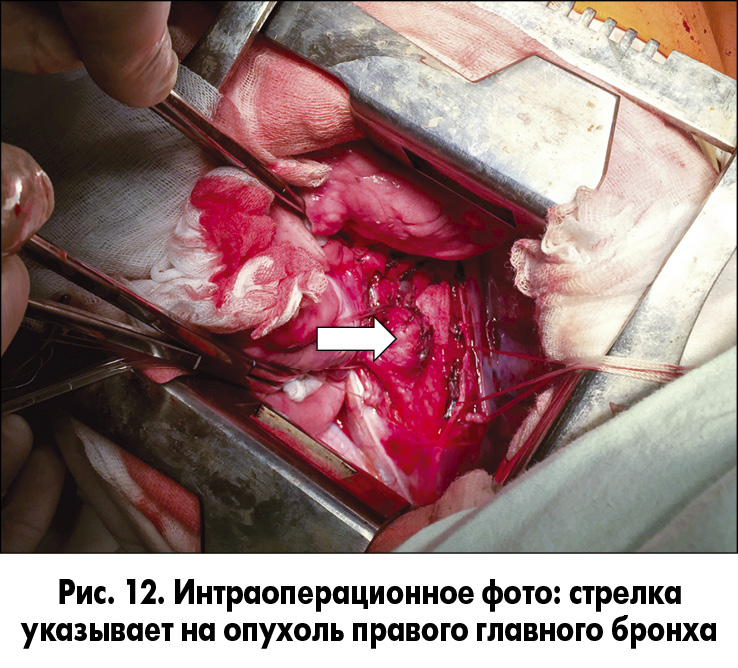
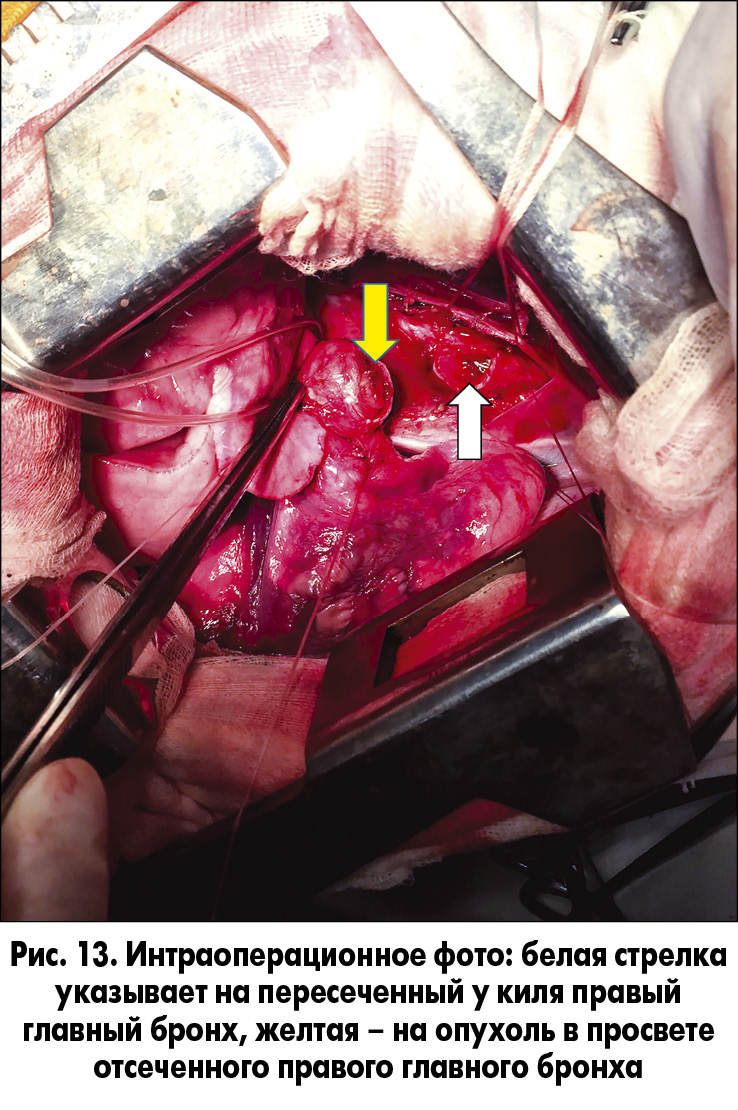
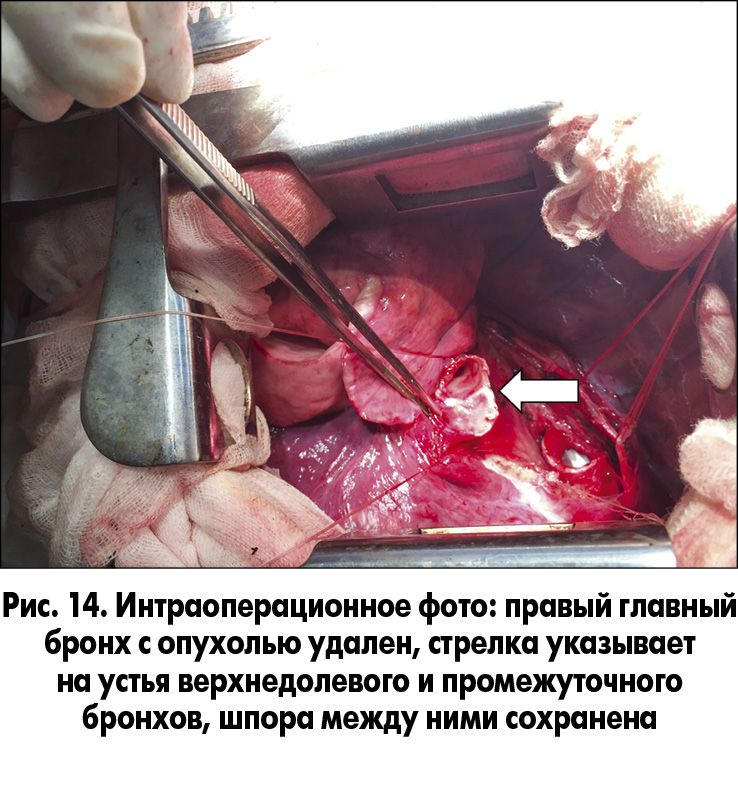
19.09.2016 из правостороннего бокового торакотомного доступа мы выполнили циркулярную резекцию правого главного бронха, отступив одно полукольцо от киля (проксимальная граница), и в зоне деления правого главного бронха на верхнедолевой и промежуточный бронхи (дистальная граница) (рис. 12-14).
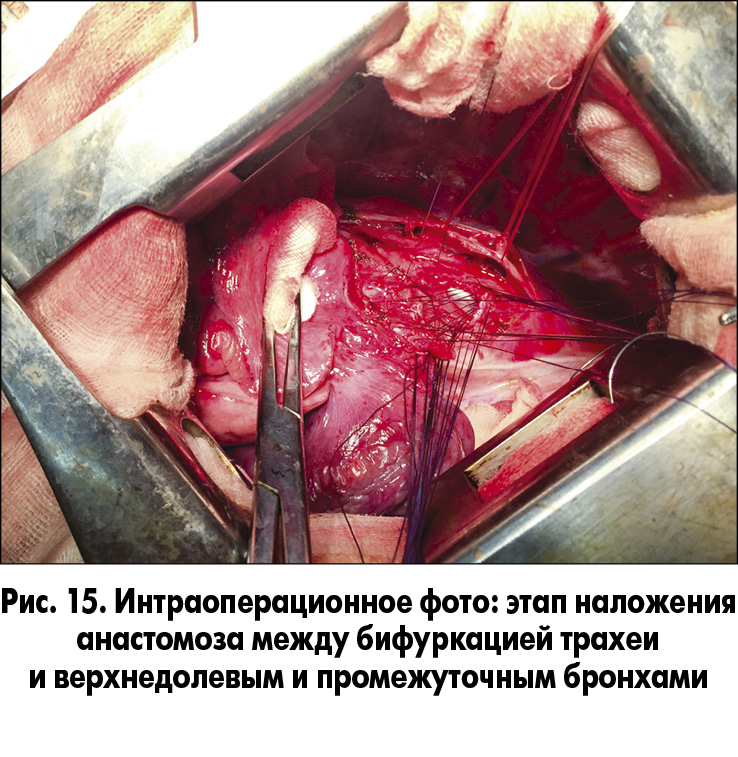
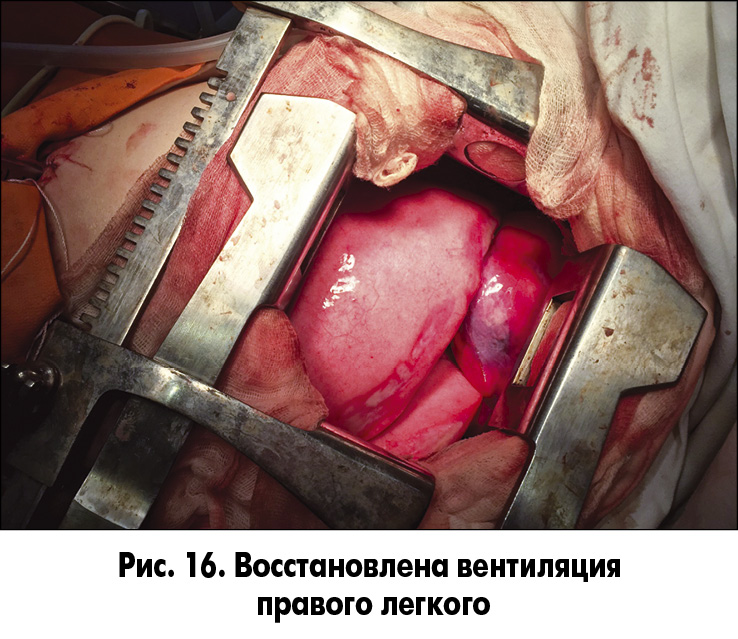
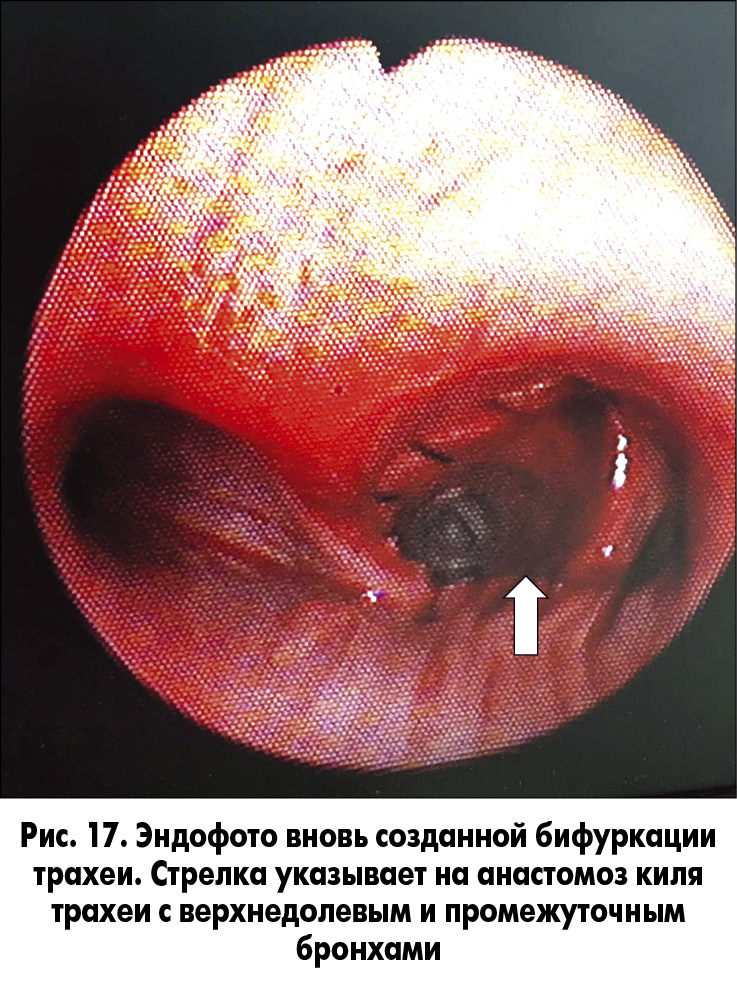
На этом этапе операции осуществлялась однолегочная (левое легкое) вентиляция. После циркулярной резекции правого главного бронха сформирован анастомоз между бифуркацией трахеи, верхнедолевым и промежуточным бронхами (рис. 15 и 16). Вентиляция правого легкого восстановлена в полном объеме. Выполнен эндоскопический контроль анастомоза (рис. 17).
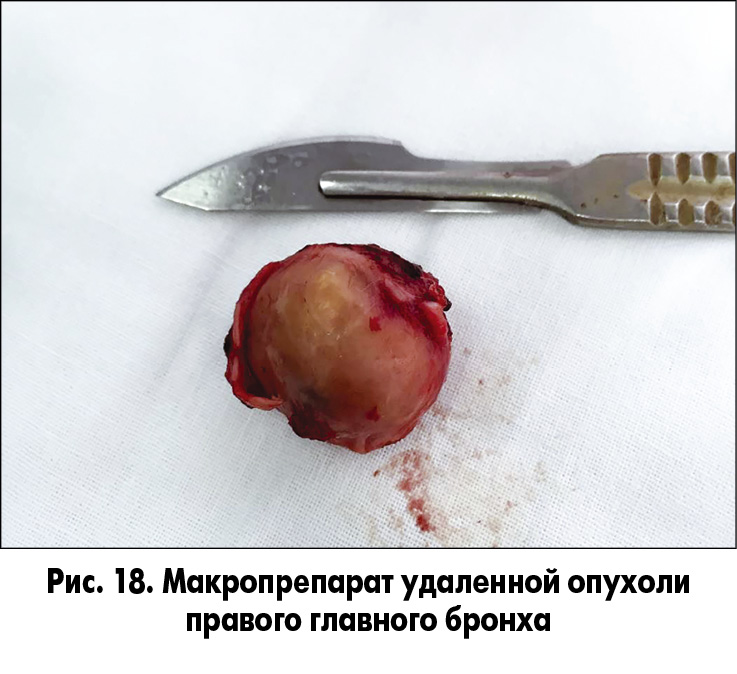
Из особенностей: опухоль не выходила за пределы правого главного бронха, регионарные лимфоузлы были не изменены, в правом легком скопилось значительное количество слизисто-гнойной мокроты (санация во время операции).
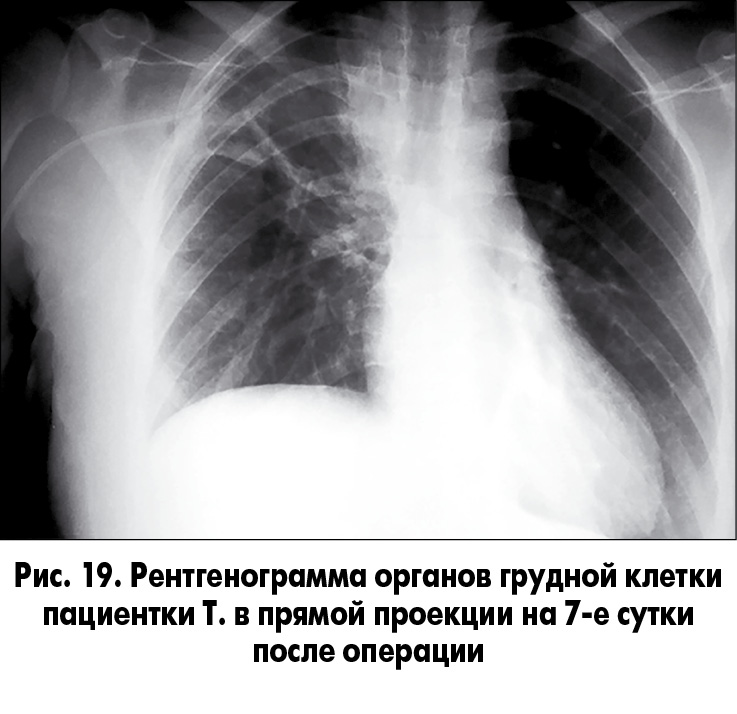
Послеоперационный период протекал без осложнений. 6.09.2017 была выполнена контрольная рентгенография органов грудной клетки (рис. 19).
ПГЗ: атипичный карциноид правого главного бронха, срезы бронха абластичны, метастазов в регионарных лимфоузлах не выявлено.
Больная регулярно проходит контрольное обследование (рентгенография органов грудной клетки, ФБС), данных о рецидиве заболевания нет.
Обсуждение
Представленные клинические наблюдения наглядно демонстрируют необходимость персонифицированного подхода в хирургическом лечении онкологической патологии. Особенно это важно при операциях на легких, поскольку от этого зависит сохранение дыхательной функции пациента, как это было в случае с молодой женщиной. Предложенная ей пневмонэктомия также была бы радикальной с онкологической точки зрения, но у 30-летней пациентки она привела бы к значительному снижению функции внешнего дыхания, ограничению физической активности с ухудшением качества жизни, а в последующем – к развитию сердечной недостаточности.
В случае с пациентом, описанном в первом клиническом наблюдении, выполненная операция была радикальной с онкологической точки зрения, позволила сохранить здоровую нижнюю долю левого легкого и не допустить снижения качества жизни пациента. При этом удалось избежать химиолучевого лечения по паллиативной программе с пессимистическим прогнозом.
Выводы
- Персонифицированный подход к проведению сложных реконструктивных операций в торакальной онкохирургии, как и в медикаментозном лечении опухолей, позволяет у определенной группы больных достичь онкологической радикальности и при этом сохранить высокое качество их жизни.
- Проведение таких операций возможно только в подразделениях, медицинский персонал которых имеет высокую квалификацию и достаточный опыт их выполнения.
Литература
- Berthet J.P., Paradela M., Jimenez M.J., Molins L., Gomez-Caro A. Extended sleeve lobectomy: one more step toward avoiding pneumonectomy in centrally located lung cancer // Ann Thorac Surg, 2013. – Vol. 96. – № 6. – p. 1988-97.
- Eichhorn F., Storz K., Hoffmann H., Muley T., Dienemann H. Sleeve pneumonectomy for central non-small cell lung cancer: indications, complications, and survival // Ann Thorac Surg, 2013. – Vol. 96. – № 1. – p. 253-258.
- Gomez-Caro A., Garcia S., Jimenez M.J., Matute P. et al. Lung sparing surgery by means of extended broncho-angioplastic (sleeve) lobectomies // Arch Broncopneumol, 2011. – Vol. 47. – № 2. – p. 66-72.
- Ibrahim M., Maurizi G., Venuta F., Rendina E.A. Reconstruction of the bronchus and pulmonary atery // Thorac Surg Clin, 2013. – Vol. 23. – № 3. – p. 337-347.
- Kaya S.O., Sevinc S., Ceylan K.C., Usluer O., Unsal S. One-stoma carinoplasty: right upper sleeve lobectomy with hemicarinectomy for resection of right-tracheobronchial-angle tumors // Tex Heart Inst J, 2013. – Vol. 40. – № 4. – p. 435-438.
- Schirren J., Schirren M., Passalacqua V., Bolukbas S. Pneumonectomy: an alternative to sleeve resection in lung cancer patients? // Chirurg, 2013. – Vol. 84. – № 6. – p. 474-478.
- Sun Y., Zheng H., Chen Q. et al. Triple plasty of bronchus, pulmonary artery, and superior vena cava for non-small cell lung cancer // Ann Thorac Surg, 2013. – Vol. 95. – № 2. – p. 420-424.
- Yang H., Ma S., Shen L., Chen K. The evaluation of pneumonectomy and bronchoplasty lobectomy in the treatment of non-small cell lung cancer: a report of 64 cases // Zhongguo Fei Ai Za Zhi, 2012. – Vol. 15. – № 4. – p. 218-222.
Тематичний номер «Онкологія» № 5 (51), грудень 2017 р.