28 грудня, 2017
Ефективність і переносимість німесуліду в контролі болю при аноректальних та пахвинно-калиткових хірургічних втручаннях
Незважаючи на постійне вдосконалення надання медичної допомоги хворим у післяопераційному періоді, проблема лікування післяопераційного болю усе ще залишається актуальною, адже від вираженого больового синдрому страждають від 30 до 75% пацієнтів. Відтак швидке й максимально повне купірування болю належить до першочергових завдань фармакотерапії.
У післяопераційному періоді запальні медіатори (серотонін, цитокіни, лейкотрієни, простагландини), що виділяються в ділянці пошкодження тканин, стимулюють полімодальні ноцицептори, які підсилюють їх виділення, таким чином знижуючи поріг больової чутливості (первинна гіпералгезія). Розвиток місцевого набряку тканини внаслідок порушення проникності капілярів, а також під впливом гістаміну й брадикініну ще більше сенситизує рецептори (вторинна гіпералгезія). Простагландини підвищують проникність капілярів і збільшують чутливість ноцицепторів такою мірою, що навіть нешкідливі в нормі стимули (наприклад, тиск) викликають біль. Усе це робить патогенетично обґрунтованим призначення у післяопераційному періоді нестероїдних протизапальних препаратів (НПЗП), які шляхом інгібування цилооксигенази (ЦОГ) зменшують активність запальних медіаторів і забезпечують знеболюваний ефект.
Німесулід (Німесил®) – унікальний представник НПЗП із потужною знеболювальною, протизапальною та антипіретичною активністю, підтвердженою експериментально й доведеною в клінічних дослідженнях. Німесулід справляє вплив на обидві ізоформи ЦОГ із переважним інгібуванням ЦОГ‑2. У терапевтичних концентраціях німесулід пригнічує 88% активності ЦОГ‑2 і 45% активності ЦОГ‑1.
При цьому якщо вплив на ЦОГ‑1 припиняється через 24 год, то дія на ЦОГ‑2 продовжується, і ця різниця зберігається й при тривалому застосуванні. Така збалансована дія німесуліду на ізоформи ЦОГ пояснює знижений ризик ускладнень із боку шлунково-кишкового тракту (ШКТ) порівняно із неселективними НПЗП і відсутність вираженої кардіоваскулярної токсичності на відміну від коксибів.
Німесулід також має низку фармакологічних ефектів, які не залежать від клас-специфічного впливу на ЦОГ‑2. Зокрема, препарат пригнічує гіперпродукцію головних прозапальних цитокінів (інтерлейкіну‑6, фактора некрозу пухлини α), знижує активність металопротеїназ, справляє антигістамінну дію. До не-ЦОГ‑2-асоційованих ефектів німесуліду належить його здатність пригнічувати фермент фосфодіестеразу 4 типу, тим самим знижуючи активність макрофагів і нейтрофілів, які відіграють неабияку роль у патогенезі гострої запальної реакції. Для хірургічної практики важливо, що німесулід не збільшує час кровотечі.
Метою цього дослідження було оцінити ефективність і переносимість німесуліду в пацієнтів після виконання аноректальних або пахвинно-калиткових хірургічних втручань.
Методи
У дослідження залучили чоловіків і жінок віком від 20 до 70 років, яким планувалися хірургічні втручання на аноректальній або пахвинно-калитковій ділянці. Критеріями виключення були: тяжкі серцеві, ниркові, печінкові, легеневі, метаболічні або неврологічні захворювання; підвищена чутливість до НПЗП; алкоголізм; вагітність або лактація.
Учасники отримували німесулід у дозі 100 мг перорально 2 р/добу. Першу дозу препарату призначали через 2 год після операції, другу – увечері о 20:00. Починаючи з другого дня пацієнти приймали німесулід о 8:00 та о 20:00. Інші НПЗП у ході дослідження приймати не дозволялося.
Хірургічні втручання проводили під спинальною або локальною анестезією. Седативні препарати призначали за потребою через 1 год після прийому вечірньої дози німесуліду. Всі пацієнти отримували антибіотикопрофілактику.
Пацієнти оцінювали ефективність знеболення за зміною інтенсивності болю, яку вимірювали за допомогою 100 мм візуальної аналогової шкали (ВАШ) щопівгодини протягом перших 2 год після операції, тоді кожні 2 год упродовж 12 год і надалі з інтервалом у 6 год.
Лікарі оцінювали ефективність контролю болю з урахуванням таких параметрів: швидкість настання аналгетичної дії та її тривалість, потреба у седативних і снодійних засобах, профіль побічних ефектів.
Безпеку та переносимість оцінювали за частотою побічних ефектів та зміною лабораторних показників (загальний аналіз крові, показники печінкової і ниркової функції).
Порівняння інтенсивності болю та інших показників аналізували з використанняма t-критерію Стьюдента або тесту χ2; різницю вважали статистично значущою при p<0,05.
Результати
 У дослідженні взяли участь 176 пацієнтів (139 чоловіків і 37 жінок).
У дослідженні взяли участь 176 пацієнтів (139 чоловіків і 37 жінок).
Показаннями для хірургічного втручання були геморой (n=36), анальна фістула (n=32), анальна тріщина (n=20), гідроцеле (n=54), пахвинна грижа (n=20) і варикоцеле (n=14).
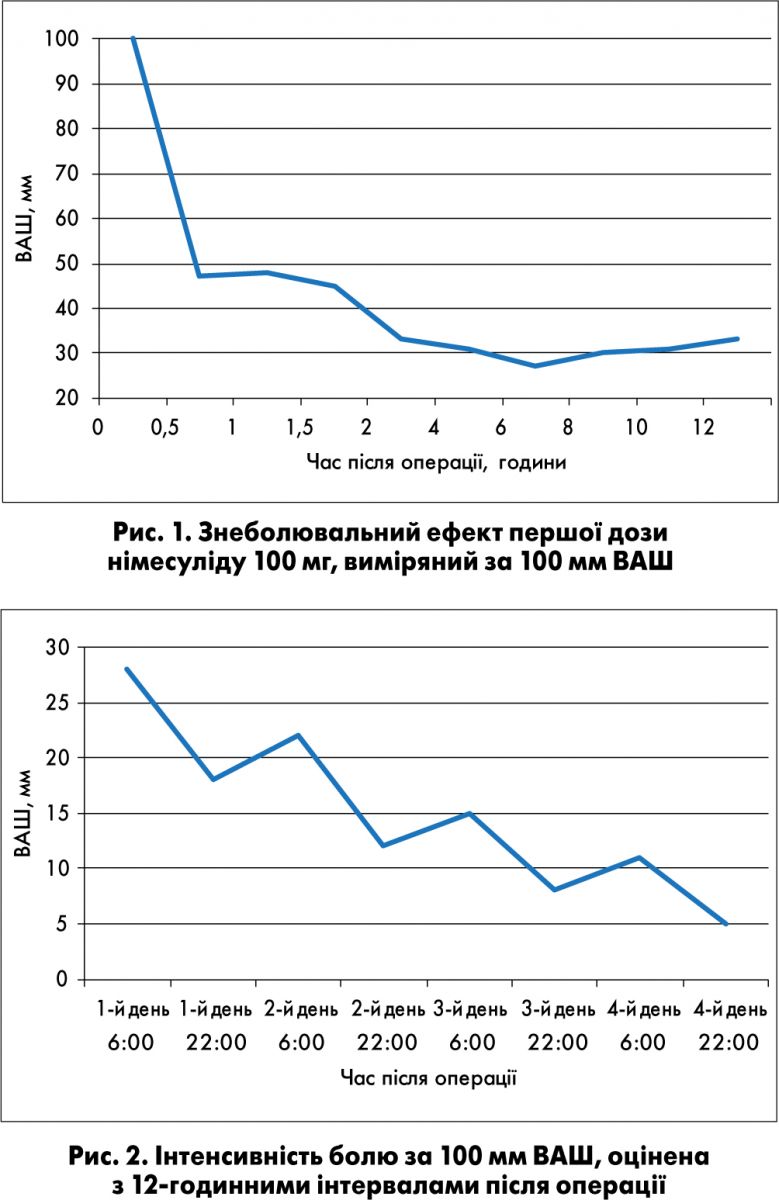
Виражений знеболюваний ефект розвивався приблизно через 0,5 год після прийому першої дози німесуліду, значно посилювався через 4 год і зберігався протягом наступних 12 год (р<0,01) (рис. 1).
Інтенсивність бою зменшилась із початкових 100 мм за ВАШ до 31 мм через 4 год і на 4-й день спостереження становила лише 4,5 мм (рис. 2).
Додаткової аналгезії петидином потребували в 1-й день 33 пацієнти (18,75%), на 4-й день – 11 хворих (6,25%).
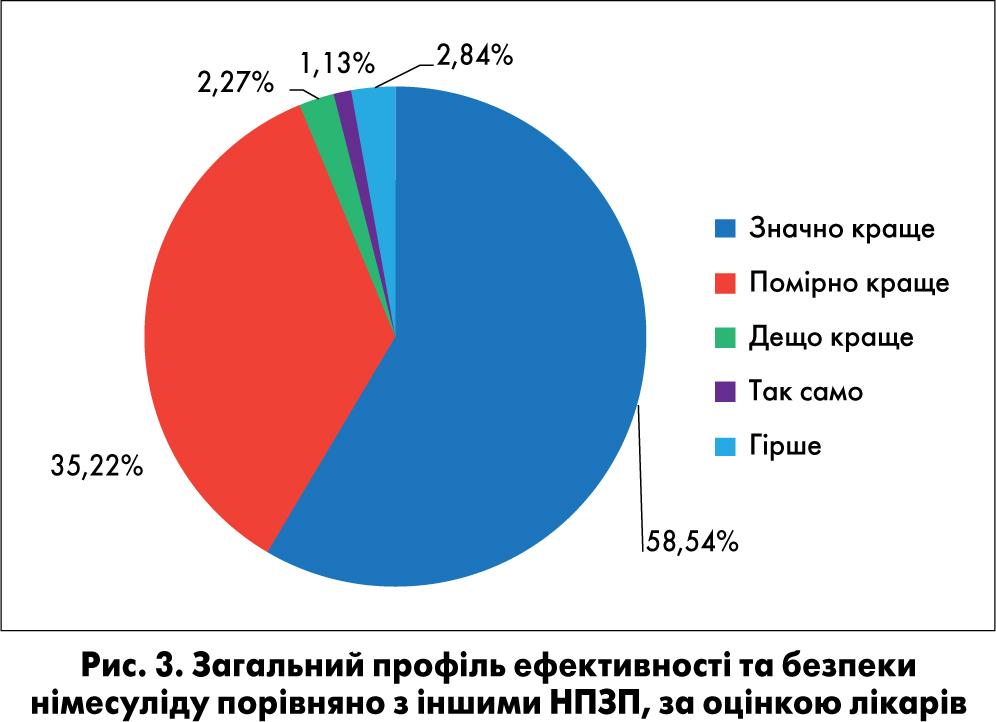
За оцінкою лікарів, загальний профіль ефективності й безпеки німесуліду був значно кращий порівняно з таким в інших НПЗП у 103 (58,54%) пацієнтів, помірно кращий – у 62 (35,22%), дещо кращий – у 4 (2,27%), порівнянний – у 2 (1,13%) та гірший – у 5 (2,84%) пацієнтів (рис. 3).
 Після 4 днів лікування німесулідом показники гемограми, печінкової та ниркової функції суттєво не змінилися.
Після 4 днів лікування німесулідом показники гемограми, печінкової та ниркової функції суттєво не змінилися.
Німесулід добре переносився; побічних ефектів, потенційно пов’язаних із прийомом препарату, не спостерігалося.
Обговорення
Проведене дослідження свідчить про високу аналгетичну ефективність і безпеку німесуліду в пацієнтів із болем після виконання аноректальних або пахвинно-калиткових хірургічних втручань. Виражений знеболювальний ефект розвивався вже через 30 хв після прийому першої дози препарату.
Отримані дані узгоджуються з результатами інших досліджень з вивчення ефективності німесуліду. Наприклад, у багатоцентровому дослідження A. Binning (2007) пацієнтів із помірним або тяжким болем після артроскопії та меніскектомії (n=94) рандомізували для прийому німесуліду у дозі 100 мг, напроксену у дозі 500 мг або плацебо 2 р/добу протягом 3 днів. Німесулід виявився набагато ефективнішим за плацебо за первинною кінцевою точкою – різницею інтенсивності болю протягом 6 год після першого прийому препарату, а також значно краще зменшував біль порівняно з напроксеном. Усі три препарати добре переносилися, але в групі німесуліду було зареєстровано менше побічних реакцій і не виявлено жодного ускладнення з боку ШКТ на відміну від групи напроксену.
В інших дослідженнях німесулід продемонстрував високу знеболювальну ефективність у пацієнтів після оториноларингологічних, загальнохірургічих, стоматологічних втручань, після пластики грижі та мастектомії (M. Zuccurman et al., 1993; G. Stafanoni et al., 1990; G. Romella et al., 1993; S. Coscarelli et al., 1993; P. Pierleoni et al., 1993).
Висновки
У пацієнтів, які перенесли аноректальні й пахвинно-калиткові хірургічні втручання, німесулід забезпечує швидке й потужне післяопераційне знеболення та добре переноситься. Призначення німесуліду у дозі 100 мг перорально через 30 хв після операції з подальшим прийомом по 100 мг 2 р/добу є раціональною альтернативою ін’єкційним НПЗП та опіоїдам у комплексному веденні післяопераційного болю.
Список літератури знаходиться в редакції.
Gupta R.L., Chaudhary A., Sethi H.C.
Efficacy and Tolerability of Nimesulide in Post Operative
Pain of Anorectal and Inguinoscrotal Surgery, 2007.
Переклав з англ. Олексій Терещенко


