29 грудня, 2017
Лікування хворих на гострий панкреатит: спільна проблема інтенсивної терапії та хірургії
 Гострий панкреатит (ГП) – це асептичне/септичне запалення підшлункової залози (ПЗ) та парапанкреатичної клітковини, яке, як і кожен запальний процес, супроводжується змінами гомеостазу.
Гострий панкреатит (ГП) – це асептичне/септичне запалення підшлункової залози (ПЗ) та парапанкреатичної клітковини, яке, як і кожен запальний процес, супроводжується змінами гомеостазу.
ГП характеризується низкою симптомів – від місцевого запального процесу до більш тяжкої його форми (гострий некротичний панкреатит), яка розвивається як відповідь організму на запалення і відзначається високою смертністю. Розвиток гострого некротичного панкреатиту, як правило, пов’язаний із некрозом ацинусів ПЗ. Апоптоз ацинарних клітин, вивільнення цитокінів, активація коагуляції, ішемія та некроз тканин є ключовими факторами в погіршенні стану й розвитку відповідних екстрапанкреатичних ускладнень [7].
У цій системі важливу роль відіграють тромбоцити, оскільки вони є першою ланкою, яка реагує на порушення цілісності судинної стінки (судинно-тромбоцитарний гемостаз). Необхідно враховувати і те, що більшість реакцій ферментного гемостазу теж відбувається на поверхні тромбоцитів [5]. Вони залучаються до цього процесу на ранніх стадіях, які ще важко виявити й оцінити. Одним із факторів, який сприяє погіршенню стану хворого з ГП, є виникнення тромботичної мікроангіопатії та тромбування мікросудинного русла різних органів та систем.
Незважаючи на сучасні успіхи анестезіології та хірургії, проблеми лікування хворих із ГП досі не тільки не втратили своєї актуальності, а й набули нової гостроти. Насамперед це зумовлено розгортанням дискусії навколо питань про кількісний та якісний склад інфузійної терапії, неоднозначними позиціями щодо застосування антиферментних препаратів та появою мультирезистентних штамів бактерій: метицилінрезистентних стафілококів (MRSA), ванкоміцинрезистентних ентерококів (VRE), бактерій сімейства Enterobacteriaceae (E. coli і K. pneumoniae) із розширеним спектром b-лактамаз (Extended-spectrum b-lactamases ESBL).
Приблизно 1/3 летальних наслідків трапляється упродовж першого тижня перебігу хвороби через розвиток системних ускладнень ГП і прогресування синдрому поліорганної дисфункції (СПОД). Наступні смертельні випадки (переважно через 2 тиж захворювання) пов’язані з місцевими ускладненнями, зокрема інфікуванням панкреатичних некрозів і розвитком на цьому тлі сепсису й СПОД.
У більшості хворих (70-80%) спостерігається легкий перебіг ГП, але у 20-30% пацієнтів захворювання триває тяжко, а летальні наслідки сягають 30-40% (S. Agarwal et al., 2016; C.C. Popa et al., 2016; X. Shen et al., 2016). Органна недостатність є провідним фактором визначення тяжкості і основною причиною ранньої смерті, тоді як вторинні інфекції (інфікований панкреонекроз і сепсис) є причиною більш пізніх смертельних випадків (P.A. Banks et al., 2013). Головними завданнями терапії при ГП є запобігання системним ускладненням захворювання та інфікуванню у разі розвитку некрозу. Поліпшення результатів лікування тяжкого ГП в останні роки пов’язане не так з удосконаленням техніки хірургічних втручань і проведенням інтенсивної терапії, як із розробленням раціональної стратегії ведення цих хворих. Дуже важливим моментом є розуміння того, що панкреонекроз, навіть інфікований, не є показанням до термінового хірургічного втручання.
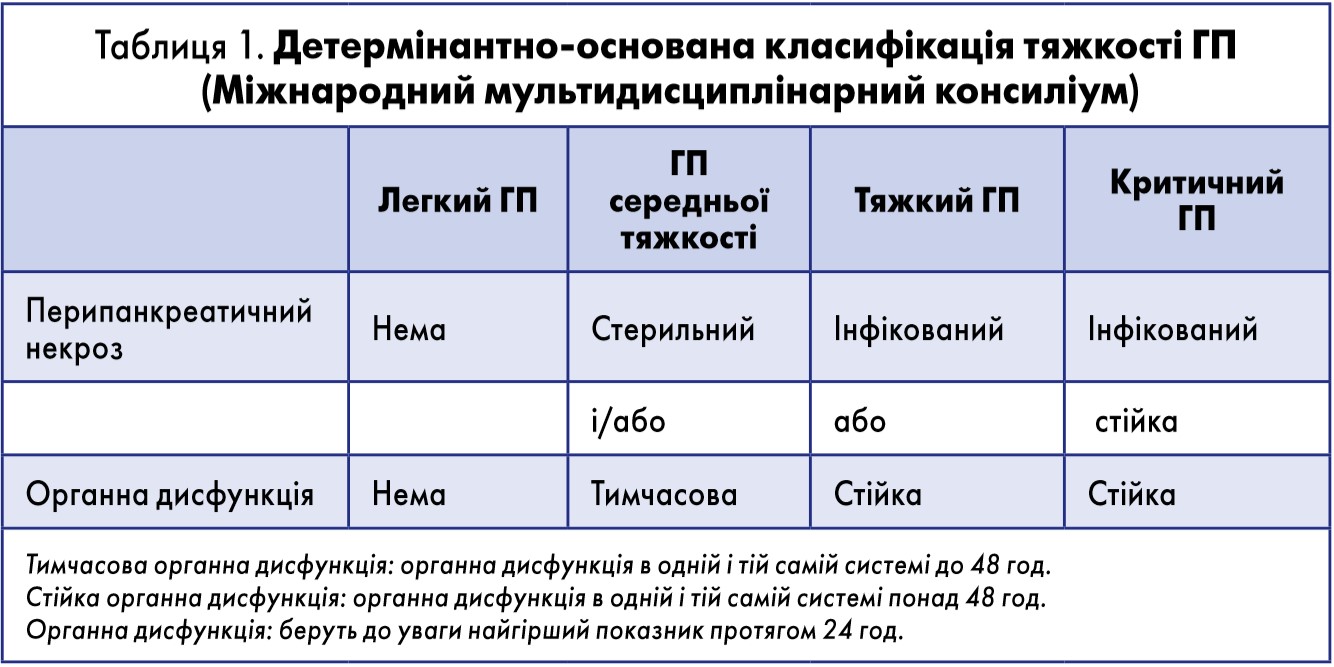
Протягом багатьох років учені намагаються удосконалити технологію діагностики та оцінювання тяжкості стану у хворих із ГП. На сьогодні запропоновано практичну й доступну для більшості лікувально-профілактичних закладів охорони здоров’я детермінантно-основану класифікацю тяжкості ГП (Міжнародний мультидисциплінарний консиліум, 2015) [6].
У зв’язку з тим що патофізіологічні механізми розвитку ГП остаточно не вивчені, лікування хворих на ГП нерідко має симптоматичний характер. Відповідно до міжнародних настанов призначення симптоматичної терапії передбачає інфузійну терапію, знеболення, антибіотики (АБ) за показаннями, лікування органної дисфункції (штучна вентиляція легень, гемофільтрація, кардіоциркуляційна підтримка тощо). Проте в різних країнах діють свої підходи, часто протилежні, до лікування хворих на ГП.
Волемічна ресусцитація досі викликає чимало дискусій на сторінках наукової літератури [2]. E.P. Rivers і співавт. у 2001 році в рейтинговому журналі N Eng J Med опублікували статтю, яку часто цитують різні автори і на основі якої було розроблено загальновідомий алгоритм волемічної та інотропної терапії хворих із сепсисом / септичним шоком. В основу цього алгоритму було покладено досягнення рівня центрального венозного тиску (ЦВТ) 8-12 мм рт. ст. Вважаємо, що оптимальними орієнтирами адекватно проведеної інфузійної терапії є середній артеріальний тиск (серАТ) >65-70 мм рт. ст. і темп сечовиділення >0,5- 1 мл/ кг/ год. Показник ЦВТ відображає внутрішньосудинний тиск. На нашу думку, зміни показника ЦВТ у динаміці дають лікарю інформацію про необхідний темп інфузійної терапії для конкретного хворого. J.H. Boyd і співавт. (2011) зазначають, що ЦВТ у хворих із септичним шоком корелювало з водним балансом лише в перші 12 год інфузійної терапії. У наступні 4 дні позитивний водний баланс, який ґрунтувався на ЦВТ, був пов’язаний із ризиком збільшення летальності. У зв’язку з цим автор робить висновок, що ЦВТ можна використовувати для контролю інфузійної терапії тільки в перші 12 год. P.E. Marik і співавт. на підставі аналізу великого метааналізу дійшли висновку, що моніторинг ЦВТ не може передбачити відповідь на волемічне навантаження при проведенні ІнфТ, тому для цього в клініці недоцільно використовувати ЦВТ, а M. Cessoni і співавт. (2011) акцентують на тому, що АТ, ЦВТ і темп сечовиділення є грубими індикаторами гемодинамічного статусу.
Золотим стандартом для моніторингу відповіді на ІнфТ є постійне вимірювання серцевого викиду [6-8].
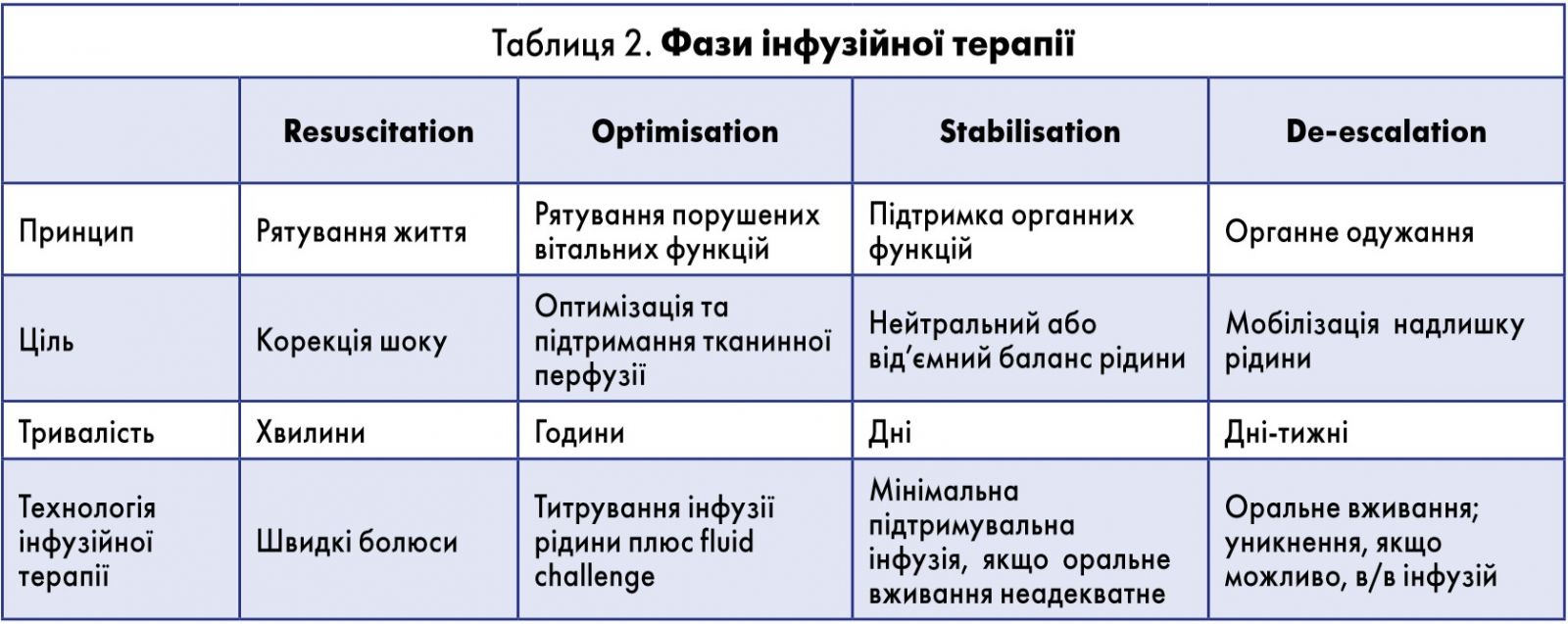
J.L. Vincent, D. de Backer (2013) у своїй статті Circulatory shock, опублікованій у журналі N Engl J Med, виділяють кілька етапів інфузійної терапії та визначають її цілі на кожному етапі. Наприклад, на етапі «волемічної ресусцитації» основною метою є корекція шоку та рятування життя. Тривалість цього етапу, як правило, оцінюється хвилинами; інфузійну терапію проводять болюсним введенням рідини.
На етапі «оптимізації» протягом декількох годин необхідно забезпечити тканинну перфузію шляхом титрування інфузії рідини плюс fluid challenge. А у фазі «стабілізації» забезпечують нейтральний або від’ємний баланс рідини шляхом мінімальної підтримувальної інфузії, якщо неможливий оральний прийом рідини. Надалі (de-escalation) необхідне виведення з організму надміру рідини та проведення нутрітивної терапії (табл. 2).
На етапі resuscitation у хворих із септичним шоком інфузійну терапію ми проводили за ліберальною технологією. Пацієнтам вводили кристалоїдні розчини у дозі 25-30 мл/кг маси тіла (МТ), а при серАТ <70 мм рт. ст. додавали інотропні препарати. На етапі «оптимізації» інфузійну терапію проводили за рестриктивною технологією (1-1,5 мл/кг МТ), а її адекватність контролювали темпом сечовиділення пацієнтки. Слід ураховувати, що протягом 3 діб у хворих на ГП в організмі можуть накопичуватися до 6-12 л рідини і 600-1200 ммоль Na+ (М.Ш. Хубутия, 2014). Це призведе до перевантаження інтерстиціального простору й сприятиме розвиткові респіраторного дистрес-синдрому, інтраабдомінального компартмен-синдрому, набряку/набухання головного мозку.
Сьогодні стартовими розчинами для волемічної реанімації розглядають кристалоїди [4], серед найважливіших характеристик яких – ступінь збалансованості та наявність носіїв резервної лужності. З огляду на те що у процесі перебігу токсико-септичного шоку виникає артеріоло-венулярне шунтування крові (небезпека виникнення лактацидозу), з-поміж кристалоїдів препаратами вибору є розчини, у яких носієм резервної лужності є ацетат. Слід зауважити, що реакція перетворення в печінці лактату в бікарбонат потребує великої кількості кисню, що сприяє тканинній гіпоксії, яка, у свою чергу, супроводжує всі критичні стани. Тому препарати, у яких носієм резервної лужності є лактат, слід обережно застосовувати практично при всіх критичих станах. Ацетат і малат перетворюються в бікарбонат у клітинах всіх тканин організму, що особливо важливо у хворих із гострим пошкодженням печінки. І ацетат, і малат метаболізуються в еквівалентну кількість бікарбонату (1 моль ацетату = 1 молю гідрокарбонату, 1 моль малату = 2 молям гідрокарбонату) протягом 1-1,5 годин. Для перетворення малату й ацетату в бікарбонат необхідно в 1,5-2 рази менше кисню, ніж для аналогічної реакції лактату, а для критичних хворих – це вкрай важливий момент, оскільки гіпоксія – універсальний фактор, що сприяє поглибленню мультиорганної дисфункції.
Крім того, слід ураховувати, що малат – це субстрат орнітинового циклу синтезу сечовини, який залучається до зв’язування аміаку в м’язах, що поліпшує детоксикаційну функцію печінки. Лактат також сприяє виникненню інтерстиційного набряку головного мозку, підвищує агрегацію тромбоцитів та еритроцитів.
Недоліком усіх кристалоїдів є низький волемічний ефект і невеликий період їх перебування в судинному руслі. Для «затримки» рідини в ньому було застосовано гідроксиетил крохмаль (ГЕК) у дозі не більш як 5-10 мл/кг МТ. В настанові Surviving Sepsis Campaign: International Guidelines for Management of Sepsis and Septic Shock’ 2016 відсутні рекомендації щодо застосування препаратів ГЕК (але й не забороняється їх призначення!). Тому ми використовували ГЕК у хворих на ГП на тлі попередньо застосованих кристалоїдів.
Препаратами вибору ми вважаємо ГЕКи з молекулярною масою 130 кДа і ступенем молярного заміщення – 0,4-0,42. Доза ГЕКів, на нашу думку, не має перевищувати 5-10 мг/кг/добу.
При гіповолемії, крім кристалоїдів і препаратів ГЕК, ми використовували препарати желатини. Вони майже не справляють негативного впливу на систему гемостазу, їх можна застосовувати у хворих з ознаками синдрому дисемінованого внутрішньосудинного зсідання крові, тромбоцитопенією та тромботичною мікроангіопатією.
Комбінуючи застосування кристалоїдів, препаратів ГЕК і препаратів желатини, ми намагалися якомога швидше ліквідувати ознаки гіповелемії, збільшити серцевий викид і, як наслідок, відновити адекватну перфузію всіх органів та систем. Комбінація кристалоїдів, ГЕКів і препаратів желатини забезпечувала зменшення сумарного об’єму інфузійної терапії, затримку рідини у внутрішньосудинному руслі, зменшення інтерстиційних набряків.
Особливу увагу було приділено осмолярності та рівню Na+ плазми крові(!). За наявності гіпернатріємії >24 год доцільно зменшувати його рівень зі швидкістю не більш як 0,5-1 ммоль/л/год (у середньому 8-10 ммоль/л/24 год) (!!!) залежно від тривалості гіпернатріємії у плазмі крові хворого. В протилежному випадку існує небезпека посилити набряк/набухання клітин головного мозку! При корекції гіпонатріємії слід звертати увагу на те, щоб рівень натрію у плазмі крові зростав не більш як на 0,5-1 ммоль/л/год.
Швидкість внутрішньовенного введення калію не має перевищувати 10-20 ммоль/год. Якщо у хворого спостерігаються значні втрати калію через шлунково-кишковий тракт (ШКТ), за відсутності можливості лабораторного визначення концентрації калію у сироватці крові його добову потребу можна розрахувати за такою формулою (для країн з обмеженими економічними ресурсами не така вже й рідкість):
ДП калію (ммоль/л) = (30 + 15 × об’єм втрат, л) × 2, де 30 – середня величина екстракції калію із сечею (ммоль); 15 – середня концентрація калію у секретах ШКТ (ммоль/л).
При лікуванні хворих на ГП необхідно звертати особливу увагу на концентрацію фосфору – головного аніону внутрішньоклітинної рідини. Слід зауважити, що концентрація фосфору в плазмі крові не завжди корелює з такими його змінами в клітині. Фосфор є важливою складовою тканин організму та бере активну участь у його функціонуванні. Він залучається до утворення макроергічних сполук (АТФ, 2,3-ДФГ), які сприяють постачанню О2 у клітини, бере участь у метаболізмі білків, жирів та вуглеводів і впливає на кислотно-лужний стан (КЛС). Гіпофосфатемія виникає при респіраторному алкалозі, застосуванні глюкози та інсуліну, оскільки РО43– входить усередину клітини.
Гіпофосфатемія (фосфор сироватки крові <0,8ммоль/л) може бути результатом переходу фосфору у внутрішньоклітинний простір, підвищення його втрати із сечею, зменшення реабсорбції в ШКТ або підвищеного його споживання клітинами. Гіпофосфатемія легкого та середнього ступеня тяжкості (0,4-0,8 ммоль/л) у більшості випадків перебігає безсимптомно, а тяжка гіпофосфатемія (0,3-0,4 ммоль/л) може призвести до летального наслідку у зв’язку з апоптозом клітини.
Наразі для корекції гіпофосфатемії в Україні на фармацевтичному ринку представлений єдиний лікарський засіб – езафосфіна. Препарат поляризує мембрани, полегшуючи входження в клітину К+, виводить Nа+ і блокує вхід Са2+, стимулює процес насичення тканин О2 за рахунок збільшення утворення 2,3-ДФГ в еритроцитах, підвищує стійкість еритроцитів до гемолізу, поліпшує обмін глюкози за інсуліннезалежним механізмом, стимулює фосфофруктокіназу й прискорює синтез дифосфату фруктози зі збільшенням аденильного пулу.
Слід зауважити, що сучасні препарати для парентерального та ентерального харчування містять фосфор, але вищезазначений препарат (езафосфіна) містить його добову потребу, що необхідна людині. У разі дефіциту фосфору його коригують езафосфіною. Разом із тим не слід забувати, що у хворих на ниркову дисфункцію (здебільшого хронічну), в організмі виникає гіперфосфатемія, оскільки процес виведення фосфору нирками у таких хворих обмежений.
Ознаками відновлення об’єму циркулюючої крові та забезпечення перфузії периферичних органів є відновлення темпу сечовиділення >0,5-1 мл/кг/год; зменшення часу наповнення капілярного ложа нігтя <2 с; зниження лактату крові до 2-2,5 ммоль/л.
Агресивну інфузійну терапію проводять протягом 3-6 год, надалі розглядають необхідність застосування нутрітивної терапії. Порушення білкового обміну при тяжких формах панкреатиту виникає вже через 2-6 год розвитку захворювання (М.Ш. Хубутия, 2014). За даними літературних джерел, хворі на ГП за добу втрачають 14-17 г азоту, що еквівалентно 90-105 г білка/24 год (втрата МТ 420-510 г/ добу).
За необхідності проведення інотропної терапії, але без наростання доз інотропних препаратів (оптимально при їхньому зменшенні) та швидкості зникнення білої плями нігтьового ложа <2 с, ми також розпочинали нутрітивну терапію.
Під час проведення адекватної нутрітивної терапії виникає проблема визначення кількості кілокалорій, необхідних конкретному хворому (ми не маємо змоги проведення непрямої калориметрії з визначенням респіраторного коефіцієнта: RQ=VCO2/VO2). Для оптимізації нутрітивної терапії можна використовувати технологію визначення енергетичної потреби на основі розрахунку необхідної кількості нутрієнтів, яка наведена в таблиці 3.
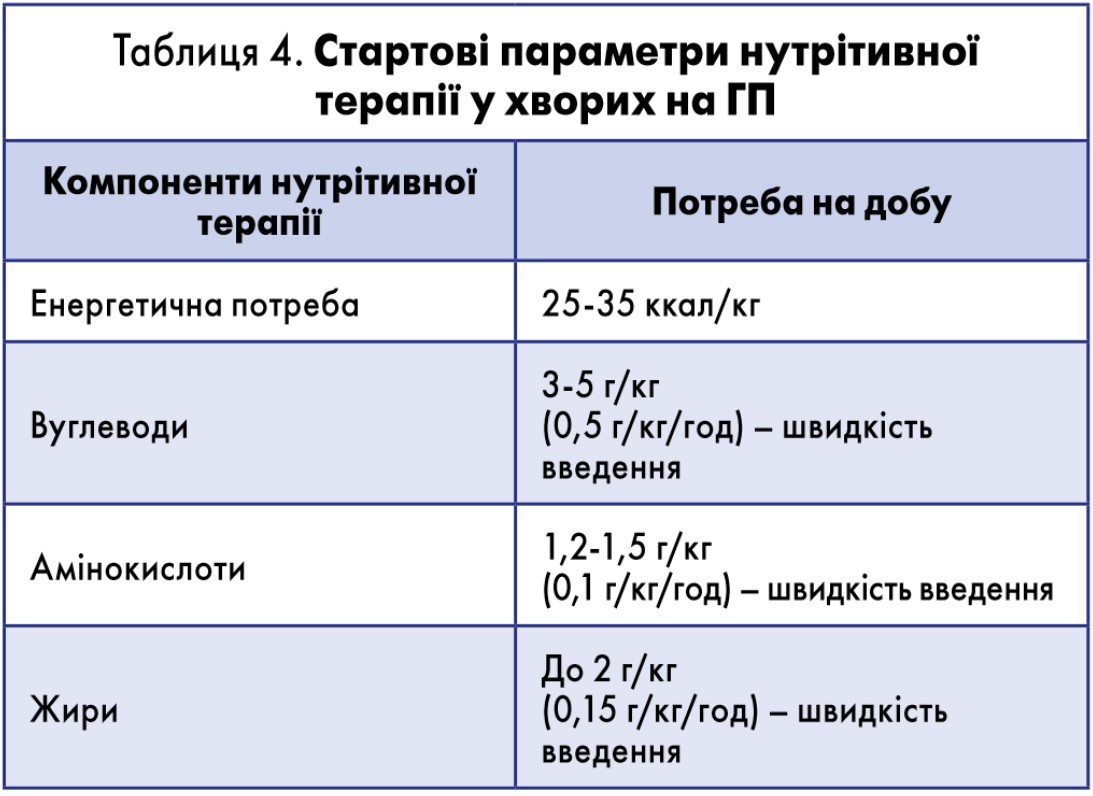
Стартовими параметрами нутрітивної терапії були показники, наведені в таблиці 4.
Наразі точаться дискусії щодо застосування антипротеазних і антисекреторних препаратів при лікуванні хворих на ГП. Упродовж багатьох років при цьому широко застосовують апротинін (контрикал). Однак клінічні дослідження показали, що застосування препарату жодним чином не впливає на результати лікування цих хворих.
Октреотид – синтетичний аналог соматостатину, який інгібує продукування ензимів ПЗ. Механізм дії препарату зумовлений зниженням захоплення ацинарними клітинами ПЗ амінокислот із плазми. Це, у свою чергу, призводить до зменшення синтезу панкреатичних ферментів. Пригнічення активності ацинарних клітин і зниження акумуляції в них ферментів, що супроводжується пригніченням базальної та стимульованої панкреатичної секреції і виділення секретину й холецистокініну. На жаль, результати клінічних досліджень доволі неоднозначні. Разом із позитивними відгуками повідомляється про повну відсутність будь-якого ефекту. Слід зауважити, що застосування октреотиту призводить до вазоконстрикції судин черевної порожнини (Б.Р. Генфальд і співавт., 1998).
Антагоністи Н2-гістамінових рецепторів і блокатори протонної помпи зменшують вивільнення секретину дванадцятипалою кишкою, що сприяє забезпеченню функціонального спокою ПЗ. Водночас препарати підвищують рН шлунка, тим самим провокуючи транслокацію бактерій із дистального відділу кишок у проксимальний, а звідти – у легені, викликаючи нозокоміальну пневмонію у хворих на ГП.
Улінастатин (Ю-Тріп) – це інгібітор серинових протеїназ. Препарат зменшує загальну відповідь організму на запалення. Застосовується для лікування сепсису, панкреатиту (Yu-Xin Leng et al., 2014). Улінастатин – полівалентний інгібітор протеази серину типу Кунітц, інгібує маркери запалення (СРП, TNF-α та інших прозапальних інтерлейкінів), трипсин, підшлункову, поліморфонуклеарну та лейкоцитарну еластази. Важливо, що улінастатин інгібує коагуляцію та фібриноліз, адже відомо, що запалення та гіперкоагуляція – це дві взаємозв’язані ланки одного і того самого патологічного процесу. За даними різних авторів, препарат пригнічує протеази серину (трипсин, хімотрипсин калікреїн, еластазу, катепсин) і фактори коагуляції та фібринолізу (тромбін, плазмін, Ха, ХІа та ХІІа, плазмін).
Улінастатин справляє локалізований протизапальний ефект і пригнічує протеолітичну дію трипсину на низку тканин, насамперед на тканину ПЗ. У клініці анестезіології та інтенсивної терапії Львівського національного медичного університету ми використовували препарат у дозі 100 тис. ОД розведеного в 100 мл 0,9% розчині NaCl. Клінічно був отриманий гарний ефект, але у зв’язку з невеликою кількістю хворих, які отримували терапію улінастатином, робити якісь узагальнювальні висновки завчасно. На нашу думку, вкрай важливим є позитивний вплив улінастатину на коагуляцію і фібриноліз у цієї категорії хворих.
Актуальним питанням лікування хворих на ГП є аналгоседація. З метою забезпечення адекватного знеболення пацієнтів ми віддаємо перевагу комбінованій технології: пролонгована епідуральна аналгезія + наркотичні аналгетики (бажано пролонговим шляхом введення) + нестероїдні протизапальні препарати.
З огляду на літературні джерела у понад 80% випадків збудниками інфікування ГП є бактерії з родини Enterobacteriaceae (E. coli – 45%, K. pneumoniae – 17%). У нашому випадку E. coli виділяли у 40%, K. pneumoniae – у 23% досліджень. Зважаючи на те що продукція ESBL була виявлена у 21% позалікарняних і 59% нозокоміальних штамів бактерій із родини Enterobacteriaceae, стартовим антибактеріальним препаратом можна вважати Ертапенем, який не володіє антисинегнійною активністю, проте активно діє як на мікроорганізми родини Enterobacteriaceae, так і на Г(+) мікроорганізми.
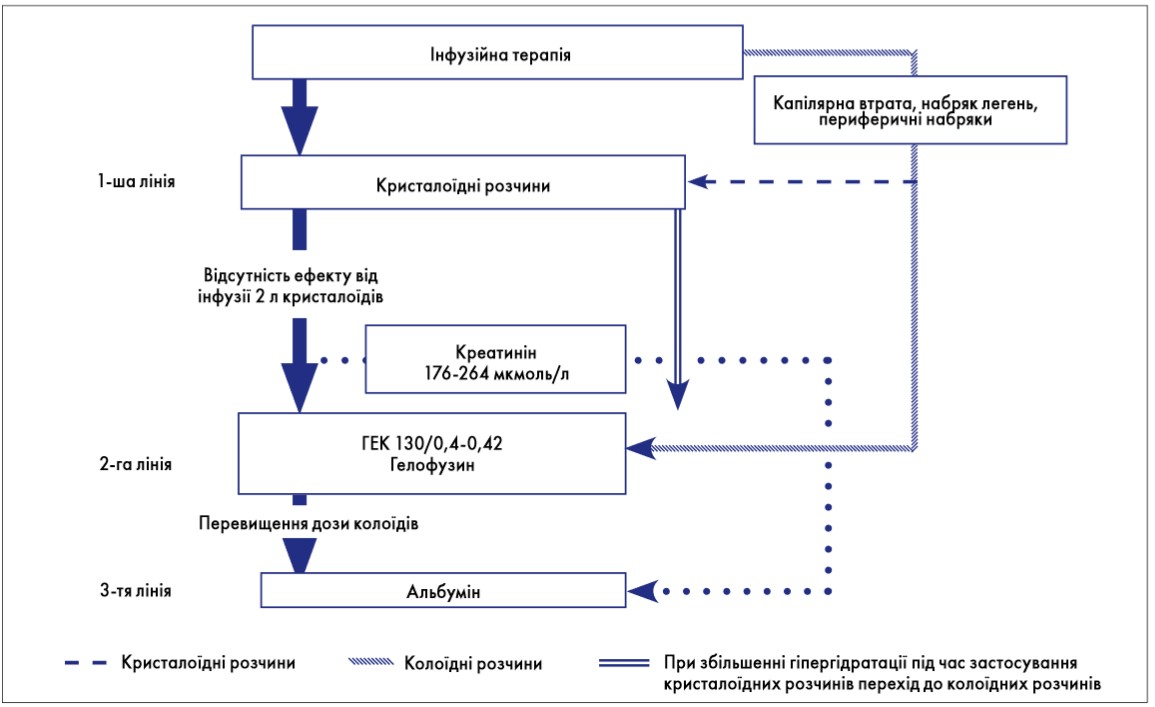
Рис. Алгоритм інфузійної терапії у хворих на ГП
Показаннями до початку антибактеріальної терапії у хворих на ГП може бути зростання рівня С- реактивного білка як індикатора гострої фази запального процесу (>5 мг/л) і прокальцитоніну (>0,5-1,0 нг/мл) у плазмі крові.
Дослідження останніх років продемонстрували, що збільшення концентрації прокальцитоніну (попередника кальцитоніну) в крові <1,8 нг/мл у двох послідовних дослідженнях – важливий лабораторний маркер бактеріального інфікування вогнищ некротичної деструкції.
Маємо дані про те, що його рівень корелює із тяжкістю ГП і вираженістю поліорганних порушень. Для підтвердження інфікування також використовують пункцію вогнищ під контролем ультрасонографії з наступним бактеріоскопічним і бактеріологічним дослідженнями.
 В останні роки зростає кількість наукових робіт, автори яких висвітлюють значення для діагностики інфікованого панкреонекрозу черезшкірної тонкоголкової аспірації під контролем ультразвукового дослідження, УЗД (В.Т. Зайцев і співавт., 1999; M.N. Schoenberg et al., 1999), хоч і зазначається, що цей метод має дещо меншу чутливість і специфічність (88 і 90% відповідно) порівняно з комп’ютерною томографією (КТ).
В останні роки зростає кількість наукових робіт, автори яких висвітлюють значення для діагностики інфікованого панкреонекрозу черезшкірної тонкоголкової аспірації під контролем ультразвукового дослідження, УЗД (В.Т. Зайцев і співавт., 1999; M.N. Schoenberg et al., 1999), хоч і зазначається, що цей метод має дещо меншу чутливість і специфічність (88 і 90% відповідно) порівняно з комп’ютерною томографією (КТ).
Однією з переваг УЗД вважають можливість його багаторазового виконання біля «ліжка хворого» (УЗД-моніторинг) (О.Е. Бобров, 2000; Б.С. Запорожченко і співавт., 2001; B. Rau et al., 1998).
Крім того, чутливим діагностичним тестом для виявлення інфікування є виявлення повітря в зоні некрозів при КТ. Для поліпшення результатів хірургічного лікування до операції проводять 3D-реконструкцію зображень, отриманих при КТ.
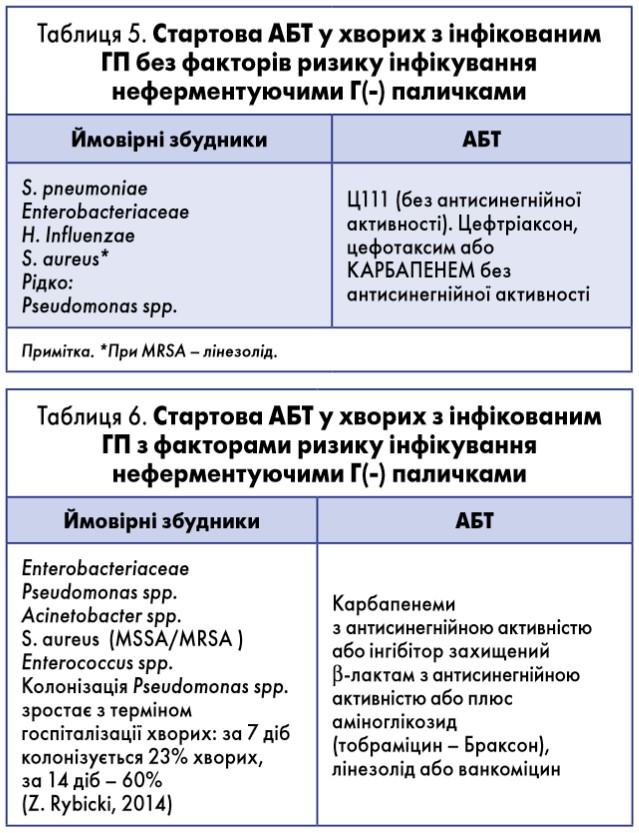
Орієнтовні схеми емпіричної АБТ подані в таблицях 5 і 6.
Операційні втручання бажано виконувати не раніше другого-третього тижня захворювання – у цей період найчастіше відбувається інфікування некротичних вогнищ і демаркація ділянок некрозу.
Отже, лікування хворих на ГП потребує застосування мультидисциплінарного підходу із залученням анестезіологів, хірургів, бактеріологів, радіологів та інших спеціалістів, і рішення кожного з них має бути пріоритетним на певному етапі терапії.
Список літератури знаходиться в редакції.