26 лютого, 2018
Диагностика и лечение железодефицитной анемии у пациентов с воспалительными заболеваниями кишечника и желудочно-кишечным кровотечением
Введение
Железодефицитная анемия (ЖДА) представляет собой проблему первостепенной важности для гастроэнтерологов в связи с ее высокой распространенностью в гастроэнтерологической практике. Желудочно-кишечное кровотечение (ЖКК), как явное, так и скрытое, – самая распространенная причина ЖДА у взрослых; для его диагностики, как правило, необходимо эндоскопическое обследование. Патология ЖКТ и скрытое кровотечение могут привести к ежедневной потере 1-2 мг железа. Существует множество возможных причин ЖКК, в том числе: варикозно расширенные вены пищевода, пептическая язва, гастрит, полипы, ангиодисплазия, дивертикулярная болезнь, воспалительные заболевания кишечника (ВЗК), геморрой, анальная трещина, рак. ВЗК (болезнь Крона (БК), язвенный колит (ЯК) представляют собой хронические заболевания, их течение характеризуется периодами ремиссии и обострения. ЖДА в зависимости от разных факторов развивается у 17-76% больных ВЗК и, как правило, манифестирует внекишечными проявлениями, а также различными клиническими осложнениями. ЖДА ассоциируется со снижением качества жизни, частыми госпитализациями, ростом смертности. Кроме того, она увеличивает вероятность аллогенного переливания крови у стационарных больных и возникновения различных нежелательных явлений и исходов, обусловленных трансфузией крови. Для пациентов с ВЗК и ЖКК решающее значение имеют точность диагностики и адекватность лечения ЖДА.
Рекомендация
- Пациентов с ВЗК и ЖКК следует обследовать для выявления дефицита железа и ЖДА
Анемия при ВЗК
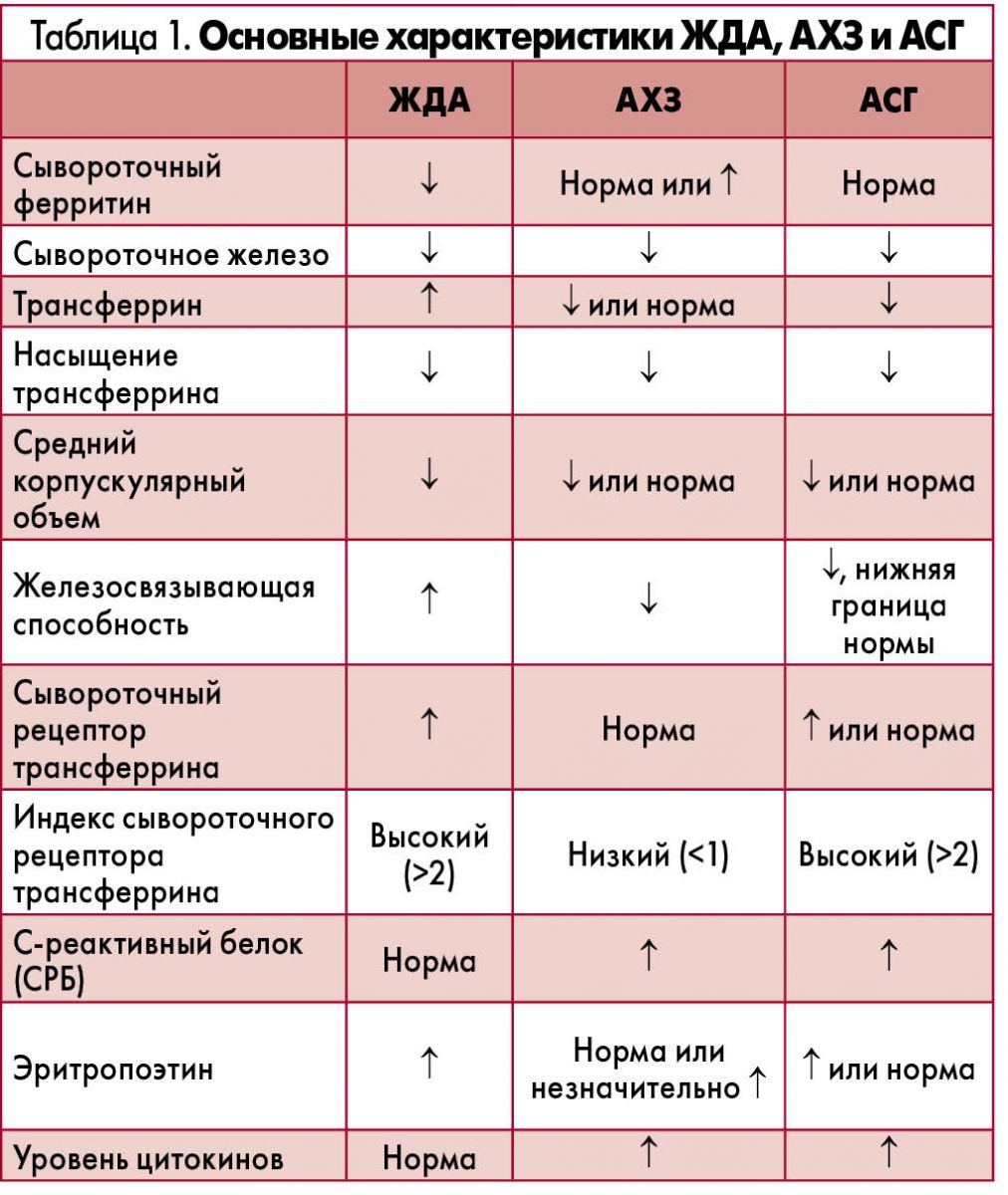
К основным видам гипохромных микроцитарных анемий, встречающихся при ВЗК, относят ЖДА, анемию хронического заболевания (АХЗ) и анемию смешанного генеза (АСГ). Также могут диагностироваться макроцитарные анемии, обусловленные дефицитом кобаламина и фолиевой кислоты. Несмотря на то что значимость анемии у больных ВЗК обусловлена высокой распространенностью, ее часто недооценивают и неадекватно лечат. Различные исследования показали, что анемия широко распространена при ВЗК. Hoivik и соавт. провели популяционное исследование (n=756; из них 237 пациентов страдали БК, 519 – ЯК) и сообщили, что на момент диагностики основного заболевания 48,8% больных БК и 20,2% пациентов с ЯК имели признаки анемии. В другом популяционном исследовании (n=749) Sjoberg и соавт. продемонстрировали, что распространенность анемии у больных ВЗК на момент подтверждения диагноза составляет 30% (БК – 42%; ЯК – 24%). По данным одноцентрового когортного исследования, выполненного Toruner и соавт., распространенность анемии у больных ВЗК (n=398; из них 188 – БК и 212 – ЯК) составляет 22% при ЯК и 24% при БК.
Анемия при ЖКК
ЖКК является распространенной медицинской проблемой, которая может возникать остро при неотложных состояниях и иногда при хронических заболеваниях. В таких случаях ЖДА представляет собой потенциально сложную задачу. Bager и соавт. провели ретроспективную оценку историй больных, госпитализированных по поводу острого кровотечения из верхних отделов ЖКТ. В этом исследовании представлен ретроспективный анализ данных 169 пациентов. Распространенность анемии у больных, выписывающихся из стационара, составила 82%. Из них только 16% получили рекомендацию принимать препараты железа после выписки. У пациентов с частыми рецидивами ЖКК, которые наблюдаются при ВЗК, следует регулярно оценивать сывороточную концентрацию железа после остановки кровотечения, потому что ЖКК может привести к истощению его запасов в организме.
Клиника и диагностика анемии при ВЗК и ЖКК
 Клинические проявления анемии включают усталость, головную боль, головокружение, тахикардию, одышку, снижение либидо, тошноту, шум в ушах, снижение массы тела, нарушение способности к самопроизвольному движению, летаргию, обмороки; пациенты также могут не иметь признаков заболевания или отмечать минимальные клинические проявления. Дефицит железа сам по себе, еще до развития анемии, может вызывать аналогичные проявления или протекать бессимптомно.
Клинические проявления анемии включают усталость, головную боль, головокружение, тахикардию, одышку, снижение либидо, тошноту, шум в ушах, снижение массы тела, нарушение способности к самопроизвольному движению, летаргию, обмороки; пациенты также могут не иметь признаков заболевания или отмечать минимальные клинические проявления. Дефицит железа сам по себе, еще до развития анемии, может вызывать аналогичные проявления или протекать бессимптомно.
Danese и соавт. использовали онлайн-опросник для анализа врачебных назначений, сделанных больным ВЗК по поводу анемии; анкету заполнил 631 пациент. Большая часть из них страдали анемией и полагали, что последняя при ВЗК обусловлена потерей крови, недостатком железа, воспалительным процессом. Основными симптомами, которые отметили большинство пациентов, являлись усталость и слабость.
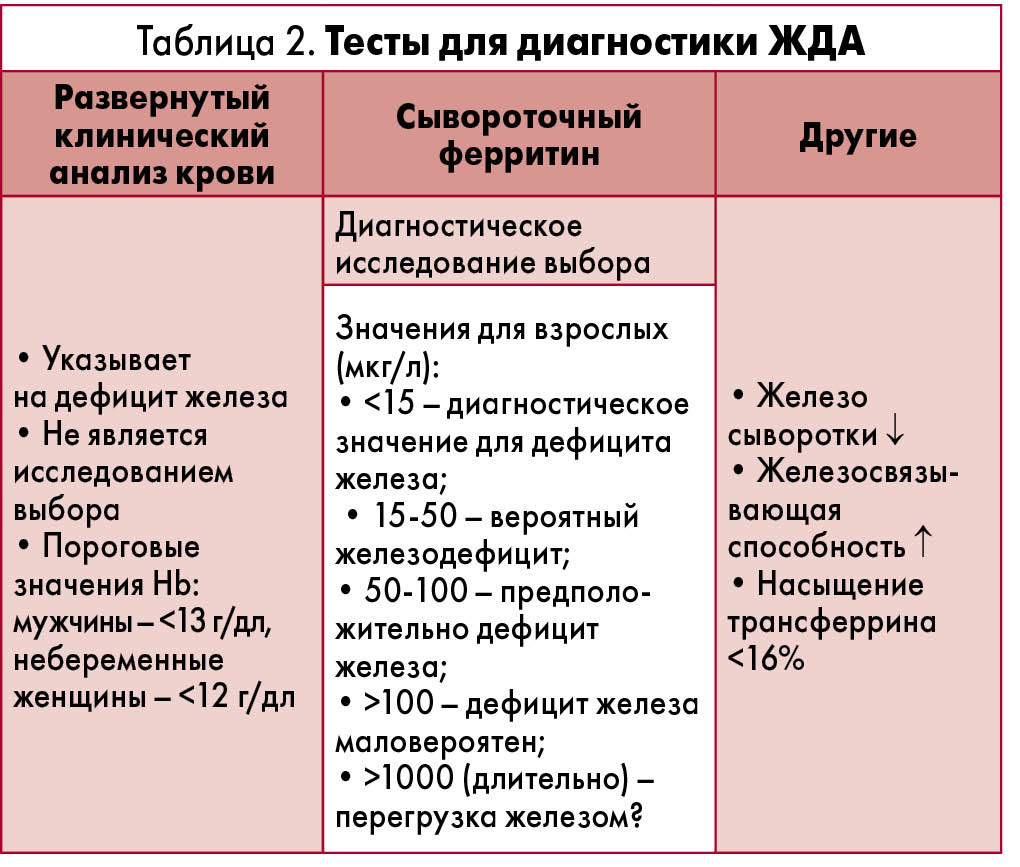 Всемирная организация здравоохранения определяет анемию как снижение уровня гемоглобина (Hb) <13 г/дл и 12 г/дл у мужчин и небеременных женщин соответственно. Несмотря на это, следует проводить тщательный дифференциальный диагноз и использовать необходимые диагностические исследования для подтверждения анемии (табл. 1, 2).
Всемирная организация здравоохранения определяет анемию как снижение уровня гемоглобина (Hb) <13 г/дл и 12 г/дл у мужчин и небеременных женщин соответственно. Несмотря на это, следует проводить тщательный дифференциальный диагноз и использовать необходимые диагностические исследования для подтверждения анемии (табл. 1, 2).
При обычных обстоятельствах сывороточная концентрация ферритина <15 мкг/л считается индикатором дефицита железа. С другой стороны, сывороточный ферритин является белком острой фазы, поэтому существует значимая корреляция между диагностическими значениями и уровнем воспаления при дефиците железа. 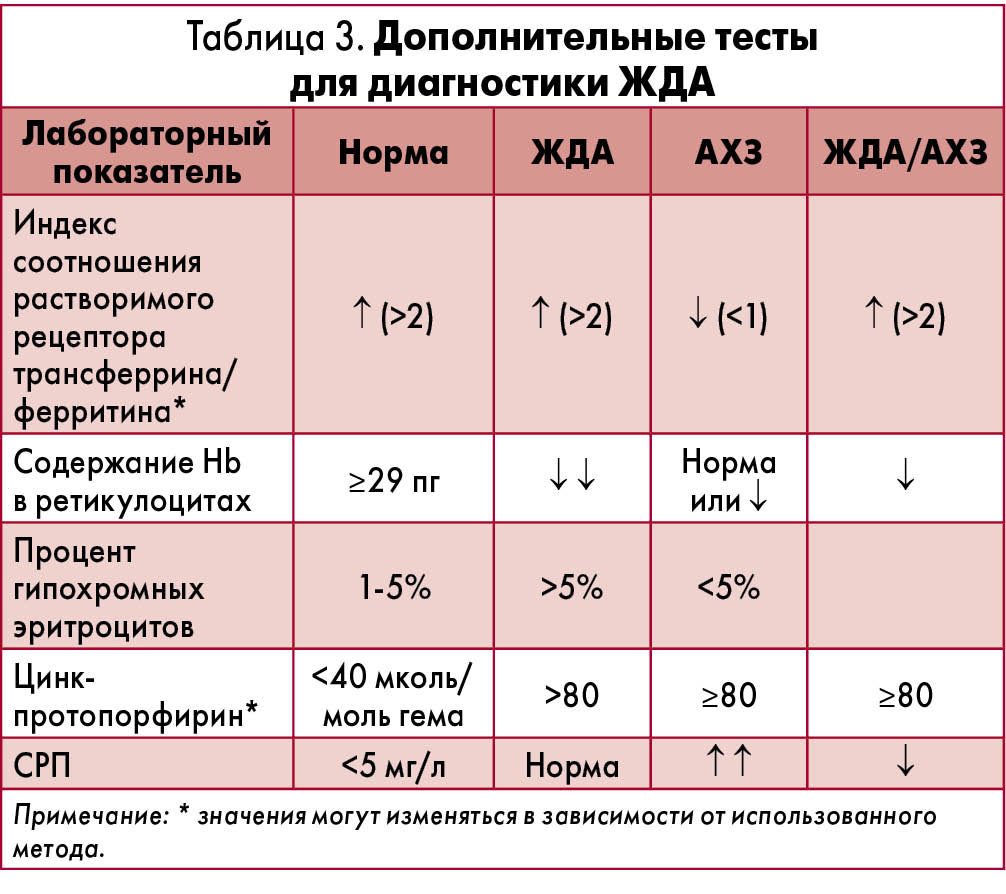 У пациентов, не имеющих признаков активности заболевания, концентрацию сывороточного ферритина <30 мкг/л можно считать соответствующим критерием. При наличии воспаления нельзя исключить вероятность дефицита железа при уровне ферритина в сыворотке крови >100 мкг/л. Вместе с тем трансферрин и железосвязывающая способность также являются ненадежными показателями, поскольку воспаление оказывает на них значительное влияние. При таком заболевании, как ВЗК, может потребоваться более тщательное лабораторное обследование для подтверждения ЖДА, в т. ч. определение содержания Hb в ретикулоцитах, процента гипохромных эритроцитов, индекса насыщения трансферрина, цинк-протопорфирина, но эти исследования не получили пока широкого распространения (табл. 3). Поэтому в сомнительных случаях рекомендуется направить пациента к гематологу для получения экспертной оценки.
У пациентов, не имеющих признаков активности заболевания, концентрацию сывороточного ферритина <30 мкг/л можно считать соответствующим критерием. При наличии воспаления нельзя исключить вероятность дефицита железа при уровне ферритина в сыворотке крови >100 мкг/л. Вместе с тем трансферрин и железосвязывающая способность также являются ненадежными показателями, поскольку воспаление оказывает на них значительное влияние. При таком заболевании, как ВЗК, может потребоваться более тщательное лабораторное обследование для подтверждения ЖДА, в т. ч. определение содержания Hb в ретикулоцитах, процента гипохромных эритроцитов, индекса насыщения трансферрина, цинк-протопорфирина, но эти исследования не получили пока широкого распространения (табл. 3). Поэтому в сомнительных случаях рекомендуется направить пациента к гематологу для получения экспертной оценки.
Лечение анемии, обусловленной ВЗК и ЖКК
Несмотря на то что ЖДА может быть следствием активного ВЗК, лечение основного заболевания не всегда приводит к нивелированию ЖДА, которая остается чрезвычайно распространенной. Именно поэтому необходимо непосредственно лечить ЖДА.
Рекомендации
- Диагноз ЖДА следует подтвердить различными диагностическими исследованиями перед назначением лечения
- Направить пациента к гематологу, если генез анемии остается неясным, несмотря на проведенные исследования
Цель дополнительного приема железа при ЖДА заключается в повышении уровня Hb (>2 г/дл), достижении нормативных значений Hb через 4 нед, увеличении концентрации ферритина (насыщение трансферрина >30%), уменьшении клинических проявлений анемии и, следовательно, повышении качества жизни.
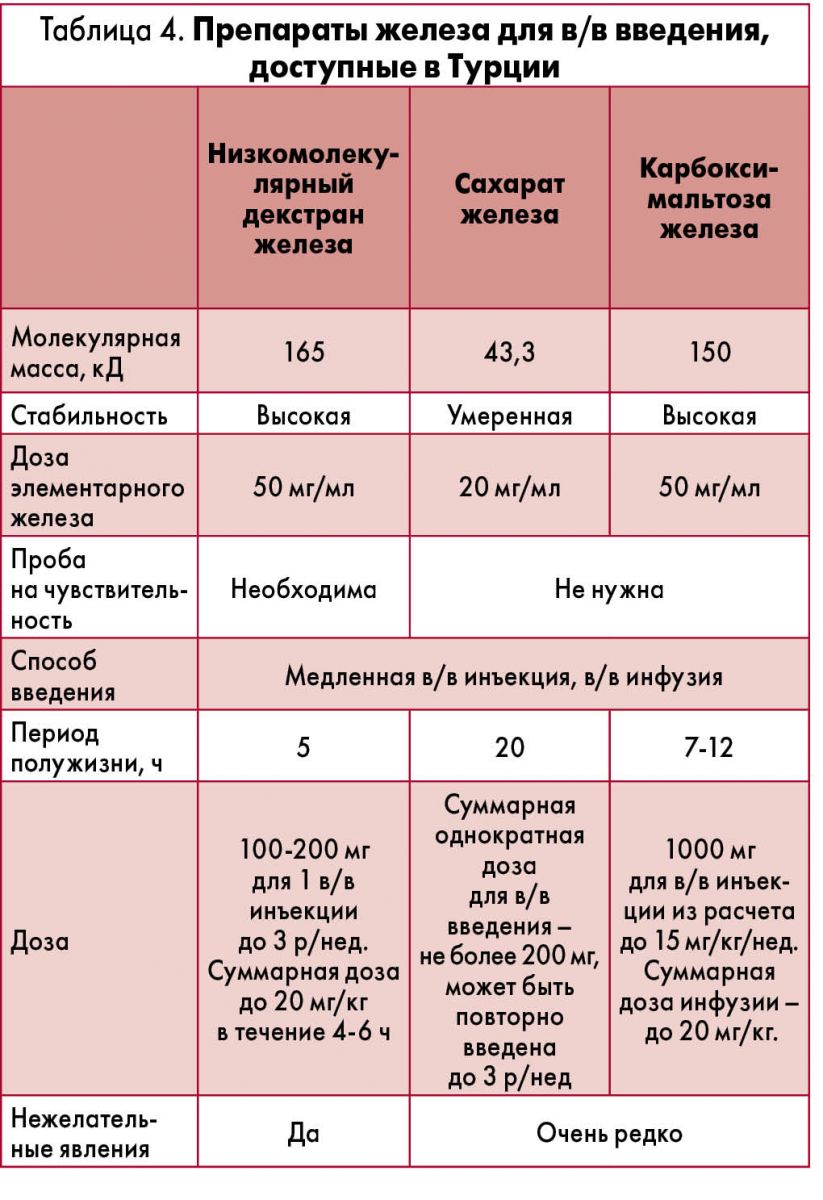 Существует два способа введения железа: пероральный и внутривенный (в/в). Пероральный прием является общепринятым способом лечения ЖДА; при этом он характеризуется появлением нежелательных явлений со стороны ЖКТ, низкой приверженностью к лечению и недостаточной эффективностью. В некоторых случаях, вероятно, пероральный прием железа может спровоцировать обострение заболевания за счет образования активных форм кислорода. Однако применение в/в форм железа все еще вызывает обеспокоенность у многих врачей, несмотря на появление в/в препаратов железа нового поколения с улучшенным профилем безопасности и существующие практические рекомендации (табл. 4).
Существует два способа введения железа: пероральный и внутривенный (в/в). Пероральный прием является общепринятым способом лечения ЖДА; при этом он характеризуется появлением нежелательных явлений со стороны ЖКТ, низкой приверженностью к лечению и недостаточной эффективностью. В некоторых случаях, вероятно, пероральный прием железа может спровоцировать обострение заболевания за счет образования активных форм кислорода. Однако применение в/в форм железа все еще вызывает обеспокоенность у многих врачей, несмотря на появление в/в препаратов железа нового поколения с улучшенным профилем безопасности и существующие практические рекомендации (табл. 4).
В настоящее время существует два подхода к лечению ЖДА при ВЗК:
1. Пероральный прием препаратов железа, если:
- у пациента имеет место ЖДА легкой/среднетяжелой степени тяжести (Hb >10 г/дл);
- основное заболевание находится в неактивной фазе (СРБ <5 мг/л);
- наблюдаются хорошая переносимость, высокая приверженность и достаточная эффективность (прирост Hb составляет >2 г/дл спустя 4 нед).
2. Начало в/в введения железа, несмотря на уровни Hb и СРП.
В недавно опубликованном метаанализе, выполненном Bonovas и соавт., обобщены данные рандомизированных контролированных исследований (РКИ), показавших, что в/в введение железа быстрее повышает уровень Hb (≥2,0 г/дл) и лучше переносится по сравнению с пероральными препаратами железа при ВЗК. В другом метаанализе, представленном Tolkien и соавт., пероральный препарат железа (железа сульфат) чаще провоцировал появление значимых нежелательных явлений со стороны ЖКТ у взрослых по сравнению с плацебо или в/в введением железа. Результаты открытого многоцентрового РКИ продемонстрировали, что сахарат железа, предназначенный для в/в введения, имеет лучший гастроинтестинальный профиль безопасности, чем пероральный сульфат железа; 5 (20,8%) пациентов, рандомизированных для перорального приема, и 1 (4,5%) больной, получавший в/в лечение, прервали терапию в связи с появлением нежелательных явлений со стороны ЖКТ. Кроме того, только в/в введение железа способствовало росту сывороточной концентрации ферритина. Lindgren и соавт. провели многоцентровое РКИ, замаскированное для оценивающих экспертов; его результаты показали, что в/в введение сахарата железа превосходило пероральный сульфат железа в улучшении уровня Hb и восстановлении запасов железа у больных ВЗК; кроме того, сахарат железа характеризовался лучшим гастроинтестинальным профилем безопасности. Avni и соавт. сравнили способы лечения анемии у больных ВЗК в рамках систематического обзора и провели метаанализ РКИ. В исследовании сделан вывод, что лечение анемии при ВЗК следует основывать на в/в введении железа, а не на пероральном приеме препаратов железа в связи с их благотворным воздействием на уровень Hb, минимальной токсичностью и отсутствием негативного влияния на течение заболевания.
Рецидив анемии у больных ВЗК после лечения является еще одной важной проблемой. В ретроспективном исследовании, проведенном Kulnigg и соавт., сообщалось, что рецидив дефицита железа в среднем возникает спустя 19 мес и является индикатором необходимости поддерживающей терапии. Частота рецидивов выше у пациентов с низким уровнем ферритина после лечения (<100 мкг/л; медиана – 4 мес) по сравнению с больными с нормальной концентрацией ферритина (100-400 мкг/л; медиана – 49 мес). Поэтому цель заместительной терапии железом заключается в достижении уровня ферритина после лечения как минимум 400 мкг/л (верхняя безопасная граница – 800 мкг/л); пациентов следует регулярно осматривать для предупреждения рецидива дефицита железа. Evstatiev и соавт. провели многоцентровое, рандомизированное плацебо-контролированное исследование, чтобы определить, можно ли при помощи карбоксимальтозы железа предотвратить рецидив анемии у больных ВЗК. Они пришли к выводу, что последняя по сравнению с плацебо более эффективна и безопасна в профилактике рецидивов анемии.
Безопасность в/в терапии железом
Рекомендации
- Цель терапии ЖДА заключается в повышении уровня Hb на 2 г/дл в течение 4 нед и восполнении запасов железа.
- Целевые значения сывороточного ферритина при заместительной терапии железом должны превышать 400 мкг/л.
- У больных ВЗК заместительная терапия в/в препаратами железа восполняет запасы указанного микроэлемента более эффективно, чем пероральный прием.
- Распространенная ошибка: высокие дозы перорального железа позволят решить проблему мальабсорбции железа при ВЗК, а в/в введение целесообразно только при тяжелом течении анемии.
- Содержание железа и уровень ферритина следует оценивать регулярно для предупреждения рецидива ЖДА.
- Если концентрация ферритина <100 мкг/л, то заместительную терапию железом следует назначать до появления анемии.
- В свете литературных данных и клинического опыта Рабочей группы по ЖДА для лечения ЖДА у больных ВЗК рекомендуется сразу начинать в/в введение железа, несмотря на тяжесть анемии и активность ВЗК.
- Направить пациента к гематологу при отсутствии ответа на проводимую терапию.
Во время динамического наблюдения следует проводить лабораторное обследование, включающее развернутый клинический анализ крови, сывороточную концентрацию ферритина, СРП. Пациентов, пребывающих в состоянии ремиссии, или с легким течением заболевания следует регулярно осматривать каждые 6-12 мес, тогда как состояние больных с активным течением болезни необходимо контролировать как минимум каждые 3 мес. При наличии макроцитоза необходимо ежегодно мониторировать сывороточные концентрации кобаламина и фолиевой кислоты. Целевые значения сывороточного ферритина при заместительной терапии железом должны превышать 400 мкг/л.
После успешного лечения ЖДА с использованием в/в препаратов железа повторную терапию с применением в/в инфузий железа следует начать сразу же, как только концентрация ферритина в сыворотке крови снизится <100 мкг/л.
Проблема безопасности парентеральных форм железа ассоциирована с серьезными нежелательными явлениями (анафилаксия, шок, смерть); они, как правило, возникают при использовании высокомолекулярного декстрана железа, который больше не доступен на фармакологических рынках Европы. Профиль безопасности современных препаратов, таких как сахарат железа и карбоксимальтоза железа, гораздо благоприятнее.
Chertow и соавт. провели исследование, использовав данные американской программы Medwatch; они определили, что частота появления нежелательных явлений, ассоциированных с в/в введением железа, несколько снижается, а частота их развития чрезвычайно низкая. Увеличение риска связано с использованием высокомолекулярного декстрана железа.
Среди всех препаратов железа сахарат железа обладает наибольшей доказательной базой (в результате интенсивных наблюдений). В исследовании Van Wyck и соавт. сделан вывод, что введение сахарата железа является безопасным и эффективным способом лечения анемии у пациентов, чувствительных к декстрану железа, и может проводиться без пробы на чувствительность посредством в/в болюсного введения или в/в инфузии.
Карбоксимальтоза железа представляет собой новый препарат железа для в/в введения, который, как сообщается, является таким же безопасным, как сахарат железа, но более эффективным. Поскольку карбоксимальтоза железа – это очень стабильное вещество, обладающее низкой токсичностью, то такие состояния, как нестабильное высвобождение железа и некроз печени, при ее применении не развиваются. Она характеризуется низким риском анафилаксии или анафилактоидной реакции, поскольку не содержит декстран. Карбоксимальтоза железа позволяет вводить большие дозы железа за короткий промежуток времени, что дает возможность предотвратить проблемы, ассоциированные с низкой приверженностью пациентов и дополнительной стоимостью множественных инъекций. Сведений об эффективности применения карбоксимальтозы железа становится все больше.
В недавнем исследовании, охватившем 55 гастроэнтерологических центров, показано, что только 43,5% больных анемией и ВЗК получали лечение по поводу анемии. По данным другого исследования, проведенного в 9 европейских странах, большинство больных ВЗК и анемией принимали пероральные препараты железа (67%) и только 28% пациентов назначили в/в введение железа. В реальной клинической практике большинство больных ВЗК и анемией либо не получают заместительную терапию железом, либо употребляют пероральные препараты железа, несмотря на существующие данные доказательной медицины и международные руководства, рекомендующие в/в введение как наиболее предпочтительный способ.
Рекомендации
- Заблуждение: в/в препараты железа опасны.
- Препараты железа нового поколения, предназначенные для в/в введения, лучше подходят для быстрой инфузии; нет необходимости в определении чувствительности
Обоснование пероральной заместительной терапии железом
- Простой способ приема.
- Большой клинический опыт применения.
- Редкие летальные нежелательные явления, ассоциированные с препаратом (анафилаксия).
- Низкая стоимость.
- Предпочтение пациента.
Обоснование заместительной терапии в/в препаратами железа
 Быстрое достижение результатов, большая эффективность.
Быстрое достижение результатов, большая эффективность.- Восстановление запасов железа независимо от факторов, влияющих на абсорбцию железа.
- Высокая приверженность и комплайенс.
- Минимальное количество побочных эффектов и хорошая переносимость.
- Отсутствие токсичности в отношении слизистых оболочек и обострения заболевания.
- Предпочтение пациента.
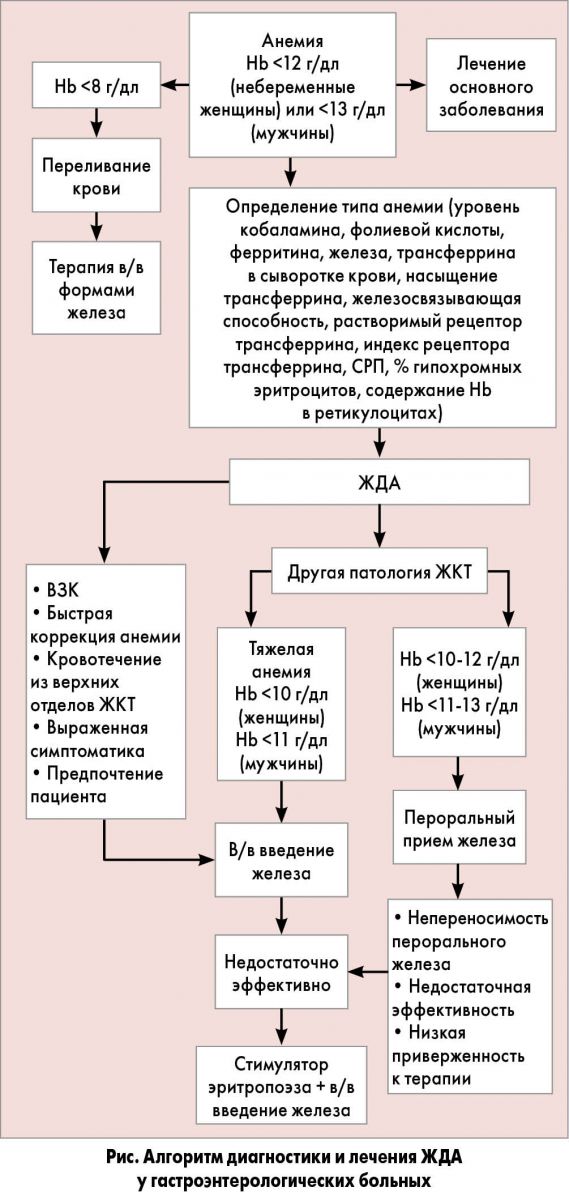
На рисунке представлен подход к диагностике и лечению ЖДА у гастроэнтерологических больных в соответствии с литературными данными и собственным опытом.
Таким образом, ЖДА остается наиболее распространенной причиной анемии у пациентов с ЖКК и ВЗК. Она существенно снижает качество жизни, если не корригируется должным образом. Диагностика ЖДА может быть сложной задачей; в таких ситуациях большое значение имеют выбор необходимого исследования и тщательная оценка полученных результатов. В случаях, когда рутинных диагностических тестов недостаточно, следует прибегнуть к дополнительным исследованиям, если это возможно. Определение СРБ необходимо для исключения воспаления и оценки активности ВЗК. Современные литературные данные подтверждают, что в/в заместительная терапия железом более эффективна в лечении ЖДА, чем пероральный прием железа. Значительная эффективность, лучшая переносимость, высокая приверженность к лечению, отсутствие токсичности в отношении слизистых оболочек являются преимуществами в/в способа введения железа. Однако многие врачи по-прежнему настаивают на использовании перорального способа приема железа, несмотря на его побочные эффекты, проблемы с приверженностью, низкой скоростью восстановления запасов железа, недостаточным ответом на терапию. Им необходимо подумать над тем, действительно ли они хотят вылечить пациентов или просто выписать рецепт, не будучи заинтересованным в результатах терапии.
Справка "ЗУ"
Информация для профессиональной деятельности врачей и фармацевтов
Среди множества железосодержащих препаратов, зарегистрированных на украинском фармацевтическом рынке, особо выделяется препарат Суфер, представляющий собой гидроксидсахарозный комплекс железа (III). Суфер производит один из флагманов отечественной фармацевтической индустрии – компания «Юрия-Фарм». Он предназначен для быстрой клинической и гематологической коррекции дефицита гемоглобина и дефицита железа посредством исключительно внутривенной капельной или струйной инъекции. Препарат выпускается в ампулах по 5 мл № 5 в упаковке и во флаконах 10 мл и 100 мл растворителя (NaCl-Солювен) в упаковке; 1 мл раствора содержит 20 мг железа; непосредственно перед введением Суфера содержимое флакона следует растворить в 0,9% растворе хлорида натрия в соотношении 1:20. Стандартная доза Суфера составляет 5-10 мл (100-200 мг) железа 1-3 раза в неделю в зависимости от уровня гемоглобина. Более детальная информация по особенностям применения Суфера представлена в инструкции к препарату.
Статья печатается в сокращении.
Akpinar H., Cetiner M., Keshav S. Diagnosis and treatment of iron deficiency anemia in patients with inflammatory bowel disease and gastrointestinal bleeding: iron deficiency anemia working group consensus report.
Turk J Gastroenterol. 2017 Mar; 28(2):81-87. doi: 10.5152/tjg.2017.17593. Epub 2017 Jan 25.
Перевела с англ. Лада Матвеева
Медична газета «Здоров’я України 21 сторіччя» № 3 (424), лютий 2018 р.


