17 березня, 2018
Оптимальная коррекция дефицита витамина D: значимость плейотропных свойств
 На протяжении последних нескольких лет пристальное внимание различных научных и медицинских организаций, фармакологической и пищевой промышленности, органов государственного регулирования и общественности приковано к витамину D. Бум научных публикаций (более 30 тыс. статей за 10 лет), значительный рост количества проводимых исследований, пересмотр основных положений целого ряда международных руководств и диетических рекомендаций, увеличение числа пищевых добавок, содержащих этот жирорастворимый витамин, и резкий скачок их продаж наглядно подтверждают данный факт.
На протяжении последних нескольких лет пристальное внимание различных научных и медицинских организаций, фармакологической и пищевой промышленности, органов государственного регулирования и общественности приковано к витамину D. Бум научных публикаций (более 30 тыс. статей за 10 лет), значительный рост количества проводимых исследований, пересмотр основных положений целого ряда международных руководств и диетических рекомендаций, увеличение числа пищевых добавок, содержащих этот жирорастворимый витамин, и резкий скачок их продаж наглядно подтверждают данный факт.
Появление новых научных знаний о витамине D привело к глобальному изменению представлений об этом нутриенте. Если ранее ему отводилась относительно небольшая роль в регуляции кальций-фосфорного обмена, то теперь ученые именуют витамин D гормоном, подчеркивая тем самым его регулирующее влияние на экспрессию генов, ассоциированных с многочисленными физиологическими процессами, и дифференцируя так называемые скелетные и внескелетные свойства (Pludowski P. et al., 2018).
Актуальность
Согласно современным эпидемиологическим данным, подавляющее большинство населения земного шара страдает дефицитом/недостаточностью витамина D: распространенность этого состояния настолько велика, что многие ученые говорят о пандемии D-дефицита (Pludowski P. et al., 2018).
В настоящее время не существует унифицированного подхода к диагностике дефицита витамина D; как правило, для определения данного состояния используют сывороточную концентрацию 25-гидроксивитамина D – 25(OH)D. Поэтому во многих международных программах по изучению распространенности D-дефицита используется специально разработанная стандартизованная программа (Vitamin D Standardization Program), или так называемый VDSP-протокол. В одной из самых масштабных работ, основанной на анализе результатов 14 популяционных европейских исследований, в которых использовался VDSP-протокол (n=55 844), зафиксирована высокая распространенность дефицита витамина D. По данным К. Cashman и соавт. (2016), у 13% жителей Центральной Европы сывороточная концентрация 25(OH)D не превышает 30 нмоль/л, при этом в зимний период (октябрь – март) количество таких пациентов возрастает до 17%, а в летний – несколько уменьшается (8,3%). Авторы этого исследования уточняют, что при использовании другой дефиниции D-дефицита (уровень 25(OH)D <50 нмоль/л) распространенность данной патологии увеличивается до 40,4%. Представители Международной организации остеопороза подчеркивают, что в отдельных популяциях (пожилые лица, находящиеся в домах престарелых) этот показатель может достигать 75% (Lips B., 2009).
Немаловажную роль в актуальности проблемы дефицита витамина D играет значительное экономическое бремя. В 2009 г. в странах Западной Европы приблизительная стоимость ежедневного приема 2000-3000 МЕ витамина D3 с учетом дополнительных затрат на образовательные мероприятия / лабораторные исследования составила 10 млн евро (Grant W. et al., 2009). Более современное эпидемиологическое исследование, проведенное этими же авторами, подтверждает экономическую целесообразность коррекции D-дефицита. W. Grant и соавт. (2018) установили: если у всех жителей Канады поддерживать уровень 25(OH)D >100 нмоль/л, то данная мера позволит уменьшить ежегодное экономическое бремя дефицита витамина D на 12,5±6 млн долларов США (исходя из экономического бремени этого заболевания в 2016 г.), а также предотвратить, в среднем 23 тыс. преждевременных летальных исходов в течение года (исходя из уровня смертности в 2011 г.).
Витамин D: традиционный подход
Витамин D традиционно относят к группе жирорастворимых витаминов, которая объединяет несколько форм, сходных по химическому строению: D1-D5. Наибольшее клиническое значение имеют две формы – эргокальциферол (витамин D2) и холекальциферол (D3), которые существуют в организме в виде неактивных форм – провитаминов (эргостерола и 7-дегидростерола соответственно). Однако в отличие от всех других витаминов витамин D не является собственно витамином в классическом смысле этого термина, поскольку он:
- биологически не активен;
- способен синтезироваться в организме в отличие от большинства других витаминов, которые поступают извне;
- за счет двухступенчатой метаболизации в организме превращается в активную форму – гормональную (D-гормон) – и оказывает разнообразные биологические эффекты за счет взаимодействия со специфическими рецепторами, локализованными в различных ядрах клеток многих тканей и органов.
Основным источником поступления витамина D3 в организм является его синтез в коже, где 7-дегидростерол под воздействием ультрафиолетовых лучей в процессе двухэтапного метаболизма превращается вначале в провитамин D3, а затем – в витамин D3. Другой естественный путь поступления витаминов D3 и D2 в организм человека – употребление пищи, содержащей относительно небольшие количества этих нутриентов, и продуктов питания, искусственно ими обогащенными, или биологических добавок. По сравнению с другими продуктами рыбий жир, рыба жирных сортов и яичные желтки содержат максимально высокое количество витамина D3; однако даже чрезвычайно разнообразный рацион не может обеспечить организм необходимым количеством данного витамина (Pludowski Р. et al., 2018). Поступивший с пищей витамин D абсорбируется преимущественно в тонком кишечнике и в составе хиломикронов поступает в нижнюю полую вену, а далее – в печень.
После попадания в системный кровоток (независимо от источника поступления – всасывания в кишечнике или синтеза в коже) витамин D под воздействием 25-гидроксилазы превращается в 25-гидроксивитамин D (25(OH)D, или кальцидиол) в печени и, затем, уже под действием 1α-гидроксилазы в почках – в 1,25-дигидроксивитамин D (1,25(OH)2D, или кальцитриол).
Для количественной оценки витамина D в крови рекомендуется определять содержание его метаболита
25(ОН)D, поскольку время его полураспада составляет 2-3 нед, тогда как время полураспада 1,25(OH)2D – примерно 4 ч. Кроме того, концентрация 1,25(OH)2D в крови в 1000 раз меньше по сравнению с таковой 25(ОН)D, она не отражает запасов витамина D в организме и не подходит для мониторинга уровня витамина D. Количественная оценка 25(ОН)D в крови показывает наличие двух основных форм: кальцидиола (D3) и эргокальциферола (D2); обе формы измеряются эквимолярно.
Обе изоформы циркулируют в крови при помощи специального транспортного белка-переносчика (витамин D-связывающего белка); после поступления в ткани 1,25(OH)2D, самая активная, наиболее количественно и качественно значимая форма, воздействует на различные внутриклеточные рецепторы витамина D, обусловливая его разнообразную метаболическую активность в организме. В этом отношении активный метаболит витамина D ведет себя как истинный гормон, в связи с чем и получил название D-гормон. При этом, следуя исторической традиции, в научной литературе его продолжают называть витамином D.
Освободившись от белка-переносчика, 1,25(OH)2D связывается с многочисленными внутриклеточными рецепторами, индуцируя появление различных универсальных метаболических эффектов в тканях и органах. Основная функция 1,25(OH)2D состоит в поддержании гомеостаза кальция и фосфора в организме (обмен этих микроэлементов также регулирует паратиреоидный гормон – ПТГ). Органы-мишени, на которые воздействует 1,25(OH)2D, – тонкий кишечник, почки и кости. В почках 1,25(OH)2D стимулирует ПТГ-зависимую тубулярную реабсорбцию кальция (при этом ПТГ усиливает трансформацию 25(OH)D в 1,25(OH)2D в проксимальных почечных канальцах).
В скелетной мускулатуре 1,25(OH)2D и ПТГ совместно контролируют процессы ремоделирования костной ткани. 1,25(OH)2D взаимодействует с внутриклеточными рецепторами остеобластов, увеличивая экспрессию различных генов и стимулируя образование многоядерных остеокластов. Зрелые остеокласты после связывания с поверхностью кости синтезируют различные коллагеназы и соляную кислоту, что приводит к деградации коллагена, высвобождению и поступлению кальция/фосфора в общий кровоток.
В кишечнике 1,25(OH)2D увеличивает абсорбцию кальция и фосфора, а также контролирует собственную концентрацию в сыворотке крови. При повышении уровня 1,25(OH)2D происходит угнетение активности 1α-гидроксилазы и увеличение активности 24-гидроксилазы, что приводит к образованию из 25(ОН)D метаболита 24,25(OH)2D, не обладающего биологической активностью. Синтез 1,25(OH)2D зависит от уровня ПТГ, кальция и фосфора крови, фактора роста фибробластов 23 (FGF-23). Повышение уровня ПТГ и гипофосфатемия стимулируют синтез фермента 1α-гидроксилазы и, соответственно, 1,25(OH)2D. FGF-23 (вырабатывается остеоцитами и остеобластами) ингибирует синтез 1,25(OH)2D, уменьшает экспрессию почечных натрий-фосфорных транспортеров и стимулирует переход в неактивную форму 24,25(OH)2D. Выводится из организма витамин D через желчь и, частично, через почки.
Таким образом, в соответствии с классическими представлениями дефицит витамина D приводит к нарушению метаболизма костной ткани, что проявляется развитием рахита у детей и остеомаляцией у взрослых. Эти состояния обусловлены изменением минерализации кости вследствие неадекватной продукции кальция/фосфора.
Витамин D: плейотропное действие
Многочисленные современные исследования доказали, что витамин D не только влияет на метаболизм кальция/фосфора и процессы минерализации костной ткани, но и обладает различными плейотропными эффектами. Установлено, что локальный синтез 1,25(OH)2D и последующее его связывание с соответствующими рецепторами влияет на экспрессию 2 тыс. генов, вовлеченных в различные метаболические реакции. Вероятно, именно активация этих генов инициирует появление самых разнообразных свойств, приписываемых витамину D и не связанных с гомеостазом кальция и фосфора. Доказано, что 1,25(OH)2D не только принимает участие в процессах клеточного роста и дифференцировки, но и влияет на состояние иммунной системы: изменяет синтез β-дефензина и кателицидина, способствует выработке противовоспалительных цитокинов – интерлейкинов 4 и 5 (Pludowski P. et al., 2013; Souberbielle J. C. et al., 2010). Он также увеличивает активность лимфоцитов и стимулирует продукцию инсулина. Эти данные объясняют способность витамина D снижать вероятность возникновения различных заболеваний.
Витамин D обладает мощными иммуномодулирующими свойствами: высокая концентрация рецепторов к витамину D (VDR) обнаружена в макрофагах, дендритных клетках, Т- и В-лимфоцитах; данный факт поддерживает фундаментальную концепцию о роли этого витамина в борьбе с бактериями, профилактике аутоиммунных заболеваний и хронической воспалительной патологии (Sabetta J. R. et al., 2010; Bergman P., 2012). В исследовании J. R. Sabetta и соавт. (2010) показано, что относительно высокий уровень витамина D (≥38 нг/л, или 95 нмоль/л) ассоциирован с 2,7-кратным снижением распространенности острой респираторной вирусной инфекции (р=0,015) и 4,5-кратным сокращением длительности этого заболевания по сравнению с его более низкими значениями. Авторы данного исследования предполагают, что увеличение концентрации 25(OH)D в общей популяции до уровня 38 нг/мл (95 нмоль/л) приведет к значительному сокращению распространенности острых вирусных инфекций.
Другой точкой приложения эффектов витамина D является кардиоваскулярная система: в сосудах и сердце содержится много VDR. Основываясь на этом факте, многие исследователи объясняют сезонные и географические особенности распространенности сердечно-сосудистых заболеваний и D-дефицита. Подобный вывод сделан в многоцентровом исследовании, в котором анализировались факторы, предшествующие появлению атеросклероза у детей и подростков (Juonala M. et al., 2015). Длительное наблюдение за рандомизированной когортой лиц (n=2148), у которых в возрасте 3-18 лет были получены образцы сыворотки крови и проведено ультразвуковое исследование толщины комплекса интима-медиа сонной артерии (маркера атеросклероза), выявило интересную зависимость. Оказывается, низкое содержание 25(OH)D в сыворотке крови (минимальный квартиль – <40 нмоль/л) в детском возрасте ассоциируется со значительным возрастанием риска увеличения толщины комплекса интима-медиа в зрелом возрасте (относительный риск – ОР – 1,70; 95% доверительный интервал – ДИ – 1,15-2,31; р=0,0007) и появлением соответствующих факторов риска (ОР 1,80; 95% ДИ 1,30-2,48; р=0,0004).
Витамину D приписываются антиканцерогенные свойства. S. L. McDonnell и соавт. (2016) доказали, что риск развития инвазивного рака (за исключением рака кожи) у женщин с высокой концентрацией 25(OH)D (≥40 нг/мл, или 100 нмоль/л) на 67% ниже, чем у пациенток с уровнем этого нутриента <20 нг/мл, или 50 нмоль/л (отношение рисков 0,33; 95% ДИ 0,12-0,90). В другом исследовании зафиксирована связь между развитием неоплазий у постменопаузальных женщин и сывороточной концентрацией 25(OH)D, а также доказано, что ежедневное употребление биологических добавок, содержащих витамин D в дозе 1100 МЕ/сут, способствует достоверному снижению риска развития рака любой локализации (Lappe J. M. et al., 2007). В настоящее время статус витамина D считается важным фактором, способствующим уменьшению вероятности возникновения рака грудной железы, колоректального рака, аденом толстого кишечника. Оптимальной профилактической концентрацией 25(OH)D в отношении неоплазий любых локализаций, по мнению W. B. Grant и соавт. (2016), является уровень витамина D 30-40 нг/мл (75-100 нмоль/л).
Установлена зависимость между возникновением болезни Альцгеймера, деменции, других форм нейродегенеративных заболеваний и сывороточной концентрацией 25(OH)D. В исследовании CHIANTI показано возрастание риска когнитивных нарушений у пожилых больных с тяжелым дефицитом витамина D (<10 нг/мл, или 25 нмоль/л) в течение 6 лет (ОР 1,6; 95% ДИ 1,2-2,0) по сравнению с лицами, у которых уровень 25(OH)D в крови превышал 30 нг/мл, или 75 нмоль/л (Llewellyn D. J. et al., 2010).
Высказывается предположение, что низкая концентрация 25(OH)D ассоциирована со значительным повышением риска летального исхода (Pilz S. et al., 2016). Широкомасштабный анализ 73 когорт (n=849 412), проведенный R. Chowdhury и соавт. (2014), показал, что при снижении уровня 25(OH)D <10 нг/мл (25 нмоль/л) относительный риск смерти возрастает в 1,5 раза (95% ДИ 1,21-1,87) по сравнению с таковым при содержании этого витамина >30 нг/мл (75 нмоль/л).
Количество публикаций, подтверждающих внескелетные свойства витамина D и его благотворное влияние на состояние различных органов и систем, непрерывно увеличивается. Зафиксирована положительная взаимосвязь между уровнем 25(OH)D и снижением риска развития неопластической и аутоиммунной патологии (рассеянного склероза, сахарного диабета 1 типа), бронхиальной астмы, сердечно-сосудистых заболеваний и инсульта, системной красной волчанки, атопического дерматита, нейрокогнитивной дисфункции (болезни Альцгеймера, аутизма), инфекционных заболеваний (включая грипп и туберкулез), осложнений беременности, сахарного диабета 2 типа, падений, остеопороза и переломов, рахита, остеомаляции и др., а также уровня общей летальности.
Витамин D: минимум, максимум или оптимум?
В настоящее время продолжаются активные дебаты в отношении дефиниций дефицита и недостаточности витамина D: разные международные сообщества предлагают использовать различный диапазон значений для указанных состояний. Несмотря на это, ведущие эксперты единодушны в определении цели дополнительного введения витамина D: она заключается в достижении и поддержании оптимальных концентраций 25(OH)D без развития побочных эффектов.
Авторы обзора современных рекомендаций по дополнительному приему витамина D считают, что минимальный уровень этого нутриента необходимо определять, исходя из особенностей его метаболизма: установлено, что концентрация 25(OH)D, равная 40 нг/мл (100 нмоль/л), обеспечивает 50% максимальной активности 1α-гидроксилазы, что позволяет обеспечить синтез адекватного количества активной формы витамина D. Поэтому минимальная концентрация 25(OH)D, необходимая для обеспечения скелетных эффектов витамина D, будет одна, в то время как для поддержания внескелетных свойств требуется другой уровень. Данную гипотезу наглядно иллюстрирует работа S. Spedding и соавт. (2013), которые доказали, что минимальная эффективная сывороточная концентрация 25(OH)D при рахите составляет 10 нг/мл, остеопоротических переломах – 20 нг/мл, тогда как для реализации внескелетных свойств необходимы совсем другие показатели: профилактика преждевременного летального исхода – 30 нг/мл, депрессии – 30 нг/мл, сахарного диабета и сердечно-сосудистых заболеваний – 32 нг/мл, падений и заболеваний респираторного тракта – 38 нг/мл, рака – 40 нг/мл.
Международные рекомендации: выбор дозы витамина D
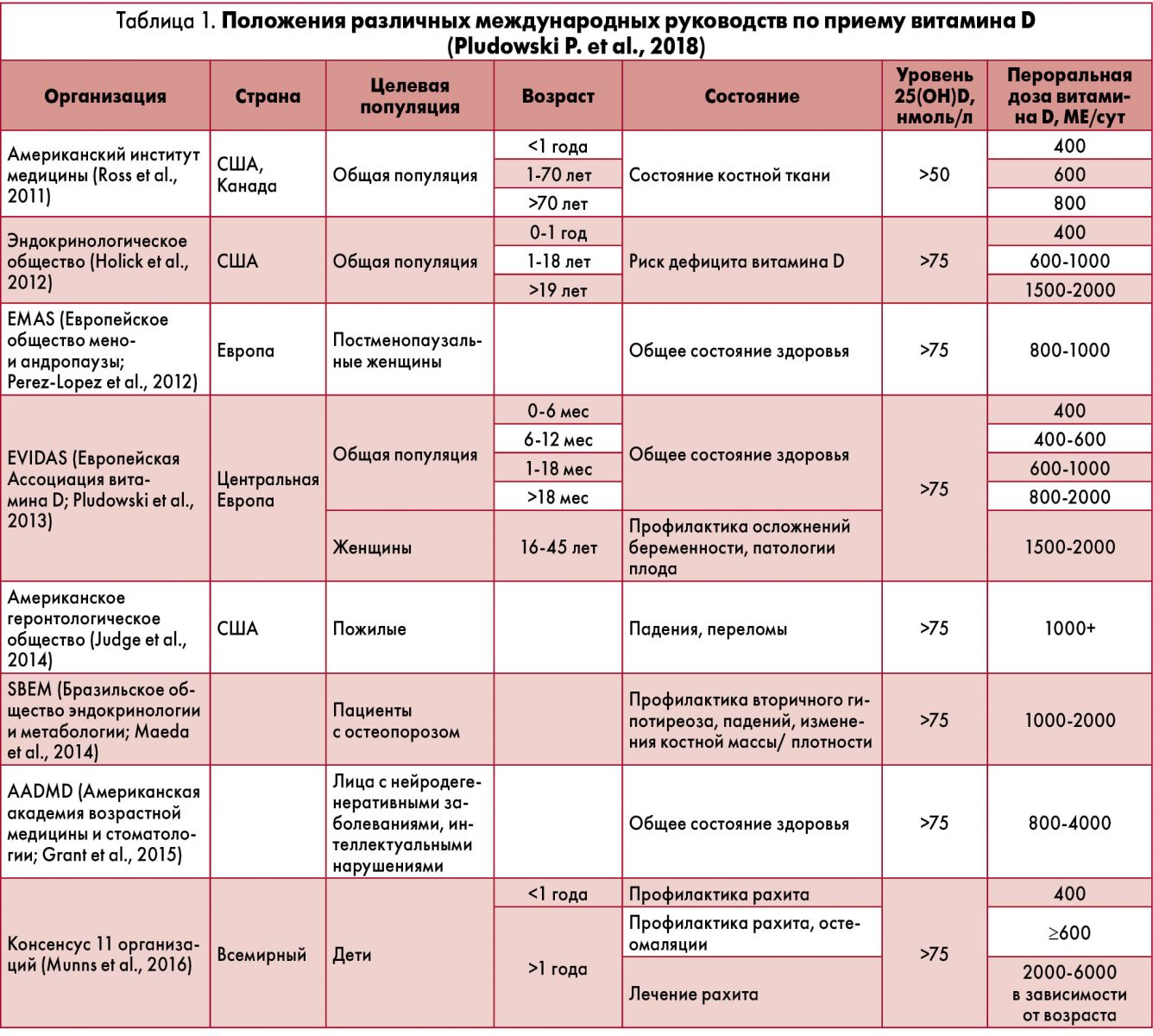 Одними из первых указания по профилактическому приему витамина D сформулировали эксперты Американского института медицины: в 1990-2000 гг. рекомендованная суточная доза витамина D для лиц в возрасте <50 лет составляла 200 МЕ/сут (5 мг/сут).
Одними из первых указания по профилактическому приему витамина D сформулировали эксперты Американского института медицины: в 1990-2000 гг. рекомендованная суточная доза витамина D для лиц в возрасте <50 лет составляла 200 МЕ/сут (5 мг/сут).
Представители данной организации полагали, что прием витамина D в указанной дозировке позволит предупредить развитие рахита. Однако в 2010 г. они пересмотрели свое мнение и рекомендовали детям раннего возраста назначать 400 МЕ/сут, дошкольникам, подросткам и взрослым – 600 МЕ/сут, лицам старше 70 лет – 800 МЕ/сут (табл. 1).
Аналогичная ситуация сложилась с минимальной концентрацией 25(OH)D: если первоначально необходимый порог этого витамина составлял 20 нг/мл (50 нмоль/л), то в настоящее время он увеличен до 30-50 нг/мл или 40-60 нг/мл (в зависимости от литературного источника). Для предупреждения субклинической остеомаляции рекомендуется создавать более высокие концентрации 25(OH)D: >30 нг/мл (75 нмоль/л).
В Европейских практических рекомендациях по профилактике D-дефицита (2013) не только учитывается способность витамина D влиять на метаболизм костной ткани, но и принимаются во внимание его основные клинически значимые плейотропные эффекты. В данном руководстве оптимальной считается концентрация 25(OH)D в диапазоне 30-50 нг/мл. При выборе суточной дозы витамина D эксперты советуют учитывать географический регион, интенсивность солнечного излучения, пигментацию кожи, национальные диетические и культурные привычки (в том числе особенности повседневной одежды), уровень практического здравоохранения и многие другие специфические факторы (возраст, массу тела, тип кожи).
Таким образом, во многих международных руководствах оптимальной дозировкой витамина D, необходимой для коррекции его скелетных и внескелетных эффектов, является доза 1000 МЕ/сут.
Детримакс®: оптимальная коррекция дефицита витамина D
Прием биологических добавок, содержащих витамин D, считается эффективным и безопасным способом коррекции дефицита этого нутриента. Относительно недавно на отечественном фармацевтическом рынке появился Детримакс® (компания Unipharm Inc. USA). Характерной чертой, выгодно отличающей Детримакс® от других D-содержащих средств, является оптимальная концентрация витамина D3 – 1000 МЕ в 1 капсуле. Сафлоровое масло, использующееся в качестве вспомогательного вещества, увеличивает усвояемость витамина D3, а также представляет собой источник жирорастворимых витаминов К и Е и целого ряда полиненасыщенных жирных кислот (линолевой, олеиновой, пальмитиновой, стеариновой, арахидоновой, миристиновой). Детримакс® может использоваться для профилактики и лечения нарушений фосфорно-кальциевого обмена, назначаться при недостаточном потреблении продуктов, содержащих витамин D, кратковременном пребывании на солнце, обусловленном особенностями работы, соблюдении вегетарианской или низкокалорийной диеты, нарушениях сна, использовании кремов с УФ-фильтрами. Удобный режим приема (1 р/сут во время еды), отличное качество, свойственное нутриентам американского производства, служат гарантией эффективности и безопасности препарата Детримакс®, а также высокой приверженности пациентов к лечению.
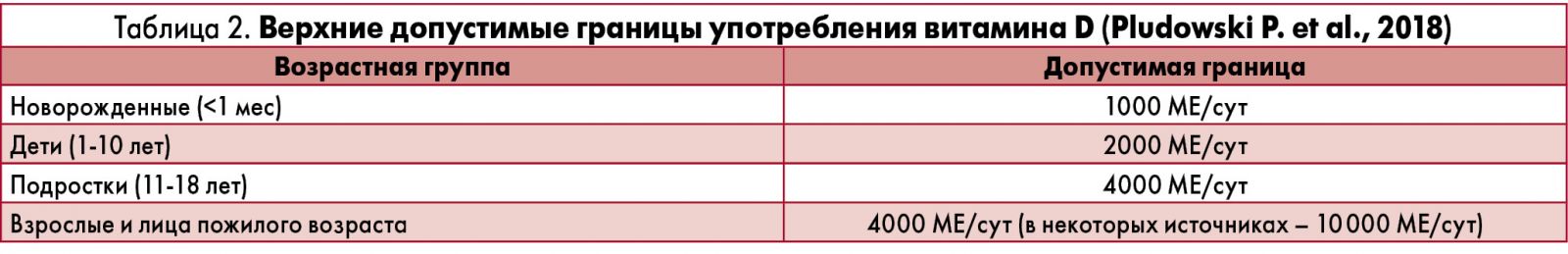 Некоторые практические врачи, не привыкшие к использованию новых рекомендованных доз витамина D, высказывают опасения, что высокое содержание нутриента в сочетании с безрецептурным отпуском D-содержащих биологических добавок может привести к их передозировке и развитию гиперкальциемии и гиперкальциурии. По мнению Р. Pludowski и соавт. (2018), простым и эффективным способом предотвращения неконтролируемого приема витамина D в общей популяции является использование содержащих витамин D биологических добавок в пределах верхней границы максимально переносимой дозы, которая, по данным международных/региональных и национальных руководств, достаточно велика и составляет 4000-10 000 МЕ/сут (ее прием не сопровождается развитием неблагоприятных побочных действий; табл. 2).
Некоторые практические врачи, не привыкшие к использованию новых рекомендованных доз витамина D, высказывают опасения, что высокое содержание нутриента в сочетании с безрецептурным отпуском D-содержащих биологических добавок может привести к их передозировке и развитию гиперкальциемии и гиперкальциурии. По мнению Р. Pludowski и соавт. (2018), простым и эффективным способом предотвращения неконтролируемого приема витамина D в общей популяции является использование содержащих витамин D биологических добавок в пределах верхней границы максимально переносимой дозы, которая, по данным международных/региональных и национальных руководств, достаточно велика и составляет 4000-10 000 МЕ/сут (ее прием не сопровождается развитием неблагоприятных побочных действий; табл. 2).
Таким образом, высокая распространенность дефицита/недостаточности витамина D во всем мире и подтверждение его взаимосвязи с различными внескелетными заболеваниями (сердечно-сосудистой, неврологической, онкологической патологией) обусловливает целесообразность широкого применения витамина D3 (Детримакс®). Предпочтение следует отдавать биологическим добавкам, содержащим оптимальную дозу витамина D, что позволяет свести к минимуму риск развития побочных эффектов и наряду с предупреждением возникновения переломов, увеличением устойчивости к вирусным инфекциям способствует улучшению качества жизни пациентов.
Список литературы находится в редакции.
Медична газета «Здоров’я України 21 сторіччя» № 4 (425), лютий 2018 р.


