18 березня, 2018
Японское руководство по лечению атопического дерматита (2017): краткий обзор основных положений
В 2017 г. ведущие эксперты одного из самых известных и авторитетных медицинских сообществ – Японского общества аллергологии (Japanese Society of Allergology, JSA) – опубликовали практическое руководство по лечению атопического дерматита (АД). В нем представлены современные взгляды на этиологию, патофизиологию АД, а также изложены актуальные концепции лечения этого заболевания. Представляем вашему вниманию основные положения данного руководства.
Дефиниция, этиология и диагностика АД
 Несмотря на то что руководство разработано и представлено JSA, в нем использованы терминология и диагностические критерии АД, предложенные Японской дерматологической ассоциацией (табл. 1).
Несмотря на то что руководство разработано и представлено JSA, в нем использованы терминология и диагностические критерии АД, предложенные Японской дерматологической ассоциацией (табл. 1).
В руководстве подчеркивается, что АД возникает при наличии генетической предрасположенности и воздействии целого ряда факторов окружающей среды. Эксперты JSA различают этиологические и усугубляющие факторы АД; считается, что их значимость меняется у пациентов различных возрастных групп. Например, в первой половине жизни большое значение в возникновении АД отводится пищевым привычкам (употребление яиц, коровьего молока, пшеницы), а также повышенной потливости/сухости кожи, расчесыванию и физико-химическим раздражителям (воздействие слюны, мыла, детергентов, тесной одежды), тогда как роль клещей, пыли, микробов, грибов и шерсти домашних питомцев относительно невелика. У детей младшего дошкольного возраста и взрослых в перечне этиологических причин доминируют чрезмерное потоотделение, сухость кожи, расчесывание кожных покровов, физико-химические раздражители, возрастает неблагоприятное влияние микробов/грибов, клещей, пыли и эмоционального стресса, тогда как значимость пищевого фактора значительно снижается.
По мнению экспертов JSA, для подтверждения диагноза АД следует прибегнуть к лабораторной диагностике и определить такие показатели, как:
- общий уровень IgЕ (у 80% больных отмечается значительное возрастание этого показателя; высокий уровень общего IgЕ коррелирует с тяжестью течения заболевания);
- количество эозинофилов в крови (в большинстве случаев обнаруживается выраженная эозинофилия; данные изменения развиваются достаточно быстро в отличие от повышения уровня общего IgE, поэтому динамику течения заболевания оценивают именно по уровню эозинофилов);
- уровень специфических IgE-антител;
- концентрация сывороточного хемокина, регулируемого тимусом и при активации (TARC; он является полезным вспомогательным маркером, использующимся для оценки степени тяжести АД).
 В опубликованном руководстве JSA предлагается несколько способов оценки степени тяжести АД: международная система SCORAD и критерии Японской дерматологической ассоциации. SCORAD предусматривает определение клинической формы АД, площади поражения, интенсивности зуда и степени нарушения сна. Критерии Японской дерматологической ассоциации основаны на определении морфологических характеристик сыпи (эритема / острая папула, влажность/корки, хронические папулы / бугорки / лихенификация) и ее локализации (голова и шея, передняя/задняя поверхность туловища, верхние и нижние конечности). По мнению экспертов JSA, активное использование вышеперечисленных методик в повседневной деятельности врача общей практики несколько затруднительно, поскольку их применение требует специальной подготовки. Поэтому в данном руководстве вводятся новые, упрощенные критерии тяжести АД, основанные на использовании терминов «легкая сыпь» и «высыпания с выраженным воспалением» (табл. 2).
В опубликованном руководстве JSA предлагается несколько способов оценки степени тяжести АД: международная система SCORAD и критерии Японской дерматологической ассоциации. SCORAD предусматривает определение клинической формы АД, площади поражения, интенсивности зуда и степени нарушения сна. Критерии Японской дерматологической ассоциации основаны на определении морфологических характеристик сыпи (эритема / острая папула, влажность/корки, хронические папулы / бугорки / лихенификация) и ее локализации (голова и шея, передняя/задняя поверхность туловища, верхние и нижние конечности). По мнению экспертов JSA, активное использование вышеперечисленных методик в повседневной деятельности врача общей практики несколько затруднительно, поскольку их применение требует специальной подготовки. Поэтому в данном руководстве вводятся новые, упрощенные критерии тяжести АД, основанные на использовании терминов «легкая сыпь» и «высыпания с выраженным воспалением» (табл. 2).
В руководстве приводится несколько клинических примеров оценки степени тяжести АД в соответствии с предложенной методикой (рис. 1).
Клинические проявления
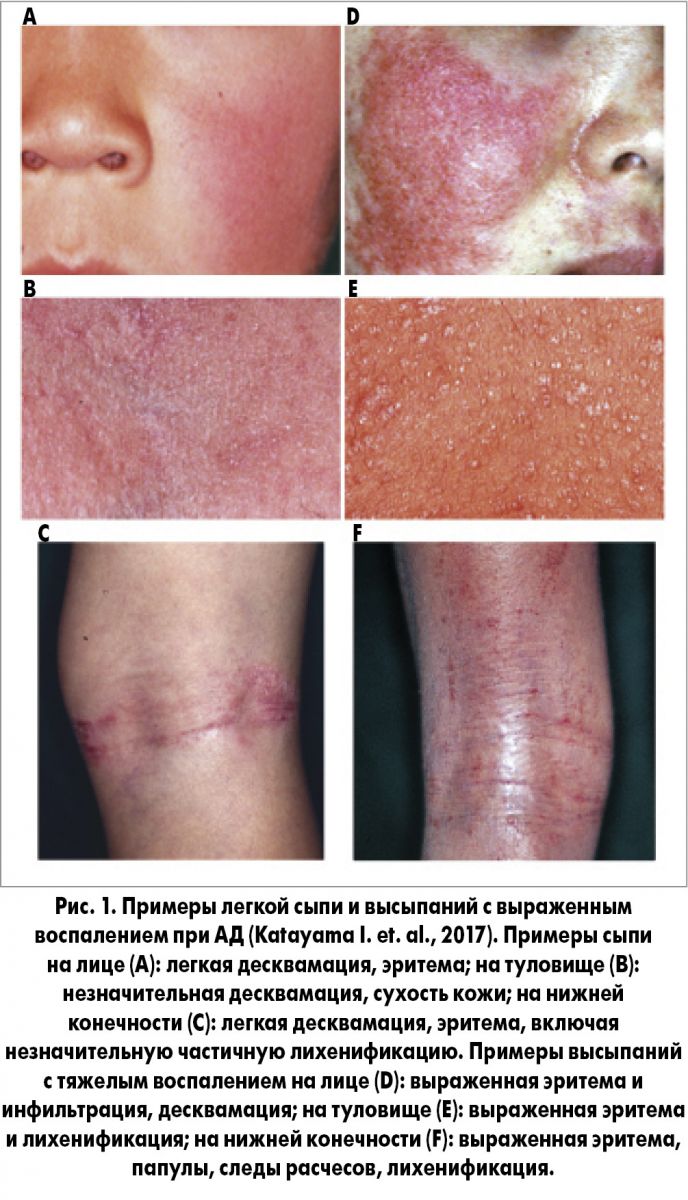 Характеризуя современные особенности клинической картины АД, представители JSA подчеркивают чрезвычайное многообразие симптомов заболевания и отдельно рассматривают дерматологические и экстрадермальные проявления АД.
Характеризуя современные особенности клинической картины АД, представители JSA подчеркивают чрезвычайное многообразие симптомов заболевания и отдельно рассматривают дерматологические и экстрадермальные проявления АД.
Дерматологические симптомы
В данном руководстве симптоматика поражения кожных покровов представлена с учетом трех основополагающих характеристик: возраста больного, морфологии и распространенности сыпи, а также ее локализации.
Кожный статус больных АД рассматривается в трех возрастных группах: у детей раннего возраста (<2 лет), дошкольников/школьников (2-12 лет), подростков/взрослых (≥13 лет). Высыпания у детей раннего возраста носит острый экзематозный характер. Сыпь, как правило, локализуется на шее, лбу или голове, при расчесывании может подвергаться эрозированию и экссудации, а при высыхании образуются корочки из экссудата. Высыпания у дошкольников/школьников представлены в основном эритематозными, отечными папулами, склонными к образованию сплошных очагов поражения. Многочисленные расчесы провоцируют появление узловатого пруриго, эрозий, кровянистых корочек. Высыпания локализуются преимущественно в локтевых и подколенных сгибах, на боковых поверхностях шеи, верхней части груди и кистях. У подростков и взрослых больных очаги поражения представлены папулами и участками лихенификации. Представители этой возрастной группы могут страдать также себореей или акне, что обусловлено увеличением секреции сальных желез. Излюбленная локализация сыпи – верхняя часть туловища, шея, лоб (так называемый портретный тип поражения).
Другим основополагающим симптомом АД является зуд кожных покровов. Его появление провоцирует повышение температуры кожи во время купания и физических упражнений, потливость, контакт с шерстью (при непереносимости последней). Сильный зуд становится причиной нарушения ночного сна: пациенты с трудом засыпают и часто просыпаются. В отличие от расчесывания во время сна (бессознательного рефлекторного движения), почесывание в дневное время является частично осознанным действием. Понимание того факта, что расчесывание усиливает выраженность кожных проявлений, приходит только в подростковом возрасте одновременно со стремлением удержаться от почесывания. Поэтому для ослабления негативного влияния расчесывания на состояние детей раннего возраста / дошкольников эксперты рекомендуют использовать специальные повязки, надевать одежду или носить перчатки.
Кроме основных дерматологических проявлений АД, эксперты JSA описывают вторичные изменения кожных покровов: белый дермографизм, «гусиную» кожу, себорейную экзему, пигментацию (потемнение кожи в области орбитальной складки, точечная пигментация губ), формирование складок на лице (инфраорбитальная складка Денни-Моргана – складка от внутреннего до наружного угла глаза, спускающаяся к нижнему веку), шее, животе, ладонях; выпадение волос (у детей раннего возраста – в затылочной области, у школьников и взрослых – в височных областях) и бровей (симптом Хертога – выпадение волос из наружной части бровей), жемчужноподобный блеск ногтей.
Экстрадермальные проявления
Течение АД часто сопровождается поражением других органов и систем. У больных АД обнаруживают дерматопатическую лимфоаденопатию. Она возникает вследствие отека региональных поверхностных лимфатических узлов, появление которого провоцируют обширные и тяжелые поражения кожных покровов. Дерматопатическая лимфоаденопатия имеет вялотекущий характер и не является признаком инфекционного поражения.
К офтальмологическим проявлениям АД относят катаракту и отслоение сетчатки. Кортикальная катаракта с передним субкапсулярным / задним подкапсулярным помутнением хрусталика чаще развивается у молодых лиц (15-24 лет) с тяжелым течением АД и преимущественной локализацией высыпаний на лице. Катаракту диагностируют у 2% всех больных АД и 5,5% пациентов с тяжелым течением заболевания. Отслоение сетчатки, ассоциированное с АД, обнаруживают у больных в возрасте 16-25 лет, которые часто трут глаза, веки или имеют привычку похлопывать себя по лицу. Это осложнение возникает у 0,5% всех больных АД и у 2% пациентов с тяжелым течением заболевания.
АД часто ассоциируется с психическими и неврологическими расстройствами. Неудовлетворенность проводимой терапией, недовольство врачебными рекомендациями, низкая вероятность излечения, косметические проблемы провоцируют социальную самоизоляцию и развитие депрессии. Усиление выраженности дерматита может ассоциироваться с появлением парестезий в конечностях.
Поражение гастроинтестинального тракта проявляется неспецифическими симптомами: диареей, запором, вздутием живота, метеоризмом, синдромом избыточного бактериального роста.
Аспекты базовой терапии АД
Эксперты JSA выделяют три основных направления в лечении АД: противодействие влиянию этиологических и усугубляющих факторов, коррекция дисфункции кожи (уход за кожными покровами) и фармакотерапия. Данный подход японские специалисты объясняют тем, что АД является воспалительным заболеванием, которое протекает с формированием очагов экзематозного поражения кожи на фоне имеющегося атопического диатеза и приводит к нарушению функционирования кожных покровов.
Уход за кожей
I. Katayama и соавт. подчеркивают важность ухода за кожей, так как нарушение барьерной функции этого органа обусловливает снижение способности удерживать воду, увеличение чувствительности к зуду и повышение восприимчивости к инфекциям.
Авторы руководства выделяют несколько важных моментов в уходе за кожей, одним из которых является применение гидрофильных мазей и средств, способных удерживать большое количество влаги (препараты мочевины, гепариноиды, водорастворимый коллаген, лактат натрия, гидролизованный эластин) и эффективно увлажняющих кожу. Повреждения кожных покровов можно избежать при помощи наружного применения масляных мазей (мазей в узком смысле этого слова). Большое значение придается ежедневной адекватной гигиене: прием душа, ванны рекомендуется сочетать с нанесением увлажняющего/защитного средства.
Эксперты JSA дают несколько советов по уходу за кожей в домашних условиях. Несмотря на то что во многих международных руководствах подчеркивается необходимость нанесения увлажняющего средства непосредственно после купания, японские ученые считают (опираясь на результаты нескольких широкомасштабных исследований), что увлажняющий эффект не зависит от времени применения эмолентов, и поэтому просто рекомендуют пациентам не забывать производить внешние аппликации увлажняющих средств. I. Katayama и соавт. поощряют активное использование водных процедур в летний период времени, полагая, что смывание водой избыточного количества выделившегося пота уменьшает активность АД. При этом ученые настаивают на необходимости тщательного удаления шампуня и мыла с волосистой части головы и лица, поскольку остатки моющих средств усиливают высыпания.
Основы фармакотерапии
По мнению японских ученых, к назначению медикаментозных средств следует прибегать при недостаточной эффективности простого ухода за кожей и неудовлетворительной результативности мер, направленных на уменьшение влияния этиологических и усугубляющих факторов.
Конечной целью фармакотерапии является полное нивелирование симптоматики заболевания или минимизация тяжести клинических проявлений, при этом резидуальные симптомы не должны ограничивать повседневную активность и контролироваться минимальным количеством лекарственных средств.
Японские специалисты выделяют два вида фармакотерапии: лечение, направленное на индукцию ремиссии, и терапию, нацеленную на поддержание ремиссии. При проведении индукционной терапии рекомендуется осматривать пациента каждые 1-2 нед для определения эффективности проводимой терапии, выявления нежелательных изменений и своевременной коррекции проводимого лечения. При отсутствии улучшения в течение 1 мес или усилении клинической симптоматики следует направить пациента в специализированное медицинское учреждение.
В тех случаях, когда симптомы заболевания не контролируются или часто рецидивируют после завершения индукционной терапии, эксперты рекомендуют прибегнуть к лечению, направленному на поддержание ремиссии. Оно основано на наружном применении такролимуса. Если ремиссия заболевания не достигнута спустя 6 мес, пациента следует госпитализировать в специализированную клинику для подтверждения диагноза и рассмотрения целесообразности длительного применения топического такролимуса.
При тяжелом, очень тяжелом течении заболевания или некупирующихся состояниях показано стационарное лечение с наружной аппликацией высокоактивных стероидов, пероральным приемом иммуносупрессантов (циклоспорина) или кортикостероидов, ультрафиолетовым облучением и медикаментозной коррекцией сопутствующей психосоматической патологии. Пероральный прием стероидов является крайней мерой, продолжительность такой терапии должна быть минимальной.
Фармакотерапия АД
Наружные средства
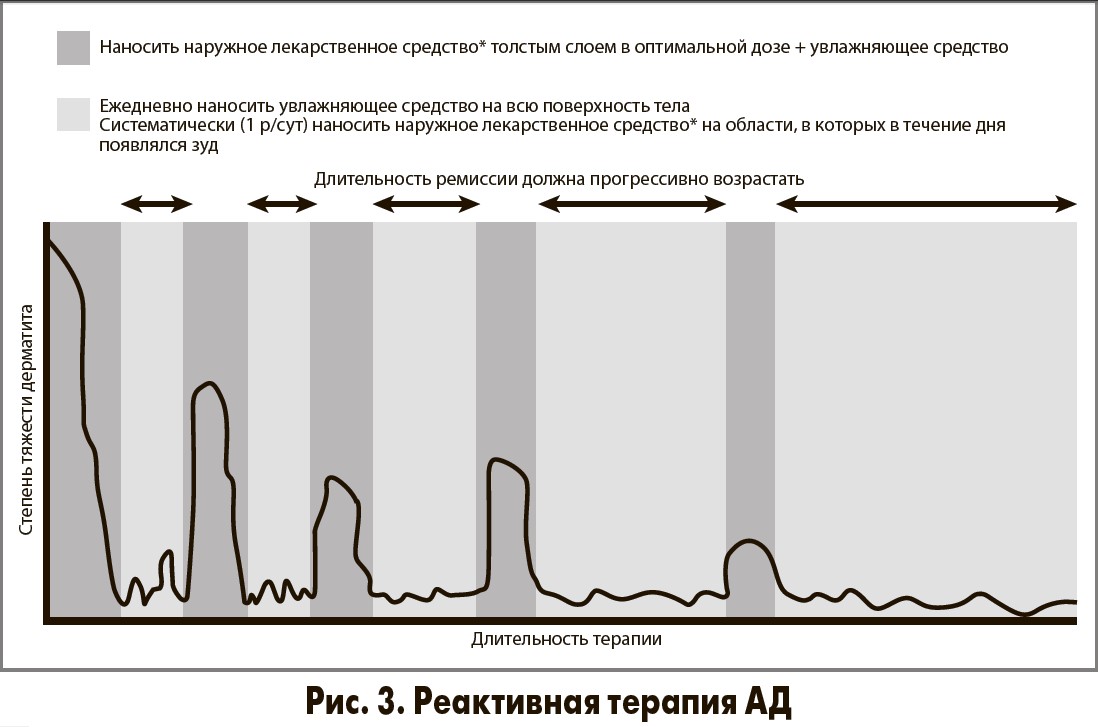
 Топическая терапия предполагает уход за кожей при помощи увлажняющих средств и контроль над воспалительным процессом за счет применения топических стероидов (ТС) или мази такролимуса. Эксперты JSA различают два вида топического лечения: проактивную и реактивную терапию (рис. 2, 3).
Топическая терапия предполагает уход за кожей при помощи увлажняющих средств и контроль над воспалительным процессом за счет применения топических стероидов (ТС) или мази такролимуса. Эксперты JSA различают два вида топического лечения: проактивную и реактивную терапию (рис. 2, 3).
Проактивная терапия предполагает применение ТС, а также мази такролимуса в комбинации с активным использованием увлажняющих средств для поддержания ремиссии. При реактивной терапии топические препараты назначаются только при усилении сыпи. Авторы руководства отдают предпочтение проактивной терапии, так как она позволяет не только предотвратить рецидив дерматологической симптоматики, но и является экономически эффективной.
 Увлажняющие средства. Выбирая увлажняющее средство, японские специалисты рекомендуют учитывать температуру атмосферного воздуха, влажность и удобство применения. Лечение мокнущих повреждений желательно проводить посредством наложения повязки с цинковой мазью. Эксперты настаивают на осторожном применении препаратов мочевины, поскольку они могут стимулировать образование эрозий или спровоцировать усиление воспаления кожи. Положения руководства JSA предусматривают возможность длительного профилактического использования увлажняющих средств, начиная с раннего детского возраста, так как такой подход позволяет уменьшить заболеваемость или отсрочить развитие АД.
Увлажняющие средства. Выбирая увлажняющее средство, японские специалисты рекомендуют учитывать температуру атмосферного воздуха, влажность и удобство применения. Лечение мокнущих повреждений желательно проводить посредством наложения повязки с цинковой мазью. Эксперты настаивают на осторожном применении препаратов мочевины, поскольку они могут стимулировать образование эрозий или спровоцировать усиление воспаления кожи. Положения руководства JSA предусматривают возможность длительного профилактического использования увлажняющих средств, начиная с раннего детского возраста, так как такой подход позволяет уменьшить заболеваемость или отсрочить развитие АД.
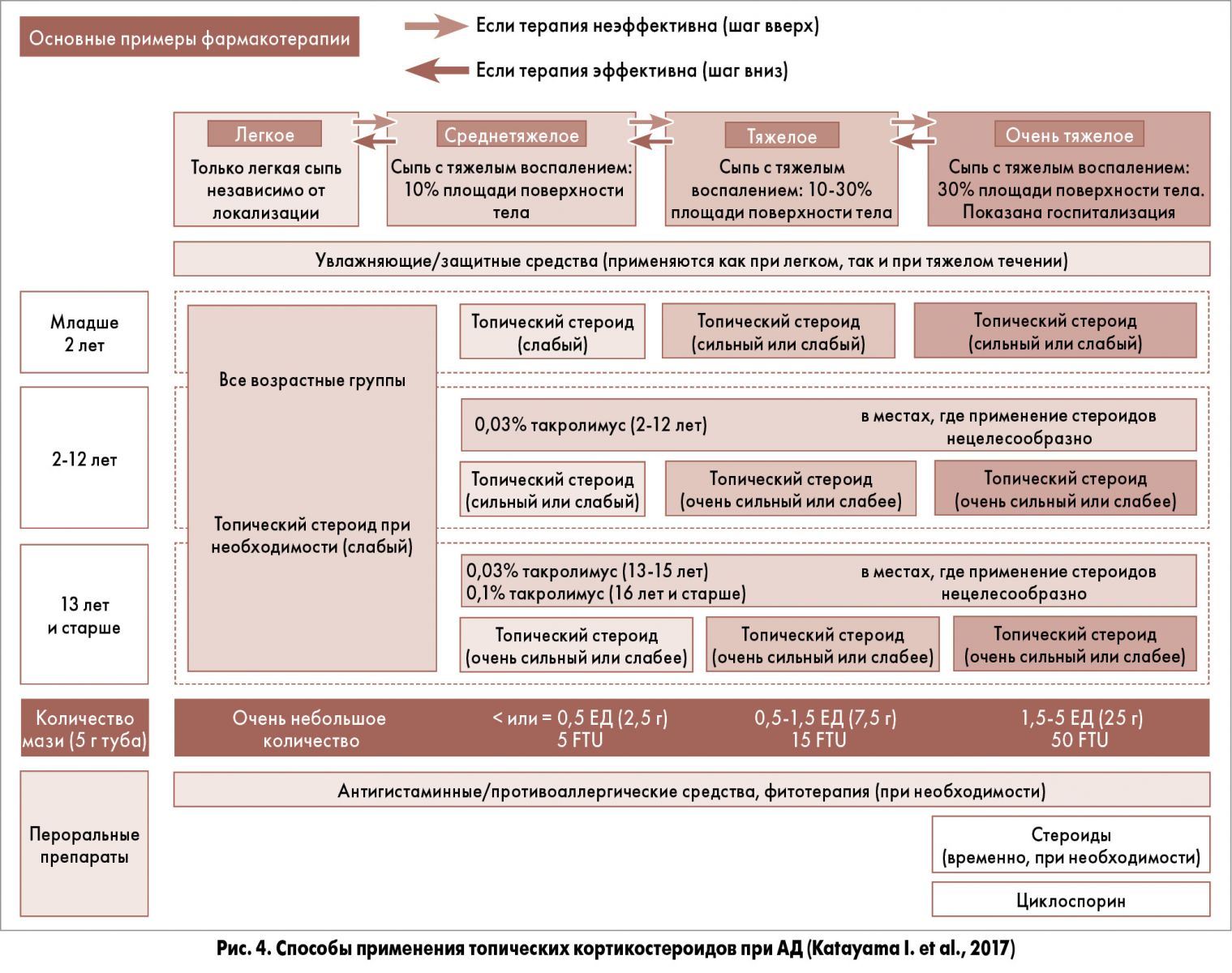 Топические стероиды. Указывая на необходимость применения сильных ТС при тяжелом и очень тяжелом течении АД, представители JSA рекомендуют придерживаться следующей тактики (рис. 4).
Топические стероиды. Указывая на необходимость применения сильных ТС при тяжелом и очень тяжелом течении АД, представители JSA рекомендуют придерживаться следующей тактики (рис. 4).
Следует избегать нанесения ТС на участки тела, обладающие высокими абсорбционными свойствами (шею, лицо); в случаях их вынужденного использования длительность терапии должна быть минимальной и предполагать быструю последующую замену мазью такролимуса. Следует проводить контрольные осмотры каждые 1-2 нед после начала применения ТС для раннего выявления побочных эффектов и своевременной коррекции дозы препарата.
Оптимальное количество препарата, содержащего ТС, определяется при помощи правила фаланги пальца (finger tip unit, FTU, – единица, равная кончику пальца). Количество необходимых единиц FTU зависит от возраста пациента, тяжести течения АД. Одна доза FTU – это такое количество мази, которое выдавливается из тубы диаметром 5 мм на дистальную ладонную поверхность указательного пальца взрослого, и эквивалентна приблизительно 0,5 г. Одна доза FTU может покрыть две ладони взрослого (2% площади поверхности тела). Количество мази, необходимой для покрытия всего тела, составляет 50 FTU, или 25 г.
Японские ученые считают клиническую эффективность сильных и очень сильных ТС практически сопоставимой и рекомендуют сначала назначать сильный ТС 2 р/сут, а затем, при достижении ремиссии, перейти на однократный прием препарата в течение суток. Данный подход позволит увеличить приверженность пациентов к лечению, уменьшить вероятность возникновения побочных эффектов и снизить стоимость терапии. Эксперты рекомендуют максимально доступно объяснять пациентам нюансы применения ТС и настаивать на недопустимости самостоятельного изменения схемы и дозы принимаемого препарата. В случае обострения заболевания, вызванного самовольной отменой / изменением дозы ТС, следует возобновить аппликации ТС с использованием адекватной дозы и кратности нанесения препарата. Если невыполнение рекомендаций врача повлекло системное обострение АД, пациента следует госпитализировать и назначить пероральные системные кортикостероиды (при необходимости).
Топические иммуносупрессанты (мазь такролимуса). Мазь такролимуса назначается, если проводимая терапия ТС недостаточно эффективна или невозможна в связи с появлением значимых побочных эффектов.
Такролимус для местного применения (Протопик) выпускается в двух формах: 0,1% мазь (назначается пациентам ≥16 лет) и 0,03% мазь (применяется у детей 2-15 лет). Механизм действия такролимуса заключается в ингибировании функции Т-лимфоцитов, играющих основную роль в развитии аллергического воспаления и изменении барьерной функции кожи. Как правило, мазь такролимуса наносится на проблемные участки 1 р/сут после купания. Максимальная частота применения этого препарата – 2 р/сут, в таких случаях рекомендуемый интервал между аппликациями составляет 12 ч. Эксперты советуют назначать 0,1% мазь такролимуса взрослым в дозе ≤5 г; доза 0,03% мази у детей 2-5 лет (<20 кг) составляет <1 г; у детей 6-12 лет (20-50 кг) – 2-4 г, у лиц ≥13 лет (>50 кг) – <5 г. При наружном применении этого препарата следует избегать чрезмерного воздействия ультрафиолетового света; также не рекомендуется использование окклюзионных повязок, поскольку они могут увеличивать концентрацию действующего вещества в крови.
Японские специалисты считают мази такролимуса относительно безопасными: постмаркетинговое исследование безвредности их длительного применения не выявило существенных побочных действий. Однако эксперты обращают внимание на тот факт, что наружные аппликации такролимуса могут ассоциироваться с появлением ощущения жжения и вероятным развитием локального инфекционного процесса. Несмотря на то что стимулирующий эффект мази нивелируется самостоятельно через несколько дней, уменьшить интенсивность жжения можно при помощи заблаговременного нанесения (перед аппликацией мази) увлажняющего средства или кратковременного сочетанного применения мази такролимуса и ТС. Следует избегать одновременного нанесения такролимуса и других наружных средств, так как это может привести к изменению стабильности и абсорбционных свойств мази, содержащей ингибитор кальциневрина. Мазь такролимуса нельзя наносить на эрозированные поверхности по причине ее стимулирующего действия и абсорбции; такролимус противопоказан пациентам с ихтиозоформной эритродермией (синдром Нетертона), пациентам с нефропатией, беременным женщинам, детям <2 лет и больным, получающим фототерапию. Эксперты JSA подчеркивают, что наружные аппликации мази такролимуса не сопровождаются ростом заболеваемости лимфомой и раком кожи.
Топические нестероидные противовоспалительные препараты. В настоящее время отсутствуют убедительные данные доказательной медицины, подтверждающие эффективность нестероидных противовоспалительных препаратов в лечении экзематозных поражений при АД. Американское и Европейское руководства по лечению АД также не предполагают применения этих препаратов у больных АД.
Пероральная терапия
Антигистаминные/противоаллергические препараты. Японские специалисты предусматривают возможность назначения данных лекарственных средств, поскольку их применение позволяет уменьшить интенсивность зуда.
Пероральные кортикостероиды. Принимая во внимание большой спектр разнообразных побочных действий, присущих системным кортикостероидам, эксперты рекомендуют избегать длительного приема этих препаратов. По мнению I. Katayma и соавт., оптимальная доза преднизолона у взрослых больных составляет 10-15 мг/сут; он может назначаться в комбинации с антигистаминными или противоаллергическими препаратами.
Иммуносупрессанты. С 2008 г. циклоспорин разрешен для лечения АД в Японии. Циклоспорин может назначаться пациентам ≥16 лет, резистентным к проводимой терапии с обязательным 3-месячным отмывочным периодом перед его назначением. Этот препарат, как правило, назначают 2 р/сут в дозе 3-5 мг/кг/сут; длительность терапии должна быть минимальной (≤12 нед).
Ichiro Katayama. Japanese guidelines for atopic dermatitis 2017. Allergology International 66 (2017) 230e247. http://dx.doi.org/10.1016/
j.alit.2016.12.003.
Подготовила Лада Матвеева
Медична газета «Здоров’я України 21 сторіччя» № 4 (425), лютий 2018 р.


