18 березня, 2018
Цирроз печени и гепатоцеллюлярная карцинома: эффективная профилактика глицирризином
Фиброз печени представляет собой сложный фиброгенный и воспалительный процесс, который развивается на фоне длительного воздействия различных этиологических факторов: инфекции (вирусные гепатиты), метаболических нарушений (неалкогольная жировая болезнь печени), токсинов (алкогольная жировая болезнь печени), а также аутоиммунной патологии (первичный билиарный холангит, аутоиммунный гепатит, первичный склерозирующий холангит) – и является первым шагом в прогрессировании заболевания и развитии цирроза печени (ЦП).
ЦП – широко распространенное во всем мире заболевание – совместно с последующей портальной гипертензией, печеночной энцефалопатией и/или печеночной недостаточностью увеличивает вероятность развития гепатоцеллюлярной карциномы (ГЦК), которая является основополагающей причиной печеночной недостаточности и летального исхода. Несмотря на эффективную этиотропную противовирусную терапию, у многих пациентов явления фиброза и ЦП сохраняются; аналогичная ситуация наблюдается при хронических заболеваниях печени невирусного генеза. Поэтому риск возникновения осложнений, свойственных ЦП, в том числе – ГЦК, остается чрезвычайно высоким.
На протяжении двух последних десятилетий во всем мире отмечается увеличение количества летальных исходов, ассоциированных с ГЦК: ежегодно от ГЦК умирает более 600 тыс. человек (Ferenci Р. et al., 2009), а диагностируется 78 200 новых случаев (Masao А. et al., 2017). Прогноз у больных ГЦК крайне неблагоприятный – общая летальность при данном заболевании превышает 95%.
Эпидемиология и факторы риска ЦП и ГЦК
В обновленном практическом руководстве по лечению ГЦК (2017), подготовленном экспертами Азиатско-Тихоокеанской ассоциации по изучению заболеваний печени (Asian Pacific Association for the Study of the Liver, APASL), подчеркивается связь между инфицированием вирусом гепатита В (HBV) и/или С (HСV), а также ЦП и прогрессирующим фиброзом печени. Наиболее часто ГЦК страдают жители стран Восточной Азии, а также Центральной и Западной Африки, при этом первичный рак печени чаще диагностируют у мужчин, чем у женщин (соотношение 2:1 или 4:1).
ЦП любой этиологии считается одним из наиболее значимых факторов риска развития ГЦК: необратимое замещение паренхимы печени фиброзной соединительной тканью диагностируют у 70-90% пациентов с первичным раком печени. В практическом руководстве Всемирной гастроэнтерологической организации (ВГО) по ГЦК (Ferenci Р. et al., 2009), а также в руководстве APASL (2017) указывается, что вероятность возникновения ГЦК у пациентов с хронической HBV-инфекцией в 10-100 раз (в зависимости от использованных диагностических маркеров и популяций, подвергшихся скринингу) превышает таковую у неинфицированных лиц. Относительный риск (ОР) развития ГЦК у больных с серологически подтвержденной HСV-инфекцией возрастает в 17 раз; коинфекция HBV/HСV также ассоциируется с высокой вероятностью формирования ГЦК.
К значимым факторам риска развития ГЦК эксперты APASL и ВГО отнесли злоупотребление алкоголем (ежедневный прием >80 г алкоголя на протяжении >10 лет ассоциирован с 5-кратным возрастанием риска) и курение (вероятность возникновения ГЦК у курильщиков в 1,5 раза превышает таковую у лиц, некурящих в настоящее время). Установлена взаимосвязь между дозой принятого алкоголя и развитием первичного рака печени: ежедневное употребление 25, 50 и 100 г алкоголя сопровождается возрастанием ОР ГЦК в 1,19 (95% ДИ 1,12-1,27), 1,40 (95% ДИ 1,25-1,56) и 1,81 (95% ДИ 1,50-2,19) раза соответственно (Corrao G. et al., 2004). В то же время А. Masao и коллеги (2017) приводят факты, подтверждающие превентивные свойства кофе и чая: употребление этих напитков снижает риск ГЦК на 40% (р<0,05) и 23% (р>0,05) соответственно.
Относительно недавно перечень факторов риска ГЦК пополнили ожирение, сахарный диабет 2 типа, неалкогольная жировая болезнь печени. В метаанализе 17 исследований, в которых приняли участие больные с избыточной массой тела (n=5037) и ожирением (n=6042), установлено, что при наличии лишних килограммов риск ГЦК возрастает на 17%, а при сопутствующем ожирении – на 89% по сравнению с лицами, имеющими нормальную массу тела (Larsson S. et al., 2007). В настоящее время неалкогольный стеатогепатит (НАСГ) считается одним из значимых факторов риска развития ГЦК. Эксперты APASL подчеркивают, что в течение 2002-2012 гг. количество пациентов, перенесших трансплантацию печени по поводу НАСГ-индуцированной ГЦК, возросло практически в 4 раза, тогда как число больных с HCV-ассоциированным раком печени увеличилось только в 2 раза.
На протяжении последних лет все чаще появляются доказательства того, что ГЦК может возникать даже при отсутствии ЦП. Высказываются предположения, что ожирение, инсулинорезистентность и провоспалительные изменения, присущие НАСГ, могут непосредственно спровоцировать развитие ГЦК. Например, ученые, анализировавшие особенности ее возникновения (n=1419) у больных НАСГ (n=120), хронической HСV-инфекцией (n=1013), пациентов с алкогольной зависимостью (n=286), подчеркивают, что ЦП обнаружен только у 58% больных НАСГ-ассоциированной ГЦК.
Высока вероятность возникновения ГЦК при наличии другой гепатобилиарной патологии, такой как гемохроматоз в сочетании с ЦП (ОР развития рака печени возрастает в 20 раз), синдром Бадда-Киари (распространенность ГЦК при этой патологии колеблется от 2,0 до 51,6%), аутоиммунный гепатит с ЦП, болезнь Вильсона-Коновалова, первичный билиарный холангит.
Лечение и профилактика
Подходы к лечению ГЦК зависят от стадии заболевания на момент установления диагноза и доступности комплексных методов лечения. К сожалению, в далеко зашедших стадиях заболевание является некурабельным, его ведение достаточно дорогостоящее и эффективно только в отношении увеличения показателя «качество обеспеченных годов жизни» (Ferenci Р. et al., 2009). В большинстве случаев такие хирургические методы лечения, как резекция, радиочастотная абляция или трансплантация печени, не осуществимы, что подчеркивает важность первичной и вторичной профилактики. В настоящее время в таких случаях все чаще обращаются за помощью к препаратам природного происхождения, обладающим противовоспалительным, антиоксидантным и антифибротическим действием. Одним из таких препаратов является глицирризин (глицирризиновая кислота), получаемый из корня солодки.
Биологические эффекты глицирризина
Глицирризин и его производные (глицирретовая кислота, глицирризат аммония и др.) обладают различными биологическими эффектами, включая гепатопротекторное, антиульцерогенное, противовоспалительное, противовирусное и антиканцерогенное свойства. Противовоспалительное действие глицирризина связывают с его способностью ингибировать 11β-оксистероиддегидрогеназу, что способствует накоплению в организме эндогенного кортизола (т. н. псевдокортикостероидный эффект). Кроме того, глицирризин оказывает стимулирующее действие на кортикостероидные рецепторы, ингибирует фосфолипазу А2, угнетает синтез медиаторов воспаления, уменьшает экспрессию макрофагального воспалительного белка (MIP-1α) на клетках Купфера, ингибирует активацию ядерного фактора NF-κB, снижает активность ЦОГ-2 (Rino Y. et al., 2015) и стимулирует синтез ряда противовоспалительных цитокинов. Доказано, что глицирризин уменьшает структурные повреждения митохондрий гепатоцитов, активирует процессы β-окисления в митохондриях, увеличивает экспрессию карнитинпальмитоилтрансферазы (Korenaga М. et al., 2011).
Антиоксидантное действие обусловлено способностью глицирризина блокировать свободные радикалы кислорода и снижать уровень индуцируемой синтазы оксида азота; антифибротические свойства связаны с подавлением экспрессии гена коллагена I типа и угнетением его синтеза звездчатыми клетками печени (Буеверов А. О., 2014).
Противовирусная активность глицирризина заключается в ингибировании репликации вирусов и регуляции иммунных реакций: это производное солодки влияет на клеточные сигнальные пути (протеинкиназа С и казеинкиназа 2) и факторы транскрипции (активирующий белок-1 и ядерный фактор NF-κB). Доказано противовирусное действие глицирризина в отношении вируса простого герпеса 1 типа, вирусов гепатита А, В и С (Van Rossum Т. et al., 2015). Имеются убедительные доказательства цитопротекторного (достоверно снижает активность трансаминаз и лактатдегидрогеназы, ингибирует активацию фосфолипазы А2) и иммуномодулирующего (улучшает иммунологический статус пациентов, инфицированных HBV, изменяет иммуногенетические свойства HBsAg) эффектов глицирризина (Van Rossum Т. et al., 2015).
Антиапоптотическое действие глицирризина связывают с супрессией ФНО-α, каспазы-3, а также ядерного негистонового белка с высокой подвижностью (HMGB1), продуцируемого клетками Купфера. G. Gwak и соавт. (2012) доказали, что глицирризин предупреждает HMGB1-индуцированное высвобождение цитохрома С и активацию р38 в культуре клеток человеческой ГЦК – Huh-BAT. По мнению C. Hsiang и соавт. (2015), угнетение активности NF-κB, происходящее под воздействием глицирризина, обусловливает супрессию генов апоптоза и оксидативного стресса.
В ряде экспериментальных исследований зафиксированы антиканцерогенные свойства глицирризина, объясняемые многими учеными с позиций аутофагии (свойства живых организмов удалять поврежденные/стареющие органеллы и длительно живущие циркулирующие белки для обеспечения стабильности клеток). Большое значение в процессе аутофагии отводится клеточному сигнальному пути mTOR и киназе ERK1/2: они играют значимую роль в генезе различных опухолевых клеток, в том числе ГЦК (Zhang Х. et al., 2017). Известно, что под контролем mTOR находится фосфорилирование основных факторов, инициирующих процессы трансляции; именно сигнальный путь mTOR обеспечивает необходимое повышение синтеза белка при получении клеткой митогенного или антиапоптотического сигнала. Поэтому блокирование сигнального пути mTOR и активности ERK1/2 позволяет достичь трех основных задач: снизить скорость роста опухоли, увеличить чувствительность опухолевых клеток к химио- и лучевой терапии, преодолеть приобретенную резистентность новообразований к действию таргетных препаратов. По данным Х. Zhang и соавт. (2017), глицирризин эффективно ингибирует активность mTOR и ERK1/2 при ГЦК. Z. Tang и соавт. (2015) подчеркивают, что производные корня солодки обладают и другими выраженными антиканцерогенными свойствами: ингибируют пролиферацию клеток, индуцируют остановку клеточного цикла, стимулируют дифференцировку клеток, угнетают скорость метастазирования и неоангиогенеза.
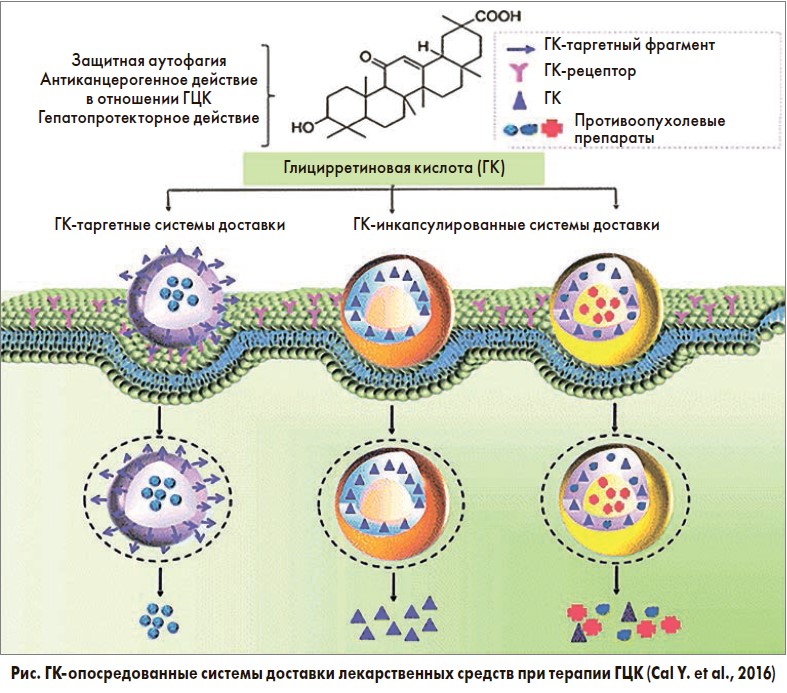 Наличие таких выраженных противоопухолевых свойств обусловило использование глицирризиновой и глицирретиновой кислот (ГК) в качестве систем доставки лекарственных средств, использующихся для лечения ГЦК, включая липосомы, мицеллы и наночастицы (рис.).
Наличие таких выраженных противоопухолевых свойств обусловило использование глицирризиновой и глицирретиновой кислот (ГК) в качестве систем доставки лекарственных средств, использующихся для лечения ГЦК, включая липосомы, мицеллы и наночастицы (рис.).
На ГК-модифицированные системы доставки лекарственных средств возлагают большие надежды по увеличению эффективности лечения ГЦК, поскольку последние обладают чрезвычайно благоприятными фармакокинетическими свойствами и положительными эффектами на гепатоциты (Cai Y. et al., 2016).
Результаты клинических и экспериментальных исследований
Клиническая эффективность глицирризина подтверждена во многих клинических и экспериментальных исследованиях. Комбинация глицирризина с глицином и цистеином давно и успешно используется в Японии в лечении гепатитов различного генеза (Rino Y. et al., 2015).
Российские ученые во главе с А. О. Буеверовым (2014) успешно использовали экстракт корня солодки в лечении больных хроническим вирусным гепатитом С (ВГС). Всем больным, принявшим участие в исследовании, назначали противовирусную терапию (ПВТ) интерфероном α и рибавирином, а некоторым дополнительно рекомендовали глицирризин. Режим аддитивного применения глицирризина предполагал внутривенное (в/в) введение препарата (2,5 г/сут 5 р/нед) перед назначением ПВТ, а также на протяжении первых 4 нед ПВТ с последующим переходом на прием пероральной формы вплоть до завершения курса ПВТ. Оказалось, что глицирризин способствовал достоверному снижению средних значений аланинаминотрансферазы (АЛТ) уже после 4 нед монотерапии этим препаратом (до назначения ПВТ), тогда как у больных, получавших только ПВТ, достичь такого эффекта удалось только после 2 нед приема интерферона и рибавирина. Кроме того, терапия глицирризином ассоциировалась с улучшением гистологической картины печени: результаты биопсии печени, проведенной через 24 нед после завершения ПВТ, подтвердили положительную динамику индекса гистологической активности в обеих группах, которая достигла статистической значимости только у пациентов, получавших глицирризин (р<0,05). Аналогичная ситуация зафиксирована в отношении фиброза печени: выраженность фибротических изменений достоверно снизилась у пациентов, получавших аддитивную терапию глицирризином, в отличие от больных, принимавших только противовирусные препараты.
Не менее интересна работа М. Manns и соавт. (2012): ученые назначали глицирризин больным хроническим активным ВГС, не ответившим на терапию интерфероном и рибавирином. Оказалось, что схема лечения, предполагавшая 5- и 3-разовое введение глицирризина, способствовала ≥50% снижению уровня АЛТ после 12 нед терапии у большего количества пациентов (28,7 и 29,0% соответственно) по сравнению с плацебо (7,0%; р<0,00001). Спустя 52 нед лечения активность некровоспалительного процесса значительно уменьшилась у 44,9 и 46,0% больных, получавших инъекции глицирризина 5 и 3 р/нед соответственно. Терапия глицирризином способствовала уменьшению выраженности фиброза (≥1 балл) у 37,2 и 28,6% пациентов, принимавших глицирризин 5 и 3 р/нед соответственно.
Выявленные уникальные свойства глицирризина оказались особенно значимы для больных ЦП с высокой активностью цитолитических процессов. Т. Kazuo и соавт. (1999) доказали, что у пациентов с гистологически подтвержденным HCV-ассоциированным ЦП и высоким уровнем АЛТ (≥80 МЕ/л) в течение >5 лет ГЦК развивалась в 71,4% случаев, тогда как при низкой активности цитолиза (АЛТ <80 МЕ/л) за этот период времени рак печени возникал у 25% больных. Ожидаемый временной интервал с момента диагностики ЦП до развития ГЦК при высоких значениях АЛТ составлял 6,0±0,7 года, а при низкой активности АЛТ – 12,7±1,2 года (р<0,001). Поэтому для больных ЦП очень важна минимальная активность цитолитического синдрома, чего можно достичь назначением глицирризина.
Y. Arase и коллеги (1997), авторы ретроспективного исследования, установили, что профилактический прием глицирризина уменьшает ОР развития ГЦК у больных хроническим гепатитом различного генеза. К такому выводу исследователи пришли, проанализировав течение заболевания у пациентов, принимавших указанный гепатопротектор (n=84; 100 мл/сут на протяжении 8 нед, затем 2-7 р/нед в течение 2-16 лет; медиана наблюдения – 10,1 года) и не получавших глицирризин (n=109; медиана наблюдения – 9,2 года). Оказалось, что кумулятивная частота возникновения ГЦК в течение 10 лет при использовании глицирризина составила 7%, в группе сравнения – 12%, значения этого показателя через 15 лет в рассматриваемых группах были равны 12 и 25% соответственно. Таким образом, глицирризин в 2,49 раза снижал ОР развития ГЦК.
Подобные данные получили К. Ikeda и соавт. (2007), проанализировавшие вероятность возникновения ГЦК у больных хроническим ВГС, резистентным к интерферону, с/без сопутствующего ЦП (n=1249). В подгруппе больных с высоким (≥2 верхних границ нормы) уровнем АЛТ (n=346) 244 пациента получали инъекции глицирризина. Спустя 5 лет ГЦК диагностирована у 13,3% больных, принимавших гепатопротектор, и у 26,0% участников, не пользовавшихся глицирризином (р<0,05); через 5 лет эти показатели составили 21,5 и 35,5% соответственно (р=0,021). Терапия глицирризином достоверно снижала вероятность появления ГЦК (ОР 0,49; 95% ДИ 0,27-0,86; р=9,014) у больных хроническим активным ВГС.
Эффективность длительной терапии глицирризином анализировалась в многоцентровом двойном слепом исследовании, в котором приняли участие больные хроническим ВГС, не ответившие на терапию интерфероном, а также пациенты, имевшие противопоказания к назначению данного противовирусного препарата (Kumada Н. et al., 2002). Участников рандомизировали для приема глицирризина (n=178) или плацебо (n=109). Низкие суточные дозы глицирризина (40 мл/сут на протяжении 4 нед) способствовали нормализации уровня АЛТ (р<0,001), более длительный прием стандартных доз (100 мл/сут в течение 8 нед) ассоциировался не только с уменьшением активности цитолиза, но и с улучшением гистологической картины печени (n=40). На протяжении 13 лет ЦП реже развивался у пациентов, принимавших глицирризин, по сравнению с контролем (28 vs 40%; р<0,002); ГЦК чаще диагностировали в контрольной группе, чем в группе гепатопротекторной терапии (25 vs 13% соответственно; р<0,002; длительность наблюдения – 15 лет). Основываясь на полученных данных, ученые утверждают, что длительная терапия глицирризином предупреждает развитие ГЦК у пациентов с хроническим ВГС.
Особое внимание следует уделить экспериментальной работе Т. Wakamatsu и соавт. (2007): исследователи анализировали уровень экспрессии белков, ассоциированных с множественной лекарственной устойчивостью (MRP) и определяющих резистентность к цисплатину (препарату, использующемуся для химиотерапии ГЦК) в культуре клеток ГЦК – Huh7. Ученые зафиксировали высокую резистентность клеток линии Huh7 к цисплатину: она в 14,1 раза превышала таковую в линии клеток ГЦК дикого типа. Отмечено значительное усиление экспрессии мРНК MRP2 (в 6,29 раза), MRP3 (3,2 раза), MRP4 (11,3 раза) и MRP5 (3,39 раза) в культуре клеток Huh7 по сравнению с клетками ГЦК дикого типа. Комбинация цисплатина с глицирризином/ламивудином значительно снижала жизнеспособность резистентных клеток по сравнению с монотерапией цисплатином (76,8 vs 79,5% соответственно). Одновременный прием цисплатина, глицирризина и ламивудина позволял уменьшить жизнеспособность Huh7-клеток до 65,1%. Внутриклеточное содержание цисплатина в резистентных клетках составляло 36,4%, тогда как в клетках ГЦК дикого типа оно возрастало до 47,7; 48,4 и 60% при дополнительном введении глицирризина, ламивудина или их комбинации соответственно. Основываясь на полученных данных, ученые резюмировали: «Высокая экспрессия MRP2, MRP3, MRP4 и MRP5 ассоциирована со снижением концентрации цисплатина в цисплатинрезистентных клетках ГЦК; глицирризин
и/или ламивудин способствуют накоплению химиопрепарата в резистентных клетках, препятствуя оттоку цисплатина из них; комбинированная терапия глицирризином и цисплатином обладает модуляторными свойствами и способствует преодолению резистентности к цисплатину».
Наличие убедительной доказательной базы позволило представителям Японского общества гастроэнтерологов в практическом руководстве по лечению ГЦК (2013) сформулировать следующее положение:
- в/в введение глицирризина рекомендуется для профилактики ГЦК у пациентов с хроническим ВГС (степень доказательности В).
Гепаризин
В настоящее время отечественные специалисты могут воспользоваться накопленным мировым опытом в отношении первичной и вторичной профилактики цирроза и гепатоцеллюлярной карциномы печени при помощи глицирризина – на украинском фармацевтическом рынке появился препарат Гепаризин («Валартин Фарма»). Он имеет две формы выпуска (капсулы, ампулы), которые используются для перорального или парентерального введения соответственно. Помимо глицирризина (25 и 40 мг соответственно), в капсулах и ампулах содержится глицин (25 и 400 мг), а также метионин (25 мг, капсулы) или
L-цистеин (20 мг, ампулы). Дополнительное введение этих аминокислот неслучайно: наличие глицина в составе Гепаризина позволяет предупредить возникновение побочных эффектов при длительной терапии и усилить антиоксидантное действие, а включение цистеина/метионина – инактивировать свободные радикалы и улучшить переносимость препарата. Более высокая концентрация действующих веществ, использующаяся в ампулах, позволяет применять двухступенчатую схему терапии Гепаризином: добиться насыщающей дозы посредством парентерального введения препарата, а затем максимально раскрыть антифибротический потенциал Гепаризина при помощи длительного перорального приема.
Гепаризин оказывает гепатопротекторное, противовоспалительное, антифибротическое, антиоксидантное, антиканцерогенное, противовирусное и иммуномодулирующее действие. Гепаризин рекомендован для эффективной и безопасной профилактики/лечения фиброза печени, ЦП и ГЦК.
Список литературы находится в редакции.
Подготовила Татьяна Можина
Медична газета «Здоров’я України 21 сторіччя» № 4 (425), лютий 2018 р.


