5 квітня, 2018
Забезпеченість організму дітей дошкільного віку довголанцюговими поліненасиченими жирними кислотами і можливості корекції їх дефіциту
Огляд літературних даних та результати власного дослідження
Являясь единственным источником веществ, из которых строятся клетки организма человека,
пища во многом определяет состояние его здоровья и продолжительность жизни.
Известно, что для нормальной жизнедеятельности организма в ежедневном
пищевом рационе необходимо около 600 питательных компонентов,
что соответствует применению 32 наименований пищевых продуктов.
С.А. Батечко, Н.А. Деревянко (2006)
Поліненасичені жирні кислоти, низка яких належить до незамінних складників харчування, є одними з найважливіших мікронутрієнтів, що забезпечують нормальний розвиток організму і підтримку балансу між фізіологічними і патологічними процесами в ньому [1, 2, 45]. Поліненасиченими є жирні кислоти з двома і більше подвійними зв’язками між вуглецевими атомами. Довголанцюгові поліненасичені жирні кислоти (ДПНЖК) становлять собою аліфатичні вуглеводні ланцюги, що містять 18 і більше атомів вуглецю і 2 або більше подвійних зв’язки.
Частина поліненасичених жирних кислот може синтезуватися у клітині з насичених, проте у зв’язку з відсутністю в організмі людини ферментів, здатних формувати подвійні зв’язки далі 9-го атома вуглецю від карбоксильного залишку, деякі ДПНЖК є незамінними для людини. Найбільш вивчені ДПНЖК сімейств ω‑3 і ω‑6, вони відрізняються як за походженням, так і за впливом на організм. Важливість надходження цих жирних кислот для організму зумовлена тим, що в процесі еволюції здатність до їх синтезу у ссавців, у тому числі у людини, була втрачена. Омега-3 ДПНЖК виробляються морськими водоростями і планктоном, що є їжею для риб та морських тварин, через що основними джерелами ейкозапентаєнової кислоти – ЕПК (6-10%) і докозагексаєнової кислоти – ДГК (10-15%) для людини є риба й риб’ячий жир.
 У рослинних жирах представлена в основному α-ліноленова кислота: у лляній олії її вміст становить 35-65%, у гірчичній – 30-42%, конопляній – 14-28%, соєвій олії – 5-14%, в олії зародків пшениці – 4-10%. Для профілактики у здорових дітей добова доза ЕПК і ДГК становить близько 300 мг (190-300 мг), що відповідає наявності в раціоні риби (жирні сорти) не менш ніж 2 рази на тиждень.
У рослинних жирах представлена в основному α-ліноленова кислота: у лляній олії її вміст становить 35-65%, у гірчичній – 30-42%, конопляній – 14-28%, соєвій олії – 5-14%, в олії зародків пшениці – 4-10%. Для профілактики у здорових дітей добова доза ЕПК і ДГК становить близько 300 мг (190-300 мг), що відповідає наявності в раціоні риби (жирні сорти) не менш ніж 2 рази на тиждень.
За неможливості вживання риби (алергічні реакції, смакові переваги) як альтернативу можна розглядати рослинні продукти з адекватною кількістю α-ліноленової кислоти, 0,5-20% якої метаболізується в ЕПК [54], або використання якісних препаратів, що містять ω-3 ДПНЖК [3, 45, 49]. ДПНЖК ω‑6 у достатній кількості надходять в організм людини з рослинною їжею: вони містяться практично у всіх видах олії і горіхах.
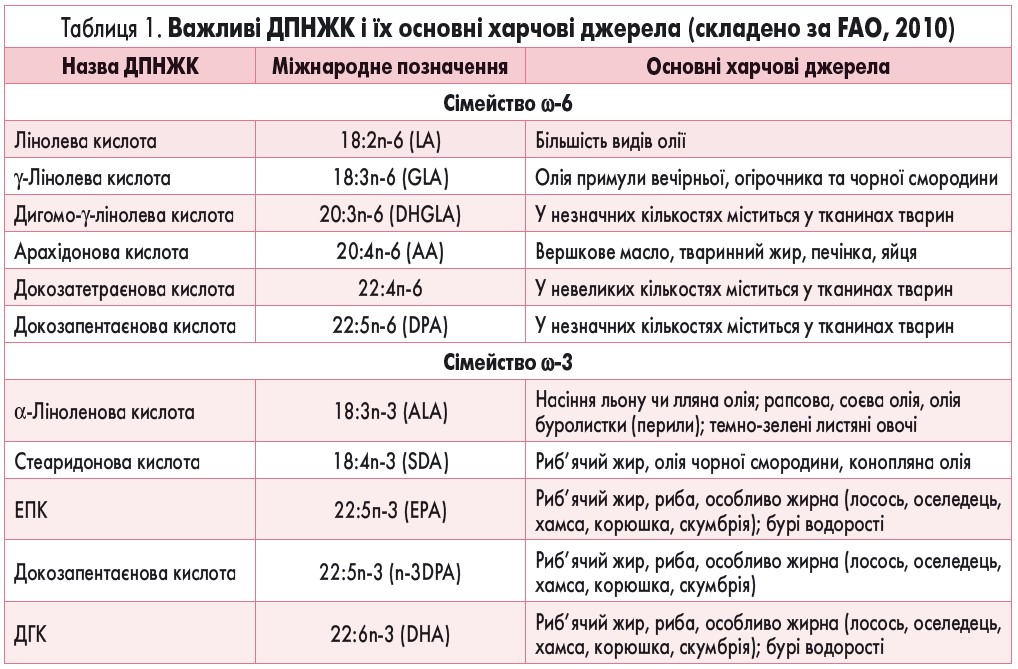
Докозапентаєнова кислота наявна у рибі, м’ясі ссавців і птахів. Важливими за нутритивною дією ДПНЖК, згідно з останніми рекомендаціями міжнародної Продовольчої та сільськогосподарської організації ООН (Food and Agriculture Organization, FAO), слід вважати ще низку менш вивчених ДПНЖК (табл. 1) [5]. До незамінних належать лінолева (18: 2n‑6; LA), α-ліноленова (18: 3n‑3; ALA) кислоти, а також ДГК [5].
Недостатнє споживання есенціальних жирних кислот нині розглядається як фактор, що сприяє формуванню різних видів патології [46, 51, 52]. Результати проведених популяційних досліджень свідчать про недостатнє споживання продуктів, що містять поліненасичені жирні кислоти [6, 7], у тому числі у регіонах, де традиційно споживають багато морепродуктів.
Незамінні жирні кислоти в організмі зазнають подальших перетворень: наприклад, ЕПК і ДГК можуть утворюватися з α-ліноленової кислоти, а арахідонова – з лінолевої. ДПНЖК ω‑3 не можуть конвертуватися в жирні кислоти сімейства ω‑6 і навпаки. У результаті жирні кислоти двох сімейств конкурують за одні й ті самі ферменти, які здійснюють елонгацію і десатурацію [8, 47].
При «західному» типі харчування (при якому 80-90% поліненасичених жирних кислот раціону представлені ω‑6, α-лінолевою кислотою) надмірне надходження з їжею ДПНЖК сімейства ω‑6 призводить до перевищення можливості дельта‑6-десатурази, у результаті чого обмежується синтез ДПНЖК ω‑3 – похідних α-ліноленової жирної кислоти.
При цьому α-лінолева кислота накопичується у крові і тканинних ліпідах. Відповідно для оптимізації балансу ДПНЖК в організмі необхідна не тільки дотація жирних кислот класу ω‑3, а й зменшення споживання жирів із високим умістом ω‑6 жирних кислот [9, 47].
Забезпеченість організму активними ДПНЖК залежить не тільки від надходження їх попередників або безпосередньо самих кислот з їжею, а й від активності десатураз, що зумовлено генетично.
Численні біологічні ефекти ДПНЖК можна умовно розділити на дві групи: перша – ефекти, пов’язані з метаболічною активністю кислот; друга – пластичні ефекти, які зумовлені участю кислот у структурній організації клітини. Метаболічна роль ω‑3 і ω‑6 визначається різноманітністю біологічно активних речовин, що утворюються у процесі їх трансформації в організмі.
! Так, ω‑3 і ω‑6 ДПНЖК є попередниками ейкозаноїдів, сигнальних гормонів з різною біологічною активністю, молекул з прозапальною, протизапальною, антитромботичною, вазоконстрикторною і вазодилатаційною активністю [3, 10, 11, 47].
Арахідонова кислота, як правило, в достатній кількості надходить в організм із тваринною їжею. При надмірному вживанні арахідонової кислоти підвищується її рівень у складі фосфоліпідів мембран клітин кишечнику, що збільшує утворення простагландину Е2. ДГК, на противагу арахідоновій кислоті, пригнічує вироблення простагландину Е2, а також продукцію прозапальних інтерлейкінів‑6, ‑8, ‑12, фактора некрозу пухлини.
Слід зазначити, що ДГК, на відміну від арахідонової кислоти, становить лише невелику частку від загальної кількості жирних кислот, які містяться у тканинах. Винятком є структури мозку та сітківки ока, що відображає активну участь ДГК у метаболізмі та структурній організації тканин цих органів.
Пластична функція ДПНЖК полягає в тому, що вони є ключовими структурними компонентами фосфоліпідів, вбудованих як у клітинні, так і у внутрішньоклітинні мембрани, та визначають цілу низку властивостей біологічних мембран, зокрема їх плинність.
Це, у свою чергу, впливає на функції всіх без винятку клітин організму. У клітинах і тканинах ДПНЖК зустрічаються не у вільному стані, а в складі ліпідів різних класів: тріацилгліцеролів (тригліцеридів), фосфогліцеридів (фосфоліпідів), кардіоліпіну, сфінголіпідів, ефірів стеролів і жирних кислот (наприклад, ефіри холестерину, воску).
Зрештою жирнокислотний склад біомембран впливає на їх електрофізіологічні властивості [12], чим, мабуть, і визначається необхідність великої кількості арахідонової кислоти і ДГК в органах, які проявляють високу електрофізіологічну активність, – у мозку і сітківці ока.
! Вивчення численних функцій ДПНЖК дало підстави останнім часом вважати їх достатнє споживання одним із найважливіших факторів, що визначає здоров’я дитини та значно впливає на дозрівання, розвиток і функціонування нервової системи і зорового аналізатора.
Відомо, що ліпіди становлять близько 60% сухої речовини мозку, 20% загального вмісту жирних кислот у складі фосфоліпідів головного мозку припадає на арахідонову кислоту і ДГК. Найвищий вміст ДПНЖК у мембранах нервових клітин [13]. На відміну від циркулюючої крові, де вміст ДПНЖК ω‑6 у 10 разів вищий, ніж ω‑3, у нервових клітинах, а також у сітчастій оболонці ока, навпаки, вища концентрація ДГК. І саме ДГК переважає у невральних синапсах [14, 15].
У фосфоліпідах мембран сітківки ока близько 60% ДПНЖК представлені ДГК, що пов’язано з її участю в фоторецепції через активацію зорового пігменту родопсину [13, 16].
! ДПНЖК беруть участь у таких процесах, як нейрогенез, синаптогенез, міграція нейронів, мієлінізація нервових волокон, що забезпечує нормальний розвиток сенсорних, моторних, поведінкових функцій людини.
ДГК разом з холіном та уридином є найважливішим нутрієнтом, що бере участь в утворенні синапсів і їх функціонуванні за рахунок концентрації в синаптичних мембранах і модуляції нейропередачі. Відповідно материнська, фетальна і неонатальна забезпеченість цим мікронутрієнтом – важливий фактор, що визначає стан здоров’я у період раннього дитинства і всього життя [1, 17].
В останній триместр вагітності відбувається посилений транспорт арахідонової кислоти і ДГК через плаценту до плода [18, 48]. Показано наявність механізмів селективного транспорту цих сполук через плаценту. При цьому ДГК переважно вбудовується у мембрани клітин кори головного мозку дитини [16, 48].
Забезпеченість ДПНЖК в антенатальний період залежить від дієти матері: рівень споживання матір’ю ДПНЖК впливає на вміст цих жирних кислот у складі фосфоліпідів крові і асоціюється з масою тіла дитини при народженні. Жирнокислотний склад раціону вагітної може мати віддалені результати у вигляді розвитку цілої низки станів у дитини не тільки в період дитинства, а й у старшому віці. Так, показано, що надлишкове надходження ДПНЖК ω‑6 під час вагітності може призвести до ожиріння у дітей [19].
Доведено, що зниження концентрації ДПНЖК у ліпідах мембран плода може зумовлювати порушення утворення специфічних структур мозку, який розвивається, і незворотних змін у ньому. Так, дефіцит ДГК у внутрішньоутробний період асоціюється зі зниженням у подальшому функціональних можливостей сітківки ока та когнітивних функцій [20].
За результатами проведених в останні роки генетичних досліджень, забезпеченість плода арахідоновою кислотою і ДГК залежить не тільки від вмісту ДПНЖК у раціоні матері, а й від генетично зумовленої активності десатурази (відповідальний ген – FADS2) матері та самої дитини. Довголанцюгові жирні кислоти проходять через плацентарний бар’єр не тільки шляхом пасивного транспорту, а й завдяки спеціалізованим транспортним білкам, активність яких залежить від відповідних факторів транскрипції [21]. Отже, всі ці фактори можуть впливати на антенатальну забезпеченість ДПНЖК.
Антенатальна недостатність ω‑3 ДПНЖК впливає не лише на розвиток мозку дитини, а й на перебіг вагітності та післяпологового періоду у матері. Згідно з рекомендаціями Всесвітньої організації охорони здоров’я (1999, 2003), вагітним і жінкам, що годують грудним молоком, потрібен додатковий щоденний прийом ДПНЖК ω‑3 не менш ніж 300 мг на добу.
Сімейства ω‑3 і ω‑6 жирних кислот привертають особливу увагу педіатрів і нутриціологів, оскільки для дітей першого року життя характерна висока потреба в арахідоновій кислоті та ДГК у зв’язку зі швидким ростом мозку, маса якого на першому році життя збільшується приблизно у 3 рази.
При цьому можливості синтезу активних форм ДПНЖК у перші місяці життя знижені: навіть у разі достатнього надходження з харчовими продуктами їх попередників у дитини може спостерігатися дефіцит метаболітів ω‑3 (ДГК) і ω‑6 (арахідонової кислоти), тим часом як дефіцит ДГК проявляється частіше через меншу активність процесів її синтезу.
Дослідження вмісту ДГК у материнському молоці в постнатальний період показало, що рівень цієї жирної кислоти збільшується між 3 і 14-м днями лактації (зростає з 0,15 до 0,29 мас%) і знижується до кінця перинатального періоду (до 29-го дня) до 0,19 мас% [22]. Результати низки досліджень свідчать, що достатня кількість жирної риби (або риб’ячого жиру) у раціоні матері в період лактації позитивно впливає на показники інтелекту дитини надалі [23-25].
Недоношені діти не отримують достатньої кількості ДПНЖК в антенатальний період: після народження ферментні системи недоношених немовлят характеризуються особливо низькою здатністю метаболізувати есенціальні жирні кислоти в ДПНЖК. Цей факт науково обґрунтував необхідність збагачення ДПНЖК сумішей, призначених для харчування недоношених дітей.
Ефективність збагачення молочних сумішей ДПНЖК доведено: за результатами досліджень, діти, які одержували грудне молоко або дитячу суміш, збагачену ДПНЖК, мали значно кращі показники когнітивних функцій і гостроти зору порівняно з дітьми, які отримували незбагачені суміші. Виявлено також позитивний кореляційний зв’язок між концентрацією арахідонової кислоти і ДГК у плазмі крові, фосфоліпідах еритроцитів та коефіцієнтом інтелекту (Intelligence Quotient, IQ) у дітей надалі [26-30].
Вплив ДПНЖК на функції нервової системи не обмежується раннім віком. Так, проведено аналіз 41 рандомізованого плацебо-контрольованого дослідження, в яких вивчали ефективність застосування ДПНЖК у хворих всіх вікових категорій з різними відхиленнями з боку нервової системи [31], а також 8 досліджень ефективності застосування есенціальних ДПНЖК у дітей із синдромом дефіциту уваги. Виявлено, що у дітей з такими порушеннями рівень поліненасичених жирних кислот у крові знижений. У подальших дослідженнях було вивчено вплив прийому ДПНЖК на когнітивні функції та поведінку у цієї категорії дітей [4, 50].
Позитивний вплив додаткового прийому ДПНЖК на когнітивні функції дітей віком 5-6 років показано також у дослідженні І.Я. Коня та співавт. [32]. У дослідженні Р. Montgomery та співавт., які вивчали рівень ДГК і ЕПК у крові 7-9-річних школярів [33], низька забезпеченість ДГК асоціювалася зі зниженням здатності до читання, емоційною гіперлабільністю і психологічними проблемами у спілкуванні з батьками. У низці робіт показана ефективність додаткового введення ДПНЖК для поліпшення здатності до навчання і корекції поведінкових реакцій у дітей шкільного віку [34-36].
Доведено вплив ДПНЖК на імунну систему. Поліненасичені жирні кислоти входять до складу мембран усіх імунокомпетентних клітин, впливаючи на спрямованість імунної відповіді [4, 37]. Збільшення кількості ω‑3 жирних кислот у мембрані змінює розташування білків-рецепторів в імунологічних синапсах і провідність сигналів через мембрану лімфоцитів, унаслідок чого змінюється продукція цитокінів, знижується активність клітин-кілерів і проліферації лімфоцитів [38].
Вищий рівень ω‑3 ДПНЖК у мембранах клітин знижує продукцію прозапальних ейкозаноїдів (простациклін (PGІ2), лейкотрієн B4 (LTB4), тромбоксан А2 (ТХА2)) з ω‑6 і збільшує продукцію ейкозаноїдів з ω‑3 жирних кислот (простагландин I3 (PGI3), лейкотрієн В5 (LTB5).
Важливо відзначити, що ейкозаноїди, які утворюються з ω‑3 ДПНЖК, перешкоджають дії прозапальних ω‑6 ейкозаноїдів або мають аналогічну, але значно слабшу дію [39]. Інший механізм можливого впливу ω‑3 ДПНЖК на імунну відповідь – зміна експресії генів, індукована ω‑3 жирними кислотами, що, мабуть, є результатом впливу жирних кислот на фактори транскрипції, відомі як рецептори, які активуються пероксисомними проліфераторами (Peroxisome Proliferator – Activated Receptors, PPARs). Відомо, що активація PPAR може пригнічувати активність макрофагів і продукцію фактора некрозу пухлини, інтерлейкінів‑1 і -6, а також активність NO-синтази [38, 40, 41].
Накопичені дані про вплив ДПНЖК на імунну відповідь стали додатковим аргументом для введення їх до складу гіпоалергенних лікувальних і профілактичних сумішей.
На рисунку 1 представлені біологічно активні метаболіти ДПНЖК, які беруть участь у реалізації імунної відповіді.

Фізіологічна потреба в ω‑6 жирних кислотах для дорослих становить 8-10 г на добу, ω‑3 жирних кислотах – 0,8-1,6 г на добу, або 5-8 і 1-2% калорійності добового раціону відповідно. Оптимальне співвідношення в добовому раціоні ω‑6 і ω‑3 жирних кислот становить 5-10:1. Для дітей віком від 1 до 14 років фізіологічна потреба в ω‑6 і ω‑3 жирних кислотах становить 4-9 і 0,8-1% калорійності добового раціону, від 14 до 18 років – 5-8 і 1-2% відповідно [42]. Згідно з європейськими рекомендаціями, для підтримки здоров’я, як мінімум, необхідно отримувати 0,45-0,50 г ЕПК і ДГК на день [43].
Враховуючи наведені вище дані, метою нашого дослідження було визначення рівня ДПНЖК (ω‑3 та ω‑6) і показників ліпідного обміну у здорових дітей дошкільного віку.
Матеріали та методи дослідження
Було обстежено 28 здорових дітей віком 3-6 років, які проживають у місті Києві. Всі діти були оглянуті педіатром і профільними спеціалістами, на момент огляду не мали вроджених, гострих і хронічних захворювань, їхній раціон харчування відповідав віку. Окрім цього, всім дітям проводили лабораторні та інструментальні дослідження.
Дослідження показників ліпідного обміну виконували на біохімічному аналізаторі StarDustFC, воно включало визначення у сироватці крові концентрації загального холестерину; тригліцеридів; ліпопротеїнів низької щільності; ліпопротеїнів дуже низької щільності; ліпопротеїнів високої щільності; коефіцієнта атерогенності за формулою Клімова.
Оцінювали рівень ω‑3 та ω‑6 ДПНЖК, співвідношення ω‑6/ω‑3 ДПНЖК і визначали індекс ненасиченості жирних кислот.
Методика дослідження включала декілька етапів. Спочатку у дитини брали до 4 мл цільної крові, яку переносили в пробірку та центрифугували протягом 7-10 хв при 3000 об./хв. Відділену від формених елементів сироватку відбирали у стерильну пробірку та заморожували при температурі –18-20 °C.
Наступним етапом було екстрагування сироватки крові. Екстракцію ліпідів проводили за найбільш поширеним методом Блая і Даєра.
За цим методом використовують однофазну систему розчинників хлороформ – метанол – вода (1:2:0,8 за об’ємом), яка швидко та ефективно виділяє ліпіди. Екстракт розбавляють одним об’ємом води та одним об’ємом хлороформу.
У результаті утворюється двофазна система, нижній шар якої складається з хлороформу, а верхній – суміші метанолу та води (1,0:0,9). Водорозчинні неліпідні домішки переходять у водно-метанольний шар, а в метанольному шарі залишаються ліпіди, майже чисті від домішок.
Ще один етап – отримання метилових ефірів жирних кислот, для чого аліквоту неомилюваного залишку жиру розчиняють у бензолі (0,5 мл) і переносять у скляну ампулу, куди попередньо додають 1,5-2,0 мл 3М HCl у метанолі. Ампулу запаюють на газовій горілці та кип’ятять на водяній бані 50 хв.
Після цього ампулу відкривають, вміст розводять водою 1:1 й екстрагують 2-3 рази перегнаним б/в гексаном. Гексанові витяжки промивають дистильованою водою H2O та сушать б/в NaSO4. Сухі екстракти випарюють на роторному випалювачі й отримують метилові ефіри жирних кислот. Метилові ефіри жирних кислот розчиняють у бензолі та наносять на пластинки Sorbifil (пластинки для тонкошарової хроматографії).
Пластинки розміщують у камері з розчинником (бензолом) та розганяють (40-50 хв). Зону очищення метилових ефірів знімають з пластинки Sorbifil, екстрагують гексаном на фільтрі Шотта. Гексан випарюють на роторному випалювачі та отримують хроматографічно етилові ефіри жирних кислот.
Далі виконують хроматографічний аналіз. Метилові ефіри жирних кислот розчиняють у гексані та проводять хроматографічний аналіз на хроматографі HRGC5300 (Італія) на скляній набивній колонці 3,5 м, заповненій Chromosorb W/HP, із нанесеною 10% рідкою фазою Silar 5CP при програмованій температурі 140-250 °C з нарощуванням 2°/хв. Ідентифікацію жирних кислот здійснюють за допомогою стандартів фірми Sigma, Serva. Вміст індивідуальних жирних кислот вказують у відсотках від загальної суми.
Статистичну обробку одержаних даних проводили на комп’ютері з використанням прикладного пакета програм Statistica 10.0 for Windows методом варіаційної статистики та коефіцієнта лінійної кореляції Пірсона.
Результати та їх обговорення
У результаті проведених досліджень були виявлені особливості забезпеченості дитячого організму насиченими та ненасиченими жирними кислотами. Співвідношення рівнів жирних кислот основних груп у здорових дітей відображено на рисунку 2.
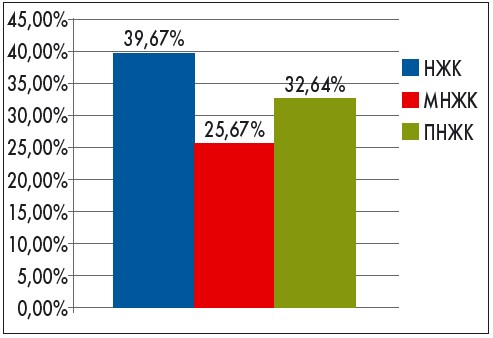
Рис. 2. Співвідношення рівнів жирних кислот у здорових дітей, %. НЖК – ненасичені жирні кислоти, МНЖК – мононенасичені жирні кислоти, ПНЖК – поліненасичені жирні кислоти
На поданій діаграмі видно, що у здорових дітей переважають насичені жирні кислоти (39,6%), рівень поліненасичених становить 32,6%, а мононенасичених – 25,6%, тобто виявлено дефіцит важливих для дитячого організму складових.
Ненасичені жирні кислоти мають один (мононенасичені) або декілька (поліненасичені) подвійних зв’язків. Залежно від положення подвійних зв’язків по відношенню до останнього вуглеводного атома метильної групи розрізняють декілька основних сімейств ненасичених жирних кислот: ω‑9, ω‑6 та ω‑3. Незважаючи на достатній рівень поліненасичених жирних кислот, виявлено порушення балансу основних класів ДПНЖК (рис. 3).
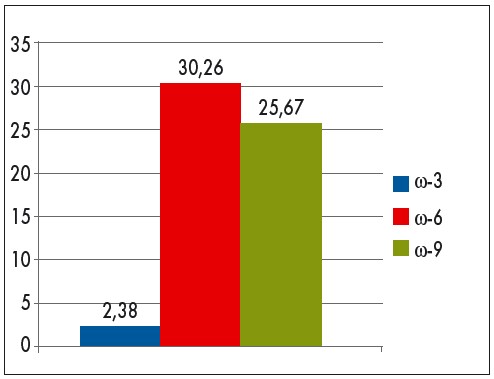
Рис. 3. Основні класи поліненасичених жирних кислот у здорових дітей, %
! Поряд із високим рівнем ω‑6 ДПНЖК у здорових дітей відзначено достатньо високий рівень МНЖК і виражений дефіцит ω‑3 ДПНЖК.
Серед виявлених ω‑3 ДПНЖК переважала ейкозатрієнова кислота, серед ω‑6 – лінолева, серед ω‑9 МНЖК – олеїнова (табл. 2).
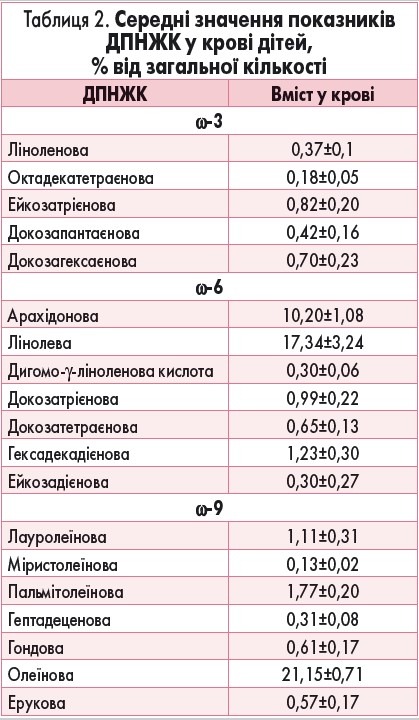
У таблиці 2 наведено дані, які свідчать про виражений дисбаланс рівня жирних кислот в організмі дітей у бік збільшення концентрації ω‑6, що може призвести до таких наслідків: запальних процесів, звуження судин і бронхів, підвищення артеріального тиску, пригнічення різних ланок імунітету, підвищення ризику розвитку атеросклерозу та ішемічної хвороби серця, алергії, хвороб шкіри тощо.
Для оцінювання показників балансу ПНЖК використовують співвідношення ω‑3/ω‑6, яке у нормі становить 1:4-9 або 5-10 (за даними різних дослідників). У обстежених дітей співвідношення ПНЖК становило від 1:6 до 1:85, середнє значення – 1:23, що свідчить про наявність вираженого дисбалансу.
У проведених раніше дослідженнях [53] виявлено, що у групі здорових дітей молодшого шкільного віку (70,5%), гетерогенній за рівнями різних фракцій ліпопротеїнів, показники відрізнялися від вікової норми. У зв’язку з цим була проведена оцінка ліпідного спектра крові у здорових дітей дошкільного віку. Як видно із таблиці 3, у дітей цієї вікової групи також виявлено різні зрушення.
Оцінювання показників за середніми значеннями виявило збільшення рівня загального холестерину (ХС) та тригліцеридів (ТГ) до пограничного та підвищення рівня ліпопротеїнів низької щільності (ЛПНЩ) і ліпопротеїнів дуже низької щільності (ЛПДНЩ) порівняно з нормою, значення ліпопротеїнів високої щільності (ЛПВЩ) зберігалися у межах норми.
Проте більш детальний аналіз показав, що рівень ХС у 76,9% дітей перевищував норму, при цьому в однакової кількості дітей (38,4%) показники були на пограничному та високому рівнях.
У 23,07% дітей виявлено підвищення вмісту ЛПНЩ, при цьому 15,3% мали пограничні значення та 7,6% – високі. Підвищення рівня ЛПДНЩ встановлено у 61,5% дітей. Концентрація ТГ була вищою за норму у 61,53% дітей, у 7,6% дітей зафіксовано пограничні значення, а у 53,8% – високі показники.
Відомо, що ω‑3 ДПНЖК забезпечують антиатерогенний ефект – зменшують кількість ЛПНЩ та збільшують ЛПВЩ за рахунок зниження синтезу аполіпопротеїну апоВ‑100 тригліцеридів, що сприяє евакуації ЛПДНЩ із кровотоку печінки та периферичних тканин.
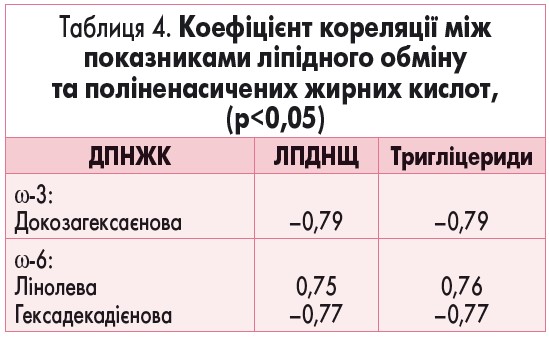
Тому був проведений лінійний кореляційний аналіз за методом Пірсона для виявлення вірогідності зв’язків між показниками ліпідів та поліненасичених жирних кислот. При оцінюванні лінійної кореляції вважали, що значення коефіцієнта кореляції (r) >0,7 свідчить про високий ступінь зв’язку між величинами, від 0,3 до 0,7 – про середній і <0,3 – про слабкий ступінь зв’язку (табл. 4).
Виявлено зворотний зв’язок між вмістом докозагексаєнової кислоти (ω‑3) та ЛПДНЩ і ТГ (r = –0,79). Відзначено також прямий кореляційний зв’язок між рівнем лінолевої кислоти та ЛПДНЩ (r = 0,76) і ТГ, зворотний зв’язок – між рівнем гексадієнової кислоти та ЛПДНЩ і ТГ (r = –0,77).
! Враховуючи виявленні порушення, всім дітям до основного раціону харчування додатково включено ДПНЖК у формі капсул Смарт Омега для дітей.
До складу Смарт Омега входять риб’ячий жир – 285 мг, який містить ω‑3 ПНЖК (ейкозапентаєнова 18%, або 51,3 мг, і докозагексаєнова – 12,0%, або 34,2 мг), вітамін А – 500 МО, вітамін С – 3,8 мг, вітамін D3 – 120 МО. Всі діти приймали препарат у дозі 1 капсула на добу протягом 2 міс. Після закінчення курсу лікування проведено повторні дослідження рівня ДПНЖК і ліпідограми (рис. 4).
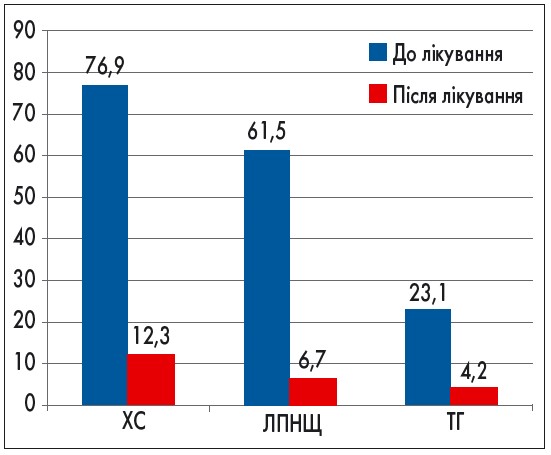
Рис. 4. Кількість дітей із порушеннями ліпідного спектра крові до та після лікування, %
Отримані дані свідчать про позитивний вплив вживання ДПНЖК, які сприяли зниженню рівня ХС у 64,6%, ЛПНЩ – у 54,8%, ТГ – у 18,9% дітей.
Дослідження концентрації ДПНЖК після лікування показало підвищення рівня ω‑3 та зниження рівня ω‑6 жирних кислот. Співвідношення ω‑3/ω‑6 після лікування становило 1:5,7 (рис. 5).
Рис. 5. Основні класи поліненасичених жирних кислот у здорових дітей, %
Висновки
Таким чином, здорові діти дошкільного віку мають певні порушення ліпідного спектра крові за рахунок дисбалансу важливих ω‑3 та ω‑6 ДПНЖК у бік різкого зниження рівня ω‑3 та підвищення ω‑6. При цьому співвідношення зазначених ДПНЖК у середньому становило 1:23.
У здорових дітей дошкільного віку, незважаючи на ранній вік, вже визначаються різні порушення ліпідного обміну: середні показники загального ХС та ТГ перебувають на пограничному рівні, вміст ЛПНЩ і ЛПДНЩ підвищений, і, можливо, залежить від рівня ДПНЖК, що підтверджує високий кореляційний зв’язок між ω-3 (докозагексаєнова) і ω‑6 (ленолева і гексадекадієнова) та ЛПДНЩ і ТГ.
Прийом Смарт Омега для дітей сприяв поліпшенню показників ліпідного спектра крові у 86,2% дітей, а також покращенню якості складу ДПНЖК у бік підвищення рівня ω‑3 та зниження – ω‑6, нормалізації співвідношення ω‑3/ω‑6 до 1:5,7. Отримані дані дають змогу рекомендувати Смарт Омега для дітей як для профілактики, так і для лікування. Курс терапії має становити не менше 2 міс.
Токсичних та алергічних проявів під час застосування Смарт Омега для дітей не виявлено, що дає змогу характеризувати його як високотолерантний продукт і рекомендувати для широкого використання у педіатрії.
Таким чином, ДПНЖК є одними із найважливіших есенціальних нутрієнтів, що забезпечують повноцінний розвиток дитини в усі вікові періоди, починаючи з антенатального. Результати проведених досліджень свідчать про недостатнє споживання дітьми ДПНЖК при сучасному типі харчування. Відповідно, потрібна корекція жирнокислотного забезпечення матерів у період вагітності та лактації, а також дітей всіх вікових категорій за рахунок збагачення продуктів дитячого харчування або використання нутрицевтиків і препаратів, що містять ω‑3 ДПНЖК.
Крім цього, існує певна категорія хворих, раціон яких обмежений у зв’язку з медичними показаннями, наприклад, діти з множинною харчовою алергією, які тривалий час дотримуються дієти. Оскільки рибу як високоалергенний продукт традиційно виключають з харчування, раціон цієї категорії хворих стає ще більш дефіцитним за ДПНЖК. Для корекції раціону дітей з харчовою алергією доцільно використовувати препарати ДПНЖК [44], які призначають під контролем переносимості та за умови відсутності в анамнезі тяжких і виражених реакцій на рибу.
Література
1. Second International Conference on Nutrition Rome, 19-21 November 2014 Conference Outcome Document: Rome Declaration on Nutrition ICN2 2014/2. URL: http://www.fao.Org/3/a-ml542e.
2. Шилина H.M. Современные представления о физиологических и метаболических функциях полиненасыщенных жирных кислот / H.M. Шилина, И.Я. Конь // Вопросы детской диетологии. – 2004. – № 2 (6). – С. 25-30.
3. Левачев М.М. Значение жира в питании здорового и больного человека: Справочник по диетологии / Под ред. В.А. Тутельяна, М.А. Самсонова. – М.: Медицина, 2002. – С. 25-32.
...
54. Jensen C.L., Maude M., Anderson R.E., Heird W.C. Effect of docosahexaenoic acid supplementation of lactating women on the fatty acid composition of breast milk lipids and maternal and infant plasma phospholipids. Am J Clin Nutr 2000. 71: 292-299.
Повний список літератури знаходиться в редакції.
Тематичний номер «Педіатрія» №1 (44), березень 2018 р.