5 квітня, 2018
Витамины группы В в неврологической практике
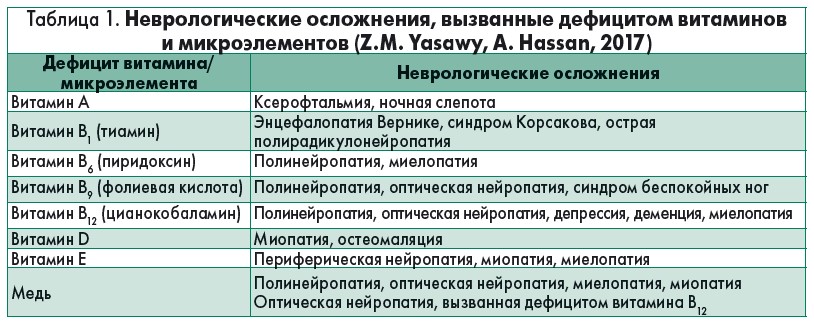
Витамины группы В, прежде всего В1 (тиамин), В6 (пиридоксин), В12 (цианокобаламин), относятся к нейротропным и многие годы применяются в лечении заболеваний периферической и центральной нервной системы. Дефицит этих витаминов в организме может стать причиной развития нейропатий, поэтому ранняя диагностика и коррекция недостатка витаминов указанной группы необходимы для предотвращения необратимых неврологических нарушений. В представленном обзоре приведены последние данные о состояниях, дефицитных по витаминам группы В (табл. 1) и путям их коррекции.
 Коррекция дефицита витаминов группы В при постхирургических полинейропатиях
Коррекция дефицита витаминов группы В при постхирургических полинейропатиях
Увеличение распространенности ожирения неизбежно влечет за собой рост числа и бариатрических операций, и, как следствие, серьезных постхирургических неврологических осложнений в результате дефицита микроэлементов (H.A. Algahtani et al., 2016; Z.M. Yasawy, A. Hassan, 2017).
Здесь следует отметить, что у 20-30% людей, страдающих ожирением, еще до оперативных вмешательств отмечается дефицит микроэлементов, в частности витаминов B1, B12, D, фолиевой кислоты, а также меди, который в послеоперационный период усугубляется (M. Tabbara et al., 2016).
В целом неврологические осложнения вследствие дефицита витаминов и микроэлементов могут проявляться через 3-20 мес после бариатрической операции.
Назначение в послеоперационном периоде пероральных пищевых добавок, содержащих витамины B1, B12, D, E, K, фолиевую кислоту, кальций, железо и медь, может быть нецелесообразным из-за риска возникновения рецидивирующих рвот, наблюдаемых еще до развития неврологической симптоматики у пациентов, перенесших рукавную гастрэктомию (Z.M. Yasawy, A. Hassan, 2017).
К тому же длительная рвота и потеря веса могут быть дополнительными факторами риска развития неврологических осложнений. Так, А. Landais описал быстро прогрессирующую острую полинейропатию (полирадикулонейропатию), связанную с дефицитом тиамина, которая развилась уже через 6 нед после операции. Также присутствовал дефицит витаминов В12, D и фолиевой кислоты (А. Landais, 2014).
Очевидно, что раннее выявление неврологических симптомов и коррекция дефицита витаминов группы В может помочь уменьшить риск неврологических осложнений.
Поскольку дефицит витаминов B1 и B12 – наиболее распространенная причина полинейропатий после универсальной хирургии, целесообразно парентеральное введение (внутримышечно) витамина B12 в дозе 1000 мкг/сут в течение 1 нед, затем – 1000 мкг еженедельно, а также витамина B1 в дозе 500 мг/сут в течение 3 дней, затем – 100 мг/сут. Также рекомендуют назначение фолиевой кислоты перорально в дозе 5 мг/сут (Z.M. Yasawy, A. Hassan, 2017).
Такая терапия способствует устранению в течение 3-4 нед сенсорных симптомов, в том числе болевого синдрома и парестезии, и общему улучшению состояния в следующие 6-8 нед после оперативного вмешательства.
Необходимо подчеркнуть, что указанная схема должна быть адаптирована к каждому индивидуальному случаю в соответствии с результатами регулярных биохимических лабораторных исследований. В то же время у пациентов с острой полинейропатией (от умеренной до тяжелой степени) в послеоперационный период парентеральную терапию витаминами B1 и B12 необходимо назначать как можно раньше, дабы снизить риск прогрессирования заболевания и его необратимых последствий.
Оптическая нейропатия, вызванная дефицитом витамина В12
Витамин B12 играет ключевую роль в синтезе ДНК, поддержании нормальной функции мозга, метаболизме белков и эритропоэзе. Дефицит витамина B12 может привести к мегалобластическому эритропоэзу, снижению количества гомоцистеина плазмы, а также к повышенным уровням метилмалонила-КоА (кофермент A), что препятствует синтезу жирных кислот и способствует аномальному миелинообразованию (S.L. Schrier et al., 2016). Цианокобаламин действует как кофактор в образовании сукцинила-КоА, неотъемлемой части цикла Кребса, в результате которого образуется аденозинтрифосфат (АТФ). И напротив, нарушенный окислительный метаболизм вызывает истощение запасов АТФ. Предполагается, что вследствие высокой метаболической потребности папилломакулярного пучка сетчатки именно истощение АТФ, вызванное дефицитом витамина В12, приводит к атрофии зрительного нерва и центральной скотоме.
Распространенность дефицита цианокобаламина в общей популяции составляет около 4% (Y.P. Qi, H.C. Hamner, 2014). Функциональный дефицит B12 обнаруживается у 10-30% пациентов старше 65 лет, с увеличением возраста процент таких пациентов растет (W. Herrmann et al., 2005). Дефицит цианокобаламина, а также фолиевой кислоты может приводить к мегалобластной анемии, но только недостаток витамина B12 вызывает неврологические нарушения. При этом фолиевая кислота способна свести к минимуму гематологические нарушения дефицита витамина B12, но не неврологические симптомы. Показано, что добавление фолиевой кислоты может вызывать более быстрое прогрессирование неврологической симптоматики, если витамин B12 не является биодоступным или его дефицит не подвергается первоочередной коррекции (A.R. Scharnweber, R.J. Zimbalist, 2017).
Оптическая нейропатия с дефицитом витамина B12 может приводить к прогрессирующей двусторонней потере зрения, которая часто ассоциируется с центральными скотомами. Неполное устранение дефицита витамина B12 при пероральном введении в сочетании с пероральной фолиевой кислотой может усугубить неврологические нарушения, вторичные по отношению к дефициту цианокобаламина. Так, сообщается о безболезненном прогрессирующем поражении зрения при появлении блеска зрительного диска и центральных скотомах на фоне перорального приема витамина B12 и фолиевой кислоты. В свою очередь, назначение парентеральной терапии B12 (внутримышечно 1000 мкг/мл 1 р/нед в течение 4 нед и затем ежемесячно) с последующим добавлением фолиевой кислоты (1 мг/сут перорально) способствовало улучшению остроты зрения, а также цветового зрения (табл. 2).
Необходимо подчеркнуть, что биодоступность цианокобаламина имеет первоочередное значение прежде всего для пациентов с мальабсорбцией.
В большинстве случаев после потери аксонов и формирования бледности диска зрительного нерва восстановление зрения не происходит (F.С. Roessler, S. Wolff, 2017).
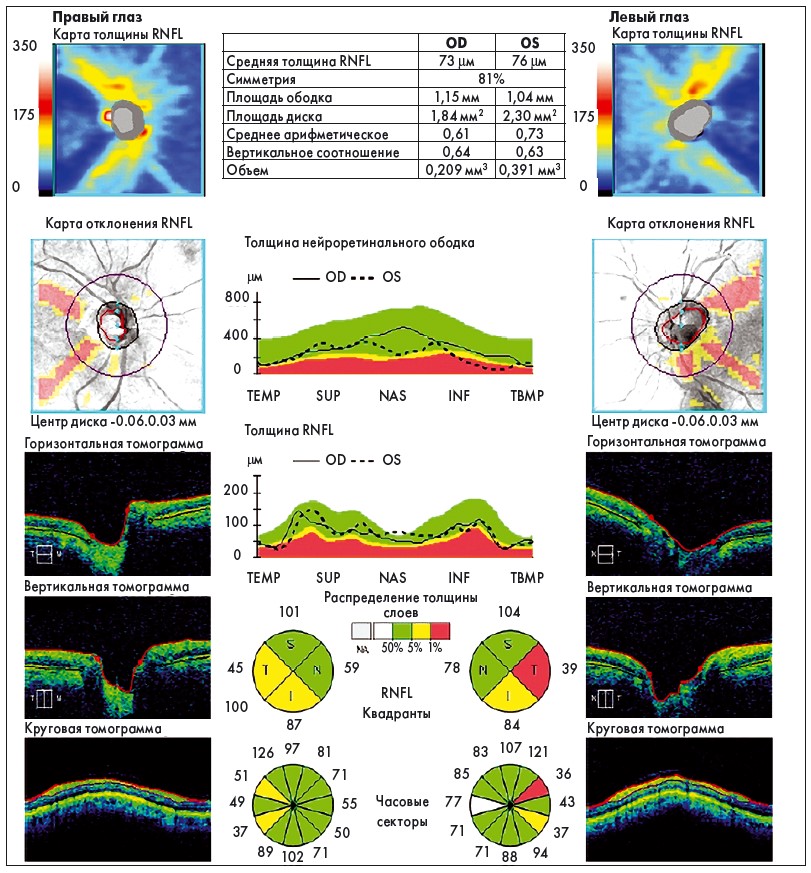
Примечательно, что сообщается о восстановлении зрения, несмотря на наличие бледности диска зрительного нерва (рис. 1). Таким образом, быстрая диагностика и распознавание оптической нейропатии с дефицитом витамина B12 имеют первостепенное значение для восстановления зрения.
Рис. 1. Диск зрительного нерва у пациента с оптической нейропатией (у пациента развилась задняя субкапсулярная катаракта левого глаза, что, скорее всего, несколько ограничивало лучшую коррекцию зрения) (A.R. Scharnweber, R.J. Zimbalist, 2017)
Примечания. RNFL – толщина слоя нервных клеток сетчатки; OD – правый глаз; OS – левый глаз.
Цианокобаламин при неврологических жалобах после травмы шейного отдела позвоночника
Частым следствием дефицита цианокобаламина является подострая комбинированная дегенерация спинного мозга. В большинстве случаев это заболевание ограничено верхнешейным и верхнегрудным отделами и ассоциируется с нарушением тактильной чувствительности и проприоцептивными проблемами (F.С. Roessler, S. Wolff, 2017). Однако определение сывороточного витамина В12 – ненадежный критерий, поскольку клинические признаки могут указывать на недостаток цианокобаламина, в то время как его значения все еще могут находиться в нормальном диапазоне. Поэтому необходимы другие диагностические маркеры. К примеру, гомоцистеин является самым ранним, а метилмалоновая кислота (ММК) – самым специфическим маркером дефицита цианокобаламина (W. Herrmann, R. Obeid, 2012).
В цитоплазме высвобожденный цианокобаламин преобразуется в метилкобаламин. В митохондриях кобаламин превращается в аденозилкобаламин. Метилкобаламин и фолаты являются сопутствующими факторами в опосредуемом метионин-синтазой превращении гомоцистеина в метионин, необходимый для синтеза нуклеотидов и геномного и негеномного метилирования. Поэтому недостаток метилкобаламина приводит к нарушению деления клеток. В то же время происходит накопление гомоцистеина, высокие концентрации которого связаны с повышением риска сердечно-сосудистых заболеваний(О. Stanger et al., 2004). Кроме того, гомоцистеин, по-видимому, обладает нейротоксическими свойствами, вызывающими сосудистую деменцию и болезнь Альцгеймера.
Аденозилкобаламин является сопутствующим фактором для метилмалонил-КoA-мутазы, превращающим метилмалонил-КоА в сукцинил-КоА, который играет решающую роль в цикле Кребса. Поэтому отсутствие аденозилкобаламина нарушает пролиферацию, созревание и регенерацию нейронов, приводя к накоплению ММК. Для деградации гомоцистеина необходимы метилкобаламин, пиридоксин и фолиевая кислота.
Повреждения белого вещества соответствуют аномальной миелинизации в результате снижения активности аденозилкобаламинзависимого метилмалонила-КoA, тогда как локальный глиоз обусловлен непосредственным цитотоксическим влиянием гомоцистеина на эндотелий. При неврологической симптоматике после травмы шейного отдела позвоночника с клинически и лабораторно подтвержденной подострой комбинированной дегенерацией спинного мозга рекомендуется парентеральное введение цианокобаламина в дозе 1000 мкг/сут в течение 5 дней с последующей заменой на 1000 мкг еженедельно в течение следующих 3 мес, а затем – 1000 мкг 1 р/мес (табл. 3) (F.С. Roessler, S. Wolff, 2017).
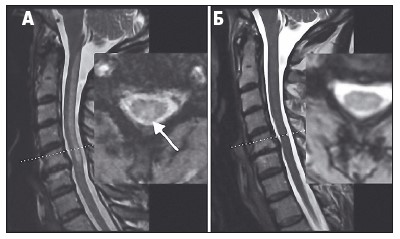
При этом раннее начало терапии имеет решающее значение для улучшения результатов лечения (рис. 2).
Рис. 2. Магнитно-резонансная томография пациента, страдающего подострой комбинированной дегенерацией спинного мозга до (а) и после (Б) терапии цианокобаламином (F.С. Roessler, S. Wolff, 2017)
Тиамин в терапии пациентов с алкогольной зависимостью и энцефалопатией Вернике
Дефицит тиамина (витамин B1) распространен у пациентов с алкогольной зависимостью и может привести к энцефалопатии Вернике – поражению головного мозга, острому и потенциально опасному для жизни неврологическому расстройству. Ранними проявлениями дефицита тиамина являются когнитивные нарушения. В целом классические симптомы расстройства (измененный психический статус, атаксия и окулярные признаки, включая нистагм и офтальмоплегию) могут присутствовать только у 16-38% пациентов, хотя энцефалопатию Вернике можно дополнительно охарактеризовать различными изменениями, наблюдаемыми во время магнитно-резонансной томографии (А. Nishimoto et al., 2017).
Энцефалопатия Вернике ассоциируется с высоким уровнем заболеваемости и смертности (17-20% пациентов), при этом примерно у 80-85% выживших развивается хроническое заболевание, сопровождаемое амнестическими расстройствами, в том числе дефектами обучения и кратковременной потерей памяти (психоз Корсакова).
Пациентам с установленной энцефалопатией Вернике назначают парентеральное введение тиамина в дозе 200-500 мг 3 р/сут в течение 3-5 дней с последующим пероральным приемом тиамина в дозе 250-1000 мг/сут. При этом следует отметить, что дозы парентерального тиамина 100-250 мг не всегда способны предотвратить как летальный исход, так и психоз Корсакова, который развивается у 56-84% пациентов после наблюдения. В свою очередь, внутривенное введение высоких доз тиамина (500 мг) 3 р/сут в течение 2 дней с последующим переходом на внутривенное или внутримышечное введение тиамина в дозе 500 мг/сут у 70% пациентов позволяет добиться улучшения состояния (А. Nishimoto et al., 2017).
У пациентов с подозрением на энцефалопатию Вернике следует назначать парентерально тиамин в дозе 250-300 мг 2 р/сут в течение 3-5 дней с последующим переходом на пероральный прием в дозе 250-300 мг/сут. У пациентов с высоким риском дефицита тиамина назначают последний парентерально в дозе 250-500 мг/сут курсом 3-5 дней с последующим пероральным приемом в дозе 250-300 мг/сут (А. Dervaux, Х. Laqueille, 2017).
В то же время представляется целесообразным проведение дальнейших исследований для оптимизации режима дозирования и продолжительности лечения тиамином при таком потенциально опасном для жизни состоянии, как энцефалопатия Вернике.
Нейротропный эффект витаминов группы В (В1, В6, В12) в комплексном лечении болевого синдрома
Проблема лечения боли, несмотря на все современные разработки, остается актуальным вопросом для большинства специалистов. Наряду с простыми аналгетиками, нестероидными противовоспалительными препаратами, мышечными и эпидуральными блокадами, для купирования острой боли в терапевтических дозах назначают комбинированные витаминные препараты. Использование комбинации тиамина, пиридоксина и цианокобаламина хорошо купирует боль, нормализует рефлекторные реакции, устраняет нарушения чувствительности (О.А. Шавловская, 2017).
Недостаток каждого из витаминов группы В (В1, В6, В12) приводит к формированию полинейропатии. При хроническом дефиците тиамина развивается дистальная сенсорно-моторная полинейропатия, напоминающая алкогольную и диабетическую. Дефицит пиридоксина приводит к возникновению дистальной симметричной, преимущественно сенсорной, полинейропатии, проявляющейся ощущением онемения и парестезиями в виде покалывания иголками. Недостаток цианокобаламина проявляется в первую очередь пернициозной анемией. У многих больных с дефицитом В12 развивается подострая дегенерация спинного мозга с поражением задних канатиков, а у относительно небольшого числа пациентов формируется дистальная сенсорная периферическая полинейропатия, характеризующаяся онемением и выпадением сухожильных рефлексов.
В свою очередь, нейротропные витамины группы В оказывают благоприятное действие при воспалительных и дегенеративных заболеваниях нервов и опорно-двигательного аппарата. Их назначают для устранения дефицитных состояний, а в высоких дозах они действуют как аналгетики, улучшают кровообращение, нормализуют работу нервной системы и процесс кроветворения. Инъекционные формы комбинированных препаратов тиамина, пиридоксина и цианокобаламина успешно применяют в лечении неврологических заболеваний различного генеза: невритов, невралгий, полинейропатий (диабетической, алкогольной), корешкового синдрома, ретробульбарного неврита, поражений лицевого нерва.
На украинском рынке зарегистрирован препарат Мильгамма®, который выпускается в двух формах: ампулах (раствор для инъекций) и таблетках.
Тематичний номер «Неврологія, Психіатрія, Психотерапія» № 1 (44), березень 2018 р.