6 квітня, 2018
Фармакологічні властивості холіну альфосцерату та його роль у лікуванні когнітивних розладів у неврологічних хворих
Частота захворювань, що супроводжуються деменцією, постійно зростає. Щороку в усьому світі виявляють 4,6 млн хворих на деменцію. Більша частина цих випадків припадає на розвинені країни з більшою тривалістю життя населення.
Вплив на нейромедіатор ацетилхолін є прийнятним методом лікування у випадках, коли холінергічні нейрони пошкоджені незначно. Напівсинтетичний холінергічний попередник холіну альфосцерат починає знаходити клінічне застосування в лікуванні когнітивних порушень у неврологічних хворих. У низці досліджень була продемонстрована здатність холіну альфосцерату індукувати синтез і підвищувати вивільнення ацетилхоліну в пацієнтів із деменцією на тлі хвороби Альцгеймера (ХА), цереброваскулярними захворюваннями та в осіб похилого віку. Крім того, попередні дослідження показали позитивний вплив холіну альфосцерату на когнітивні функції у хворих із черепно-мозковою травмою (ЧМТ) різних ступенів тяжкості та хворобою Паркінсона (ХП). Деякі літературні джерела також стверджують, що при цих станах холіну альфосцерат є ефективнішим за інші холінергічні попередники (холін, лецитин, фосфатидилсерин і цитиколін), а також краще переноситься хворими та є безпечнішим. Отже, він може бути дієвим засобом для лікування деменції, що розпочалася в зрілому віці, як у поєднанні з новими інгібіторами ацетилхолінестерази, так і як монотерапія в разі непереносимості чи наявності протипоказань до призначення останніх.
Ацетилхолін виконує низку функцій у нервовій системі організму. Він відіграє критичну роль у розвитку кори мозку, забезпеченні кіркових функцій, регуляції мозкового кровообігу та циклу спання-неспання, а також у процесах когнітивної діяльності, навчання та запам’ятовування.
Базальні холінергічні нейрони переднього мозку, що чинять холінергічний вплив на кору мозку та гіпокамп, піддаються дегенеративним змінам у процесі старіння організму. Вважається, що саме з холінергічною дисфункцією, котра виникає таким чином, пов’язані розлади пам’яті, які прогресують, у осіб похилого віку.
Підсилювати холінергічну нейротрансмісію можуть деякі класи препаратів, такі як інгібітори ацетилхолінестерази та холінергічні попередники (холін, лецитин, цитиколін і холіну альфосцерат). Останні вільно проникають крізь гематоенцефалічний бар’єр (ГЕБ) і стимулюють синтез ацетилхоліну та фосфоліпідів мембран нейронів.
Обґрунтування застосування інгібіторів холінестерази в лікуванні деменції, що почалась у зрілому віці, полягає в їхній здатності покращувати холінергічну передачу на рівні синапсів, сповільнюючи катаболізм ацетилхоліну. Однак ефективність інгібіторів у лікуванні деменції, що дебютувала в зрілому віці, залежить від адекватного холінергічного тонусу центральної нервової системи. Зокрема, тяжкі стадії захворювання та втрата холінергічних синапсів кори головного мозку (ГМ) можуть значно знизити активність цих препаратів у лікуванні когнітивних порушень.
Клінічні дослідження попередників ацетилхоліну першого покоління (холіну) та фосфатидилхоліну (лецитину) не продемонстрували ефективності цих препаратів у лікуванні пацієнтів із деменцією (як у монотерапії, так і в поєднанні з інгібіторами холінестерази). Найімовірніше, це пов’язано з тим, що ці препарати лише підвищують рівень ацетилхоліну в ГМ, але не стимулюють його виділення, а також із їхньою поганою здатністю проникати крізь ГЕБ.
Препарати другого покоління (холіну альфосцерат, цитиколін) позбавлені цього недоліку. При потраплянні в організм холіну альфосцерат розщеплюється на холін і гліцерофосфат. Унаслідок значного підвищення концентрації отриманого таким чином холіну в плазмі крові та його електронейтральності він здатний проникати крізь ГЕБ і брати участь у синтезі ацетилхоліну безпосередньо в ГМ. Це призводить до підвищення холінергічної активності внаслідок стимуляції синтезу ацетилхоліну та його вивільнення.
Холіну альфосцерат є також попередником у біосинтезі фосфоліпідів у ГМ, він здатний підвищувати біодоступність ацетилхоліну в нервових структурах і сповільнювати розвиток вікових мікроструктурних змін мозку. Крім того, холіну альфосцерат покращує когнітивні функції в пацієнтів із деменцією нейродегенеративного чи судинного походження.
Фармакологічні властивості холіну альфосцерату
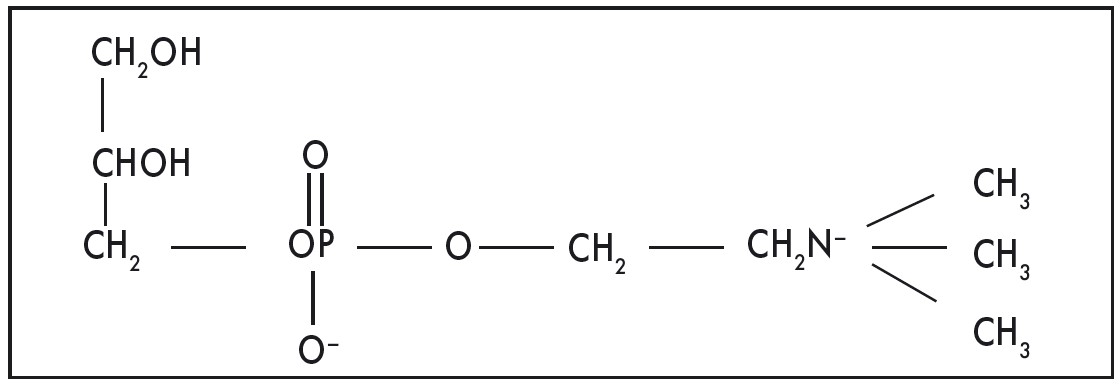
L-альфа-гліцерилфосфорилхолін, або холіну альфосцерат – це фосфоліпідний метаболіт зі структурною формулою, що зображена на рисунку 1.
Рис. 1. Структурна формула холіну альфосцерату
Після перорального введення холіну альфосцерату (в дозі 1200 мг) у здорових добровольців молодого віку середня концентрація вільного холіну в плазмі крові швидко зростає (від 10,1±0,66 мкмоль/л у першу годину до 13,6±1,04 мкмоль/л через 2 год); Сmax досягається в середньому за 3 год (14,2±1,66 мкмоль/л), при цьому його концентрація залишається вищою, ніж базальна, протягом близько 10 год.
Після перорального введення холіну альфосцерат розщеплюється в клітинах слизової оболонки кишки за допомогою ферменту гліцерилфосфорилхоліндіестерази на гліцерофосфат і вільний холін. Останній надходить у портальний кровообіг і може проникати в тканини ГМ, де приєднується до складу фосфоліпідної фракції нейронних плазматичних мембран і мікросом. Концентрація холіну альфосцерату в ГМ зростає повільно, досягаючи максимуму через 8 год після введення й залишаючись сталою протягом більш ніж 30 год.
Внутрішньом’язове введення
Клінічне дослідження за участю 12 здорових добровольців віком 20-29 років продемонструвало швидке та значне зростання концентрації холіну в плазмі крові після внутрішньом’язового (в/м) введення холіну альфосцерату (в дозі 1000 мг) (із 9,7±0,6 мкмоль/л перед введенням до 35,5±3,5 мкмоль/л через 0,25 год після введення; p<0,01), що знижувалася до вихідного рівня в середньому за 6 год. У цій самій групі пацієнтів після введення цитиколіну (попередник ацетилхоліну) в дозі 1000 мг спостерігалося швидке зростання концентрації холіну плазми (з 11,2±0,6 мкмоль/л перед введенням до 24,3±1,5 мкмоль/л через 0,25 год після введення; p<0,01) із подальшим зниженням концентрації до вихідної в середньому за 4 год. Згідно з цими даними введення холіну альфосцерату (1000 мг) за 0,25 год спричинило більш значне підвищення рівнів холіну в плазмі крові порівняно з цитиколіном (1000 мг) (p<0,05), після чого концентрація холіну в плазмі крові зменшувалася значно повільніше (6 год для холіну альфосцерату порівняно з 4 год для цитиколіну).
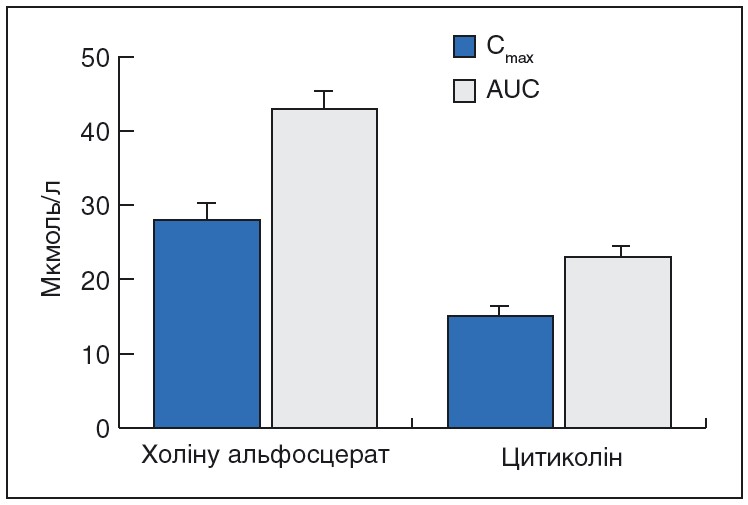
Показники пікової концентрації (Cmax) та площа під кривою (AUC) відрізнялись і були значно вищими для холіну альфосцерату (рис. 2).
Рис. 2. Максимальна концентрація (Cmax) та площа під кривою (AUC) концентрації вільного холіну після введення в/м холіну альфосцерату (1000 мг) та цитиколіну (1000 мг) у 12 здорових добровольців
Внутрішньовенне введення
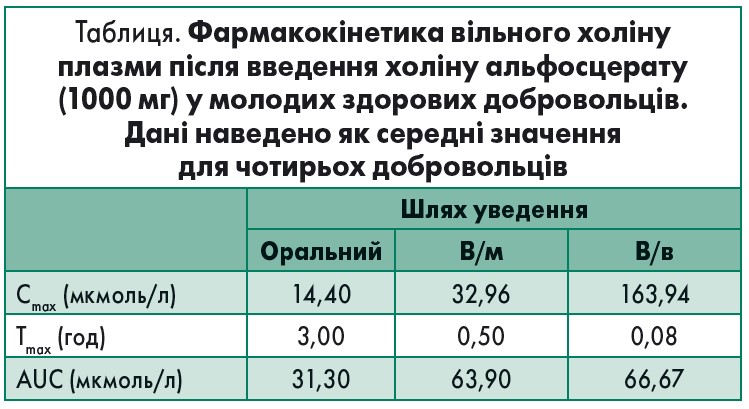
Внутрішньовенне (в/в) введення холіну альфосцерату молодим добровольцям спричиняло швидке підвищення рівня холіну в плазмі крові після 30 хв, значення фармакокінетичних показників при цьому становили: AUC – 66,67 мкмоль/год/л, Тmax – 0,08 год і Сmax – 163,94 мкмоль/л (табл.).
Клінічні аспекти застосування
Хвороба Альцгеймера
Головною характеристикою ХА є дегенерація базальних холінергічних нейронів переднього мозку, що призводить до значного обмеження механізмів холінергічної передачі, порушуючи синтез, вивільнення та захоплення ацетилхоліну, а також активність ацетилтрансферази й ацетилхолінестерази.
Отже, перші спроби лікування ХА ґрунтувалися на використанні препаратів, здатних збільшувати кількість або запобігати руйнуванню холінергічних медіаторів (інгібітори ацетилтрансферази та ацетилхолінестерази, попередники ацетилхоліну). Серед холінергічних попередників, які можуть використовуватися для лікування когнітивних порушень у зрілому віці, холіну альфосцерат є одним із найефективніших за рахунок здатності підвищувати біодоступність ацетилхоліну.
У мультицентровому подвійному сліпому рандомізованому плацебо-контрольованому дослідженні за участю 261 пацієнта з дегенеративною альцгеймерівською деменцією середнього й тяжкого ступенів застосування холіну альфосферату (1200 мг/добу протягом 180 днів) значно сповільнювало погіршення когнітивної функції з покращенням на 4-7 балів за шкалою оцінювання ХА для когнітивної дисфункції (ADAS-cog) наприкінці курсу терапії (M. De Jesus Moreno et al., 2003). Крім того, пацієнти, котрі отримували холіну альфосцерат, відзначали покращення всіх симптомів за результатами скороченої шкали оцінювання психічного статусу (MMSE), шкали загального погіршення стану (GDS), шкали оцінювання ХА для поведінкових розладів, шкали оцінювання ХА та шкали загальноклінічної оцінки (GIS) через 90 та 180 днів порівняно з вихідними значеннями, тоді як у групі плацебо не було покращення симптомів або спостерігалося їх погіршення.
У низці досліджень продемонстровано переваги комбінації холіну альфосцерату з інгібіторами холінестерази порівняно з монотерапією інгібіторами. Це зумовлено нижчими дозами інгібіторів холінестерази, необхідними для зростання рівня ацетилхоліну в мозковій тканині. Цей аспект є також корисним для зниження ймовірності виникнення побічних ефектів і зниження токсичності (переважно гастро- та гепатотоксичності) інгібіторів холінестерази. Ще одна потенційна перевага такої комбінації полягає в збільшенні кількості доступного холіну та, відповідно, ацетилхоліну в пацієнтів, для яких інгібітори холінестерази є недостатньо ефективними через низькі рівні медіатора в холінергічних синапсах.
Цереброваскулярна патологія та судинна деменція
Холінергічна система базальних ядер переднього мозку відіграє вагому роль у забезпеченні когнітивних функцій, зокрема уваги, пам’яті та емоцій, а також у регуляції мозкового кровообігу. Холінергічні структури та деякі ділянки ГМ, такі як гіпокамп (так звані СА1-нейрони), особливо чутливі до ішемічних уражень. Це може бути причиною порушень холінергічної передачі в патогенезі судинної деменції (СД), яка є другою за поширеністю причиною деменції, що дебютує в зрілому віці, після ХА.
На сьогодні не існує зареєстрованих препаратів для симптоматичного лікування когнітивних розладів при СД, оскільки наявні дані щодо впливу інгібіторів ацетилхолінестерази/холінестерази та мемантину на когнітивні функції при цьому захворюванні є неповними.
Однак, незважаючи на те що не існує конкретних препаратів для лікування пацієнтів із СД, комбінація інгібіторів ацетилхолінестерази/холінестерази та холінергічних попередників у таких хворих усе ж може виявитись ефективною. Раніше вже було висловлено припущення, що інгібітори ацетилхолінестерази/холінестерази (наприклад, такрин, донепезил, ривастигмін і галантамін) та мемантин можуть здійснювати нейропротекторний вплив, зменшуючи глутаматну нейротоксичність шляхом впливу на альфа‑4-бета‑2- та альфа‑7нікотинові ацетилхолінорецептори й інгібування апоптозу.
В усіх клінічних дослідженнях призначення холіну альфосцерату покращувало когнітивні симптоми (зменшувало дезорієнтацію, дратівливість, емоційну лабільність і байдужість до оточуючих), що підтверджувалося зниженням оцінки за геріатричною шкалою клінічної оцінки, розробленою компанією Sandoz (SCAG). Так, за даними L. Parnetti та співавт. (2001), порівняно з цитиколіном (у дозі 1000 мг в/м) холіну альфосцерат (у дозі 1000 мг в/м) більш значно покращував оцінку за шкалою SCAG.
Окрім того, при гострій цереброваскулярній патології (інсульт) лікування холіну альфосцератом (1000 мг/добу в/в протягом 4 тиж і 1200 мг/добу протягом наступних 5 міс) значно покращувало неврологічний статус, що підтверджувалося оцінками за шкалами MMSE, GDS і Крайтонською геріатричною шкалою – CGRS (C. Tomasina et al., 1991; E. Aguglia et al., 1993; G. Barbagallo Sangiorgi et al., 1994).
Хвороба Паркінсона
Деменція виявляється близько у 80% пацієнтів із ХП, у яких наявність цього синдрому пов’язана з підвищенням смертності та зниженням ефективності протипаркінсонічної терапії.
Інгібітори холінестерази, а саме ривастигмін, і мемантин, частковий агоніст глутаматних рецепторів, продемонстрували свою ефективність у лікуванні пацієнтів із ХП та деменцією, хоча цей ефект здебільшого оцінювали як помірний.
Окрім того, немає даних щодо довготривалого ефекту цих препаратів на стадіях помірних когнітивних розладів.
Левін і співавт. у недавньому відкритому 10-денному пілотному дослідженні за участю 60 пацієнтів із ХП та когнітивними порушеннями різного ступеня тяжкості порівнювали ефекти пірацетаму (в дозі 2000 мг в/в) із впливом холіну альфосцерату (1000 мг в/в) на когнітивні порушення. У цьому дослідженні автори продемонстрували доволі значну ефективність і безпечність холіну альфосцерату в пацієнтів із ХП та когнітивними розладами. Звертають на себе увагу дані про те, що холіну альфосцерат спричиняв помірне покращення когнітивного статусу хворих, яке, однак, виявилося вагомішим порівняно з пірацетамом (40 проти 25%; p<0,01). У пацієнтів із ХП, які отримували холіну альфосцерат, загальний стан та якість життя були кращими порівняно з хворими, що отримували пірацетам. Частота розвитку побічних ефектів становила 15% у пацієнтів, яким була проведена терапія холіну альфосцератом, і 35% у пацієнтів, які отримували пірацетам. Однак усі ці ефекти були незначно вираженими та не потребували припинення лікування.
Хоча теоретично можна було припускати, що покращення холінергічної передачі може погіршити симптоми у хворих із паркінсонізмом унаслідок розгальмування холінергічних нейронів смугастого тіла, під час терапії холіну альфосцератом не було помічено погіршення рухових порушень у пацієнтів із ХП.
Черепно-мозкова травма
ЧМТ – це комплексне пошкодження ГМ, що призводить до широкого спектра симптомів і клінічних синдромів.
У нещодавньому експериментальному дослідженні були докладно описані патофізіологічні механізми ЧМТ, відповідальні за втрату альфа‑7-нікотинових рецепторів, що призводить до екзайтотоксичного пошкодження, запалення та когнітивних порушень, які розвиваються після ЧМТ (P.G. Hoffmeister et al., 2011).
Банзел і співавт. також висловили думку про те, що холінергічна система блукаючого нерва здатна знижувати активність запальної реакції, спричиненої ЧМТ, імовірно, за рахунок впливу вторинного медіатора (наприклад, греліну).
Отже, вважається можливою здатність холінергічної стимуляції пригнічувати запальну реакцію, що розвинулася внаслідок ЧМТ. Це було підтверджено дослідженням Мандата та співавт., у якому оцінювали ефект холіну альфосцерату (в дозі 1000 мг/добу в/м протягом 14 днів і 800 мг/добу перорально протягом наступних 28 днів) у пацієнтів із гострим травматичним пошкодженням мозку. Було виявлено, що після 3 міс терапії неврологічний статус покращився в 96% пацієнтів без розвитку побічних ефектів (T. Mandat et al., 2003).
На підставі цих результатів автори припускали ефективність холіну альфосцерату в пацієнтів із ЧМТ.
Когнітивна функція
Як нормальне, так і патологічне старіння супроводжуються погіршенням короткотривалої пам’яті. Серед усіх нейромедіаторів ацетилхолін відіграє найважливішу роль у всіх системах пам’яті, беручи участь у різних біохімічних процесах.
Експериментальні та клінічні дослідження показали, що холіну альфосцерат є ефективним у лікуванні амнезії, індукованої введенням антагоніста мускаринових рецепторів скополаміну, але не впливає на амнестичні ефекти лоразепаму (препарат із групи бензодіазепінів) у здорових піддослідних, що дало змогу зробити висновок про вибірковий вплив холіну альфосцерату на холінергічну нейротрансмісію.
Крім того, холіну альфосцерат здатний запобігати віковому зниженню синтезу та вивільнення гормона росту (ГР).
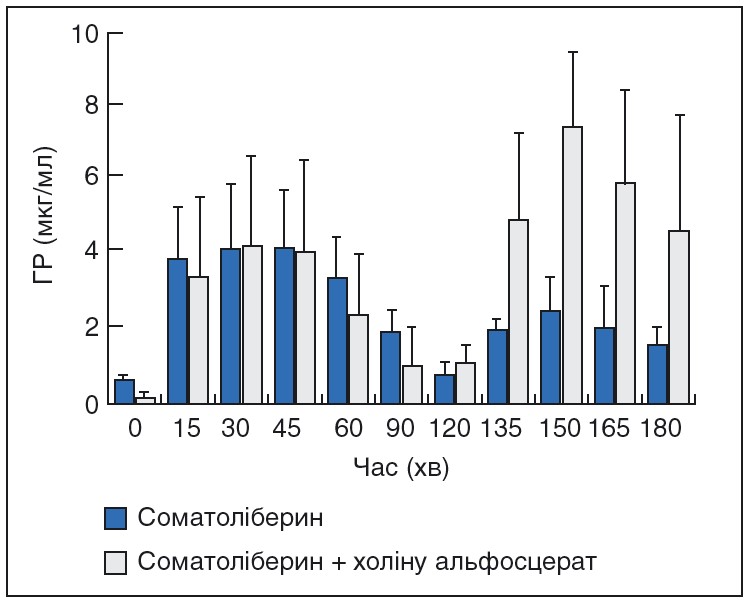
Зниження синтезу ГР пов’язують із виникненням когнітивних порушень у осіб літнього віку, при цьому відомо, що холінергічна система відіграє важливу роль у механізмі регуляції вивільнення ГР, стимульованого соматоліберином. Соматоліберин – це гіпоталамічний гормон, що стимулює секрецію ГР гіпофізом. Дані про те, що холіну альфосцерат здатний запобігати віковому зниженню чутливості секреції ГР до дії соматоліберину, є ще одним підтвердженням холінергічної активності цього препарату. Вплив на механізми секреції ГР відкриває перспективи до розширення показань до застосування цього засобу, крім лікування когнітивної дисфункції (рис. 3).
Рис. 3. Ефекти соматоліберину на секрецію ГР гіпофізом під впливом та поза дією холіну альфосцерату (2000 мг) у 6 пацієнтів похилого віку (модифіковано за G.P. Ceda та співавт., 1993)
В одному з нещодавніх експериментальних досліджень вивчався ефект цитиколіну (325 мг/кг/добу) та холіну альфосцерату (150 мг/кг/добу) на везикулярний переносник ацетилхоліну та холіну, а також на концентрацію ацетилхоліну в лобній корі, смугастому тілі та мозочку щурів (S.K. Tayebati et al., 2011). За допомогою вестерн-блоту автори виявили підвищення експресії везикулярного переносника ацетилхоліну в лобній корі, смугастому тілі та мозочку після введення цитиколіну та холіну альфосцерату порівняно з контролем, при цьому експресія транспортера холіну залишалася незмінною. Разом із тим за результатами імуноферментного аналізу (ELISA) було виявлено підвищення концентрації везикулярного транспортера ацетилхоліну під впливом холіну альфосцерату, що не підтвердилося для цитиколіну. Ці дані свідчать на користь теорії, що серед усіх описаних наразі холіновмісних фосфоліпідів холіну альфосцерат має найвищу холінергічну активність.
І нарешті, під час терапії холіну альфосцератом була зареєстрована низька частота розвитку побічних реакцій і не спостерігалося змін у частоті серцевих скорочень. Отже, зважаючи на задовільну ефективність і безпечність холіну альфосцерату, цей препарат доцільно використовувати в осіб літнього віку з деменцією та ризиком серцево-судинних катастроф.
Висновки
Літературні дані демонструють, що серед усіх холіновмісних фосфоліпідів холіну альфосцерат є найефективнішим щодо підвищення вивільнення ацетилхоліну in vivo. Його застосування показало позитивний вплив на когнітивні функції пацієнтів із різноманітними захворюваннями, включаючи деменцію легкого та середнього ступеня тяжкості нейродегенеративної, судинної чи комбінованої етіології, а також когнітивну дисфункцію при ХП та ЧМТ.
Клінічні й експериментальні дані підтверджують здатність холіну альфосцерату покращувати когнітивні симптоми (зокрема, пам’ять та увагу) більшою мірою порівняно з іншими холінерічними попередниками (наприклад, цитиколіном) і його задовільну переносимість. Отже, у зв’язку з його клінічною ефективністю та низькою частотою виникнення побічних ефектів холіну альфосцерат доцільно застосовувати в пацієнтів із деменцією, спричиненою неврологічними захворюваннями.
Список літератури знаходиться в редакції.
Functional Neurology, 2011; 26 (S1): 1-7. ISSN1971-3274.
Тематичний номер «Неврологія, Психіатрія, Психотерапія» № 1 (44), березень 2018 р.