15 квітня, 2018
Зв’язок окремих нестероїдних протизапальних препаратів із розвитком хронічних хвороб нирок: популяційне дослідження випадок-контроль
Хронічні хвороби нирок (ХХН) – важлива причина захворюваності та смертності у всьому світі [1, 2]. Протягом останніх десятиліть розповсюдженість ХХН постійно зростає. Цей показник є зіставним у країнах світу і становить близько 9-12% населення США, Австралії та Європи.
Особливо часто ХХН спостерігаються серед осіб похилого віку [3, 4]. Незначні відмінності в показниках поширеності ХХН зумовлені етнічною приналежністю популяції країни, методом визначення ХХН, формулою, яка використовується для оцінки швидкості клубочкової фільтрації, та особливостями дослідження.
Головними чинниками, що лежать в основі прогресивного зростання поширеності ХХН, є старіння населення, пандемія цукрового діабету (ЦД) 2 типу та інших коморбідних станів, зокрема артеріальної гіпертензії (АГ) [3, 5-9]. При цьому деякі широко застосовувані лікарські засоби, такі як нестероїдні протизапальні препарати (НПЗП), можуть впливати на функцію нирок [10-12]. Відомо, що НПЗП можуть призводити до гострого ураження нирок (ГУН), спричиняючи близько 16% усіх випадків ниркової недостатності (НН), пов’язаної з ліками [13]. Крім індукції зворотної НН, НПЗП можуть викликати гострий інтерстиційний нефрит з гематурією, протеїнурією та болем у боці [14], а також гострий тубулярний некроз. У рідкісних випадках можливий розвиток ниркового васкуліту та гострого папілярного некрозу [15].
Як відомо, застосування НПЗП здатне збільшувати ризик пришвидшеного прогресування ХХН через імунологічні та неімунологічні механізми. Імунологічні реакції, що розвиваються під час гострої фази, можуть продовжуватися і після розвитку первинного ураження нирки [16]. Отже, повторні епізоди НПЗП-індукованого ГУН можуть призвести до ХХН чи хронічного інтерстиційного нефриту з асоційованим інтерстиційним фіброзом або хронічним папілярним некрозом.
Хоча встановлено, що НПЗП характеризуються гострими побічними явищами з боку нирок, хронічні ниркові ефекти внаслідок прийому цих засобів описані гірше. Єдиним НПЗП, пов’язаним із хронічним негативним впливом на нирки, є фенацетин, відкликаний із фармацевтичного ринку через здатність зумовлювати папілярний некроз із подальшим розвитком ХХН [17].
Як основа нефротоксичності вивчалася роль періодів піврозпаду цих препаратів. Adams та співавт. висловили думку, що НПЗП з довшим періодом піврозпаду, найімовірніше, спричиняють нефротоксичні ефекти внаслідок тривалого пригнічення простагландинів, що призводить до тривалого зниження ниркового кровотоку, при цьому в разі використання НПЗП короткотривалої дії нирки мають можливість відновитися між прийомом окремих доз [18]. Дослідження зв’язку між вживанням НПЗП та розвитком нових випадків ХХН є складним, оскільки ХХН може передувати субклінічне ушкодження нирок [19]. Більшість попередніх досліджень оцінювали ризик гострої НН [20-22] або фокусувалися на прогресуванні вже наявної ХХН, а не на розвитку нових випадків [23-25]. У зв’язку з цим мета цього популяційного дослідження – оцінити та порівняти зв’язки між застосуванням окремих НПЗП та ризиком ХХН у загальній популяції Південної Італії.
Методи
Інформація була отримана з бази даних Arianna, що включає клінічні та демографічні характеристики близько 300 тис. жителів провінції Казерта (Італія); дані щодо призначених ліків та показань до їх застосування; статистику госпіталізацій та проведених медичних процедур. Попередні наукові роботи продемонстрували, що база даних Arianna є надійним джерелом для фармакоепідеміологічних досліджень [10, 26-32].
Обсерваційне ретроспективне неінтервенційне дослідження охопило 123 лікарів загальної практики та 158 510 пацієнтів без ХХН, зареєстрованих ними з 2006 по 2011 рік. Як випадки розглядалися всі пацієнти з діагнозом ХХН, встановленим за період дослідження (2006-2011 рр.). Початком захворювання вважалася дата першого встановлення цього діагнозу. Для кожного випадку ХХН було випадковим чином обрано до 4 осіб контролю без зазначеної патології, що відповідали за статтю та віком (± 3 роки). Застосування НПЗП оцінювалося загалом та за окремими речовинами й класами за такими категоріями: похідні оцтової кислоти та споріднені речовини, оксиками, похідні пропіонової кислоти, інші протизапальні та антиревматичні агенти нестероїдної природи, коксиби, саліцилова кислота та її похідні. Випадки використання >1 НПЗП оцінювалися окремо. Анамнез вживання НПЗП оцінювався під час 3 часових періодів: за 90, 180 та 365 діб до дня встановлення діагнозу ХХН. Пацієнти, що приймали щонайменше 1 НПЗП упродовж 90 днів до встановлення зазначеного діагнозу, вважалися поточними користувачами НПЗП та досліджувалися особливо ретельно. Щоб визначити вплив тривалості прийому НПЗП на ризик ХХН, оцінювали розрахунковий кумулятивний показник: загальну кількість призначеного препарату ділили на встановлену добову дозу НПЗП. Як незалежні змінні, що можуть впливати на результат, були розглянуті всі потенційні фактори ризику ХХН, у т. ч. коморбідні стани (злоякісні пухлини, ішемічна хвороба серця, ЦД, хвороби печінки, подагра, дисліпідемія, АГ, цереброваскулярні захворювання, системний червоний вовчак, амілоїдоз, васкуліт, мієлома, полікістоз нирок); попереднє застосування інших нефротоксичних засобів (аміноглікозидів, препаратів золота та літію) [34]. Демографічні та клінічні характеристики випадків і контролів порівнювалися за допомогою методу хі-квадрат та t-тесту для категорійних та неперервних змінних. Оцінювання нормальності розподілу проводилося за методами Шапіро-Уїлка та Колмогорова-Смірнова. Щоб оцінити ризик ХХН, асоційованої з прийомом окремих НПЗП, було проведено логістичний аналіз. Ризик ХХН представлено як скориговане відношення шансів (ВШ) та 95% довірчий інтервал (ДІ). Оцінювали також ризик ХХН для кожного наступного місяця прийому НПЗП. Дані вважалися значущими при p<0,05. Аналіз було проведено за допомогою програмного забезпечення SAS Release 9.3.
 Результати
Результати
Упродовж 2006-2011 рр. було ідентифіковано 2128 пацієнтів із діагнозом ХХН, з них 1989 особам діагноз було встановлено вперше, для контролю автори обрали 7906 учасників.
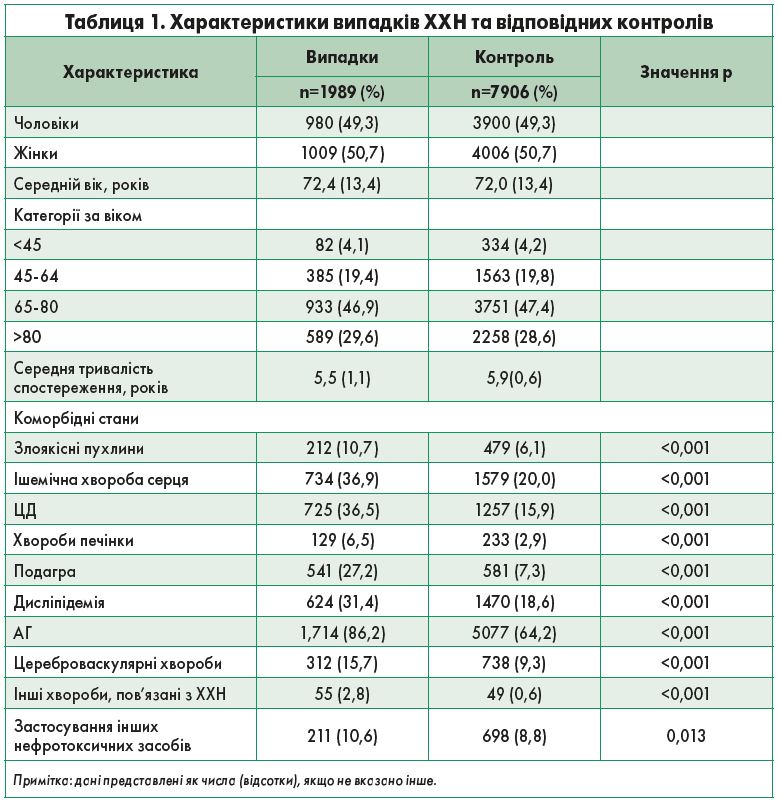
У таблиці 1 представлені характеристики випадків ХХН та контролів. В обох групах спостерігалася однакова кількість чоловіків та жінок, >75% учасників були віком старше 65 років.
У порівнянні з групою контролю пацієнти з ХХН частіше мали злоякісні новоутворення, ішемічну хворобу серця, ЦД, хвороби печінки, подагру, дисліпідемію, АГ, цереброваскулярні захворювання, а також частіше приймали нефротоксичні засоби (крім НПЗП; p=0,013).
Усі коморбідні стани та застосування нефротоксичних засобів (сульфонаміди, аміноглікозиди, препарати золота та літію, золедронат, колістин) оцінювалися у всі проміжки часу до встановлення діагнозу.
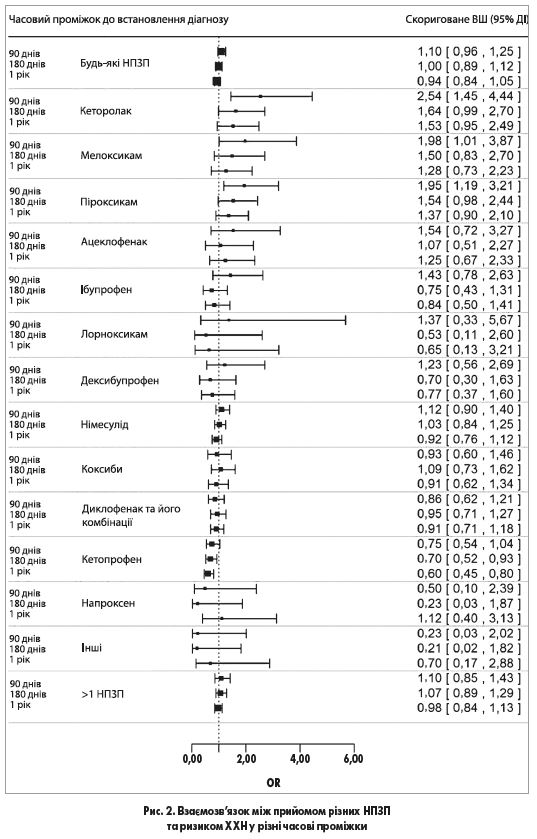
Р езультати мультиваріантних моделей для всіх НПЗП та окремих речовин представлені на рисунках 1 та 2.
езультати мультиваріантних моделей для всіх НПЗП та окремих речовин представлені на рисунках 1 та 2.
Статистично достовірне зростання ризику ХХН було відзначено в осіб, які застосовували оксиками (ВШ 1,74; 95% ДІ: 1,20-2,54; p=0,004); якщо розглядати окремі речовини, то в пацієнтів, що вживали мелоксикам (ВШ 1,98; 95% ДІ: 1,01-3,87; p=0,046), піроксикам (ВШ 1,95; 95% ДІ: 1,19-3,21; p=0,008) та кеторолак (ВШ 2,54; 95% ДІ: 1,45-4,44; p=0,001).
У межах більших часових проміжків достовірних асоціацій виявлено не було.
 Наявність АГ чи ЦД не впливала на зв’язок між прийомом піроксикаму, мелоксикаму чи кеторолаку та підвищеним ризиком ХХН.
Наявність АГ чи ЦД не впливала на зв’язок між прийомом піроксикаму, мелоксикаму чи кеторолаку та підвищеним ризиком ХХН.
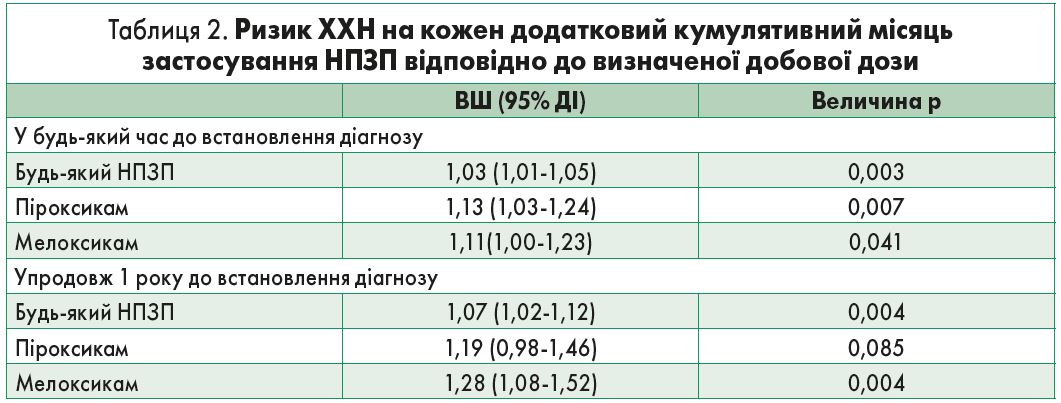
Ризик ХХН зростав на 28% (ВШ 1,28; 95% ДІ: 1,08-1,52; p=0,004) та на 11% (ВШ 1,11; 95% ДІ: 1,00-1,23; p=0,041) на кожен кумулятивний місяць терапії мелоксикамом упродовж 1 року до встановлення діагнозу ХХН та протягом будь-якого часу до діагнозу відповідно (табл. 2).
Ризик ХХН також збільшувався на 19% (ВШ 1,19; 95% ДІ: 0,98-1,46; p=0,085) та на 13% (ВШ 1,13; 95% ДІ: 1,03-1,24; p=0,007) на кожен кумулятивний місяць терапії піроксикамом упродовж 1 року до встановлення діагнозу ХХН та протягом будь-якого часу до діагнозу відповідно (табл. 2).
Серед пацієнтів, що вживали піроксикам, найбільш значуще статистично достовірне зростання ризику ХХН спостерігалося при кумулятивній тривалості прийому більше 180 днів (ВШ 5,73; 95% ДІ: 1,10-29,69; p=0,038); подібні результати були отримані і для мелоксикаму (ВШ 4,24; 95% ДІ: 1,08-16,71; p=0,039). Кеторолак завжди використовувався <3 міс.
Результати стандартизовані за наявністю злоякісних пухлин, ішемічної хвороби серця, ЦД, хвороб печінки, подагри, дисліпідемії, АГ, цереброваскулярної хвороби, системного червоного вовчака, амілоїдозу, васкуліту, мієломи, полікістозу нирок, прийому нефротоксичних засобів.
Обговорення
! Результати цього дослідження свідчать, що НПЗП як клас не зумовлюють статистично достовірного збільшення ХХН. В іспанському дослідженні випадок-контроль також було показано, що довготермінове застосування (6 міс) НПЗП не пов’язано зі зростанням ризику термінальних стадій хвороб нирок [35].
У попередніх дослідженнях, присвячених зв’язку між прийомом окремих НПЗП та ризиком ХХН, було отримано суперечливі результати [36]. Огляди McLaughlin і співавт. (1998) та Delzell і співавт. (1998) не змогли з наявних доказів зробити чіткі висновки [36, 37]. В інших двох дослідженнях випадок-контроль НПЗП продемонстрували зв’язок із підвищенням ризику ХХН [38, 39], хоча таку асоціацію було заперечено у трьох когортних випробуваннях за участю здорових осіб [23-25, 40]. Ще одне дослідження випадок-контроль виявило зв’язок між хронічним застосуванням ацетилсаліцилової кислоти в аналгетичних дозах та ризиком ХХН [41], хоча це не було підтверджено в двох інших подібних випробуваннях за даними телефонних опитувань [38, 39] та трьох когортних дослідженнях [23-25], що включали тільки чоловіків [23] чи тільки жінок [24]. Однак жодне з цих випробувань не оцінювало ризик ХХН відповідно до різних проміжків часу до встановлення діагнозу.
Великі обсерваційні когортні дослідження, наприклад Nurses’ Health Study [24] та дослідження за участю відносно здорових лікарів чоловічої статі [40], для виявлення прийому НПЗП застосовували анкети, що могло вплинути на точність результатів. Висока кумулятивна тривалість прийому НПЗП асоціювалася з підвищенням ризику швидкого прогресування ХХН в осіб похилого віку [25].
У зазначеному дослідженні ризик розвитку ХХН у пацієнтів, що вживали оксиками, зростав практично на 70%. Таке збільшення ризику було найбільш вражаючим для мелоксикаму та піроксикаму. Це може бути пов’язано з тривалим періодом піврозпаду оксикамів, зокрема піроксикаму (50 год) та мелоксикаму (20 год), що призводить до підтримання відносно стабільної концентрації діючої речовини в плазмі крові впродовж доби в разі однократного прийому та до значного накопичення препарату при кількаразовому застосуванні, що вказано в характеристиках цих ліків. Обидва оксиками діють шляхом зниження синтезу простагландинів у зв’язку з пригніченням циклооксигенази.
Відомо, що довготривале вживання НПЗП на кшталт піроксикаму призводить до ушкодження нирок, у т. ч. папілярного некрозу [42]. Цікаво, що найвищий ризик ХХН спостерігався для піроксикаму та кеторолаку, які також супроводжуються найвищим ризиком інших серйозних побічних явищ, зокрема ушкоджень верхніх відділів шлунково-кишкового тракту [43, 44]. Нефротоксичність особливо небезпечна для пацієнтів, в яких простагландини нирок відіграють головну роль у підтриманні перфузії нирки. У цих осіб зниження утворення простагландинів унаслідок прийому НПЗП може зменшувати нирковий кровоток і призводити до НН [42].
! Відповідно до вищенаведених даних дослідження виявило найвищий ризик ХХН в осіб, які вживали мелоксикам та піроксикам упродовж тривалого часу, навіть з огляду на те, що цей аналіз був обмежений малою кількістю таких пацієнтів.
Слід зазначити, що на сьогодні ХХН не вказується серед ймовірних побічних ефектів піроксикаму чи мелоксикаму в описі цих засобів. Ризик ХХН зростає на 28% та на 19% на кожен додатковий місяць терапії мелоксикамом чи піроксикамом упродовж року до встановлення діагнозу, хоча ця різниця не досягла рівня статистичної значущості.
! Отримані результати також свідчать про збільшення ризику ХХН у 2,5 раза в пацієнтів, що протягом короткого часу приймають кеторолак. Таким чином, цей потужний НПЗП здатен сприяти прогресуванню субклінічної ХХН із розвитком розгорнутої клінічно вираженої хвороби. І якщо велика кількість НПЗП призначається при хронічних станах (остеоартрит, ревматоїдний артрит), кеторолак показаний тільки для короткотривалого використання (максимум 5 днів при пероральному та 2 дні при внутрішньом’язовому введенні) з метою лікування помірного/сильного гострого болю, у т. ч. післяопераційного [45, 46].
У минулому кеторолак також застосовувався в довготривалому лікуванні хронічного ракового болю та больових синдромів іншого походження (наприклад, при остеоартритах). Упродовж років використання настороженість щодо ризику побічних явищ, особливо гастроінтестинальних кровотеч чи виразкування, внаслідок прийому кеторолаку зростала. У зв’язку з цим максимальну тривалість вживання кеторолаку було обмежено до кількох днів [47].
Відповідно до опису характеристик цього лікарського засобу кеторолак протипоказаний при ушкодженні нирок від помірного до тяжкого ступеня (креатинін сироватки >442 мкмоль/л) та в пацієнтів групи ризику НН унаслідок втрати об’єму циркулюючої крові чи дегідратації. Оскільки кеторолак є потужним інгібітором простагландинів, слід обережно застосовувати його в пацієнтів з анамнезом хвороб нирок чи порушеною будь-яким чином функцією нирки. Пов’язана з вживанням кеторолаку ниркова токсичність спостерігалася при гіповолемії та/або порушеннях кровотоку в нирці, тому що в таких випадках простагландини відіграють важливу роль у підтриманні перфузії цього органу. У такому разі прийом кеторолаку здатен призвести до зниження кількості ниркових простагландинів, що збільшує ризик розвитку ниркової недостатності [48, 49]. Взаємозв’язок між вживанням піроксикаму, мелоксикаму чи кеторолаку та ризиком ХХН не залежала від наявності АГ чи ЦД.
Зазначене дослідження має кілька переваг та обмежень. Методологія, що використовується в ньому, передбачала аналіз загальної бази даних системи охорони здоров’я, тому перевагою є однорідність інформації: вибірка була створена на основі рутинної медичної допомоги за участю всіх сімейних лікарів регіону.
Однак оскільки діагнози встановлювалися сімейними лікарями, а не нефрологами, то ймовірно, що деякі з них є неточними. Неможливо також виключити неправильну класифікацію ХХН. Для запобігання плутанини між ГУН та ХХН як індикатори ХХН застосовувалися лише ті коди, які реєструвалися більше одного разу. Точною датою розвитку ХХН вважався день реєстрації першого надання медичної допомоги з цього приводу. Проте між порушенням ниркової функції та реєстрацією ХХН міг пройти певний час, тому авторами ретельно розглядався часовий проміжок 1 рік до встановлення діагнозу. Здебільшого було неможливо визначити стадію ХХН, оскільки необхідних для цього результатів лабораторних обстежень немає в базі даних Arianna, а зареєстровані коди рідко включають постадійну класифікацію ХХН.
Коди з включенням стадії ХХН були представлені для 339 (17,0%) пацієнтів, і аналіз цієї підгрупи підтвердив результати загальної популяції дослідження. Позаяк використовувалися дані амбулаторних пацієнтів, не можна однозначно стверджувати, що ліки приймалися відповідно до призначень. При цьому НПЗП переважно призначалися як протизапальні засоби при хронічних хворобах на кшталт артриту, тому немає також підстав підозрювати, що пацієнти їх не вживали.
За допомогою використаної бази даних неможливо відстежити застосування безрецептурних НПЗП, що може призвести до недооцінювання кількості прийнятих засобів цього класу, що продаються без рецепта лікаря (ібупрофен, ацетилсаліцилова кислота, кетопрофену лізинова сіль тощо). Однак безрецептурні НПЗП містять набагато менше діючої речовини, ніж рецептурні, тому дозозалежна відповідь, що відіграє роль у розвитку НПЗП-асоційованих ХХН, є менш значущою.
Висновки
У той час як гострі ниркові розлади, асоційовані з НПЗП, широко досліджуються, хронічним розладам приділяється мало уваги. Однак результати цього дослідження показують різний ризик хронічного ушкодження нирок для різних НПЗП. Довготривалий прийом НПЗП із найдовшим періодом піврозпаду (оксиками) асоціюється зі збільшеним ризиком ХХН. При цьому із зростанням ймовірності розвитку ХХН пов’язане короткотривале вживання кеторолаку, який може діяти як тригер погіршення ниркової функції в пацієнтів із субклінічною ХХН.
Список літератури знаходиться в редакції.
Ingrasciotta Y., Sultana J., Giorgianni F. et al. Association of Individual Non-Steroidal Anti-Inflammatory Drugs and Chronic Kidney Disease: A Population-Based Case Control Study. PLoS ONE2015 Apr 16 10(4): e0122899. doi:10.1371/journal.pone.0122899
Переклала з англ. Лариса Стрільчук
Медична газета «Здоров’я України 21 сторіччя» № 6 (427), березень 2018 р.