15 квітня, 2018
Актуальные вопросы нефрологии, диализа и трансплантации
Во второй четверг марта во всем мире отмечается Международный день почки. Именно этому дню была посвящена научно-практическая конференция «Актуальные вопросы нефрологии, диализа и трансплантации», состоявшаяся 6 марта в г. Ирпене. Мероприятие было организовано Национальной медицинской академией последипломного образования (НМАПО) им. П. Л. Шупика (г. Киев).

Хронические болезни почек (ХБП) у взрослых крайне распространены: ими страдает 14,3% всего населения планеты и 36,1% лиц групп высокого риска (с артериальной гипертензией (АГ) и другими сердечно-сосудистыми заболеваниями (ССЗ), сахарным диабетом (СД)) (Ene-Iodache B. et al., 2016). Среди детей эти показатели ниже: в Европе ХБП ІІІ-V стадии фиксируются в 55-60 случаях, а в Украине – в 90 случаях на 1 млн детского населения. Основными причинами ХБП у взрослых являются гипертензивная и диабетическая нефропатии, и более редко – собственно заболевания почек. Среди детей ведущие позиции среди этиологических факторов ХБП занимают врожденные болезни и пороки развития, в т. ч. обструктивная уропатия, гипо- или дисплазия почки, рефлюкс-нефропатия, фокальный сегментарный гломерулосклероз, поликистоз почек.
Зависимость сердечно-сосудистого риска от состояния почек представлена в концепции ренокардиального континуума. Эта концепция гласит, что профилактическое воздействие на стадии отсутствия поражения органов-мишеней (в частности почек) и стадии субклинического поражения способно снизить риск развития хронической почечной недостаточности (ХПН) и уменьшить смертность. При наличии симптоматического поражения органов-мишеней возможно лишь замедление прогрессирования болезни, что также является благоприятным влиянием.
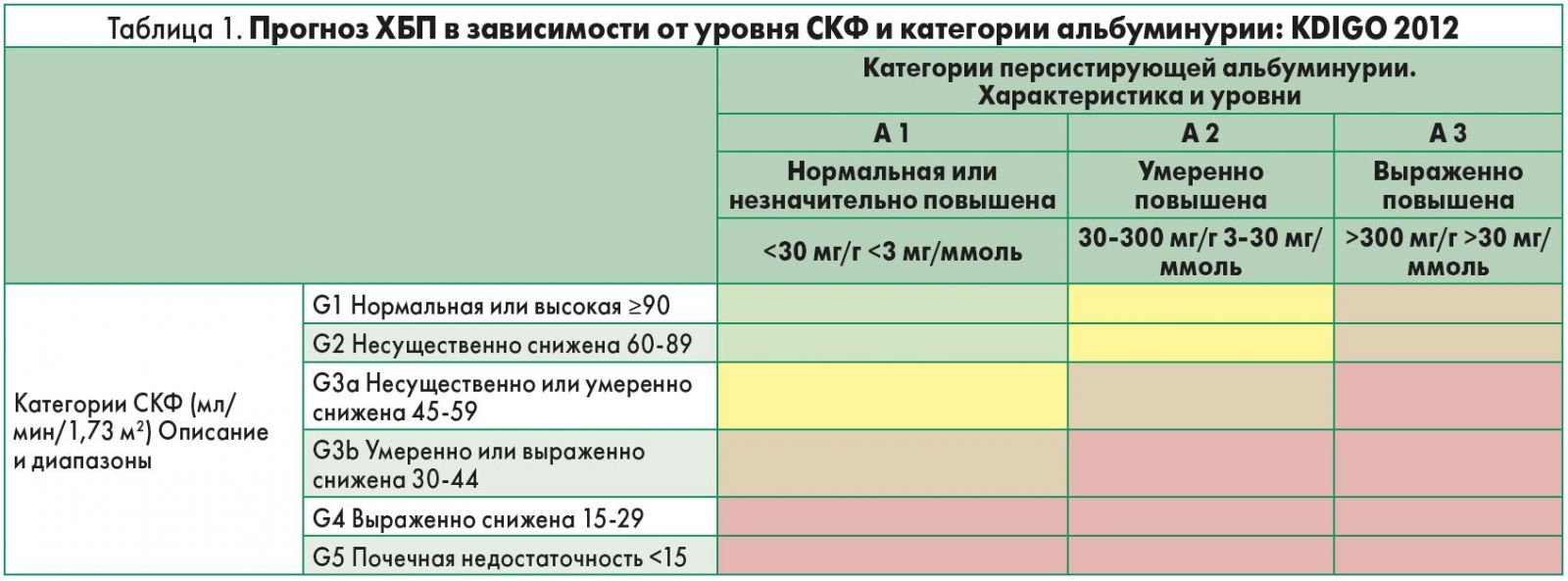
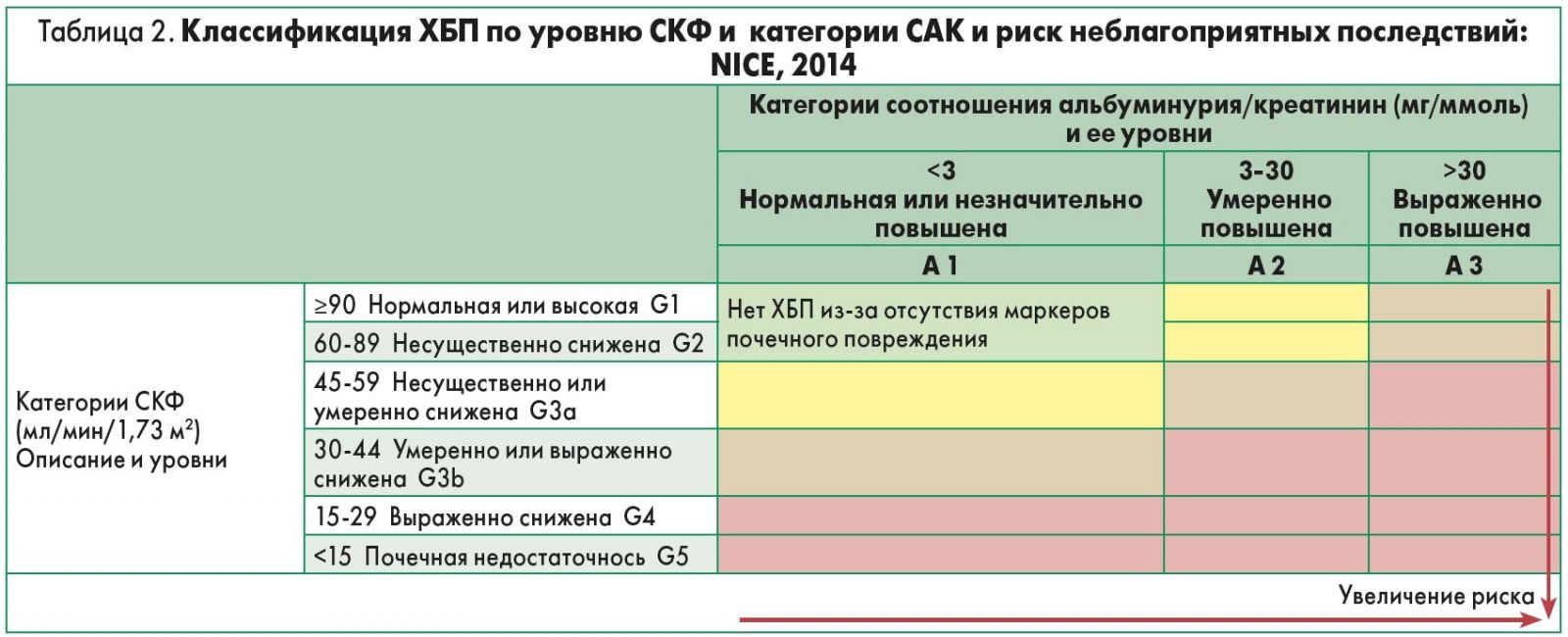
Прогноз ХБП зависит от наличия альбуминурии и ее уровня, а также от СКФ (табл. 1). Важное значение имеют также изменения соотношения альбуминурия/креатинин (САК); этому показателю придается даже большее значение, чем просто альбуминурии (мг/ммоль) (табл. 2).
Для расчета СКФ у взрослых пациентов применяется формула GFR-EPI, для детей – формула Шварца (Matsushita K. et al., 2012). Существует также специальное приложение для мобильных устройств, позволяющее рассчитать СКФ. Для пациентов с предполагаемой гиперфильтрацией используются проба Реберга-Тареева или реносцинтиграфия. В наше время гиперфильтрация рассматривается как неблагоприятный прогностический фактор, требующий коррекции с помощью ингибиторов ангиотензин-превращающего фермента (ИАПФ).
Согласно стратификации риска Европейского общества гипертензии / Европейского общества кардиологов (2013), все пациенты с ХБП характеризуются высоким и очень высоким риском, что обуславливает у них потребность в применении комбинированной терапии даже при условии незначительного повышения артериального давления (АД).
Главными признаками, на которые следует обращать внимание при определении прогноза ХБП, являются альбуминурия (или САК), креатинин (или СКФ) и АГ. Все эти признаки реализуются через сосудистый компонент ренокардиального континуума и структурные изменения почек. Для торможения развития этих опасных проявлений ХБП следует назначать корректную антигипертензивную терапию с антипролиферативными свойствами, применять иммуносупрессанты и иммунобиологические препараты, использовать ИАПФ или блокаторы рецепторов ангиотензина ІІ (БРА) с целью ренопротекции. Важно, что последнюю группу медикаментов следует назначать независимо от наличия повышенного АД. Оптимальными комбинациями являются сочетания ИАПФ с моксонидином, лерканидипином, небивололом, торасемидом, ксипамидом. Для простоты запоминания этих комбинаций существует мнемоническое слово «БРИМОНЕЛ» – БРА/ИАПФ, МОксонидин, НЕбиволол, Лерканидипин.
Раннее врачебное вмешательство при наличии у пациента альбуминурии обеспечивает динамику возрастного снижения СКФ, близкую к показателям лиц без белка в моче. Целевым уровнем АД для взрослых больных с ХБП является <130/80 мм рт. ст. У детей АД (как систолическое, так и диастолическое) следует снижать до уровня 50-го процентиля для данного возраста, пола и роста, если достижение этой цели не ограничено симптомами гипотонии.
 Основными препаратами при ХБП являются блокаторы ренин-ангиотензиновой системы (РААС), т. е. ИАПФ, БРА и прямые ингибиторы ренина, а также вазодилатирующие β-блокаторы (небиволол) и β-блокаторы с α-блокирующими свойствами (карведилол), селективные кальциевые блокаторы (лерканидипин), диуретики.
Основными препаратами при ХБП являются блокаторы ренин-ангиотензиновой системы (РААС), т. е. ИАПФ, БРА и прямые ингибиторы ренина, а также вазодилатирующие β-блокаторы (небиволол) и β-блокаторы с α-блокирующими свойствами (карведилол), селективные кальциевые блокаторы (лерканидипин), диуретики.
Выбор между ИАПФ и БРА неоднозначен и иногда зависит только от решения врача, однако, например, пациентов, перенесших инфаркт миокарда, которые ранее принимали сартаны, cледует перевести на ИАПФ. Последние также обладают преимуществом перед сартанами у пациентов с нормотензией или незначительным повышением АД, требующих, однако, ренопротекции с помощью блокаторов РААС.
Рамиприл – ИАПФ, который характеризуется крупной доказательной базой клинических исследований и обеспечивает защиту всех органов-мишеней при АГ (на 24% снижает риск прогрессирования нефропатии, на 33% – инсульта, на 26% – ишемических атак, на 13% – прогрессирования стенокардии, на 20% – сердечной недостаточности, на 22% – инфаркта миокарда (HOPE study investigators, 2000). Рамиприл улучшает кровообращение в почках и стабилизирует уровень гломерулярной фильтрации, в т. ч. у пациентов с сердечной недостаточностью. Этот ИАПФ показан для лечения ХБП (как диабетического, так и недиабетического происхождения) при любом клиренсе креатинина. Рамиприл характеризуется двойным способом выведения: почечным (60%) и печеночным (40%) (Vuong A.D., Annis L.G., 2003).
При СКФ >120 или на уровне 60-30 мл/мин/1,73 м2 применяются ИАПФ или БРА в зависимости от клинической ситуации. При наличии выраженного сердечно-сосудистого риска назначается рамиприл, с целью исключительно снижения АД – сартаны. При снижении СКФ <30 мл/мин/1,73 м2 ИАПФ и БРА отменяются с целью искусственной индукции гиперфильтрации, однако их применение можно продолжить у больных с высоким кардиоваскулярным риском (валсартан в маленьких дозах). При начале гемодиализа пациент может вернуться к терапии ИАПФ или БРА.
Профессор Иванов также возглавил заседание дискуссионного клуба, посвященное нестероидным противовоспалительным препаратам (НПВП) и ХБП. НПВП применяются в нефрологии с целью контроля воспаления и ликвидации гипертермии. Среди препаратов данной группы в этой области используются нимесулид, кетопрофен, коксибы. Важно, что при патологии почек следует отказаться от ибупрофена. В свою очередь, длительное применение коксибов ограничено их кардиотоксичными свойствами.
Метаанализ 36 рандомизированных контролированных исследований (n=4887) установил, что при эпизодах острой боли в почках, связанной с наличием конкремента, у пациентов с адекватной почечной функцией лечение НПВП обеспечивает наиболее эффективное и стойкое обезболивание с меньшим количеством побочных явлений по сравнению с опиоидами или парацетамолом (Pathan S.A. et al., 2017).
Риск использования НПВП в нефрологии зависит от СКФ. Неблагоприятными условиями считаются острое поражение почек (ОПП) как на фоне ХБП, так и само по себе. Согласно классификации 2012 г., ОПП делится на стадии в зависимости от концентрации креатинина и количества выделяемой мочи. При ОПП следует прекратить применение нефротоксических агентов (по возможности), обеспечить нормоволемию и перфузионное давление, проводить функциональный гемодинамический мониторинг, контролировать концентрацию креатинина в крови и выделения мочи, избегать развития гипергликемии, рассмотреть альтернативу проведению радиоконтрастных процедур. При второй стадии ОПП следует рассмотреть потребность в проведении почечно-заместительного лечения и в переведении больного в блок интенсивной терапии. В условиях длительного наблюдения за больным с ОПП можно также назначать ИАПФ/БРА. Во избежание контрастиндуцированного ОПП не следует проводить исследования с контрастом при СКФ <30мл/мин/1,73 м2, а при СКФ 30-45 мл/ин назначать их лишь по жизненным показаниям.
Мощным аналгетиком с низким уровнем осложнений и возможностью длительного применения является кетопрофен. Риск желудочно-кишечных кровотечений при приеме кетопрофена в 8 раз меньше, чем при приеме кеторолака. Кетопрофен характеризуется двойным механизмом действия: центральным и периферическим. Некоторые НПВП (в частности кеторолак и мелоксикам) увеличивают риск поражения почек. Это делает кетопрофен (Кетонал®, Сандоз) одним из лучших решений для контроля боли у пациентов с ХБП.

В структуре смертности в Европе кардиоваскулярные заболевания занимают большую долю у женщин, чем у мужчин. Это несколько отличается от привычной точки зрения, что ССЗ – прерогатива мужчин. Согласно статистическим данным, больные с ХБП наиболее часто умирают именно от ССЗ и онкологических заболеваний.
ХБП со СКФ 30-59 мл/мин/1,73 м2 позволяет отнести пациента с ССЗ к больным высокого риска, с СКФ <30 мл/мин/1,73 м2 – очень высокого. Рекомендации Европейского общества кардиологов / Европейского общества атеросклероза по лечению дислипидемий (2016) указывают, что показателем очень высокого риска является снижение СКФ <60 мл/мин/1,73 м2. Еще более новые рекомендации Американской ассоциации клинических эндокринологов и Американского колледжа эндокринологии (2017) характеризуют больных с ССЗ и ХБП ІІІ-IV стадии как лиц экстремально высокого риска наряду с пациентами с ССЗ и сахарным диабетом или ССЗ и гетерозиготной семейной гиперхолестеринемией. Таким образом, в большинстве регуляторных документов основным критерием кардиоваскулярного риска выступает СКФ, и только в рекомендациях Американского колледжа кардиологии по лечению АГ (2017) в качестве маркера поражения почек рассматривается протеинурия.
 Важнейшим фактором управления общественным здоровьем является контроль АГ. Пациент с ХБП должен дожить до стадии диализа, а не умереть раньше от кардиологических осложнений. Согласно Европейским рекомендациям по профилактике кардиоваскулярных заболеваний в клинической практике (2016), уровень кальцификации коронарных артерий и подтвержденное наличие атеросклеротических бляшек в сонных артериях могут выступать модификаторами кардиоваскулярного риска. Соотношение кальциевого индекса и уровней коронарного атеросклероза представлены в табл. 3.
Важнейшим фактором управления общественным здоровьем является контроль АГ. Пациент с ХБП должен дожить до стадии диализа, а не умереть раньше от кардиологических осложнений. Согласно Европейским рекомендациям по профилактике кардиоваскулярных заболеваний в клинической практике (2016), уровень кальцификации коронарных артерий и подтвержденное наличие атеросклеротических бляшек в сонных артериях могут выступать модификаторами кардиоваскулярного риска. Соотношение кальциевого индекса и уровней коронарного атеросклероза представлены в табл. 3.
Рекомендации Европейского общества кардиологов / Европейского общества гипертензии по неинвазивным визуализационным методам диагностики субклинического поражения органов у больных с АГ предусматривают ультразвуковое исследование абдоминальной аорты (у пациентов с длительной тяжелой АГ) и сонных артерий, магнитно-резонансную томографию мозга (у больных старшего возраста с неврологическими изменениями), фундоскопию (у пациентов с тяжелой и/или резистентной АГ), определение кальциевого индекса (у пациентов со средней оценкой по шкале SCORE). Четких показаний к визуализационному исследованию почек на данный момент не существует.
 Американские рекомендации 2017 г. предлагают считать нормальным уровень АД ниже 120/80 мм рт. ст., а показатели >140/90 мм рт. ст. рассматривать как АГ 2 степени, требующую комбинированной терапии.
Американские рекомендации 2017 г. предлагают считать нормальным уровень АД ниже 120/80 мм рт. ст., а показатели >140/90 мм рт. ст. рассматривать как АГ 2 степени, требующую комбинированной терапии.
Крупный метаанализ установил, что интенсивный контроль систолического АД у больных без болезней почек сопровождается уменьшением количества случаев почечной недостаточности, снижением кардиоваскулярной смертности и смертности от всех причин (Beddhu S. et al. 2017). В свою очередь, при наличии болезней почек интенсификация контроля АД сопровождается слабым позитивным влиянием, что можно объяснить развитием некоторых побочных действий антигипертензивной терапии (гипотензия, ОПП, острая почечная недостаточность). Согласно результатам исследования CLARIFY, снижение систолического АД <140 мм рт. ст. сопровождается уменьшением показателя смертности, в то время как дальнейшее его падение до <120 мм рт. ст. ведет к возрастанию количества смертей. Это обусловливает потребность в определении нижних границ целевого АД. Существуют данные, что уровень диастолического АД <60 мм рт. ст. является предиктором смерти у послеинфарктного больного с коронарным атеросклерозом.
Согласно рекомендациям Канадского кардиоваскулярного общества, целевые значения АД должны составлять <140/90 мм рт. ст., однако существуют клинические показания для интенсификации лечения пациентов высокого риска. Среди них заболевания сердечно-сосудистой системы с клиническими или субклиническими проявлениями, ХБП (недиабетическая нефропатия, протеинурия <1 г/сут, расчетная СКФ 20-59 мл/мин/1,73 м2/1,73 м2), рассчитанный по Фрамингемской шкале оценки риска 10-летний глобальный сердечно-сосудистый риск ≥15%, возраст 75 лет и старше. При наличии одного и более клинического показания пациенты должны давать согласие на интенсивную терапию.
Согласно отечественным рекомендациям, целевое АД при ХБП составляет <130/80 мм рт. ст. Начинать лечение АГ следует как можно раньше, не дожидаясь значимого повышения кардиоваскулярного риска. К сожалению, в Украине наблюдается высокий процент позднего обращения пациентов с АГ за медицинской помощью, что осложняет их полноценное лечение.
Препаратами выбора являются ИАПФ, поскольку медикаменты этого класса способны уменьшать протеинурию и замедлять прогрессирование ХБП. При наличии у больного протеинурии следует применять именно ИАПФ, а при ее отсутствии – выбирать любой антигипертензивный препарат первой линии. Следует отметить, что американские рекомендации исключили из средств первой линии β-блокаторы, применяемые лишь по особым показаниям (сердечная недостаточность, аритмия, тахикардия) или в качестве препаратов второй линии.
Представитель ИАПФ рамиприл характеризуется обширной доказательной базой (HOPE, Micro-HOPE, REIN, ONTARGET, AASK, AIRE, PLUR). В частности, в исследовании HOPE (n=9297) рамиприл продемонстрировал снижение смертности от сердечно-сосудистых причин на 37% по сравнению с плацебо. Рамиприлу также свойственны широкий спектр показаний, сбалансированность выведения и удобство в применении (1 таблетка/сут). При назначении комбинированной терапии следует учитывать, что, согласно результатам исследования ACCOMPLISH, назначение комбинации ИАПФ и антагониста кальция характеризовалось снижением риска сердечно-сосудистых осложнений на 20% по сравнению с сочетанием ИАПФ и гидрохлортиазида (Jamerson K. et al. for the ACCOMPLISH Tral Investigators, 2008).
Докладчик отметил, что в нефрологии несколько недооценена роль дислипидемий в отличие от кардиологии. Согласно рекомендациям Европейского общества кардиологов / Европейского общества атеросклероза по лечению дислипидемий (2016), при наличии умеренной / тяжелой почечной недостаточности пациент должен быть отнесен к группе высокого и очень высокого кардиоваскулярного риска. У больных с очень высоким уровнем кардиоваскулярного риска целевым уровнем холестерина липопротеинов низкой плотности (ХС ЛПНП) является <1,8 ммоль/л, или снижение по меньшей мере на 50%, если исходный уровень ХС ЛПНП составляет 1,8-3,5 ммоль/л. У больных с высоким уровнем кардиоваскулярного риска целевым уровнем ХС ЛПНП является <2,6 ммоль/л, или снижение по меньшей мере на 50%, если исходный уровень ХС ЛПНП составляет 2,6-5,1 ммоль/л. Согласно рекомендациям KDIGO (Kidney Disease: Improving Global Outcomes, 2012), взрослым пациентам старше 50 лет с СКФ <60 мл/мин/1,73 м2, не находящимся на программном диализе и не имеющим функционирующего почечного трансплантата, рекомендована статинотерапия или применение комбинации статина с эзетимибом (ІА). Значительную проблему в области здравоохранения составляет меньшее назначение статинов и ИАПФ женщинам по сравнению с мужчинами. В большинстве случаев исследования проводятся с участием мужчин, и их результаты экстраполируются на общую популяцию, в т. ч. женский контингент. Дополнительным преимуществом статинотерапии у женщин является то, что эти медикаменты способны предотвращать метастазирование рака молочной железы.
Таким образом, нефрологическая конференция, посвященная Международному дню почки, охватила важнейшие вопросы не только нефрологии, но и смежных областей медицины, в первую очередь кардиологии, поскольку почка является органом-мишенью АГ и участником кардиоренального синдрома. Полноценное лечение ХБП и АГ позволяет контролировать течение как сердечно-сосудистых, так и почечных заболеваний, а также уменьшать смертность полиморбидных пациентов.
Подготовила Лариса Стрильчук
3-12-КРД-РЕЦ-0318
Информация для специалистов сферы здравоохранения.
Медична газета «Здоров’я України 21 сторіччя» № 6 (427), березень 2018 р.