20 квітня, 2018
Альтернативные методы коррекции климактерических расстройств
Клиническая лекция
 Медицинские и социальные аспекты периода пери- и постменопаузы в последнее время привлекают внимание широкого круга специалистов. Часть женщин с климактерическими/менопаузальными расстройствами, такими как приливы, ищут альтернативу общепринятой менопаузальной/заместительной гормональной терапии, имея на то различные причины. В настоящее время на фармацевтическом рынке представлено много разных препаратов, являющихся альтернативой менопаузальной гормональной терапии (МГТ), однако особое внимание уделяется натуральным препаратам, содержащим фитоэстрогены [4, 5, 15-18, 21, 26, 27, 31].
Медицинские и социальные аспекты периода пери- и постменопаузы в последнее время привлекают внимание широкого круга специалистов. Часть женщин с климактерическими/менопаузальными расстройствами, такими как приливы, ищут альтернативу общепринятой менопаузальной/заместительной гормональной терапии, имея на то различные причины. В настоящее время на фармацевтическом рынке представлено много разных препаратов, являющихся альтернативой менопаузальной гормональной терапии (МГТ), однако особое внимание уделяется натуральным препаратам, содержащим фитоэстрогены [4, 5, 15-18, 21, 26, 27, 31].
Возрастные аспекты в жизни женщины связаны с естественными физиологическими процессами, которые часто сопровождаются резким ухудшением состояния здоровья. Климактерический период – естественный переходный этап в жизни женщины, на протяжении которого в репродуктивной системе происходят закономерные инволюционные процессы, обусловленные постепенным снижением, а в дальнейшем и прекращением функции яичников.
Даже при постепенном, «мягком» физиологическом течении климактерического периода у 40-70% женщин организм не успевает адаптироваться к этим изменениям, вследствие чего развиваются патологические симптомы, обусловленные дефицитом эстрогенов [2, 29, 32, 34, 54].
Общебиологическая роль эндогенных эстрогенов не ограничивается контролем формирования и регуляцией репродуктивной системы женского организма, а также антиандрогенной активностью, их влияние распространяется на все системы организма [2, 44, 54]. На протяжении всей жизни женщины эстрогены постоянно оказывают влияние на различные органы, ткани и системы путем взаимодействия со специфическими эстрогеновыми рецепторами, которые локализуются, кроме матки и молочных желез, в урогенитальном тракте (уретре, мочевом пузыре, клетках влагалища и мышцах тазового дна), клетках мозга, сердца и артерий, костей, кожи, в слизистых оболочках рта, гортани, конъюнктивы и пр.
Эстрогены участвуют в образовании и поддержании прочности костной ткани, снижают ее резорбцию, нормализуют баланс между остеобластами и остеокластами, имеющими рецепторы к эстрогенам. Именно поэтому расстройства продукции этих гормонов в организме в молодом возрасте сопровождаются нарушением формирования костной массы, а в периоде менопаузы или при хирургическом удалении яичников – усилением резорбции костной ткани, развитием остеопении, остеопороза и патологическими переломами [2, 10, 12, 29, 32, 34, 54].
Для представительниц европеоидной расы само понятие «менопауза» подразумевает 12-месячный период аменореи, фиксируемый от даты последней менструации; среднестатистический возраст ее наступления – 51 год, хотя отмечается некоторая этническая и региональная вариабельность [2].
Практикующие акушеры-гинекологи в нашей стране хорошо ознакомлены с периодами климактерия, и все же точное определение стадии репродуктивного возраста/репродуктивного старения [34] очень важно с клинической точки зрения. Впервые критерии определения репродуктивного возраста были сформулированы рабочей группой и опубликованы в 2001 г.
Они носили название STRAW (Stages of Reproductive Aging Workshop). Накопленный за 10 лет объем знаний привел к пересмотру некоторых критериев по стадиям старения репродуктивной системы. Группа экспертов в 2011 г. разработала новые критерии репродуктивного старения – STRAW+10 [34].
Авторы STRAW+10 полагают, что хотя курение и индекс массы тела влияют на активность гормонов и сроки перехода в другой репродуктивный возраст, эти факторы не изменяют характер менструаций или гормональные уровни, что свидетельствует о репродуктивном старении.
Таким образом, система STRAW+10 применима у женщин независимо от возраста, индекса массы тела, демографических характеристик или образа жизни, т.е. STRAW+10 можно использовать почти для всех групп пациенток. Согласно новым критериям STRAW, для более полной оценки климактерических изменений следует проводить количественный анализ маркеров овариального резерва.
Критерии STRAW+10 были включены в рекомендации Международного общества по менопаузе (IMS) в 2016 г.
Критерии STRAW+10 включают:
- количество антральных фолликулов;
- уровень фолликулостимулирующего гормона (ФСГ);
- концентрацию антимюллерова гормона и ингибина В.
Необходимо отметить, что уровень антимюллерова гормона снижается значительно раньше, чем уровень ингибина В, что характеризует этот показатель как важный дополнительный маркер наступления менопаузы. Эти два показателя помогают определить стадию климактерия при совокупном анализе выраженности вазомоторных симптомов и урогенитальной атрофии, в то время как другие менопаузальные симптомы для определения стадии репродуктивного старения не используются [34].
При терапии климактерического синдрома чрезвычайно важно достичь двух основных целей: эффективно купировать ранние и средневременные менопаузальные симптомы (психоэмоциональные, вазомоторные и урогенитальные) и одновременно предотвратить метаболические нарушения, которые могут привести к развитию таких поздних осложнений, как остеопороз, прогрессирование атеросклероза и кардиоваскулярные заболевания [2, 10, 12, 32, 50, 54].
В 2016 г. на Всемирном конгрессе по менопаузе утверждены пересмотренные показания и противопоказания к назначению МГТ [2, 34]. Безусловно, основная роль в коррекции менопаузальных расстройств и профилактике обменных нарушений по праву принадлежит системной гормональной терапии. IMS в 2016 г. предложило обновленные рекомендации по гормональной и альтернативной терапии с учетом данных новейших исследований [2, 10, 12, 54].
Основные положения МГТ (IMS, 2016) представлены ниже [2].
- Назначение МГТ следует рассматривать в случае наличия: климактерического синдрома (вазомоторные и психоэмоциональные симтомы) и урогенитальной атрофии – генитоуринарного синдрома [12]; менопаузального метаболического синдрома. Следует также учитывать и другие жалобы, связанные с менопаузой: боль в суставах и мышцах, резкую смену настроения, нарушения сна и сексуальную дисфункцию (включая снижение либидо).
- Проведение индивидуально подобранной МГТ (в том числе препаратов андрогенов при необходимости) может улучшить как сексуальные отношения между женщиной и ее партнером, так и общее качество ее жизни.
- МГТ должна быть составляющей общей стратегии, включающей рекомендации относительно образа жизни, диеты, физических упражнений, отказа от курения и безопасного потребления алкоголя, для поддержания здоровья женщины в пери- и постменопаузе.
- МГТ должна быть индивидуальной и адаптированной в зависимости от симптомов и необходимости профилактики, а также от персонального и семейного анамнеза, результатов соответствующих исследований, предпочтений и ожиданий женщины.
В настоящее время МГТ считается методом выбора при лечении женщин в климактерии и заболеваний, ассоциированных с дефицитом эстрогенов. Ее компонентами являются синтезированные эстрогены/их аналоги (выделенные из организма животных) в качестве монопрепаратов или в различных комбинациях с прогестинами.
При этом чрезвычайно важны следующие принципы: своевременность назначения препаратов МГТ, индивидуальный подбор гормональных препаратов в минимальных дозах и дальнейшая их коррекция в зависимости от возраста и состояния здоровья женщины.
В первую очередь необходимо уделить внимание абсолютным противопоказаниям к назначению МГТ: рак молочной железы (РМЖ) и эндометрия; кровянистые выделения из половых путей неясной этиологии; венозная тромбоэмболия в анамнезе или в настоящее время (тромбоз глубоких вен, легочная эмболия); артериальная тромбоэмболическая болезнь в настоящее время (стенокардия, инфаркт миокарда); заболевания печени в острой стадии или в стадии обострения; аллергия на активные вещества или любой из наполнителей препарата; кожная порфирия (ферментопатия) [2, 54].
Относительными противопоказаниями к назначению МГТ являются: миома матки, эндометриоз, мигрень, венозный тромбоз и тромбоэмболия в анамнезе, семейная гипертриглицеридемия, желчнокаменная болезнь, эпилепсия, рак яичника в анамнезе [2, 54]. Таким образом, существует ряд противопоказаний и ограничений в отношении назначения и продолжительности МГТ.
Кроме того, многие женщины отказываются от приема гормональных препаратов и ищут альтернативные способы уменьшения выраженности приливов, что определяет необходимость оценки негормональных лекарственных средств и профилактики менопаузальных расстройств [2, 6, 13, 17, 23, 30, 35, 38, 40, 45-47, 51, 54-56].
Это обусловлено тем, что у некоторых женщин при длительном использовании эти препараты вызывают побочные эффекты (болезненность молочных желез, тошнота, головная боль, отеки, маточные кровотечения и др.), повышают риск развития заболеваний сердечно-сосудистой системы (инфаркта миокарда и тромбозов) и РМЖ [2, 23, 30, 40, 42, 43, 51, 54, 56].
Неожиданные результаты исследования, проведенного Инициативой по охране здоровья женщин (WHI), способствовали усиленному поиску новых гормональных препаратов, которые могли бы эффективно, селективно и физиологично влиять на ключевые органы-мишени [1, 3, 7-9, 11, 15, 16, 20].
Необходимость разработки альтернативных методов лечения и профилактики климактерических расстройств вызвана не только существованием противопоказаний к применению МГТ или нечувствительностью к ней, но и нежеланием пациенток принимать синтетические гормональные препараты или наличием опасений по поводу них.
Согласно рекомендациям IMS (2016, [2]), при лечении менопаузальных вазомоторных симптомов следует рассматривать использование препаратов фитоэстрогенов – препаратов растительного происхождения, отвечающих требованиям натуропатии и обладающих эстрогенной активностью. Эти лекарственные средства, изготовленные из природных компонентов, не вызывают побочных, аллергических и токсических эффектов, а также синдрома отмены и привыкания.
Хотя идеального лечения климактерического синдрома не существует, клинический профиль фитоэстрогенов к этому приближается. Среди различных классов фитогормонов наибольшей эстрогенной активностью обладают изофлавоны [4, 6, 15-17, 30, 31, 35, 40, 41, 43, 47, 56].
Хотя они и не такие мощные, как синтетические эстрогенсодержащие препараты, их селективное связывание с b-рецепторами эстрогенов (РЭ-b) оказывает позитивное воздействие на кости, влагалище, мозг и сердечно-сосудистую систему, но не вызывает побочных эффектов – пролиферативной активности в миометрии и эндометрии, молочной железе, повышения тромбогенного потенциала крови [3, 7, 14, 19, 24, 28, 33, 53]. Они являются хорошим альтернативным вариантом лечения, особенно для женщин с высоким уровнем риска, которые отказываются от МГТ.
Доводы в пользу альтернативного подхода в ведении женщин, находящихся в периоде пери- и постменопаузы, базируются на известных данных о меньшей частоте приливов у женщин, проживающих в регионах, где традиционная пища богата фитоэстрогенами, а потребление изофлавонов достигает 200 мг в день [6, 15, 17, 18, 21, 25, 27, 29, 31, 39, 49].
Например, частота приливов у женщин стран Европы составляет 70-80%, в Малайзии не превышает 57%, в Китае – только 18%, в Японии – 15%, в Сингапуре – 14%. Эпидемиологические исследования также подтвердили, что в Китае, Японии, на Филиппинах у женщин реже встречаются заболевания, возникающие из-за дефицита эстрогенов, в частности сердечно-сосудистые заболевания и остеопороз.
У них также реже наблюдается РМЖ: если среди 100 тыс. женщин европеоидной расы Сан-Франциско ежегодно регистрируется 104,2 случая РМЖ, то в Японии – лишь 17,6, в Китае – 9,5.
Фитопрепараты изготавливают исключительно из растительного сырья – целого растения или его экстракта. В настоящее время для их производства используется около 500 растений. Преимущества растительных экстрактов из сои и красного клевера в качестве альтернативы традиционной МГТ широко обсуждаются [4, 6, 8, 22, 36, 41].
Хотя изучение альтернативных видов лечения симптомов менопаузы сфокусировано, в основном, на изофлавонах сои, значительно возросло количество исследований других растительных продуктов (экстракты красного клевера, Cimicifuga racemosa, дягиля лекарственного, лопуха, хмеля, семян льна и др. [16, 31, 36]).
Следует подробнее проанализировать известные данные о различных фитоэстрогенах. К трем основным категориям фитоэстрогенов относятся изофлавоны, лигнаны и куместаны. Они содержатся в высоких концентрациях в красном клевере (Trifolium pratense), бобах сои и могут абсорбироваться из пищи в желудочно-кишечном тракте.
Куместаны, содержащиеся в красном клевере в небольшом количестве, практически не обладают эстрогенным действием [9, 35, 39, 45, 47]. Основным пищевым источником фитоэстрогенов является соя, но она содержит небольшое количество эстрогеноактивных субстанций по сравнению с красным клевером.
После приема пищи лигнаны и изофлавоны подвергаются комплексной ферментативной обработке в желудке с последующим образованием комплексов со стероидными эстрогенподобными структурами. Активные формы образуются посредством деконьюгации с помощью бактерий кишечника.
Вариабельность метаболизма фитоэстрогенов, на которую влияют качественный состав миклофлоры кишечника и время прохождения пищи, играет клиническую роль, так как может повлиять на биологический ответ [9, 40].
Интерес к изофлавонам красного клевера, относящимся к фитоэстрогенам, возрос как у исследователей, так и у пациенток в связи с сообщениями о положительных эффектах фитоэстрогенов.
Именно экстракт красного клевера содержит сразу 4 изофлавона: биоканин А, формононетин, деидзеин, генистеин и дополнительно глицитеин, в то время как в сое содержится только две из этих субстанций – генистеин и деидзеин [4-6, 40-42, 45-47].
Генистеин является наиболее активным изофлавоном, содержащимся в красном клевере [8, 20, 21, 38]. Он тормозит тирозин и протеинкиназу, что крайне важно, поскольку эти ферменты вовлечены в процессы контроля митогенеза, регуляции клеточного цикла, выживаемости клеток и их трансформации.
Тирозинкиназы влияют на опухолевый рост, контролируя факторы роста – эпидермальный, тромбоцитарный и инсулиноподобные факторы роста (I и II типа), а также фактор некроза опухоли, чем и объясняются присущие изофлавонам антипролиферативный, противовоспалительный и антиоксидантный эффекты.
Основное действующее вещество лигнанов – энтеролактон, который замедляет превращение андростендиона в эстрон, снижая риск развития эстрогензависимого рака. Лигнаны также оказывают антиканцерогенный, противовирусный и бактерицидный эффекты [1, 19, 22, 24].
Применение фитоэстрогенов, включая изофлавоны красного клевера, обеспечивает различные положительные эффекты в организме человека и оказывает положительное влияние на различные ткани и типы клеток.
На основании результатов анализа данных многочисленных литературных источников [6, 8, 13, 14, 17, 19, 23, 24, 30, 35, 38, 40, 45, 46, 48, 54-56] и сравнения их с основными рекомендациями применения МГТ (IMS, 2016) можно выделить факторы, посредством которых проявляется аналогичное МГТ действие фитоэстрогенов на молекулярном уровне.
1. Фитоэстрогены/изофлавоны имеют структуру, сходную с таковой эстрадиола, и могут соединяться с рецепторами эстрогенов (РЭ) (п. 1, 2 рекомендаций IMS).
Фитоэстрогены реализуют свою биологическую активность, связываясь с РЭ, при этом они демонстрируют наибольшее сродство к связыванию с РЭ-b и являются слабыми агонистами РЭ-a [3, 19, 24].
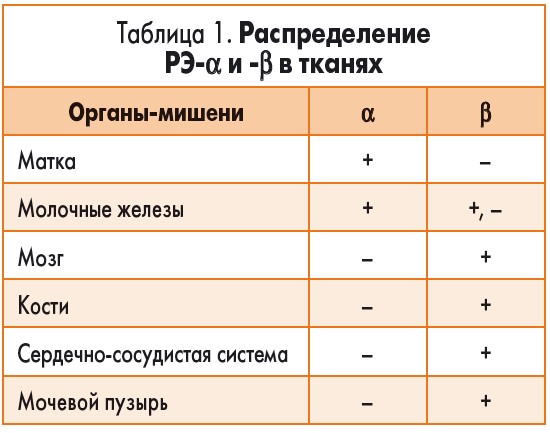
Этот положительный эстрогенный эффект достигается главным образом в тканях, где преимущественно расположены РЭ-b, – костях, сердечно-сосудистой системе, влагалище и мозге, и не характерен для матки и молочных желез (табл. 1).
Избирательный механизм действия присущ фармпрепаратам, которые получили название «селективные модуляторы рецепторов эстрогена» [28, 53]. И хотя механизм молекулярного действия фитоэстрогенов отличается от такового селективных модуляторов, результат их действия явно положительный: избирательная связь с РЭ-b в определенных типах тканей, что не противодействует связи с РЭ обоих типов (-a и -b) и эстрогенному эффекту в других тканях.
Модулируя РЭ, фитоэстрогены конкурируют за рецепторы с эстрадиолом вплоть до полной их блокировки, оказывая в 1000 раз менее выраженный по сравнению с эстрадиолом пролиферативный эффект.
Из четырех протестированных изофлавонов красного клевера генистеин является веществом с самой высокой эстрогенной активностью по отношению к обоим типам РЭ. Эффективность всех четырех субстанций в отношении РЭ-b выше, чем в отношении РЭ-a. Это может быть причиной тканеспецифических эффектов экстрактов красного клевера при лечении симптомов менопаузы [3, 8, 14, 19, 24, 28].
2. Фитоэстрогены снижают активность ароматазы, способствуют повышению уровня глобулина, связывающего половые гормоны, и регулируют метаболизм эстрогенов (п. 7 рекомендаций IMS).
Среди населения Азии заболеваемость раком молочной железы, эндометрия и предстательной железы так же, как и частота сердечно-сосудистых заболеваний, ниже по сравнению с этими показателями в странах Европы и США. Средний объем потребления изофлавонов японками составляет от 20 до 80 мг в день, в то время как американки потребляют от 1 до 3 мг изофлавонов [25].
Фитоэстрогены, включая изофлавоны красного клевера, также оказывают влияние на различные энзимы, регулирующие метаболизм стероидных гормонов. Ароматаза – фермент, который конвертирует андростендиол в эстрон и тестостерон в эстрадиол, ингибируется фитоэстрогенами.
Ингибирование фитоэстрогенами ароматазы может обеспечивать защитный эффект от развития РМЖ в популяциях, употребляющих пищу с высоким содержанием изофлавонов [1, 22, 25, 28].
Другими ключевыми энзимами метаболизма эстрогенов и андрогенов являются различные типы 17b-гидроксистероиддегидрогеназ (17b-HSD). Эти энзимы отвечают за конверсию эстрона в эстрадиол и андростендион в тестостерон. Самый высокий ингибирующий потенциал в отношении 17b-HSD имеют биоканины А – вещества из группы изофлавонов красного клевера [4, 22, 25, 43, 48].
Они способны подавлять пролиферацию клеток РМЖ также за счет воздействия на процессы метаболизма витамина D3 и их сродства с РЭ-b. Их эффективность подтверждается снижением маммографической плотности, которая является одним из диагностических критериев развития пролиферативных процессов в молочной железе и риска формирования РМЖ [1, 22].
3. Классические геномные эффекты фитоэстрогенов – антиоксидантный, противовоспалительный, противосклеротический (п. 2 и 7 рекомендаций IMS).
К классическим геномным эффектам фитоэстрогенов относится также влияние на клеточный цикл и антиоксидантную активность. Считается, что в основе развития атеросклероза, сердечно-сосудистых заболеваний лежит воспалительный процесс. Важную роль в его возникновении играет нуклеарный фактор (NF)-kВ, который влияет на выработку цитокинов и других протеинов острой фазы воспаления.
Известно, что изофлавоны оказывают противовоспалительное, противосклеротическое и противоаллергическое действие, которое реализуется за счет ингибирования NF-kВ. В частности, в исследованиях Мураока и соавт. было доказано такое ингибируещее действие изофлавона генистеина. Изофлавоны оказывают положительный эффект на состояние сосудистой стенки артерий и уровень холестерина крови, тем самым в какой-то степени замедляя прогрессирование атеросклероза [7, 33, 44, 49].
4. Изофлавоны активно участвуют в обменных процессах костной ткани (п. 3 рекомендаций IMS).
В частности, деидзеин, содержащийся в экстракте красного клевера, может ингибировать дифференциацию и активность остеокластов в той же степени, что и 17b-эстрадиол.
В ряде исследований показано, что изофлавоны способны стимулировать развитие остеобластов (клеток, отвечающих за рост костной ткани), т.е. обладают свойством, которое не характерно для эстрогенов. Это позволяет предотвратить процесс резорбции костной ткани и развитие остеопороза [7, 21].
5. Изофлавоны оказывают андрогеноподобный эффект (п. 2, 4, 5, 7 рекомендаций IMS).
Было продемонстрировано, что изофлавоны биоканин А и генистеин подавляют экспрессию генов, регулируемую андрогенами, что проявляется в виде снижения уровня дигидротестостерона – выработки простатспецифического антигена (биологического маркера рака предстательной железы) при РМЖ, но не в клеточной линии рака простаты.
Биоканин А (изофлавон красного клевера) продемонстрировал тот же эффект на андроген-регулируемую транскрипцию простатспецифического антигена [11].
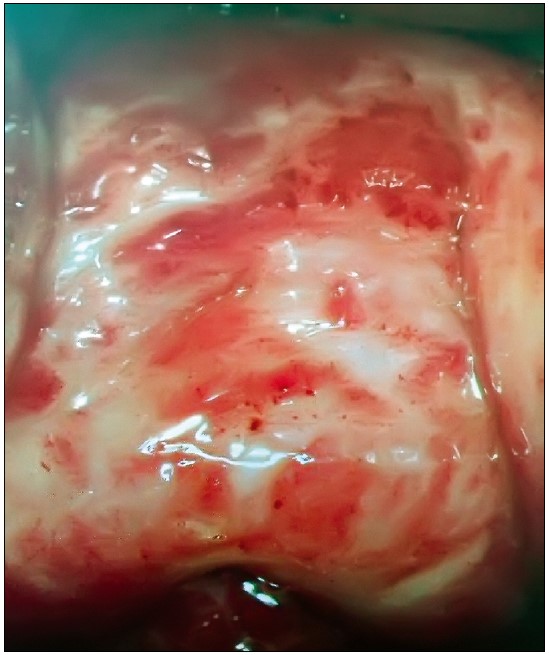
Есть необходимость акцентировать внимание на пункте рекомендаций IMS, который касается урогенитальной атрофии [12]. На фоне эстрогендефицита с нарастанием прогрессирующих атрофических изменений вагинального эпителия (рис. 1) прослеживается изменение микробиоценоза влагалища и ослабление механизмов локальной защиты.
 Рис. 1. Прекращение пролиферации эпителия у женщин в возрасте старше 50 лет
Рис. 1. Прекращение пролиферации эпителия у женщин в возрасте старше 50 лет
В зависимости от степени эстрогенного дефицита и возрастных метаболических нарушений в клетках эпителия влагалища уменьшается содержание гликогена, элиминируется основной компонент влагалищного биотопа – лактобациллы, что приводит к значительному уменьшению количества молочной кислоты, повышению рН влагалища до 6,5-8,0.
Происходит колонизация вагинального биотопа как экзогенными, так и эндогенными микроорганизмами с последующим повышением риска развития восходящей инфекции. Следует отметить, что наиболее частой патологией у женщин в постменопаузе является бактериальный вагиноз [10, 12, 14].
Наиболее частыми клиническими симптомами атрофического вагинита являются сухость, зуд, жжение во влагалище, диспареуния, контактные кровянистые выделения, рецидивирующие вагинальные инфекции, экзо- и эндоцервицит, урологические нарушения [10, 12, 50, 52, 54].
При осмотре женщин зрелого возраста с эстрогендефицитом необходимо своевременное выявление так называемой молчаливой атрофии (рис. 2): истончение эпителия, кровоточивость субэпителиальных сосудов стромы, особенно при контакте. Эти симптомы характерны для начальной стадии развития урогенитальных расстройств.
Рис. 2. Атрофический вагинит: «молчаливая атрофия»
У пациентки при этом либо не возникают неприятные ощущения со стороны мочеполовых органов (особенно в тех случаях, когда женщина не имеет сексуальных контактов в течение длительного времени), либо она не считает нужным рассказать о них врачу [50].
Основными методами диагностики атрофического вагинита являются [12]:
- расширенная кольпоскопия (определяется истончение слизистой оболочки влагалища, кровоточивость, петехиальные кровоизлияния, многочисленные просвечивающиеся капилляры – рис. 2);
- кольпоцитологическое исследование (при развитии атрофических процессов кариопикнотический индекс снижается до 15-20);
- определение рН вагинального содержимого (при развитии атрофических процессов влагалища рН может достигать 8,0, однако у сексуально активных женщин данной возрастной группы этот показатель всегда ниже);
- микробиологическое исследование;
- оценка состояния местного иммунитета.
Вызывают чрезвычайный интерес рандомизированные плацебо-контролируемые исследования, проведенные R. D’Anna и соавт., L.A. Hidalgo и P.A. Chedraui [8, 14].
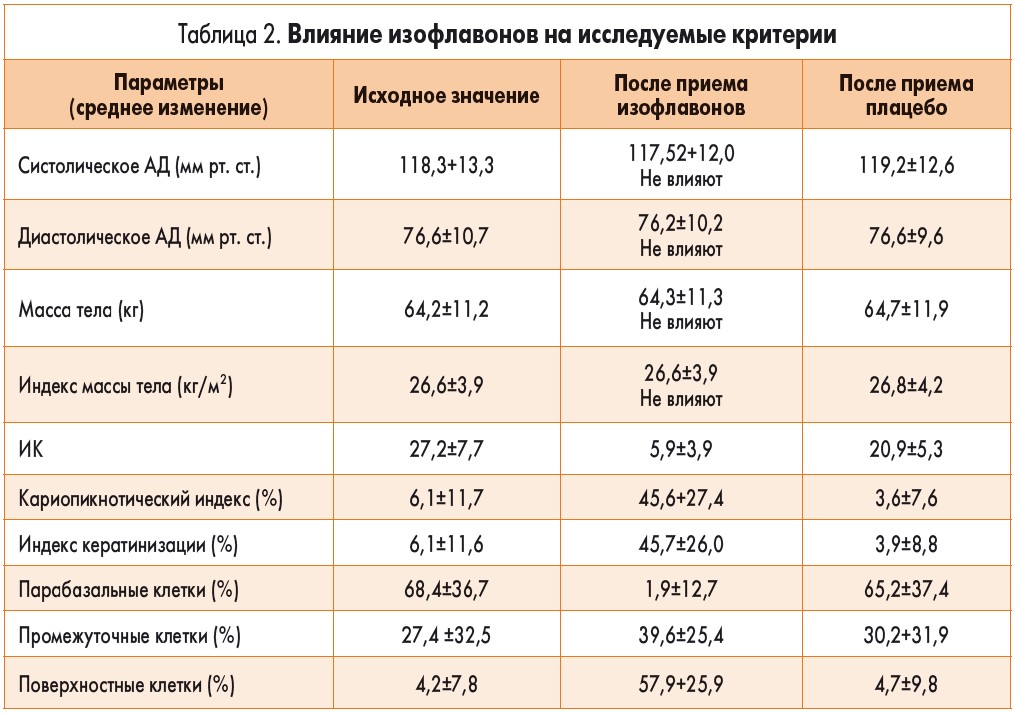
В исследование L.A. Hidalgo и соавт. были включены 60 женщин в период постменопаузы, ранее не получавших системную МГТ. Они имели высокие показатели индекса климактерических расстройств – индекс Купермана (ИК) ≥15, определенные изменения в липидограмме и цитологические показатели атрофического вагинита. Участницы принимали препарат красного клевера или плацебо в течение 90 дней.
Проводилась оценка влияния изофлавонов красного клевера на показатели артериального давления (АД), массы тела (индекс массы тела), ИК, уровень липидов крови и цитологию влагалища у женщин в период менопаузы (табл. 2).
Полученные результаты исследования препарата на основе изофлавонов красного клевера свидетельствуют, что изофлавоны красного клевера:
- эффективно устраняют симптомы менопаузы по параметрам ИК;
- положительно воздействуют на цитологические показатели влагалищного эпителия: повышение митотической активности, улучшение процессов кератинизации и созревания клеток;
- снижают уровень холестерина на 4,4%, липопротеидов низкой плотности – на 11,5% и триглицеридов – на 9,5%.
Завершая обзор литературных данных и сравнительный анализ действия изофлавонов красного клевера, можно сделать вывод: изофлавоны могут быть адекватной альтернативой общепринятой МГТ. Они эффективны в плане купирования климактерических расстройств и обеспечивают важное профилактическое действие в отношении остеопороза, сердечно-сосудистых и онкологических заболеваний.
В свете вышесказанного значительный интерес представляет препарат Клеверол® – экстракт красного клевера, который содержит 4 важнейших изофлавона: генистеин, даидзеин, биоканин А и формононетин.
В каждой капсуле Клеверол® содержится не менее 40 мг чистых изофлавонов. Вспомогательными веществами являются целлюлоза микрокристаллическая, кремния диоксид и магния стеарат, являющийся кофактором оптимизации метилирования и экскреции катехолэстрогенов и способствующий детоксикации эстрогенов через прямое повышение активности глюкуронилтрансферазы – фермента, вовлеченного в процесс глюкуронидации в печени. Клеверол® не содержит сахара, сахарозаменителей и консервантов.
Нами было проведено клиническое изучение эффективности и безопасности применения препарата Клеверол® (фармацевтическая компания «Ядран», Хорватия) в купировании перименопаузальных психоэмоциональных и вегетососудистых нарушений.
В задачи исследования входила оценка переносимости препарата, его влияния на липидный профиль (уровни триглицеридов, липопротеидов низкой и высокой плотности), основные гормональные показатели (уровни эстрадиола, ФСГ), а также на состояние эндометрия (данные ультразвукового исследования – УЗИ – органов малого таза) у женщин в перименопаузе и ранней постменопаузе.
Было отобрано 45 амбулаторных пациенток в возрасте от 45 до 53 лет с легкой и средней степенью выраженности климактерического синдрома без органической патологии органов малого таза, сердечно-сосудистой системы, ЦНС, эндокринных и онкологических заболеваний.
Мы следовали общепринятой практике включения пациенток в исследование:
- женщины в период перименопаузы, впервые отметившие проявления климактерического синдрома – вегетососудистые и психоэмоциональные нарушения;
- отсутствие МГТ и приема фитоэстрогенов в анамнезе;
- отсутствие приема лекарственных препаратов, предназначенных для снижения уровня липидов.
Пациентки получали препарат Клеверол® в дозе 2 капсулы в день во время еды в течение 6 мес. Все исследования проводились пациентки перед началом и через 6 мес лечения. Во время исследования пациентки заполняли опросные листы, в которых фиксировали динамику симптомов и нежелательные явления, оценивали результаты применения препарата.
Переносимость препарата Клеверол® оценивалась с использованием шкалы побочных симптомов, которая фиксировала дату и описание нежелательного явления, продолжительность, связь с приемом исследуемого препарата, степень выраженности (легкая, средняя, тяжелая). Сразу следует отметить, что в течение всего времени наблюдения и приема препарата Клеверол® побочные эффекты отсутствовали.
Не отмечены также дискомфорт/болезненность в молочных железах. Переносимость монотерапии препаратом оценена как отличная 65% пациенток, хорошая – 33%, удовлетворительная – 2%.
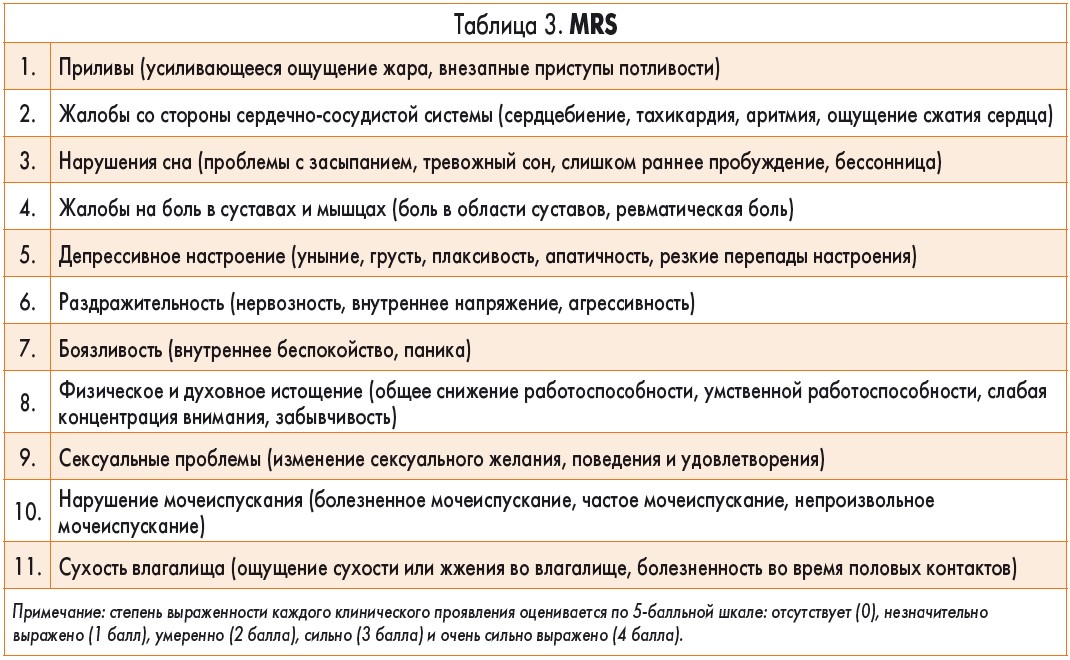
Тяжесть климактерического синдрома оценивалась по опроснику менопаузальной рейтинговой шкалы (MRS, [23]; табл. 3).
Опросник включает в себя балльную оценку (от 0 до 4 баллов) нейровегетативных, метаболических, психоэмоциональных и урогенитальных проявлений климактерического синдрома.
Пациенткам проводились УЗИ органов малого таза, консультация эндокринолога по показаниям. Оценка состояния пациенток и исследуемых показателей проводилась до лечения и через 6 мес приема препарата Клеверол®.
Практически все пациентки отметили улучшение памяти и настроения, повышение работоспособности, нормализацию сна. На фоне приема препарата Клеверол® планомерно уменьшалась выраженность всех проявлений климактерического синдрома уже с 3-го месяца (табл. 4), но в большей степени препарат влиял на нейровегетативные (приливы, потливость, сердцебиение) и психоэмоциональные (снижение повышенной возбудимости, уменьшение проявлений лабильности эмоционального статуса и депрессивных расстройств).
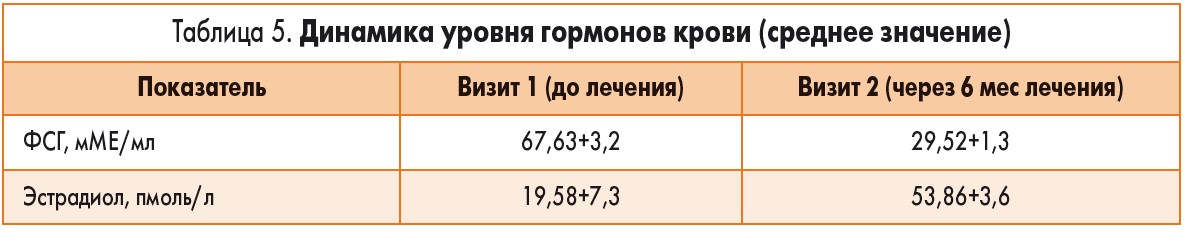
На основании полученных данных гормонального профиля можно сделать вывод о том, что в результате проведенной 6-месячной терапии препаратом Клеверол® появилась выраженная тенденция к снижению уровня ФСГ и повышению уровня эстрадиола (табл. 5).
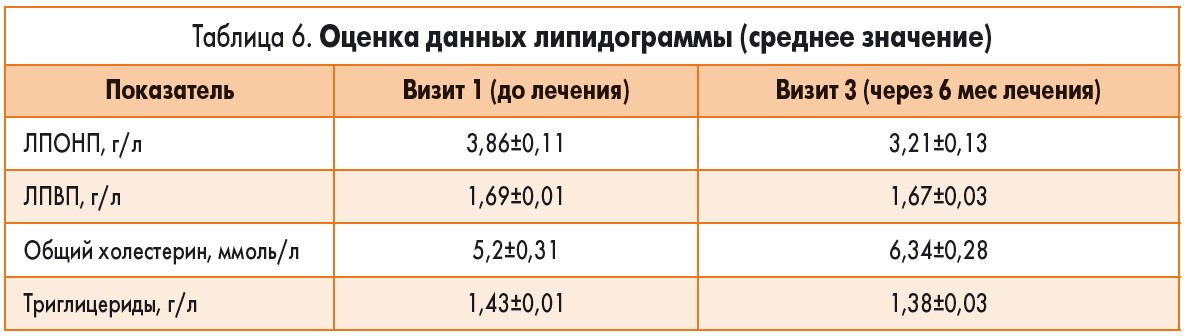
При оценке липидограммы (табл. 6) обращает на себя внимание то, что уровень триглицеридов у всех пациенток до исследования был в пределах нормы. На фоне приема препарата Клеверол® при сравнении данных показателей с исходными не отмечено клинически значимых изменений уровней липопротеидов высокой плотности (ЛПВП), липопротеидов очень низкой плотности (ЛПОНП) и общего холестерина.
В исследование были включены пациентки без органической патологии органов малого таза, т.е. при УЗИ отсутствовала какая-либо гинекологическая патология. За период приема препарата не зарегистрированы какие-либо изменения размеров и структуры матки и яичников, изменения толщины и структуры эндометрия.
Требует отдельного рассмотрения влияние препарата Клеверол® на проявления урогенитальной атрофии (п. 1 рекомендаций IMS), а также необходимость и возможность коррекции вагинального микробиоценоза. Из 45 пациенток, включенных в исследование и принимавших Клеверол®, 18 имели субъективные симптомы, характерные для атрофического вагинита.
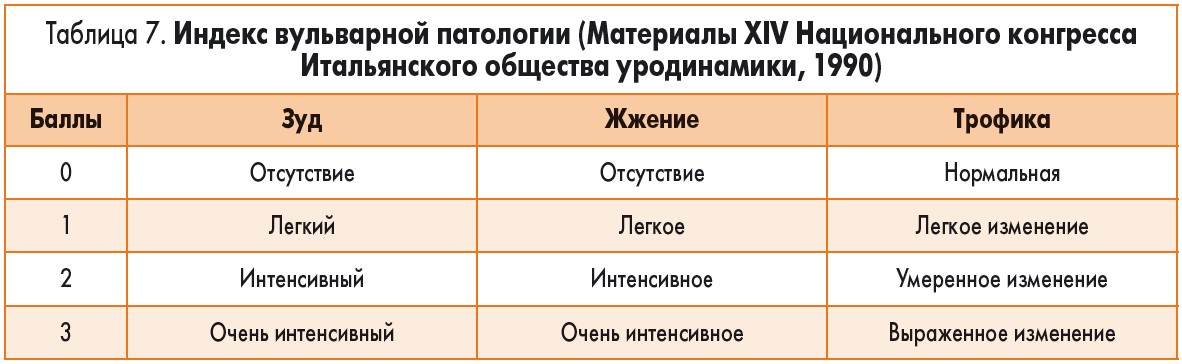
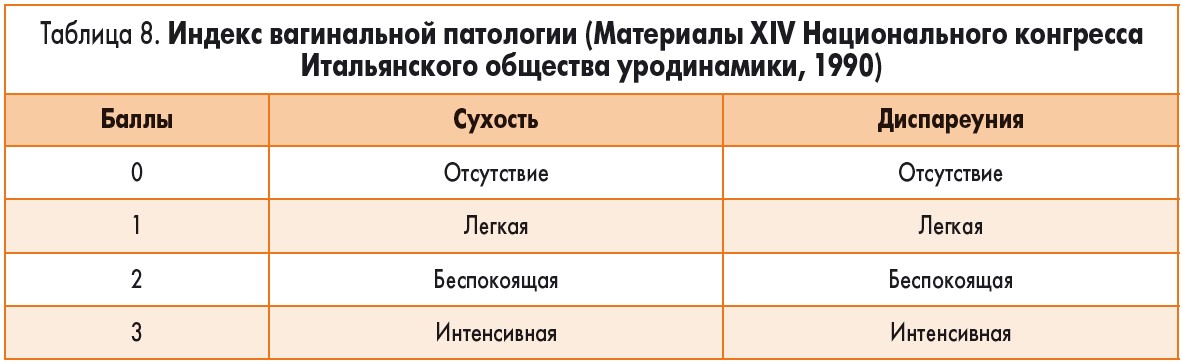
Кроме бактериологического и цитологического исследования мазков, мы выявляли субъективные жалобы пациенток – зуд, жжение, сухость и диспареунию. Эти показатели являются основой для оценки индекса вульварной и вагинальной патологии (табл. 7 и 8). Единственный показатель – состояние трофики – оценивается акушером-гинекологом во время осмотра и забора материала для исследования.
Данная группа пациенток в определенной последовательности принимала препарат Клеверол® и препараты линейки Вагисан®.
Препараты линейки Вагисан® широко применяются для восстановления лактофлоры влагалища в двух формах – пероральной (содержит высокоспецифичные штаммы L. rhamnosus GR‑1™ и L. reuteri RC‑14™ в дозе 109 КОЕ) и вагинальной. Вагинальная форма препарата Вагисан® содержит двойную дозировку L. rhamnosus GR‑1™ и L. reuteri RC‑14™ – 2 × 109 КОЕ, фруктоолигосахариды (способствуют усиленному росту и размножению лактобактерий) и молочную кислоту, которая быстро снижает уровень рН, угнетает жизнедеятельность патогенных микроорганизмов и создает оптимальные условия для развития лактофлоры.
Применение вагинальной формы препарата Вагисан® позволяло достичь быстрого и выраженного эффекта при дисбиозе влагалища, который практически всегда сопровождает вагинальную атрофию.
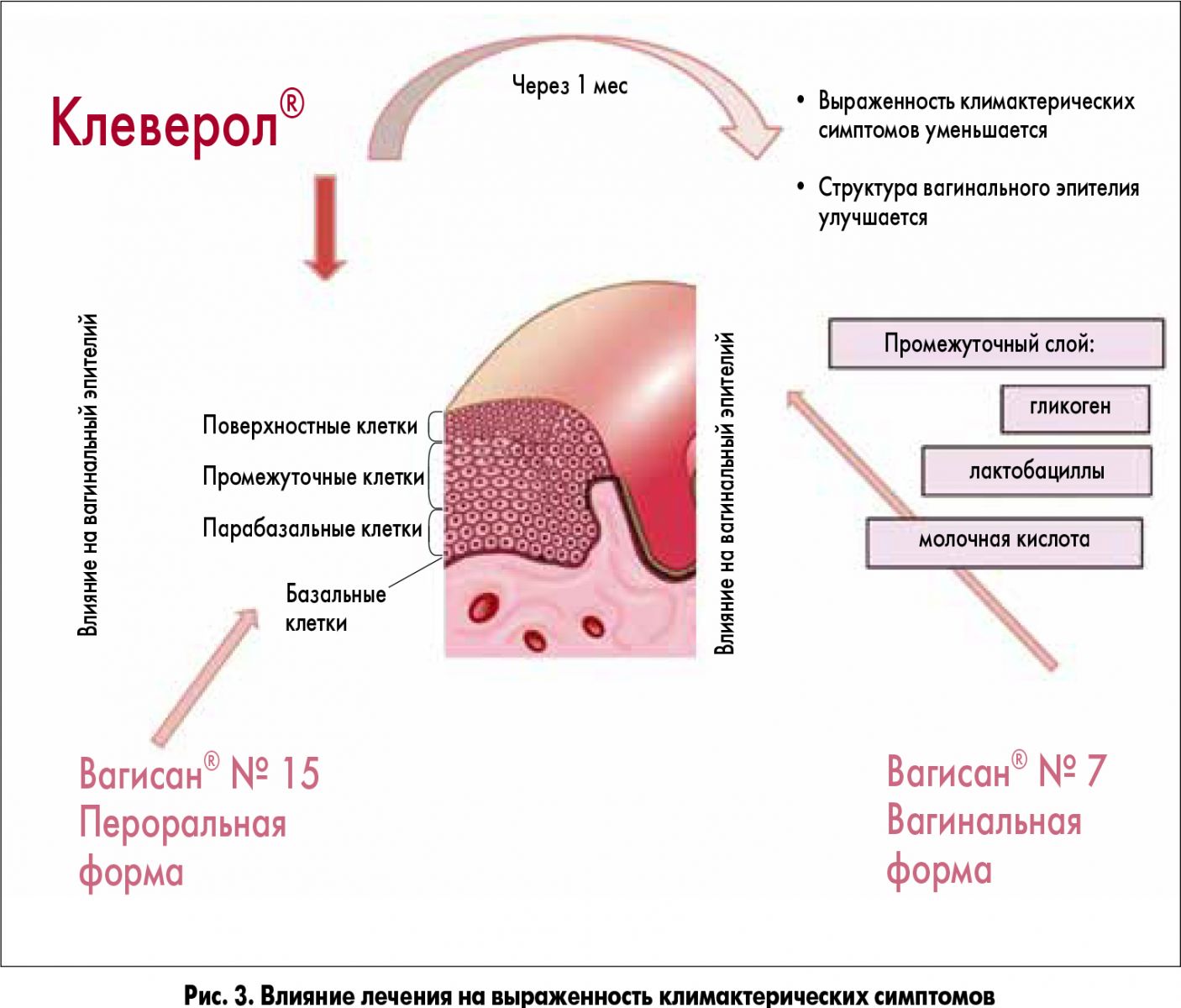
Схематически механизмы воздействия препарата Клеверол® на вагинальный эпителий и восстановления микробиоценоза влагалища путем применения пероральной и вагинальной форм препарата Вагисан® представлены на рисунке 3.
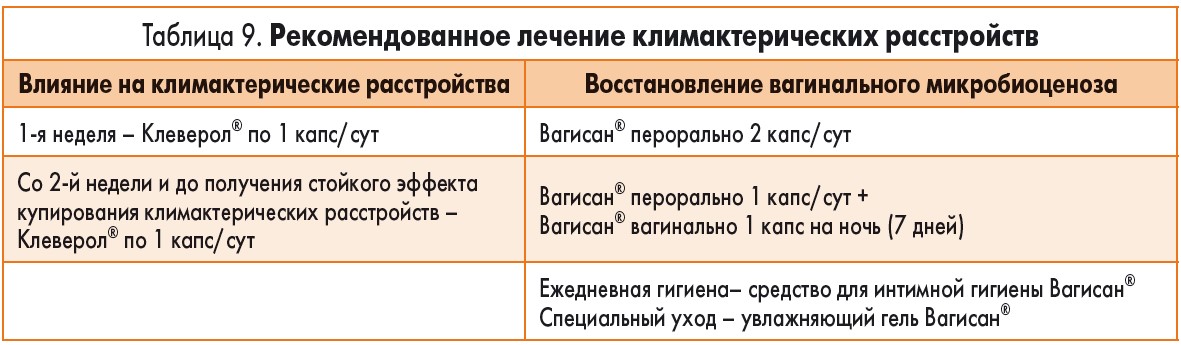
Мы применяли сочетанное лечение препаратами Клеверол® и линейки Вагисан® (табл. 9) как с целью купирования климактерических расстройств (вегетососудистых и психоэмоциональных), так и симптомов урогенитальной атрофии (атрофического вагинита, вагиноза, дисбиоза).
Результаты кольпоцитологического исследования через 3 недели лечения показали наличие положительного ваготропного эффекта изофлавонов красного клевера (Клеверол®) – пролиферацию многослойного плоского эпителия; отмечено также восстановление микробиоценоза влагалища.
Контроль состояния эндометрия с помощью УЗИ подтвердил отсутствие утеротропного эффекта на фоне применения препарата Клеверол®, что полностью соответствует данным, изложенным в публикациях: эстрогенное влияние изофлавонов красного клевера недостаточное для стимуляции пролиферации эндометрия [3, 8, 14].
Пациентки отметили положительные изменения сексуального желания и поведения, что, очевидно, было связано с уменьшением выраженности всех проявлений климактерического синдрома, но не отметили изменений либидо.
Выводы. Многие женщины с климактерическими расстройствами заинтересованы в использовании альтернативных МГТ методов их коррекции.
В нашем исследовании применение препарата на основе экстракта красного клевера (Клеверол®) на протяжении 6 мес оказало положительное влияние на купирование климактерического синдрома, изменения гормонального профиля, не оказывая негативного воздействия на состояние эндометрия.
Препарат Клеверол® является эффективным альтернативным МГТ методом лечения климактерического синдрома, особенно легкой и средней тяжести, что позволяет значительно улучшить качество жизни женщин зрелого возраста.Изофлавоны, входящие в состав препарата Клеверол®, благодаря их селективному связыванию с РЭ-b оказывают позитивное воздействие на кости, влагалище, мозг и сердечно-сосудистую систему и не влияют на матку и молочные железы.
Применение препарата Клеверол® также является альтернативным вариантом лечения для женщин с высоким уровнем риска, которые отказываются от МГТ.
Восстановление эстрогензависимой структуры вагинального эпителия при приеме фитоэстрогенов (препарат Клеверол®) можно дополнить назначением специфических урогенитальных лактобактерий, которые представлены пероральной и вагинальной формами препарата Вагисан®.
Многочисленные исследования доказали положительное воздействие изофлавонов красного клевера (препарат Клеверол®) на вазомоторные, психоэмоциональные проявления менопаузы, на симптомы урогенитальной атрофии, сексуальную функцию, что в итоге значительно улучшает качество жизни женщин зрелого возраста.
Список литературы находится в редакции.