1 травня, 2018
Почки и женское здоровье
По материалам научно-практической конференции с международным участием «Актуальные вопросы репродуктивной медицины в Украине», 22-23 марта, г. Днепр
В этом году по стечению обстоятельств Всемирный день почки, который традиционно отмечается во второй четверг марта, пришелся на 8-е число – Международный женский день, поэтому был выбран соответствующий девиз – «Почки и женское здоровье». Это событие не могло остаться без внимания украинских акушеров-гинекологов: в рамках конференции, посвященной репродуктивному здоровью, состоялся тематический симпозиум, который объединил нефрологов, урологов и акушеров-гинекологов для обсуждения междисциплинарных проблем заболеваний мочеполовой системы у женщин.
 Мероприятие открыл директор ГУ «Институт нефрологии НАМН Украины» (г. Киев), член-корреспондент НАМН Украины, доктор медицинских наук, профессор Николай Алексеевич Колесник, в начале доклада напомнив присутствующим основные маркеры повреждения органов мочевой системы.
Мероприятие открыл директор ГУ «Институт нефрологии НАМН Украины» (г. Киев), член-корреспондент НАМН Украины, доктор медицинских наук, профессор Николай Алексеевич Колесник, в начале доклада напомнив присутствующим основные маркеры повреждения органов мочевой системы.
– Согласно KDIGO 2012 на патологические изменения указывают:
- протеинурия/альбуминурия;
- изменение осадка мочи (эритроцитурия / эритроцитарные цилиндры, лейкоцитурия / лейкоцитарные цилиндры);
- лабораторные проявления тубулярных дисфункций или синдромов (патологические изменения концентрации электролитов сыворотки крови и/или мочи, нарушение кислотно-щелочного равновесия);
- структурные изменения, выявленные с помощью методов визуализации (камни, кисты, гидронефроз, увеличение или уменьшение размеров почки, асимметрия размеров почки, ретроперитонеальный фиброз и т. д.);
- повышение креатинемии или снижение скорости клубочковой фильтрации (СКФ) <60 мл/мин/1,73 м2.
Для оценки альбуминурии/протеинурии предложено выделять три степени в зависимости от суточных потерь протеина/альбумина (табл.).
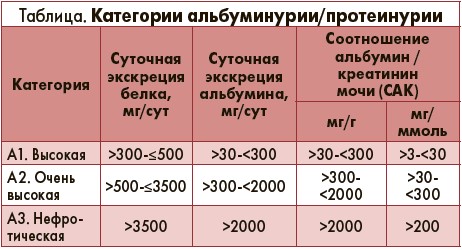 Следует подчеркнуть, что уровень креатинина сам по себе не является надежным критерием оценки почечной функции. Необходим расчет СКФ по одной из стандартизованных формул, которые эмпирически подобраны для типичных ситуаций, однако иногда их использование неприемлемо. В таких обстоятельствах клиренс креатинина следует определять по общепринятой методике на основании измерения его концентрации в крови и моче.
Следует подчеркнуть, что уровень креатинина сам по себе не является надежным критерием оценки почечной функции. Необходим расчет СКФ по одной из стандартизованных формул, которые эмпирически подобраны для типичных ситуаций, однако иногда их использование неприемлемо. В таких обстоятельствах клиренс креатинина следует определять по общепринятой методике на основании измерения его концентрации в крови и моче.
Использование клиренсовых методик показано в таких случаях, как:
- нестандартные размеры тела (пациенты после ампутации нижних конечностей, бодибилдеры);
- выраженное истощение или ожирение (индекс массы тела <15 или >40 кг/м2);
- заболевания скелетной мускулатуры (миодистрофии);
- пара- и квадриплегия;
- вегетарианская диета;
- быстрое снижение функции почек (острый и быстропрогрессирующий гломерулонефрит, острое повреждение почек);
- необходимость назначения токсичных препаратов, которые выводятся почками (например, химиотерапия), для определения безопасной дозы;
- при решении вопроса о начале почечнозаместительной терапии;
- у больных с почечным трансплантатом;
- у беременных.
Острая болезнь почек (ОБП) характеризуется наличием патологических уровней протеинурии (>300 мг/сут), альбуминурии (>30 мг/сут) либо САК (≥30 мг/сут или 3 мг/ммоль) вместе с другими маркерами патологических изменений мочевой системы или без них длительностью <12 нед.
Стадии ОБП:
0 – креатинин крови в норме или повышен (<26,5 мкмоль/л); диурез – >20 мл/ч/сут или 400 мл/сут;
I – креатинин крови повышен в 1,5-1,9 раза от предыдущего уровня или ≥26,5 мкмоль/л; диурез <0,5 мл/кг/сут в течение 6-12 ч;
II – креатинин крови повышен в 2,0-2,9 раза в сравнении с предыдущим уровнем; диурез <0,5 мл/кг/ч в течение 12-24 ч;
III – креатинин крови повышен в ≥3 раза по сравнению с исходным или ≥353,6 мкмоль/л либо начата почечнозаместительная терапия; диурез <0,3 мл/кг/ч в течение >24 ч или анурия ≥12 ч.
Для хронической болезни почек (ХБП) характерными являются патологические уровни протеинурии (>300 мг/сут), альбуминурии (>30 мг/сут) либо САК (≥30 мг/сут или 3 мг/м моль) в сочетании с другими маркерами патологических изменений мочевой системы или без них длительностью 12 нед.
Стадии ХБП:
I – поражение почек с нормальной или повышенной почечной функцией (СКФ ≥90 мл/мин/1,73 м2);
II – поражение почек с незначительным снижением СКФ (60-89 мл/мин/1,73 м2);
IIIа – почечная функция незначительно или умеренно снижена (СКФ 45-59 мл/мин/1,73 м2);
IIIб – почечная функция умеренно или значительно снижена (СКФ 30-44 мл/мин/1,73 м2);
IV – выраженно сниженная СКФ (15-29 мл/мин/1,73 м2);
V – почечная недостаточность <15 мл/мин/1,73 м2.
Выявляемость ХБП на уровне оказания первичной медицинской помощи остается низкой: приблизительно в половине случаев ХБП не диагностируется. Более чем у трети пациентов скрининговые тесты проводятся, но по их результатам не устанавливается правильный диагноз. В то время как распространенность ХБП в Европейском регионе составляет около 10%, в США – 12%, в Украине этот показатель оценивается на уровне всего 0,75%.
Скрининг на болезни мочевой системы обязателен для таких категорий населения: больные сахарным диабетом; пациенты с артериальной гипертензией (АГ); больные после острого повреждения почек даже при нормальных уровнях креатинина; пациенты с системными заболеваниями соединительной ткани; лица старше 55 лет; пациенты с патологической альбуминурией, протеинурией или показателем САК; беременные, роженицы, особенно с гипертензивными нарушениями.
Системное осуществление скрининговых мероприятий позволит уменьшить частоту острого повреждения почек, в том числе на фоне ХБП, преэклампсии/эклампсии, а также повысит объективность данных о заболеваемости и распространенности этой патологии.
 Руководитель отдела эфферентных технологий ГУ «Институт нефрологии НАМН Украины», доктор медицинских наук, профессор Ирина Алексеевна Дударь продолжила тему ХБП с акцентом на влиянии этого заболевания на течение и исходы беременности.
Руководитель отдела эфферентных технологий ГУ «Институт нефрологии НАМН Украины», доктор медицинских наук, профессор Ирина Алексеевна Дударь продолжила тему ХБП с акцентом на влиянии этого заболевания на течение и исходы беременности.
– По разным данным, ХБП болеют 10-16% популяции, женщины чаще за счет системных заболеваний соединительной ткани (ревматоидный артрит, системная склеродермия, системная красная волчанка). В глобальном масштабе ХБП страдают 195 млн женщин. У пациенток с ХБП повышен риск неблагоприятных исходов как для матери, так и для плода.
Беременность сама по себе может служить фактором риска заболевания почек или ухудшать течение уже существующей ХБП. Объем плазмы и сердечный выброс беременной увеличиваются в среднем на 30-50%, СКФ возрастает до 120-150 мл/мин/1,73 м2, а почечный кровоток повышается на 80%. Наличие преэклампсии у беременной повышает риск формирования ХБП в 4-5 раз.
Наличие ХБП у беременной сопряжено с определенными рисками как для матери (снижение СКФ, возможна потребность в диализе во время беременности или в короткие сроки после родов, тяжелая АГ; риск тромбоцитопении, кровопотери, тромбоза и сепсиса), так и для плода (задержка развития или внутриутробная смерть вследствие плацентарной недостаточности, преждевременные роды, побочное действие лекарственных средств, наследственные заболевания).
Характер течения ХБП во время беременности зависит от исходного функционального состояния почек. При исходном уровне креатинина <130 мкмоль/л вероятность снижения СКФ составляет 10%, основная причина – АГ. Более чем у 90% таких пациенток рождаются живые дети.
При уровне креатинина 130-220 мкмоль/л наблюдается снижение СКФ у 30% женщин, при неконтролированной АГ – у 50%. Терминальная стадия ХБП в короткие сроки развивается в 10% случаев. Рождение живых детей отмечают у 85% таких пациенток, за исключением женщин с неконтролированной АГ. При этом 60% подобных родов – преждевременные.
При высоких исходных уровнях креатинина (>220 мкмоль/л) резко увеличивается риск развития терминальной хронической почечной недостаточности во время беременности или в короткие сроки после родов. У таких женщин высок риск потери плода.
Принципы антенатального ведения беременных женщин с ХБП: коррекция АГ; назначение аспирина в дозе 75-150 мг/сут при уровне креатинина >130 мкмоль/л; наблюдение в динамике за уровнем креатинина сыворотки крови; контроль и оценка протеинурии, в том числе нефротического синдрома (НС); выявление и лечение инфекций мочевыводящих путей; оценка и поддержание водного баланса; оценка состояния плода, неотложное родоразрешение по показаниям.
Беременность оказывает выраженное отрицательное влияние на течение хронического гломерулонефрита, что связано с гиперфильтрацией. Увеличение протеинурии до нефротического уровня наблюдается у трети беременных с гломерулонефритом. НС существенно увеличивает риск перинатальной смерти плода (до 23%), задержки внутриутробного развития плода, преждевременных родов (до 35%), присоединения АГ и ухудшения функции почки у матери (до 45%). При наличии НС необходимо проводить дифференциальную диагностику с преэклампсией (внезапное развитие с тяжелой АГ), обострением гломерулонефрита (постепенное нарастание протеинурии) и развитием нефрита de novo. В период гестации чаще всего дебютируют фокально-сегментарный гломерулосклероз, IgA-нефропатия, люпус-нефрит, другая патология почек манифестирует редко.
Биопсия почки во время беременности показана при внезапном неуточненном ухудшении функции почки задолго до окончания срока гестации (при ранней диагностике быстропрогрессирующего гломерулонефрита может быть целесообразна агрессивная терапия – пульс-терапия кортикостероидами, плазмаферез) или при НС, который возник de novo на временном отрезке до 24 нед гестации. Во всех случаях при беременности >30 нед биопсия противопоказана – необходимо срочное родоразрешение.
Хронический гломерулонефрит с мочевым синдромом у беременных не требует специального лечения. При хроническом гломерулонефрите с НС необходимы возмещения потери белка за счет увеличения его содержания в рационе, ограничение поваренной соли не показано. Применение диуретиков исключено, поскольку исходная гиповолемия и дальнейшее снижение внутрисосудистого объема ухудшают маточно-плацентарную перфузию, провоцируют коллаптоидные состояния, повышают риск тромбообразования.
У женщин с хроническим гломерулонефритом, НС и АГ рекомендуются умеренное ограничение поваренной соли в диете, умеренные дозы диуретиков. Иммуносупрессивная терапия должна включать только кортикостероиды в невысоких дозах, применение циклоспорина не показано. Для профилактики гиперкоагуляции назначают гепарин, аспирин.
Неотложное родоразрешение следует проводить в случае неконтролируемого обострения или быстрого прогрессирования гломерулонефрита, неконтролируемой АГ, негативной динамики почечной функции. У таких женщин в I триместре выполняют прерывание беременности, при >34 нед – досрочное родоразрешение. Во II-III триместре решение вопроса зависит от клинических и морфологических данных.
У пациенток с ХБП, получающих гемодиализ, беременность нежелательна. Меньше половины беременностей у таких женщин заканчивается родами, часто – преждевременными.
В мире описано несколько тысяч беременностей у женщин с почечным трансплантатом, более 90% из них окончились благополучно. Беременность не противопоказана женщинам с трансплантированной почкой, у которых стабильная функция трансплантата в течение 1-2 лет; отсутствует протеинурия; АГ отсутствует или контролируется; отсутствуют нарушения уродинамики трансплантата; проводится терапия низкими дозами иммуносупрессантов.
У женщин после трансплантации наибольший риск связан с осложнениями, ассоциированными с иммуносупрессией (септические осложнения, врожденные аномалии, надпочечниковая и почечная недостаточность у плода, тромбоцитопения, разрыв матки, эктопическая беременность, преждевременные роды).
Таким образом, большинство изменений при беременности – уровень артериального давления (АД), экскреция белка, изменение водно-солевого гомеостаза – носят физиологический характер. ХПН сама по себе не является противопоказанием к беременности, прогноз зависит от функционального состояния почек и АД. Появление отеков, АГ, изменений в анализах мочи требует тщательной дифференциальной диагностики.
 Старший научный сотрудник отдела нефрологии и диализа ГУ «Институт нефрологии НАМН Украины», кандидат медицинских наук Константин Николаевич Законь рассказал о современных подходах к ведению беременных с острым повреждением почек (ОПП).
Старший научный сотрудник отдела нефрологии и диализа ГУ «Институт нефрологии НАМН Украины», кандидат медицинских наук Константин Николаевич Законь рассказал о современных подходах к ведению беременных с острым повреждением почек (ОПП).
– ОПП характеризуется повышением креатинина крови ≥26,5 мкмоль/л или в ≥1,5 раза по сравнению с исходным уровнем (если он известен, или предполагается, что это произошло в течение предыдущих 7 дней, или диурез <0,5 мл/ч/сут), которое продолжается не менее 48 ч и сочетается с другими маркерами повреждения мочевой системы.
В развивающихся странах ОПП, которое требует диализа, регистрируется в 10% случаев, а обусловленная ОПП материнская смертность составляет 6,4%.
Основные причины ОПП:
- преренальные – hyperemesis gravidarum, кровотечение, сердечная недостаточность, сепсис;
- ренальные – острый канальцевый некроз, острый кортикальный некроз, острый жировой гепатоз беременных, преэклампсия/эклампсия, HELLP-синдром, тромбоцитопеническая пурпура / атипичный гемолитико-уремический синдром, пиелонефрит, эмболия амниотической жидкостью, тромбоэмболия почечной артерии, люпус-нефрит, гломерулонефрит, острый тубулоинтерстициальный нефрит;
- постренальные – гидронефроз вследствие компрессии плодом, повреждение мочевого пузыря и мочеточников (например, при кесаревом сечении), обструкция конкрементом или опухолью.
Лечение ОПП должно быть направлено на причину, вызвавшую повреждение. Поддерживающая терапия имеет целью сохранение функции почек и предполагает отмену нефротоксичных препаратов, коррекцию электролитных нарушений, ацидоза и анемии, а также АГ (блокаторы рецепторов ангиотензина ІІ, ингибиторы ангиотензинпревращающего фермента противопоказаны, диуретики не рекомендованы), поддержание эуволемии. Наконец, при наличии показаний проводится диализная почечнозаместительная терапия.
В работах последних лет показано, что интенсивный режим гемодиализа улучшает прогноз у беременных. Диализная почечнозаместительная терапия у беременных имеет такие особенности:
- раннее начало (мочевина – 10-15 ммоль/л, креатинин – <550 мкмоль/л, pH <7,2);
- рекомендованный режим диализа 6 р/нед по 6 ч (минимальный – 4 р/нед по 5 ч);
- использование высокопоточного диализатора;
- рекомендованная скорость потока крови – 200-300 мл/мин, диализата – 500 мл/мин;
- в качестве антикоагулянта используют гепарин в минимально необходимой дозе;
- показан частый контроль АД (целевые цифры составляют 120/70-140/90 мм рт. ст.);
- необходимо учитывать увеличение массы тела беременной (прирост составляет в среднем 250 г/нед до 20-й недели беременности и 300-500 г/нед после);
- бикарбонат диализата – 25 ммоль/л, калий – 3 ммоль/л, кальций диализата – 1,25 ммоль/л;
- целевой уровень гемоглобина – 100-110 г/л; гематокрит >25%.
Важными аспектами при проведении гемодиализа у беременных являются аккуратное применение витамина D (только под контролем его уровня в крови), назначение фолиевой кислоты и комплекса водорастворимых витаминов. Контроль биохимических маркеров и общего анализа крови проводят каждую неделю. После 20-й недели беременности необходимо во время диализа обеспечить женщине такое положение тела, которое будет предупреждать компрессию нижней полой вены.
Таким образом, ОПП у беременных – состояние, угрожающее здоровью матери и ребенка. Причины ОПП не обязательно связаны с беременностью. Принципы терапии ОПП у беременных такие же, как и в общей популяции; лечение должно осуществляться мультидисциплинарной командой.
 Вопросам нарушения фосфорно-кальциевого обмена у женщин с ХБП в менопаузе посвятила свой доклад заведующая кафедрой внутренней медицины № 3 Тернопольского государственного медицинского университета им. И. Я. Горбачевского, доктор медицинских наук, профессор Лилия Петровна Мартынюк.
Вопросам нарушения фосфорно-кальциевого обмена у женщин с ХБП в менопаузе посвятила свой доклад заведующая кафедрой внутренней медицины № 3 Тернопольского государственного медицинского университета им. И. Я. Горбачевского, доктор медицинских наук, профессор Лилия Петровна Мартынюк.
– Нарушения минерального обмена у пациентов с ХБП сопряжены с нарушениями обмена кальция, фосфора, паратгормона, витамина D, кальцификацией сосудов и мягких тканей, нарушением костного ремоделирования, минерализации, объема, роста и прочности костей. Клиническими последствиями этих нарушений являются боль в костях, переломы, гиперплазия паращитовидных желез, паратиреоидэктомия, кардиоваскулярные события, госпитализации, смерть.
Ренальная остеодистрофия – это нарушение морфологии кости у пациентов с ХБП. По мере ухудшения функции почек прогрессируют нарушения минерального обмена, которые приводят к формированию минерально-костных нарушений, ассоциированных с ХБП (МКН-ХБП).
Различные варианты ренальной остеодистрофии отличаются по скорости ремоделирования кости, степени минерализации, нарушениям костного объема и представлены такими формами: высокообменное заболевание скелета – вторичный гиперпаратиреоз, фиброзный остеит; низкообменное заболевание скелета – остеомаляция, адинамическая болезнь кости; смешанная форма – вторичный гиперпаратиреоз с нарушением минерализации костной ткани.
Для диагностики МКН-ХБП используют такие тесты:
- уровень кальция крови (общий, ионизированный, корригированный);
- уровень фосфора крови;
- активность щелочной фосфатазы;
- концентрация паратгормона;
- уровень 25-гидроксивитамина D.
Морфологическое подтверждение диагноза позволяет получить костная биопсия.
В лечении таких пациентов возникают значительные трудности. При персистирующей гиперфосфатемии показано ограничение фосфатов в пище. Если на фоне гипофосфатной диеты гиперфосфатемия сохраняется, могут быть назначены фосфорсвязывающие препараты. Если не удается купировать гиперфосфатемию на фоне диеты и медикаментозного лечения, показан ночной или удлиненный диализ. При невозможности последнего используют кальцимиметики или паратиреоидэктомию для снижения уровня паратгормона. Кальцимиметики повышают чувствительность к кальцию кальциевых рецепторов (CaSR) в паращитовидных железах. Кальциевые рецепторы – основной фактор регуляции секреции паратгормона и гиперплазии паращитовидных желез. Кальцимиметики (цинакальцет) уменьшают концентрацию паратгормона в крови, а также снижают уровни кальция и фосфора.
Может ли развиваться остеопороз у женщин с ХБП в менопаузе? Диагноз остеопороза может быть установлен при наличии сниженной минеральной плотности костной ткани (МПКТ) и высокого риска низкоэнергетических переломов при условии исключения других видов МКН-ХБП. Как правило, диагноз остеопороза более вероятен у женщин в постменопаузе с ХБП при СКФ >60 мл/мин/1,73 м2 и отсутствии признаков МКН-ХБП.
Модификация образа жизни имеет большое значение в лечении пациентов с ХБП. При СКФ >30 мл/мин/1,73 м2 у пациентов без признаков МКН-ХБП рекомендовано употребление кальция и витамина D согласно общепопуляционным рекомендациям. Потребление кальция должно составлять 1200 мг/день (пища и суплементация), витамина D – приблизительно 1000 МЕ/день для поддержания целевого уровня 30-50 нг/мл. У пациенток с СКФ <30 мл/мин/1,73 м2 без признаков МКН-ХБП поступление кальция должно составлять 1200 мг/день (с пищей и не менее 500 мг путем суплементации), при этом предпочтение отдается молочным продуктам; витамина D – около 800 МЕ/день.
У пациентов с ХБП высок риск развития саркопении (уменьшения мышечной массы и силы мышц). Пациенты, которые не могут подняться со стула без помощи рук, имеют выраженную саркопению и высокий риск падений, для снижения которого им следует рекомендовать ходьбу и нагрузочные упражнения, упражнения на растяжение мышц и укрепление вестибулярного аппарата, ношение протекторов бедра, установление поручней в ванной комнате и туалете.
Для пременопаузальных женщин с ХБП и гипогонадизмом, низкой костной массой и/или низкоэнергетическими переломами в анамнезе рекомендуются оральные контрацептивы (при отсутствии противопоказаний). Пременопаузальные женщины с ХБП, которые получают заместительную гормональную терапию, не требуют дополнительного лечения остеопороза.
У пациенток с СКФ ≥30 мл/мин/1,73 м2 без признаков МКН-ХБП фармакотерапия остеопороза должна быть такой же, как и у пациентов без ХБП. Препараты для лечения остеопороза у лиц с ХБП I-III стадий используются в обычных дозах. Исключением является золедроновая кислота, которая не показана лицам с СКФ <35 мл/мин/1,73 м2.
У женщин с СКФ <30 мл/мин/1,73 м2 и низкой МПКТ при отсутствии признаков МКН-ХБП или низкоэнергетических переломов в анамнезе рекомендовано не начинать фармакотерапию остеопороза. Если у пациента с СКФ <30 мл/мин/1,73 м2, низкой МПКТ нет признаков МКН-ХБП, но имеются низкоэнергетические переломы в анамнезе, то может быть рассмотрена фармакотерапия остеопороза; при этом требуется тщательное исключение других форм МКН-ХБП как причины переломов. У таких лиц лечение остеопороза может проводиться бисфосфонатами (как правило, натрия ризедронат в половинной дозе – 35 мг/нед). В качестве альтернативы можно рассматривать денозумаб, однако у пациентов на гемодиализе этот препарат ассоциировался с клинически значимой гипокальциемией. Бисфосфонаты не должны использоваться рутинно у пациентов с СКФ <30 мл/мин/1,73 м2; эти препараты следует назначать только после исключения ренальной остеодистрофии. Больным с адинамической болезнью кости противопоказаны препараты, которые уменьшают костную резорбцию и ремоделирование; потенциально полезным может быть терипаратид.
Таким образом, у женщин в менопаузе и постменопаузе МКН-ХБП требуют тщательной дифференциальной диагностики с остеопорозом. Модификация образа жизни может быть полезным инструментом в уменьшении нарушений минерального обмена, укреплении мышечного аппарата и предупреждении падений.
Подготовила Мария Марчук
Медична газета «Здоров’я України 21 сторіччя» № 7 (428), квітень 2018 р.


