7 травня, 2018
EAU-2018: когда фундаментальная наука встречается с клинической практикой
 Наиболее значимое событие для европейских урологов – ежегодный конгресс Европейской ассоциации урологов (EAU) – состоялось 16-20 марта в Копенгагене (Дания). Мероприятие, программа которого была чрезвычайно насыщенной и информативной, привлекло внимание более чем 8 тыс. специалистов этой области медицины. В ходе более чем 300 научных сессий было заслушано почти 1500 докладов ведущих экспертов. Делегаты приняли участие в лекциях по инновационным решениям, видеотрансляциях хирургических операций, практических тренингах и мастер-классах.
Наиболее значимое событие для европейских урологов – ежегодный конгресс Европейской ассоциации урологов (EAU) – состоялось 16-20 марта в Копенгагене (Дания). Мероприятие, программа которого была чрезвычайно насыщенной и информативной, привлекло внимание более чем 8 тыс. специалистов этой области медицины. В ходе более чем 300 научных сессий было заслушано почти 1500 докладов ведущих экспертов. Делегаты приняли участие в лекциях по инновационным решениям, видеотрансляциях хирургических операций, практических тренингах и мастер-классах.
Особый интерес участников конгресса вызвало совместное заседание Секции андрологической урологии (ESAU) и Секции инфекционных заболеваний в урологии (ESIU). Представляем вниманию читателей некоторые рассмотренные на этом заседании темы.
Инновации в диагностике урологических заболеваний
В частности, речь шла о некоторых аспектах диагностики: от различных опросников и систем оценки рисков до новейших методик определения возбудителей и их чувствительности к антибактериальным препаратам.
Владимир Муравьев (США) в своем докладе коснулся вопроса верификации возбудителей инфекций мочеполовых путей (ИМП). Патогены, провоцирующие развитие острых ИМП, представлены планктонными бактериями, которых успешно определяют с использованием традиционных методов выявления (культуральных). Однако возбудители хронической инфекции формируют так называемые биопленки, их вид и чувствительность к антибиотикам (АБ) наиболее эффективно верифицируются методом ДНК-секвенирования.
Секвенирование нового поколения (NGS) позволяет определять сразу несколько участков генома, что обеспечивает определение возбудителя через 1 ч, а чувствительности к АБ – через 4 ч после забора материала. Поэтому лечение после диагностики методом NGS эффективнее терапии, основанной на результатах культурального метода выявления патогена.
Недостатком нового метода диагностики является его сверхчувствительность, из-за которой определяются все микроорганизмы (включая нормальную микрофлору), что влечет за собой необходимость в дальнейшей валидации.
Темой еще одной сессии стало диагностическое значение гибкой цистоскопии при обследовании женщин с рецидивирующими инфекциями мочеполовой системы (РИМП). Было показано, что польза от этого вмешательства экстремально мала, поскольку не приводит к выявлению большего количества уретральных стенозов, поэтому ее не рекомендуется проводить рутинно у женщин моложе 65 лет. У пациенток более пожилого возраста цистоскопия показана для выявления опухолей мочеполовой системы.
С большим вниманием был выслушан доклад Джахонгира Алиджанова (Германия, Узбекистан), посвященный увеличению риска возникновения острого цистита (ОЦ) у женщин с вагинальными выделениями. Ранее данная парадигма была диаметрально противоположной и наличие вагинальных выделений ассоциировали с исключением диагноза «цистит». ESIU рекомендует использовать опросник Алиджанова для установления диагноза ОЦ у женщин.
Исследования японских ученых показали, что системы оценки SOFA и quick SOFA клинически более ценные в прогнозе смерти пациентов с острым калькулезным пиелонефритом (ОКП), чем синдром системной воспалительной реакции (ССВР). Данный скрининг рекомендован пациентам высокого риска развития сепсиса.
Анализ SOFA и quick SOFA использовали на 141 пациенте с ОКП, которые не находились в отделении реанимации и интенсивной терапии (ОРИТ). В результате было установлено, что пациенты с ОКП с SOFA7 и qSOFA2 имеют высокий риск наступления смерти, перевода в ОРИТ и немедленной декомпрессии мочевых путей.
Факторы риска послеоперационного сепсиса также изучались в большом проспективном исследовании с участием 1240 пациентов (средний возраст – 64,3 года), перенесших урологические операции. Результаты показали, что факторы риска послеоперационного сепсиса включают пожилой возраст, обструкцию мочевых путей и высокий уровень лактата крови. Сопутствующие заболевания и размер камней не влияли на риски.
Ряд исследований, проведенных в Италии, Австрии и Великобритании, касался выбора наиболее оптимального предиктора развития ССВР у пациентов после урологических операционных вмешательств. Результаты двух из этих исследований (Италия и Великобритания) показали, что посев камня после перкутанной нефролитотрипсии (ПНЛТ) в плане прогноза развития инфекционных осложнений и выбора антибактериального лечения является более весомым фактором, чем посев мочи, однако это не согласуется с данными, полученными австрийскими исследователями, и требует дальнейшего изучения.
В проспективном анализе, осуществленном бельгийскими учеными, изучали корреляцию между уровнем клинической инфекции и послеоперационной бактериурии после трансуретральной резекции предстательной железы (ТУРПЖ). Положительный посев мочи наблюдался у 8,2% пациентов, среди них E.coli высевалась у 28,2%. В послеоперационном периоде процент позитивных посевов вырос до 11,4%. В основном идентифицировались E. faecalis (29,2%), K. pneumoniae (13,2%) и E. coli (13%). Спустя 3 нед после операции E. faecalis высевалась у 44,4% пациентов, а E. coli – у 36,1%. Положительный культуральный посев крови выявили у 6,1% пациентов, ирригационной жидкости – у 4,7% и ткани ПЖ – у 9,3%.
При этом клинически неосложненная лихорадка наблюдалась у 3,8% больных, а септицемия возникла только у 0,2% пациентов.
Небольшой процент случаев инфекционных осложнений, несмотря на высокий уровень послеоперационной бактериурии и положительный культуральный анализ крови, ирригационной жидкости и ткани ПЖ, указывает на отсутствие необходимости в антибиотикотерапии при отсутствии клинической картины инфекции, однако все это не отменяет необходимости проводить дальнейшие исследования.
Новое в стратегиях лечения урологических заболеваний
Прежде всего были рассмотрены новые антибактериальные препараты, а также обновленные рекомендации по ведению пациентов с различными урологическими заболеваниями; кроме того, сравнивались эффективность и безопасность различных малоинвазивных методик лечения.
Курт Набер (Германия) в своем выступлении подробно остановился на характеристиках новых АБ, применяемых в лечении ИМП.
Из-за приобретающей все более острый характер проблемы антибиотикорезистентности (АБР) пенициллины в комбинации с ингибиторами β-лактамаз, которые раньше эффективно использовались в терапии ИМП, уходят в прошлое. Сегодня для лечения неосложненных ИМП рекомендуют такие широко известные АБ, как фосфомицин, нитрофурантоин, пивмециллинам и нитроксолин.
Для терапии осложненных ИМП разработаны новые АБ:
- Цефалоспорины в комбинации с ингибиторами β-лактамаз расширенного спектра (иБЛРС): цефтолозан + тазобактам, цефтазидим + авибактам.
- Карбапенемы в комбинации с иБЛРС: имипенем + релебактам, меропенем + ваборбактам.
- Фторхинолоны: финафлоксацин, делафлоксацин.
- Тетрациклины: эравациклин, омадациклин.
- Сидерофоры цефалоспорины (цефидерокол).
- Аминогликозиды (плазомицин).
Принципиально новыми АБ являются цефидерокол и плазомицин.
В основе механизма действия цефидерокола лежат свойства молекулы активно проходить через железорегулируемые протеины наружной мембраны, которые индуцируются при железодефицитных состояниях. Спектр активности охватывает β-лактамазы расширенного спектра (БЛРС), карбапенем-резистентные энтеробактерии, мультирезистентный Acinetodacter и мультирезистентные P. aeruginosa. В III фазе клинических исследований цефидерокол показал большую результативность при лечении острых ИМП, чем комбинация имипенема с циластатином (72,6 и 54,6% соответственно).
Эффективность плазомицина обусловлена его способностью уклоняться от аминогликозид-модифицирующих ферментов. Он активен в отношении КРС-патогенов (карбапенем-резистентных штаммов), что подтверждается результатами микробиологической эрадикации, в которой плазомицин оказался более действенным, чем меропенем.
Рассмотренные антибактериальные препараты увеличивают антимикробный спектр и помогают в борьбе с резистентными возбудителями, однако не следует забывать, что главным средством в борьбе с устойчивостью к АБ является правильный подход к их назначению.
Как уже было сказано выше, на конференции были также представлены обновленные рекомендации EAU по инфекциям в урологии (2018). Основные изменения коснулись бактериального простатита, гангрены Фурнье, а также перипроцедурной антимикробной профилактики (АМП).
Для выбора наилучшей антимикробной стратегии для лечения мужчин с острым и хроническим бактериальным простатитом был проведен систематический обзор литературы с 1980 по 2017 год. Были найдены 1 систематический обзор, 6 рандомизированных клинических исследований (РКИ), 2 описательных обзора, 1 проспективное когортное исследование, 2 проспективных поперечных исследования и 1 ретроспективное когортное исследование.
Что касается эпидемиологии, этиологии и патогенеза бактериального простатита, то по-прежнему основным возбудителем острого простатита считается E. coli. При хроническом простатите этот спектр шире, включая редких возбудителей при ВИЧ-инфекции. Роль C. trachomatis остается неясной.
Была подтверждена роль фторхинолонов как первой линии терапии без значимых различий между левофлоксацином, ципрофлоксацином и прулифлоксацином по клинико-бактериологической эффективности. При наличии атипичных возбудителей подтверждена роль макролидов и тетрациклинов.
Данные одного РКИ показали, что при хроническом бактериальном простатите трихомонадной этиологии метронидазол в дозе 500 мг 3 р/день в течение 14 дней обеспечивает эффективность эрадикации 93,3% возбудителей. В результате были сформулированы следующие рекомендации в отношении антимикробной терапии (табл. 1).
Кроме этого были рассмотрены основные аспекты лечения гангрены Фурнье (некротизирующий фасциит промежности и наружных гениталий). Для этого был осуществлен литературный поиск с 1980 по 2017 год. Уровень смертности вследствие данного состояния, согласно разным источникам, колеблется в пределах 5-10%. Основными факторами риска являются сахарный диабет, высокий индекс массы тела и пожилой возраст.
Возможно использование следующих вариантов антибиотикотерапии:
- пиперацилин/тазобактам в комбинации с ванкомицином;
- имипенем/циластатин;
- меропенем;
- эртапенем;
- цефотаксим в комбинации с метронидазолом или клиндамицином.
Было показано, что смертность не зависит от того, принимают ли АБ больше или меньше 10 дней.
Систематический обзор по технике закрытия раны имеет слабую доказательную базу, однако общепринятым считается, что при дефекте тканей <50% площади мошонки заживление происходит первичным или вторичным натяжением, а при площади поражения >50% применяют лоскутную пластику.
В отношении вспомогательной терапии (гипербарическая оксигенация, смоченные медом повязки, раствор эдинбургской липы, вакуум-терапия) степень доказательности низкий либо отсутствует вовсе, что требует дальнейшего проведения РКИ.
Ряд докладов касался малоинвазивных методик лечения в урологии. Так, были представлены первые результаты мультицентрового РКИ, которое проводится в 20 академических центрах в Китае. Целью его является оценка эффективности и безопасности мини-ПНЛТ в сравнении со стандартной ПНЛТ для ведения почечных камней размером 20-40 мм.
Было установлено, что мини-ПНЛТ имеет значимые преимущества в уменьшении кровотечения, большем количестве пациентов без дренажей, более высоком уровне послеоперационного комфорта и уменьшении количества койко-дней. Для камней >3 см мини-ПНЛТ требует больше операционного времени, однако уровень «без камней» и осложнения были сопоставимы с таковыми в группе сравнения.
В еще одном исследовании сравнивали эффективность супер-мини-ПНЛТ и мини-ПНТЛ для камней >2 см. В результате показатели по времени оказались сопоставимыми, но количество койко-дней при супер-мини-ПНЛТ было значительно меньше (2,6±1,4), чем при мини-ПНЛТ (5,3±2,0; р=0,001).
Особенности профилактики ИМП
Бьорн Вульт (Швеция) в своем докладе поднял вопрос неантибактериального лечения и профилактики острого неосложненного цистита (ОНЦ).
На сегодня неантибактериальными средствами с доказанной эффективностью в лечении ОНЦ являются нестероидные противовоспалительные препараты (НПВП). Немаловажную роль в облегчении симптомов цистита играет также увеличение количества принимаемой жидкости. РКИ показали, что в 30%-59% случаев ОНЦ проходит без лечения и только в 2% случаев возникает осложнение в виде острого пиелонефрита, поэтому под вопросом остается эффективность канефрона в лечении данного заболевания.
Для успешной АМП необходимо понимание такого понятия, как внутриклеточные бактериальные сообщества. Механизм их формирования заключается в том, что уропатогенная E. сoli, проникая в мочевой пузырь, связывается с уроэпителием с помощью фимбрий 1 типа. Основным связывающим белком является уроплакин.
Данное взаимодействие индуцирует апоптоз поверхностных эпителиальных клеток и последующую инвазию бактерий в интермиттирующий слой, где формируются так называемые покоящиеся внутриклеточные резервуары – источник инфекции. Интермиттирующий слой изменяется 1 раз в 6-12 мес, вот почему борьба с рецидивирующем циститом требует столь длительного времени.
Протекторными свойствами в этом плане обладают асимптоматическая бактериурия (подсаживание непатогенных штаммов бактерий в мочевой пузырь), Uro-vaxom и местная эстрогенотерапия. Перспективным направлением считается разработка манозидов – синтетических аналогов Д-манозы (простой сахар березы и бука), которые в 200 тыс. раз активнее натуральных препятствуют адгезии E. coli. Доказано, что клюквенный сок и лактобактерии не являются эффективной профилактикой рецидивирующих ИМП.
Тема профилактики получила свое продолжение в постерной сессии, посвященной вакцинам для профилактики рецидивирующих ИМП.
Был сделан систематический обзор 559 статей, из них релевантными оказались 10, в которых представлены результаты исследований с участием 1766 пациентов. РКИ оказались гетерогенными, поэтому необходимы дальнейшие изыскания, сегодня же на фармацевтическом рынке представлены 3 вакцины для профилактики рецидивов ИМП:
- Urovac, в состав которой входят 6 убитых серотипов E. coli, P. vulgaris, K. pneumoniae, M. morganii, E. faecalis, значительно снижала число рецидивов в сравнении с двумя следующими вакцинами.
- EXPEC4V (4 биоконъюгаты, О-антиген E. coli 4 серотипов), несмотря на эффективность, в то же время вызвала много непредвиденных побочных реакций.
- Uro-vaxom продемонстрировала отличные результаты в профилактике рецидивирующих ИМП и уменьшении дизурии в течение 6 месяцев.
Согласно рекомендациям EAU по перипроцедурной АМП перед урологическими вмешательствами не может быть рекомендована ни одна из альтернативных методик, кроме стандартного культурального исследования мочи.
К неантибактериальным методам асептики относятся:
- Корректные методы мытья и стерилизации инструментов; регулярное и полное мытье операционной и соседних помещений; полная дезинфекция при любой контаминации; тщательное мытье рук (без использования мыла с хлоргексидином).
- Обрезание, а не сбривание волос с операционного поля.
- Отказ от механического очищения кишечника.
- Применение при обработке операционного поля раствора йода.
Тактика АМП в зависимости от вида урологического вмешательства с позиции доказательной медицины представлена в таблице 2.
Некоторые исследования, касающиеся профилактики, находятся в стадии доклинического изучения. В Сингапуре осуществлено исследование нового уретрального катетера, покрытого наночастицами серебра, на мышах и свиньях. Этот силиконовый катетер медленно высвобождает ионы серебра и ингибирует инкрустацию и инфекцию, что подтверждается результатами культуральных исследований, в которых наблюдается уменьшение формирования биопленок на катетерах через 2 и 3 нед, без признаков токсичности, что делает их более эффективными, чем коммерческие катетеры.
Антибиотикорезистентность в урологии
Безусловно, не могли участники конференции не коснуться одной из наиболее острых проблем мировой медицины – распространения устойчивости к АБ, в том числе и у урологических больных.
Медина Поло (Испания) и Томмазо Кай (Италия) в своих докладах акцентировали внимание на том, что сегодня 45% энтеробактерий и 21% P. аeruginosa, высеянных в урологических стационарах, являются мультирезистентными. Во всем мире наибольшую проблему представляют собой Enterobacteriaceae, продуцирующие БЛРС, карбапенем- и ванкомицин-резистентные энтерококки и метицилин-резистентный золотистый стафилококк (MRSA).
Поводом для беспокойства является также C. difficile-ассоциированная диарея, возникающая, по данным литературы, у 20-50% госпитализированных. Указанное осложнение развивается у 11% пациентов после цистэктомии и требует их изоляции ввиду высокой контаминации окружающей среды и устойчивости патогена к спиртсодержащим антисептикам. В Испании наблюдается рост АБР к E. coli, K. pneumoniae, E. faecium, P. aeruginosa, в Европе – энтеробактерий к цефалоспоринам и карбапенемам.
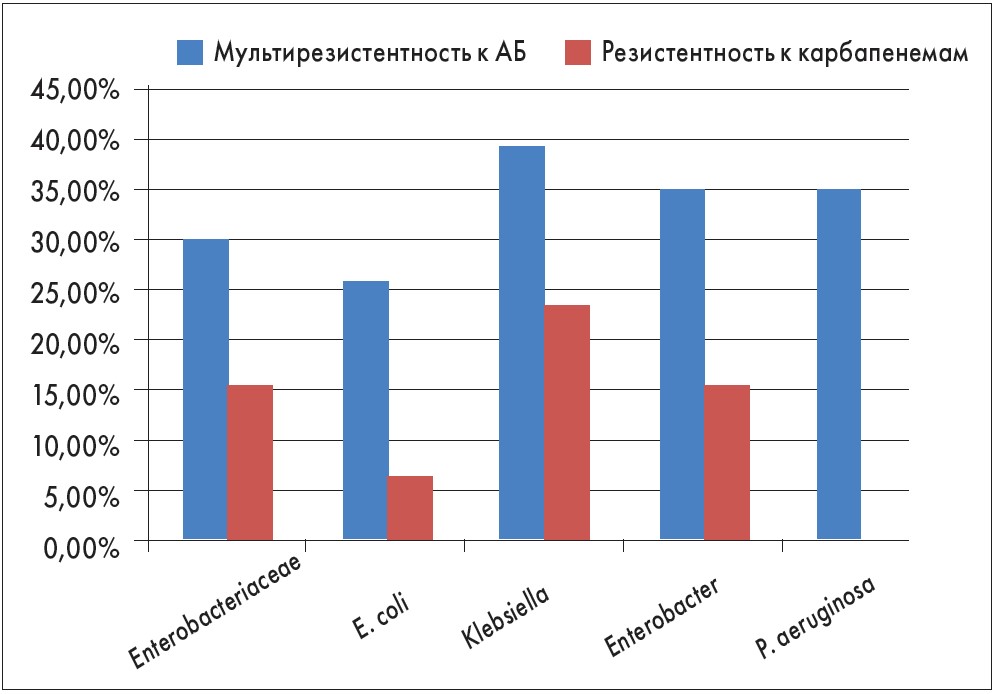
В одном из исследований испанские ученые изучали степень распространения мультирезистентных микроорганизмов у пациентов с инфекциями, связанными с медицинскими вмешательствами, госпитализированных в урологические палаты (рис. 1).
Рис. 1. Степень распространения мультирезистентных микроорганизмов у пациентов с инфекциями, связанными с медицинскими вмешательствами, госпитализированных в урологические палаты
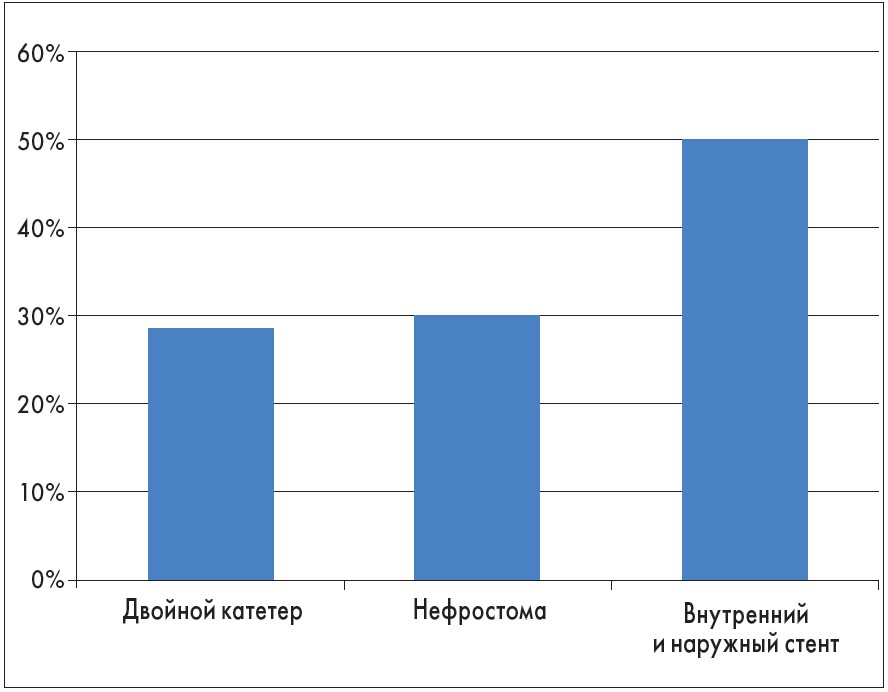
Также была представлена информация о корреляции между типом катетера и степенью мультирезистентности (рис. 2).
Рис. 2. Корреляции между типом катетера и степенью мультирезистентности микроорганизмов
Факторы риска включали иммуносупрессию, предшествующую ИМП, постоянный уретральный катетер до поступления и мочекаменную болезнь.
Первым шагом в борьбе с АБР является осведомленность о существовании подобной проблемы. Остальные меры включают:
- Корректный подход к выбору эмпирического лечения. В случае неосложненных инфекций предпочтение нужно отдавать фосфомицину и нитрофурантоину, уровень резистентности к которым низкий, а в случае серьезной инфекции (MRSA, A. baumanii, P. aeruginosa, карбапенемаза-продуцирующие бактерии) использовать антибактериальные препараты, такие как колистин и тигециклин.
- Путь введения, доза и длительность приема АБ должны быть адекватными и основываться на результатах посева мочи.
- Периоперационно АБ должны назначаться только при инфекционных заболеваниях, а не рутинно в первые 24 ч после операции.
- Асимптоматическая бактериурия подлежит лечению только у беременных женщин и при инструментальных вмешательствах.
Конгресс EAU в который раз подтвердил свой статус одного из наиболее важных мероприятий в европейской урологии. Участники форума получили не только теоретические знания относительно инноваций в вопросах диагностики, лечения и профилактики урологических заболеваний, но и четкие рекомендации применения теории в рутинной клинической практике.
Подготовила Анна Кирпач
Тематичний номер «Урологія. Нефрологія. Андрологія» № 1 (12), березень 2018 р.