10 травня, 2018
Выбор дозы аторвастатина с позиций прогноза
Пятого апреля состоялась онлайн-конференция «Рекомендации по выбору дозы статина с позиции прогноза лечения», объединившая в режиме электронной связи Киев, Одессу, Днепр и Харьков. Программа мероприятия включала доклады ведущих специалистов из Украины и Нидерландов, сессию вопросов и ответов и разбор клинических случаев.
 Ведущий научный сотрудник отдела интервенционной кардиологии ГУ «ННЦ «Институт кардиологии им. Н. Д. Стражеско» НАМН Украины (г. Киев), доктор медицинских наук, профессор Максим Юрьевич Соколов посвятил свое выступление патогенезу коронарного атеросклероза, методам его диагностики и лечения, в т. ч. использованию высоких доз статинов при острой коронарной патологии.
Ведущий научный сотрудник отдела интервенционной кардиологии ГУ «ННЦ «Институт кардиологии им. Н. Д. Стражеско» НАМН Украины (г. Киев), доктор медицинских наук, профессор Максим Юрьевич Соколов посвятил свое выступление патогенезу коронарного атеросклероза, методам его диагностики и лечения, в т. ч. использованию высоких доз статинов при острой коронарной патологии.
Холестерин (ХС) подразделяется на значительно большее количество фракций, чем обычно выделяется, а именно около 16. Чем ниже плотность фракции, тем более вредной она является. Триглицериды (ТГ) и их компоненты (жирные кислоты) – это наиболее энергоемкие молекулы человеческого организма (9,4 ккал/г). Человек с массой тела 68 кг и содержанием жира 20% способен сохранить более 120 тыс. ккал. Эквивалентный объем энергии, аккумулированный в гликогене, потребовал бы массы тела 182 кг, поскольку сохранение 1 г этого вещества требует 3-4 г воды и электролитов. Поэтому отчасти ТГ являются полезными для организма, однако их метаболизм и распад должны проходить без каких-либо нарушений. В свою очередь, липопротеиды высокой плотности (ЛПВП) являются протекторными частицами, поскольку способствуют удалению ХС из клеток и его выведению через желудочно-кишечный тракт.
Одним из звеньев патогенеза атеросклероза является повышенная проницаемость эндотелия. При наличии эндотелиальных дефектов молекулы липопротеидов низкой плотности (ЛПНП) проникают в интимальное пространство, куда затем привлекаются макрофаги. Эти макрофаги усиленно поглощают ЛПНП, превращаясь в дальнейшем в пенистые клетки. Так внутри стенки сосуда появляется жировая полоска. На данной стадии просвет сосуда еще не изменен, поэтому обнаружить что-либо при коронарографии невозможно. Так называемый эффект позитивного ремоделирования (рост бляшки внутрь стенки сосуда, а не в его просвет) обеспечивает длительное бессимптомное течение атеросклероза коронарных артерий. Поэтому первое появление симптомов ишемической болезни сердца (ИБС) не означает, что болезнь развилась недавно, а наоборот, свидетельствует о завершающем этапе патологии. В связи с этим при появлении симптоматики ИБС следует немедленно выявлять бляшки и стенозы, стабилизируя первые и подвергая стентированию вторые.
Считается, что полностью побороть атеросклероз на данном этапе развития медицины невозможно. Однако вполне реально стабилизировать его течение, в первую очередь с помощью статинотерапии. Согласно современным рекомендациям, статины следует назначать или рекомендовать продолжать их применение в высоких дозах и на ранних стадиях лечения всем пациентам с инфарктом миокарда с элевацией сегмента ST (STEMI) при отсутствии противопоказаний независимо от исходного уровня ХС пациента. Повторная оценка ЛПНП должна быть проведена через 4-6 нед, целевой уровень составляет ≤1,8 ммоль/л.
Важным аспектом статинотерапии выступают плейотропные эффекты препаратов этой группы, в частности противовоспалительное действие. Наиболее активными и часто назначаемыми статинами являются розува- и аторвастатин.
Аторвастатин обладает мощной доказательной базой при стабильной стенокардии, остром коронарном синдроме (ОКС), артериальной гипертензии. Действие различных доз аторвастатина хорошо исследовано, и эффект для 10, 20, 40 и 80 мг составляет около 37, 43, 49 и 55% снижения ЛПНП соответственно (Law M. R. et al., 2003).
У пациентов, которым проводится коронарное стентирование, статины обеспечивают миокардиальную и ренальную протекции. При условии приема статинов больными после проведения чрескожного коронарного вмешательства (ЧКВ) повышается выживаемость по сравнению с пациентами, не получавшими статинотерапии. Поэтому использование стентов позволяет корректировать грубые нарушения кровотока, после чего необходимо длительно лечить пациента статинами в необходимых дозах. Согласно исследованию ARMIDA-RECAPTURE, назначение аторвастатина уменьшает количество рестенозов и смертей через 30 дней после кардиоваскулярного события. То же исследование установило, что нагрузочные дозы аторвастатина у пациентов на постоянной статинотерапии снижают перипроцедурное повреждение миокарда при проведении вмешательств (Di Sciascio E. et al., 2009). Что касается ренопротекции, для профилактики контраст-индуцированной нефропатии рекомендовано кратковременное использование высоких доз статинов. Назначение аторвастатина пациентам, которым проводится ЧКВ, достоверно снижает количество случаев острого контраст-индуцированного повреждения почек (примерно в 2,5 раза) (Patti et al., 2011).
Неадекватное назначение статинов, в т. ч. назначение недостаточных доз, в Украине обусловлено, среди прочего, боязнью побочных эффектов – рабдомиолиза. Однако достижение снижения ЛПНП на 50% сопровождается мизерной частотой возрастания уровня аланинаминотрансферазы более чем в три раза.
 В докладе профессора Peter J. Lansberg (г. Гронинген, Нидерланды) был представлен обзор последних данных по липидоснижающей терапии.
В докладе профессора Peter J. Lansberg (г. Гронинген, Нидерланды) был представлен обзор последних данных по липидоснижающей терапии.
У пациентов часто возникает вопрос: «Я же никогда ничем не болел, почему у меня развился инфаркт?». Можно сравнить факторы сердечно-сосудистого риска с причинами дорожно-транспортных происшествий – нарушением работы тормозов, превышением скорости, обледенением дороги, недостаточным давлением в шинах и др. Атеросклероз и, соответственно, кардиоваскулярные катастрофы вызываются не одним фактором, а целым комплексом причинных воздействий, среди которых – гиперхолестеринемия, повышенное артериальное давление, сахарный диабет и курение. Но именно гиперхолестеринемия выступает ключевым звеном патогенеза.
Липиды, которых следует бояться, это ЛПНП. В наше время точно установлено, что высокая концентрация ЛПНП прямо ассоциируется с развитием тяжелых кардиоваскулярных заболеваний. Более того, снижение ЛПНП уменьшает вероятность развития болезней системы кровообращения. В подтверждение этого профессор привел клинический случай 8-летней девочки из Саудовской Аравии с семейной гиперхолестеринемией (ХС на уровне 20 ммоль/л), у которой первый инфаркт миокарда случился в возрасте 6 лет, а к 8 годам она уже прошла аортокоронарное шунтирование. К сожалению, девочку спасти не удалось, хотя ее артериальное давление не было повышено, она не курила и не имела сахарного диабета. Этот случай подтверждает важность главного фактора кардиваскулярного риска – гиперхолестеринемии. Согласно данным программы ScreenPro FH, целью которой является установление количества лиц с семейной гиперхолестеринемией в странах Восточной Европы и некоторых других, на 440 млн населения 20 стран-участниц приходится 1-1,5 млн лиц с этим нарушением обмена ХС. Подробную информацию о работе этой программы можно найти на сайте www.screenprofh.com.
Гипохолестеринемическая диета оказывает благоприятное воздействие на уровень липидов крови, однако в реальных условиях придерживаться такой диеты на протяжении всей жизни крайне сложно или даже невозможно. Согласно рандомизированным клиническим исследованиям, снижение ЛПНП на 1 ммоль на протяжении 5 лет ведет к снижению кардиоваскулярного риска на четверть. Проспективные когортные исследования утверждают, что аналогичное снижение на протяжении 12 лет способно уменьшить риск примерно на 40%. Таким образом, более раннее начало и более интенсивный контроль липидного профиля крови способен обеспечить лучшие результаты.
Правило 5/6 гласит, что каждое удвоение дозы статина сопровождается дополнительным снижением ХС ЛПНП на 5-6%. Согласно подсчетам, при начале статинотерапии в возрасте 50 лет прием 80 мг аторвастатина обеспечивает дополнительное снижение ХС ЛПНП на 7,5 мг/дл по сравнению с дозой 40 мг и на 15 мг/дл – по сравнению с дозой 20 мг. Это, казалось бы, незначительное различие ведет к разнице в 3,4 года жизни без сердечно-сосудистого заболевания (66,6 против 70 лет). Таким образом, для пациентов высокого риска обязательна интенсивная статинотерапия.
В рандомизированном исследовании с участием 290 пациентов с инфарктом миокарда без элевации сегмента ST (NSTEMI) участники были разделены на группы аторвастатина 20 мг с повышением дозы для достижения ЛПНП <100 мг/дл и аторвастатина 80 мг. Через 12 мес наблюдения в первой группе (средняя дозировка аторвастатина 24,8 мг) уровень ХС ЛПНП составил 94±5 мг/дл, а во второй – 62±5 мг/дл. Эти уровни коррелировали с частотой сердечно-сосудистых событий: в группе 20 мг аторвастатина она была на уровне 26,7%, а в группе 80 мг – 16%, что почти в два раза меньше.
Профессор Lansberg подытожил, что: 1) повышение ЛПНП – главная причина сердечно-сосудистых катастроф; 2) целевые показатели ЛПНП должны быть максимально низкими; 3) следует применять высокие дозы высокоинтенсивных статинов; 4) необходимо как можно раньше начинать контроль факторов риска.
 Старший научный сотрудник отдела реанимации и интенсивной терапии ГУ «ННЦ «Институт кардиологии им. Н. Д. Стражеско» НАМН Украины, кандидат медицинских наук Ярослав Михайлович Лутай охарактеризовал ведение пациента с острым инфарктом миокарда от острого периода до вторичной профилактики.
Старший научный сотрудник отдела реанимации и интенсивной терапии ГУ «ННЦ «Институт кардиологии им. Н. Д. Стражеско» НАМН Украины, кандидат медицинских наук Ярослав Михайлович Лутай охарактеризовал ведение пациента с острым инфарктом миокарда от острого периода до вторичной профилактики.
Докладчик представил аудитории клинический случай пациента К., 68 лет, который был доставлен в отделение неотложной кардиологии через 6 ч после начала интенсивного ангинозного приступа с диагнозом острого коронарного синдрома с элевацией сегмента ST (артериальное давление 140/100 мм рт. ст., частота сердечных сокращений 82 уд./мин, сатурация кислорода 89%). В анамнезе артериальная гипертензия на протяжении 10 лет, не лечился; сахарный диабет, в течение 2 лет принимает метформин. ИБС в анамнезе нет. Несомненно, согласно Рекомендациям Европейского общества кардиологов по ведению пациентов со STEMI (2017), пациент нуждался в неотложном интервенционном вмешательстве. До проведения перкутанного коронарного вмешательства в соответствии с рекомендациями пациенту назначена оксигенотерапия (рекомендована при сатурации менее 90%) и фармакотерапия, включавшая ацетилсалициловую кислоту и тикагрелор в нагрузочных дозах, β-блокаторы, нефракционированный гепарин и опиоиды). В рекомендациях четко не указано, когда пациент должен получить первую дозу статинов, хотя предложено назначать статинотерапию как можно раньше. В данном случае больному было назначено 80 мг аторвастатина до реперфузионного вмешательства.
Эффективность аторвастатина в дозе 80 мг у больных с ОКС была доказана в ряде исследований (MIRACLE, PROVE-IT, SECURE PCI и др.). В более старых исследованиях статины начинали назначать не сразу после инфаркта: MIRACLE – на 3-й день, PROVE-IT – на 7-й. В наше время статины рекомендованы с первых суток заболевания. Действенность этой стратегии была подтверждена в регистрах NRMI‑4, Euro Heart Survey ACS (Fonarow G. C., 2005; Lenderink T., 2006). Недавнее исследование SECURE PCI предусматривало назначение высоких доз статинов до реперфузионного вмешательства пациентам с/без элевации сегмента ST (аторвастатин 80 мг с дальнейшим продолжением статинотерапии в дозе 40 мг/сут). В группе плацебо 80 мг аторвастатина до реваскуляризации и через 24 ч после нее не назначались, рекомендовалась только длительная статинотерапия в дозе 40 мг/сут. У пациентов со STEMI, подлежавших ангиопластике, была зафиксирована существенная разница в достижении комбинированной конечной точки (смерть/инфаркт/инсульт /незапланированная реваскуляризация) в течение 30 дней в зависимости от приема аторвастатина или плацебо. Среди лиц группы аторвастатина частота вышеперечисленных событий была практически в два раза ниже (Berwander O. et al., 2018).
Терапия статинами на ранних этапах ОКС ставит своей целью не снижение уровня проатерогенных липидов, а реализацию многих плейотропных эффектов этих медикаментов. Это приводит к снижению вероятности возникновения феномена no-reflow и развития постинфарктной дилатации левого желудочка, что было подтверждено в клинических исследованиях (Iwakura et al., 2006; Пархоменко А. Н. и соавт., 2018). Кроме того, назначение статинов (высокие дозы аторвастатина) предупреждает развитие контраст-индуцированной нефропатии, о чем уже говорилось ранее (Liu L. Y. et al., 2018).
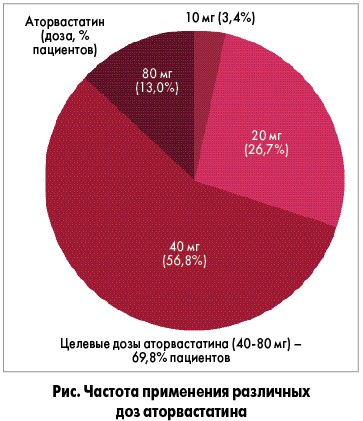 Отечественный регистр острого инфаркта миокарда (2015), включавший 505 больных с/без элевации сегмента ST, показал, что статины до события принимали 22,5% пациентов, в стационаре они были назначены 94,4% лиц. Наиболее часто рекомендовались аторва- и розувастатин (49,7 и 49,3% соответственно). В первые 24 часа после госпитализации статины назначались 69,43% пациентов, при выписке – 91%. Что касается режима дозировки, целевые дозы аторвастатина назначались лишь 69,8% больных, т. е. около трети пациентов регистра не получали достаточную дозу (рис.).
Отечественный регистр острого инфаркта миокарда (2015), включавший 505 больных с/без элевации сегмента ST, показал, что статины до события принимали 22,5% пациентов, в стационаре они были назначены 94,4% лиц. Наиболее часто рекомендовались аторва- и розувастатин (49,7 и 49,3% соответственно). В первые 24 часа после госпитализации статины назначались 69,43% пациентов, при выписке – 91%. Что касается режима дозировки, целевые дозы аторвастатина назначались лишь 69,8% больных, т. е. около трети пациентов регистра не получали достаточную дозу (рис.).
Согласно рекомендациям Европейского общества кардиологов, целевой уровень ХС ЛПНП у больных после перенесенного острого инфаркта миокарда составляет <1,8 ммоль/л (или снижение на 50% или более от исходного уровня, если он находится на уровне 1,8-3,5 ммоль/л). У пациентов с уровнем ХС ЛПНП ≥1,8 ммоль/л, несмотря на прием максимальных доз статинов, при наличии высокого риска необходимо рассмотреть терапию, направленную на дальнейшее снижение уровня ХС ЛПНП, например, добавление эзетимиба или блокаторов PCSK9 (алирокумаб).
Где же находится нижняя граница целевого уровня ХС ЛПНП? Оптимальный уровень, доказанный в исследованиях IMPROVE-IT и ODYSSEY OUTCOMES, составляет 1,4 ммоль/л. По мнению Ярослава Михайловича, целевой уровень ЛПНП скоро может быть пересмотрен и снижен.
Таким образом, статины рекомендованы всем пациентам с ОКС (без противопоказаний) независимо от уровня липидов. Преимущество следует отдавать интенсивной статинотерапии (аторвастатин 40-80 мг/сут, розувастатин 20-40 мг/сут). Особенно эффективны статины при назначении в течение первых часов после развития ОКС. Острые эффекты статинотерапии заключаются в предупреждении развития контраст-индуцированной нефропатии, перипроцедурного повреждения миокарда и феномена невосстановленного кровотока (no-reflow). В последующем длительная терапия с достижением целевых уровней ХС ЛПНП < 1,8 ммоль/л позволяет снизить частоту сердечно-сосудистых осложнений.
Подготовила Лариса Стрильчук
При поддержке Представительства «Пфайзер Экспорт Би. Ви.» в Украине.
PP-LIP-UKR‑0011
Медична газета «Здоров’я України 21 сторіччя» № 8 (429), квітень 2018 р.


