13 травня, 2018
Фиксированные комбинации в терапии глаукомы: ответы эксперта
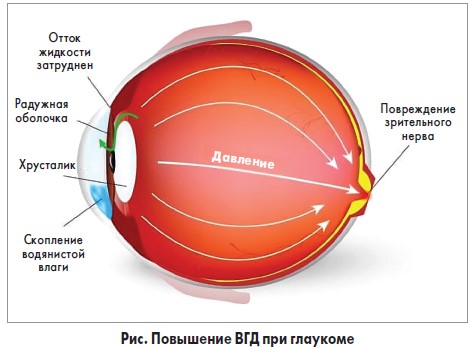
Глаукома представляет собой группу заболеваний органа зрения, характеризующуюся постоянным или периодическим повышением внутриглазного давления (ВГД), с последующим развитием типичных дефектов поля зрения, снижением остроты зрения и атрофией зрительного нерва (рис.). На вопросы редакции, посвященные современным подходам к лечению глаукомы, любезно согласился ответить заведующий кафедрой офтальмологии Харьковского национального медицинского университета, председатель Харьковского научного общества офтальмологов, член правления Украинского общества офтальмологов, член Европейского общества катарактальных и рефракционных хирургов (ERCRS) и Европейского общества ретинологов (Euroretina), доктор медицинских наук, профессор Павел Андреевич Бездетко.
 ? Павел Андреевич, расскажите, пожалуйста, об основных причинах развития глаукомы и о последствиях этого заболевания.
? Павел Андреевич, расскажите, пожалуйста, об основных причинах развития глаукомы и о последствиях этого заболевания.
– Первичная открытоугольная глаукома (ПОУГ) является крайне коварным заболеванием, которое зачастую заканчивается полной потерей зрения. Сегодня общее количество пациентов с глаукомой во всем мире составляет 60-100 млн. В структуре инвалидизации по причине нарушения зрительной функции на глаукому приходится до 15-20% случаев. Наиболее мощным фактором риска глаукомы является генетическая предрасположенность. Так, до 30% пациентов с ПОУГ имеют семейный анамнез по данной патологии. Заболевание в 6 раз чаще наследуется по материнской линии. Существуют также и другие предрасполагающие факторы, которые способствуют повреждению сетчатки и зрительного нерва: артериальная гипертензия / гипотензия, сахарный диабет, заболевания эндокринной системы. Остеохондроз шейного отдела позвоночника тоже является фактором, повышающим риск развития ПОУГ, поскольку обусловливает нарушение функции симпатических нервов и ухудшение кровотока в вертебро-базилярном бассейне. Принято считать, что ПОУГ имеет многофакторную этиологию, но именно генетический фактор является предопределяющим.
 ? Каковы патогенетические механизмы развития глаукомы?
? Каковы патогенетические механизмы развития глаукомы?
– Глаукома характеризуется патологической дегенерацией ганглиозных клеток сетчатки, структурными повреждениями в головке зрительного нерва. В результате гибели нейронов при глаукоме возникают дефект слоя нервных волокон сетчатки, истончение нейроретинального ободка с экскавацией диска зрительного нерва (ДЗН) и необратимой потерей его волокон. Дегенерация нейронов при глаукоме не ограничивается сетчаткой, изменяются также нейроны латерального коленчатого тела и зрительной коры. Патологические явления усугубляются изменениями окружающих тканей, что вызвано активацией глиальных клеток, прежде всего астроцитов. Они начинают вырабатывать различные патологические субстанции, например эндотелин, суживающий сосуды, а также матриксные металлопротеиназы, что приводит к исчезновению последнего и замещению его другим субстратом. Это явление получило название «ремоделирование тканей». Именно данный процесс лежит в основе изменений решетчатой мембраны склеры при глаукоме, а также в основе самой сути глаукомного поражения – формирования глаукомной экскавации ДЗН. Кроме того, активированные астроциты продуцируют синтаз оксида азота (NO) и тем самым секретируют NO, который легко диффундирует в окружающие ткани, включая аксоны. При одновременном усилении образования кислорода в аксонах создаются условия для синтеза достаточно агрессивной молекулы – пероксинитрита, который проникает через аксоны вглубь сетчатки, провоцируя гибель ганглиозных клеток сетчатки. А распространение пероксинитрита по направлению к мозгу приводит к потере клеток в наружных коленчатых телах.
Глаукомное поражение является следствием умеренной, но рецидивирующей реперфузии (восстановление кровообращения после его снижения в результате колебаний офтальмотонуса), что ассоциируется с усилением окислительного стресса и повышением уровня свободных радикалов, в частности супероксида. Наиболее ранние патологические изменения при глаукоме проявляются структурным повреждением митохондрий и гибелью клеток.
? Наблюдается ли рост заболеваемости глаукомой среди населения Украины?
– Основной массив статистических данных по глаукоме связан с высокой частотой инвалидизации по причине нарушения зрительной функции. В Украине доля инвалидизаций, обусловленных глаукомой, составляет около 20%. Существует также официальная статистика заболеваемости глаукомой в Украине, согласно которой за период с 2000-го по 2010 год количество случаев этой патологии во взрослой популяции возросло с 351 до 599 на 100 тыс. человек. Таким образом, только за первое десятилетие XXI века заболеваемость глаукомой в нашей стране возросла на 41%.
? Расскажите, пожалуйста, о современных подходах к лечению и профилактике данной патологии.
– На сегодняшний день рекомендации профильных офтальмологических ассоциаций США и ЕС совпадают в большинстве основных аспектов. Национальные рекомендации по лечению глаукомы также соответствуют принятым в мире, поскольку в Украине используются такие же методы диагностики и прогностические маркеры заболевания. Безусловно, главная задача терапии глаукомы – сохранение функции зрения. Основным методом, позволяющим эту задачу выполнить, является контроль ВГД. Алгоритмы лечения ПОУГ включают целевое снижение ВГД. В зависимости от стадии заболевания необходимая степень снижения ВГД может составлять от 20 до 40%. Первоначально после диагностирования ПОУГ прибегают к медикаментозным методам лечения, позволяющим снизить ВГД. Если медикаментозная терапия оказывается не эффективной, то пациенту назначают лазерные методы лечения. Если и они не позволяют добиться необходимого снижения ВГД, то пациенту показано проведение хирургического лечения.
? Какими критериями следует руководствоваться практикующему врачу при выборе препарата для лечения глаукомы? Какое влияние оказывают особенности анамнеза пациента на этот выбор?
– К главным требованиям, предъявляемым медикаментозной терапии ПОУГ, относятся способность нормализовать ВГД и обеспечивать его стабильность, т. е. не допускать суточных колебаний данного показателя, поскольку именно это позволяет сохранить зрение пациента. Следовательно, основным критерием выбора средства является не только эффективность конкретного препарата, но и фактор приверженности пациента к назначенной терапии, особенно учитывая тот факт, что пациенты с ПОУГ должны получать продолжительное, зачастую пожизненное лечение. Естественно, препарат выбора также должен обладать хорошим профилем переносимости, не приводить к развитию серьезных местных и системных побочных эффектов. Учитывая фактор комплайенса, ключевое значение в терапии ПОУГ приобретает удобство схемы приема препарата. Назначение минимально возможного количества использований препарата в сутки (<2) позволяет достичь наиболее высокого уровня приверженности и таким образом защитить пациента от потери зрения в долгосрочной перспективе. Кроме того, препарат выбора, особенно если речь идет о топической терапии, должен препятствовать прогрессированию поражения зрительного нерва при глаукоме. Следовательно, в терапию первой линии при ПОУГ входят препараты, позволяющие эффективно и стабильно снижать ВГД при минимальной кратности приема в сутки, а также обладающие нейропротекторными свойствами. При назначении терапии очень важно также учитывать анамнез пациента, поскольку коморбидные состояния, например кардиоваскулярная патология, могут не только повышать риск развития глаукомы, но и становиться противопоказанием к назначению некоторых противоглаукомных препаратов.
? Разработка и применение фиксированных комбинаций позволяют значительно увеличить эффективность лечения различных системных заболеваний. Каковы преимущества использования фиксированных комбинаций у пациентов с глаукомой?
– Как уже было сказано, ключевую роль в терапии ПОУГ играет нормализация ВГД. При подозрении на наличие глаукомы у пациента либо на начальной стадии этого заболевания достаточным является применение лекарственных средств, которые позволяют снизить ВГД на 20-30%. Прогрессирующие стадии глаукомы требуют снижения ВГД уже около 40%. К сожалению, использование монотерапии препаратами группы ингибиторов карбоангидразы или бета-блокаторов не позволяет достичь снижения ВГД более чем на 30% и не будет эффективным у пациентов с более развитой стадией глаукомы. Комбинированное лечение с использованием разных лекарственных средств позволяет добиться необходимого гипотензивного эффекта, однако такой подход имеет существенные недостатки, поскольку приводит к повышению кратности использования препаратов до 3 и более раз в сутки, что крайне негативно сказывается на приверженности к лечению.
В условиях высокого темпа жизни пациенты склонны пропускать использование препарата, а это, в свою очередь, приводит к значительным колебаниям ВГД в течение суток и существенно повышает риск потери зрения. Именно в такой ситуации оптимальным решением является применение фиксированных комбинаций. Сочетание двух действующих веществ в одном флаконе позволяет снизить необходимое количество инстилляций в сутки до 1-2 раз, что значительно повышает приверженность к лечению.
Таким образом, применение фиксированных комбинаций обеспечивает более выраженное снижение ВГД по сравнению с монотерапией и способствует приверженности пациента к назначенной схеме лечения. Важно также отметить, что только в том случае, когда пациент четко придерживается схемы лечения, у врача есть возможность объективного контроля эффективности терапии.
? Какие компоненты фиксированных комбинаций наиболее широко применяются в настоящее время?
– До 60-70% офтальмологов начинают лечить глаукому с назначения бета-блокатора. Одним из наиболее широко используемых препаратов данной группы является тимолол, его начали применять в клинической практике еще с 60-х годов ХХ века. К преимуществам тимолола относятся высокая доступность для пациентов и эффективное снижение ВГД. Однако для тимолола характерны недостатки, связанные с воздействием на сердечно-сосудистую и дыхательную системы. Тем не менее тимолол чаще всего включают в фиксированные комбинации для лечения глаукомы.
Ингибитор карбоангидразы дорзоламид, напротив, является относительно новым средством, которое начали применять в терапии глаукомы только в конце 90-х годов прошлого века. Препарат обладает достаточно высокой эффективностью в снижении ВГД (до 25-30%) и блокирует выработку водянистой влаги. Кроме эффективного снижения ВГД, дорзоламид также оказывает положительное действие на кровоток в области зрительного нерва, проявляет выраженные антиоксидантные и противоотечные свойства. Благодаря перечисленным эффектам применение тимолола в комбинации с дорзоламидом позволяет достичь комплексного воздействия на патогенетические механизмы глаукомы и более эффективно снижать ВГД по сравнению с монотерапией тимололом.
Украинская фармацевтическая компания «Киевский витаминный завод» выпустила новый комбинированный препарат Дорзитим® (дорзоламид/тимолол). Препарат выпускается во флаконах для проведения инстилляций в конъюнктивальный мешок. Дорзитим® назначают по 1 капле 2 раза в сутки. Дозировка тимолола и дорзоламида в Дорзитиме составляет 5 и 20 мг/л соответственно. Препарат обладает преимуществами комбинированного использования тимолола и дорзоламида, включая эффективное снижение ВГД, нейропротекторный, антиоксидантный и противоотечный эффекты, а также позволяет достичь высокого комплайенса за счет удобной схемы применения.
! Важно отметить, что фиксированная комбинация бета-блокатора и ингибитора карбоангидразы Дорзитим® на сегодняшний день имеет наиболее мощную доказательную базу среди препаратов, применяющихся для снижения ВГД у пациентов с глаукомой. Многоцентровыми исследованиями было обосновано, что эта комбинация улучшает кровоток в области зрительного нерва, обладает выраженным антиоксидантным воздействием. Комбинированное использование дорзоламида и тимолола обеспечивает снижение ВГД на 37%, а также обладает дополнительным нейропротекторным эффектом, не увеличивая при этом системные эффекты тимолола. С точки зрения воздействия на различные патогенетические механизмы развития глаукомы (повышение ВГД, оксидативный стресс, нарушение трофики зрительного нерва) более выгодной фиксированной комбинации для лечения глаукомы в настоящее время не существует.
Подготовил Игорь Кравченко
Медична газета «Здоров’я України 21 сторіччя» № 8 (429), квітень 2018 р.


