28 травня, 2018
Антибиотикорезистентность, исследование SOAR и Украина: какой путь выбрать?

Меньше века прошло с момента открытия и начала повсеместного использования антибактериальных средств, меньше века понадобилось для того, чтобы человечество привыкло к благам антибиотикотерапии и столкнулось с реальной угрозой глобальной антибиотикорезистентности (АБР). Каждый практикующий врач, подбирая и назначая антибактериальную терапию (АБТ), уже отчетливо ощущает дыхание АБР за своей спиной: специалистам приходится задумываться, какой препарат будет эффективен относительно вероятного возбудителя – антибиотик (АБ) выбора, второй линии или резерва?
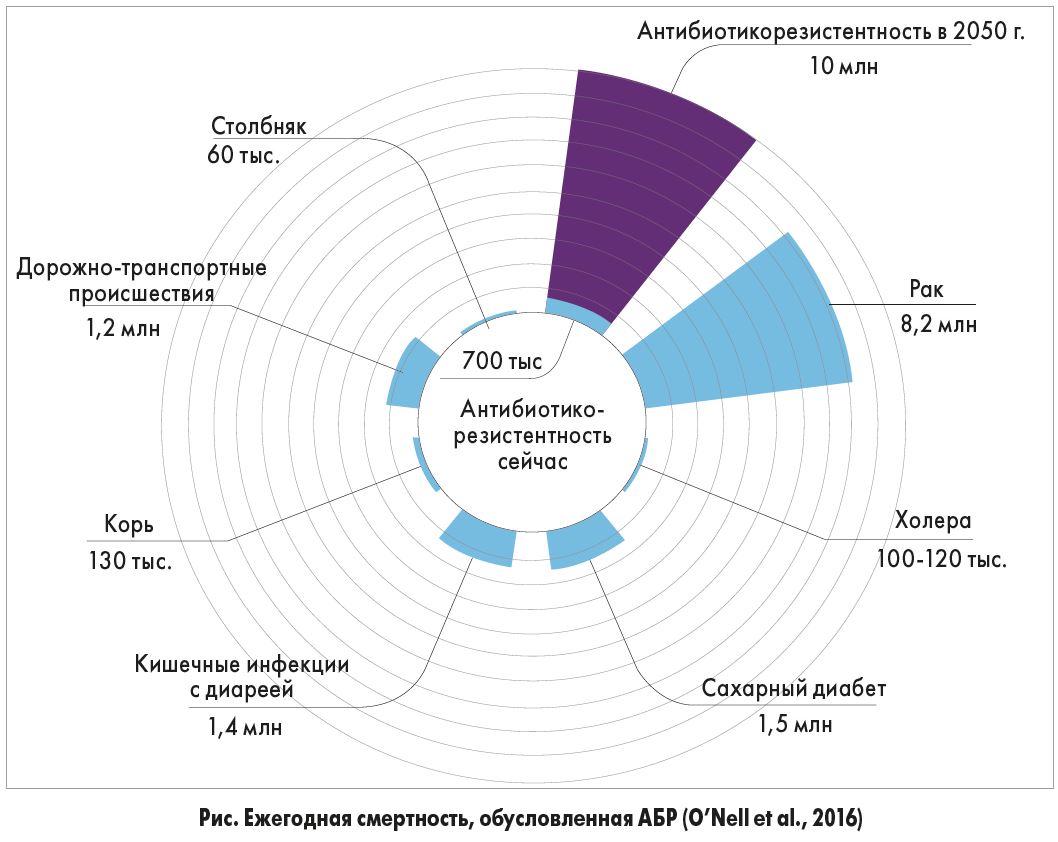 Эксперты мирового уровня и ведущие отечественные специалисты рисуют мрачные картины грядущего постантибиотического апокалипсиса: инфекционные заболевания, вырвавшись из-под контроля АБ, снова будут уносить миллионы жизней, практически все хирургические вмешательства станут невозможными, канут в Лету химиотерапия и трансплантация органов, ведь их проведение, безопасность и эффективность во многом определяются результативностью противомикробной профилактики. Остатки оптимизма медленно, но верно тают после ознакомления с результатами британского исследования Review on Antimicrobial Resistance (RAR, 2016). «Согласно прогнозируемому росту резистентности основных 6 патогенов к 2050 г., мы предположили, что если никакие меры не будут приняты, то смертность от АБР в 2050 г. возрастет до 10 млн жизней ежегодно, а совокупные затраты всемирной экономики превысят 100 трлн долларов США. В 2050 г. число погибших может стать ошеломляющим: 1 человек каждые 3 секунды вместо сегодняшнего уровня – 1 человек в сутки в мире», – подчеркивают в отчете авторы RAR. При этом смертность от АБР будет настолько велика, что значительно опередит смертность от «болезней XXI века»: онкологической патологии, сахарного диабета (рис.).
Эксперты мирового уровня и ведущие отечественные специалисты рисуют мрачные картины грядущего постантибиотического апокалипсиса: инфекционные заболевания, вырвавшись из-под контроля АБ, снова будут уносить миллионы жизней, практически все хирургические вмешательства станут невозможными, канут в Лету химиотерапия и трансплантация органов, ведь их проведение, безопасность и эффективность во многом определяются результативностью противомикробной профилактики. Остатки оптимизма медленно, но верно тают после ознакомления с результатами британского исследования Review on Antimicrobial Resistance (RAR, 2016). «Согласно прогнозируемому росту резистентности основных 6 патогенов к 2050 г., мы предположили, что если никакие меры не будут приняты, то смертность от АБР в 2050 г. возрастет до 10 млн жизней ежегодно, а совокупные затраты всемирной экономики превысят 100 трлн долларов США. В 2050 г. число погибших может стать ошеломляющим: 1 человек каждые 3 секунды вместо сегодняшнего уровня – 1 человек в сутки в мире», – подчеркивают в отчете авторы RAR. При этом смертность от АБР будет настолько велика, что значительно опередит смертность от «болезней XXI века»: онкологической патологии, сахарного диабета (рис.).
«Если мы не начнем действовать, то столкнемся почти с немыслимым сценарием, когда АБ перестанут работать, а мы вернемся в темные века медицины», – сказал Дэвид Кэмерон, действующий на тот момент премьер-министр Великобритании, ознакомившись с результатами проекта RAR. Одним из эффективных способов борьбы с АБР, по мнению британских исследователей, является усиление контроля над применением АБ у людей и животных, а также тщательное наблюдение за уровнем АБР в мире.
Эксперты Всемирной организации здравоохранения (ВОЗ) тоже обеспокоены растущей АБР. В самом начале 2018 г. эта авторитетная организация представила обновленные данные Глобальной системы по надзору за устойчивостью к антибактериальным препаратам (Global Antimicrobial Surveillance System, GLASS), согласно которой 500 тыс. человек с подозрением на бактериальную инфекцию из 22 стран мира уже столкнулись с АБР. Более того, специалисты ВОЗ, представив в 2017 г. перечень 10 лидирующих причин смерти в мире, назвали самую смертоносную инфекционную болезнь: сомнительную пальму первенства получили инфекционные заболевания нижних дыхательных путей (НДП), от которых в 2015 г. скончались 3,2 млн человек. Примечательно, что высокая смертность от этих нозологий не является уделом стран с низким уровнем экономики: инфекции НДП признаны ведущими причинами смерти в государствах как с высоким, так и с низким уровнем доходов. Даже в Европе, где летальность, обусловленная инфекционными заболеваниями, значительно ниже, чем в других регионах, инфекции НДП прочно удерживают 6-е место в общей структуре причин смерти. В списке самых распространенных и наиболее резистентных бактерий оказался стрептококк – Streptococcus pneumoniae, возбудитель пневмонии, одной из коварнейших патологий, входящих в группу инфекционных заболеваний НДП. Именно внебольничная пневмония (ВБП) является наиболее частым поводом назначения антибактериальных средств, а также наиболее вероятной причиной формирования АБР. «Наибольшую обеспокоенность вызывает тот факт, что патогены не признают государственных границ. Поэтому ВОЗ призывает все страны создавать эффективные системы эпиднадзора для выявления АБР», – отметил Марк Спренгер, руководитель департамента ВОЗ по борьбе с АБР.
Исследование SOAR
Одним из глобальных эпидемиологических исследований, охватившим практически все регионы мира, является проект SOAR (Survey of Antibiotic Resistance), в рамках которого проводится изучение АБР самых значимых патогенов, вызывающих внебольничные инфекции дыхательных путей, – S. pneumoniae и Haemophilus influenzae. Исследование SOAR стартовало в 2002 г., еще до публикации рекомендаций ВОЗ и результатов исследования RAR, и продолжается по настоящее время, в его реализации принимают активное участие страны Ближнего Востока, Африки, Латинской Америки, Азиатско-Тихоокеанского региона и Содружества Независимых Государств; Украина принимает участие в исследовании SOAR с 2011 г. SOAR – это одно из первых крупнейших эпидемиологических исследований, которое уже неоднократно представляло данные об АБР в мире. В начале этого года на страницах авторитетного медицинского издания Journal of Antimicrobial Chemotherapy (Великобритания) опубликован очередной отчет SOAR по уровню АБР в различных странах на протяжении 2014-2016 гг., одна из глав данного доклада посвящена рассмотрению проблемы АБР в двух соседних государствах – Украине и Словацкой республике (СР).
SOAR: Украина vs Словакия
Казалось бы, в двух близлежащих географических регионах показатели АБР должны быть практически одинаковыми, однако ситуация в этих государствах отличалась. Но обо всем по порядку. В нашей стране в проекте SOAR приняли участие два крупных центра: диагностический центр медицинской академии (г. Днепр) и Национальный институт фтизиатрии и пульмонологии (г. Киев), а в СР – госпиталь (г. Нитра). Все штаммы H. influenzae и S. pneumoniae, выделенные у больных инфекционными заболеваниями НДП, отправляли в центральную лабораторию (Международная ассоциация здравоохранения, Inc., Швейцария), где их повторно идентифицировали с использованием самых современных методик. Одинаковые штаммы, полученные от одного и того же пациента, исключали из анализа.
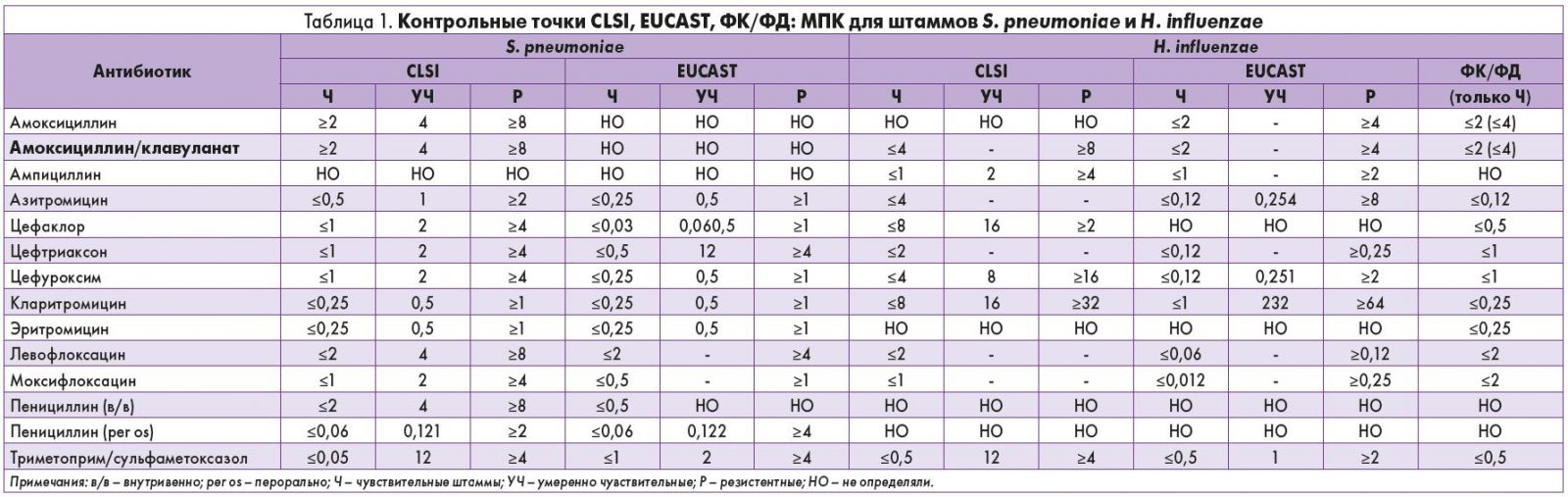
Определение чувствительности проводилось при использовании 3 различных контрольных точек: CLSI, EUCAST и фармакокинетики/фармакодинамики (ФК/ФД). CLSI разработаны Институтом клинических и лабораторных стандартов (Clinical and Laboratory Standards Institute, USA), EUCAST – Европейским комитетом по тестированию чувствительности к антимикробным препаратам; критерии ФК/ФД учитывают уровень концентрации лекарственного вещества в очаге инфекции. В стандартах CLSI, EUCAST, а также ФК/ФД приводятся пограничные значения минимальных подавляющих концентраций (МПК) и диаметров зон подавления роста для каждого микроорганизма, на основании которых определяют чувствительность к выбранному АБ (табл. 1). Данная мера позволила авторам проекта SOAR получить полную картину о распространенности АБР исследуемых штаммов в Украине и СР.
Все выделенные патогены исследовали на чувствительность к амоксициллину, амоксициллину/клавуланату (2:1), азитромицину, цефаклору, цефтриаксону, цефуроксиму, кларитромицину, эритромицину, левофлоксацину, моксифлоксацину и триметоприму/сульфаметоксазолу (1:19). Штаммы S. pneumoniae также тестировали на чувствительность к пенициллину, штаммы H. influenzae дополнительно исследовали на чувствительность к ампициллину. Также чувствительность выделенных патогенов сравнивали в зависимости от возраста пациентов, источника локализации возбудителя и чувствительности к пенициллину (только для S. pneumoniae).
И вот они, результаты!
На протяжении двух лет (2014-2016) в двух украинских и одном словацком центрах выделено 195 штаммов S. pneumoniae. Наибольшее количество штаммов идентифицировали в образцах мокроты (n=60; 30,8%) и жидкости, полученной при проведении бронхоальвеолярного лаважа (n=56; 28,7%). Реже возбудителей выявляли в экссудате из синусов (n=35; 17,9%), среднего уха (n=20; 10,3%), эндотрахеальном аспирате (n=5; 2,6%) и крови (n=3; 1,5%); 16 штаммов получили из неидентифицированных респираторных источников. Большинство образцов (n=98; 50,3%) выделили у взрослых пациентов (13-64 лет), 69 (35,4%) штаммов получили у детей (≤12 лет) и 28 (14,4%) штаммов – у пожилых больных (≥65 лет).
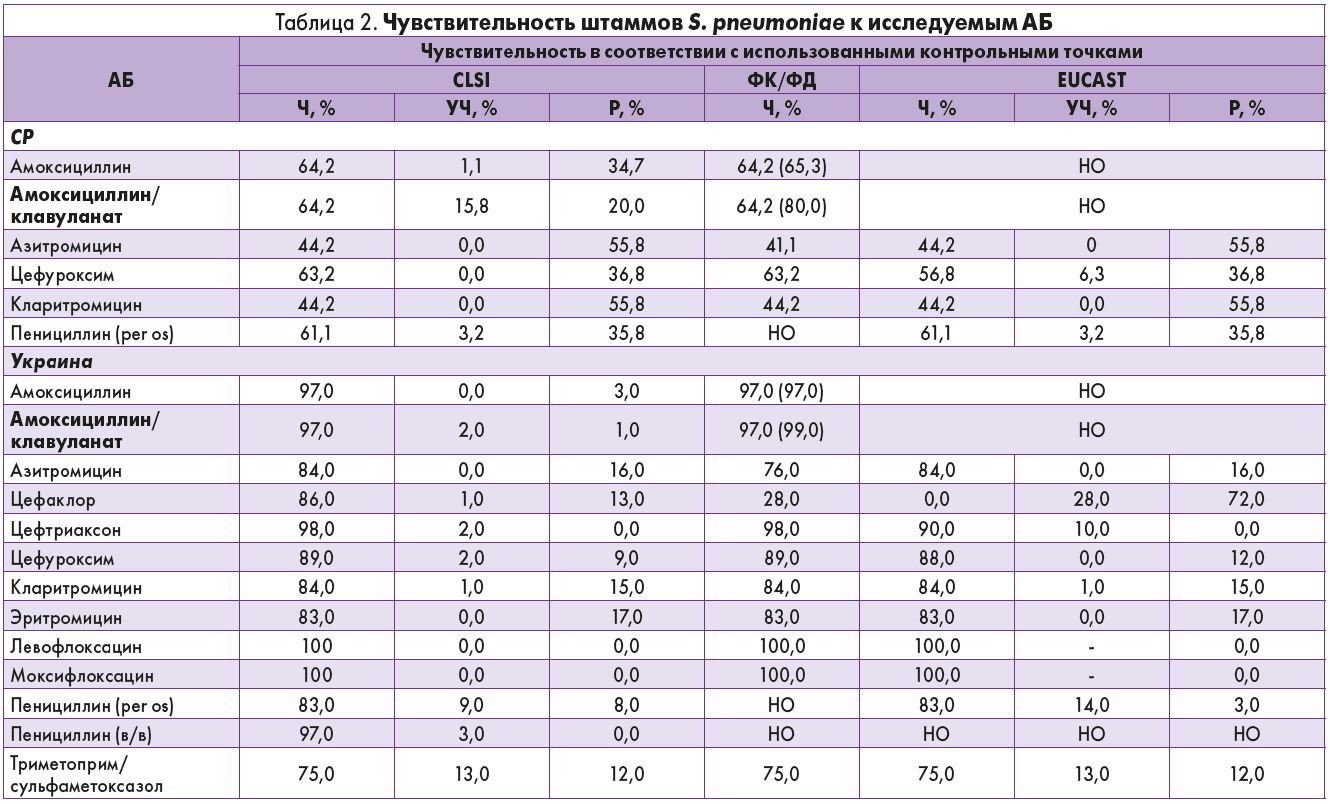
Сравнив чувствительность всех 195 штаммов S. pneumoniae в обеих странах, исследователи установили, что штаммы, выделенные в Украине, оказались более чувствительными к амоксициллину/клавуланату (табл. 2), для подавления их жизнедеятельности требовались меньшие МПК.
Среди всех штаммов S. pneumoniae, выделенных в Украине, 97% оказались чувствительными к пенициллину в соответствии с контрольными точками CLSI для внутривенного (в/в) пенициллина, при этом только 83% штаммов являлись чувствительными к пенициллину по критериям EUCAST и CLSI для перорального пенициллина. Все выделенные штаммы признаны чувствительными к респираторным фторхинолонам (левофлоксацину и моксифлоксацину) вне зависимости от использованных стандартов. Чувствительность к цефтриаксону в соответствии с контрольными точками CLSI и ФК/ФД составила 98%, и 90% в соответствии с контрольными точками EUCAST.
Чувствительность к амоксициллину и амоксициллину/клавуланату оставалась достаточно устойчивой, в соответствии с контрольными точками CLSI и ФК/ФД для низких доз она составила 97%; по критериям ФК/ФД для высоких доз чувствительность к амоксициллину сохранялась на прежнем уровне (97%), тогда как к амоксициллину/клавуланату – выросла до 99%. Чувствительность к пероральным цефалоспоринам и макролидам по критериям CLSI варьировала в пределах от 83% (для эритромицина) до 89% (для цефуроксима). Чувствительность к триметоприму/сульфаметоксазолу составила 75% в соответствии со всеми контрольными точками. Чувствительность к цефаклору в соответствии с контрольными точками CLSI составила 86%; 28,0% – ФК/ФД, и 0% – EUCAST.
Интересные данные получены при анализе чувствительности к АБ, определенной при помощи критериев CLSI, в зависимости от источника локализации возбудителя и возраста пациентов. Из 27 штаммов S. pneumoniae, выделенных в педиатрической популяции, только 70,4% были чувствительными ко всем трем макролидам, тогда как во взрослой популяции из 65 штаммов – 89,2% (р=0,03). Схожая ситуация отмечена с цефаклором: 70,4% штаммов S. pneumoniae, полученных у педиатрических пациентов, и 90,8% штаммов, полученных у взрослых, были чувствительны к данному антибактериальному препарату.
Среди всех 195 штаммов S. pneumoniae, выделенных в Украине и СР, 141 (72,3%) штамм оказался чувствительным к пенициллину (ЧП), 12 (6,2%) изолятов были умерено чувствительны (УЧП), а 42 (21,5%) штамма являлись резистентными к пенициллину (РП) в соответствии с контрольными точками CLSI для перорального пенициллина. Как ЧП-, так и РП-штаммы в Украине и СР имели практически одинаковую чувствительность к АБ. ЧПштаммы проявляли наибольшую чувствительность к фторхинолонам, амоксициллину, амоксициллину/клавуланату, цефуроксиму и цефтриаксону (100% по критериям CLSI), этот показатель был несколько ниже для цефаклора (97,9%), а для триметоприма/сульфаметоксазола и макролидов был ниже – 90,8 и 80,9% соответственно. При изучении чувствительности РП-штаммов оказалось, что фторхинолоны являются 100% активными в отношении этих штаммов, тогда как чувствительность к другим препаратам колебалась в пределах 0-12% для всех использованных АБ по сравнению с ЧП-штаммами (р<0,0001). Исключением из этого списка стал цефтриаксон: всего 54,8% РП-штаммов были чувствительны к этому препарату.
На протяжении двух лет (2014-2016) в обеих странах выделили 194 штамма H. influenzae. Очагами локализации возбудителя являлись мокрота (n=91; 46,9%), экссудат синусов (n=43; 22,2%), жидкость, полученная при проведении бронхоальвеолярного лаважа (n=30; 15,5%), эндотрахеальный аспират (n=14; 7,2%), экссудат среднего уха (n=10; 5,2%); 6 штаммов (3,1%) получили из неустановленных респираторных источников. Большинство штаммов (n=116; 59,8%) выделили у взрослых пациентов, 52 (26,8%) штамма – у детей и 26 (13,4%) – у пожилых больных. В Украине чаще идентифицировали штаммы, продуцирующие β-лактамазу, – 7,3% (7/96), тогда как в СР этот показатель был несколько ниже – 5,1% (5/98). Как в нашей стране, так и в СР выделены BLNAR-штаммы, которые, по рекомендациям CLSI, следует расценивать как резистентные к амоксициллину/клавуланату, цефуроксиму и цефаклору, даже если они проявляют чувствительность к этим АБ в условиях in vitro. В соответствии с контрольными точками CLSI (МПК ампициллина ≥4 мг/л), BLNAR-штаммами признано 6 штаммов, выделенных в СР, и 1 штамм, полученный в Украине, тогда как по стандартам EUCAST к BLNAR-штаммам отнесены 8,2% (n=8) образцов из СР и 1,0% (n=1) изолятов из Украины (МПК ампициллина ≥2 мг/л).
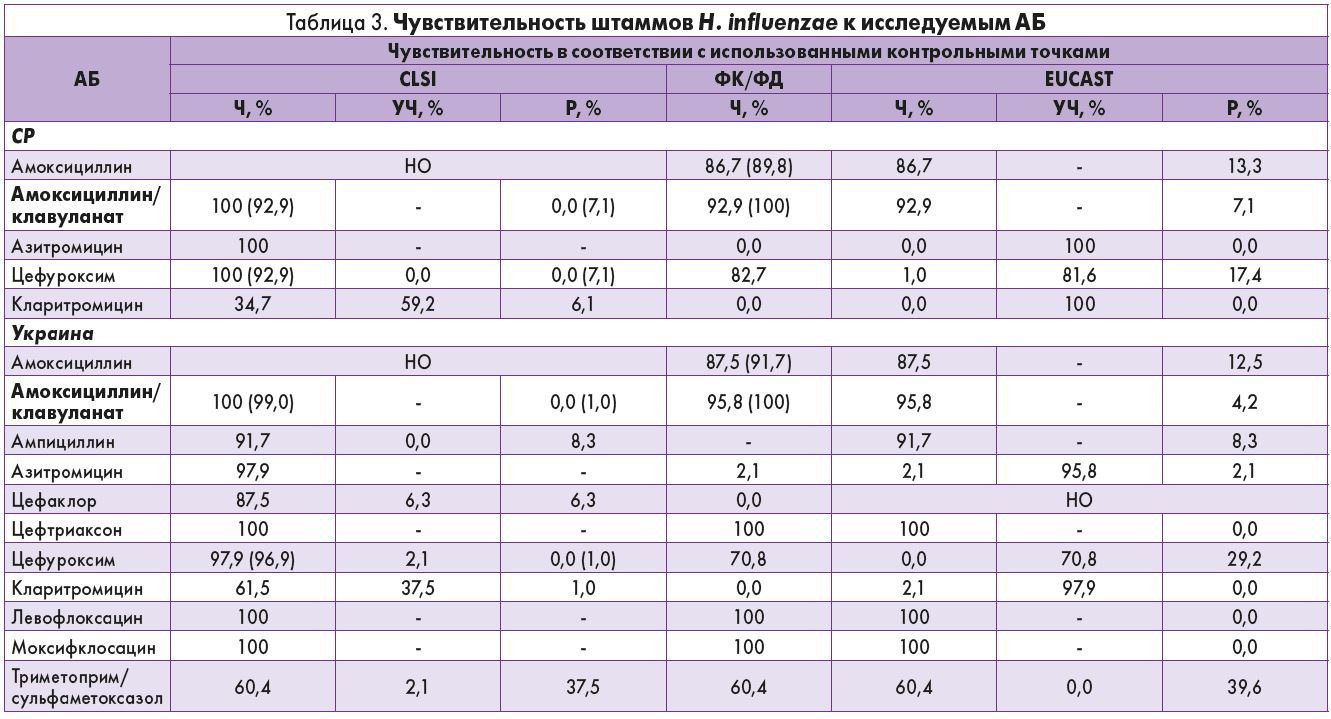
Анализ чувствительности всех штаммов H. influenzae, выделенных в обеих странах, показал, что штаммы, происходящие из Украины, более чувствительны к амоксициллину/клавуланату (табл. 3) и для подавления их жизнедеятельности требовались меньшие МПК.
Интересно, что после внесения корректив с учетом BLNAR-штаммов доля чувствительных к амоксициллину/клавуланату штаммов H. influenzae в СР снизилась со 100 до 92,9% (в соответствие с контрольными точками EUCAST и ФК/ФД для низких доз), к цефуроксиму – со 100 до 92,9%, а к цефаклору – с 89,8 до 86,7%. При этом чувствительность штаммов H. influenzae в СР не зависела от источника локализации возбудителя и возраста пациентов.
В Украине изначальная чувствительность к амоксициллину/клавуланату оценивалась в 100% (в соответствии с контрольными точками CLSI и ФК/ФД для высоких доз), после введения поправки на наличие одного BLNAR-штамма она также снизилась, но менее значимо: до 99,0% в соответствии с контрольными точками CLSI и до 95,8% EUCAST и ФК/ФД для низких доз.
Подобная картина зафиксирована в отношении цефуроксима: после внесения корректив с учетом BLNAR-штамма чувствительность к этому АБ снизилась с 97,9% до 96,9% (в соответствии с контрольными точками CLSI), тогда как при использовании других контрольных точек зафиксировано более значимое снижение чувствительности к цефуроксиму: 70,8% – ФК/ФД и 0% – EUCAST. Подобные существенные отличия имели место при использовании кларитромицина: в соответствии с контрольными точками CLSI эффективность этого АБ составила 61,5%; ФК/ФД – 0%; EUCAST – 2,1%. Чувствительность к триметоприму/сульфаметоксазолу также была невысокой – 60,4% (в соответствии со всеми контрольными точками).
Антибиотикорезистентность: две стороны одной медали
Украина и Словакия, два близлежащих географических региона, два государства, имеющие общие границы, столкнулись с одинаковой проблемой – АБР к наиболее распространенным возбудителям внебольничных инфекций дыхательных путей, однако оказались в совершенно разных условиях, более или менее благоприятных. Результаты исследования SOAR, проведенного в этих странах, свидетельствуют о высокой вариабельности чувствительности штаммов S. pneumoniae к АБ. Штаммы пневмококков, выделенные в Украине (n=100), оказались более чувствительны к АБ по сравнению со штаммами, выделенными в СР: чувствительность ко всем изучавшимся препаратам превысила ≥97%, за исключением перорального пенициллина, макролидов и цефаклора (чувствительность к этим АБ была значительно ниже и варьировала в пределах 83-86%), цефуроксима (89%) и триметоприма/сульфаметоксазола (75%). В СР фторхинолоны демонстрировали 100% эффективность в отношении S. pneumoniae в соответствии со всеми контрольными точками, а цефтриаксон в соответствии с контрольными точками CLSI – 82,1%. Остальные препараты: пенициллин (per os и в/в), амоксициллин, амоксициллин/клавуланат, цефаклор, цефуроксим и триметоприм/сульфаметоксазол – продемонстрировали меньшую активность (58-64%), а макролиды – только 44%. Штаммы S. pneumoniae, выделенные в Украине, оказались достоверно более чувствительными (в соответствии с контрольными точками CLSI) к пенициллину (в/в), амоксициллину, амоксициллину/клавуланату, цефуроксиму, цефаклору, макролидам (р<0,0001), цефтриаксону (р=0,002) и пероральному пенициллину (р=0,001) по сравнению со штаммами, выделенными в СР.
К сожалению, достоверных сведений об уровне АБР в Украине и СР относительно немного. Наиболее актуальные из них получены в рамках программы EARS-Net, однако участие в ней приняла только СР; еще одним недостатком указанного исследования является изучение АБР исключительно инвазивных штаммов, выделенных из крови и спинномозговой жидкости. Тем не менее, по данным EARS-Net, в 2015 г. 22,2% штаммов, выделенных в СР, оказались нечувствительными к пенициллину, что соответствует данным, полученным в обновленном проекте SOAR, – 38,9% (резистентных штаммов). Интересно, что высокий уровень АБР штаммов S. pneumoniae, выделенных в СР, зафиксирован еще 15 лет назад в работах Marchese и Schito: по данным Alexander Project (1997), резистентность к пенициллину составила 26,7%, к макролидам – 13,3%. Riedel и соавт. также отметили высокий уровень резистентности к пенициллину (52,3%) и эритромицину (36,4%) среди штаммов, выделенных при внебольничных инфекциях НДП в СР на протяжении 2004-2005 гг. В этой работе подчеркивается, что в 1998-2004 гг. СР занимала третье место по частоте применения АБ среди 15 европейских стран; тем самым предоставляются доказательства наличия взаимосвязи между уровнем АБР и высокой частотой применения АБ. В другом недавнем исследовании, в котором изучалась частота использования АБ в Европейском регионе в 2011 г., СР также заняла достаточно высокое место (15-е среди 42 стран) по общей частоте использования АБ.
К сожалению, Украина не принимала участия ни в одном из этих исследований, поэтому трудно судить об истинной частоте назначения АБ и распространенности АБР, однако для сравнения можно использовать данные, полученные ранее в рамках проекта SOAR – в 2011-2013 гг. Чувствительность штаммов S. pneumoniae, выделенных в 2014-2016 гг., оказалась сопоставимой с таковой, зафиксированной в 2011-2013 гг., с небольшим (25%) снижением для большинства АБ. Например, в 2011-2013 гг. чувствительность к амоксициллину/клавуланату в соответствии с контрольными точками CLSI составила 100%, в 2014-2016 гг. – 97%; к пероральному пенициллину – 87,3 и 83,0% соответственно. Исключение составил триметоприм/сульфаметоксазол, чувствительность к которому в 2011-2013 гг. была очень низкой (9,7%), но в настоящем исследовании (2014-2016) этот показатель возрос до 75%. Предположительно, такой рост чувствительности к данному АБ связывают с достаточно редким использованием триметоприма/сульфаметоксазола для лечения внебольничных инфекций дыхательных путей в Украине.
В отличие от S. pneumoniae антимикробная активность в отношении H. influenzae оказалась довольно однородной в обеих странах. Чувствительность к амоксициллину/клавуланату, цефтриаксону, цефуроксиму, азитромицину и фторхинолонам превысила 90% по критериям CLSI. Примечательно, что также в обеих странах чувствительность к кларитромицину оказалась менее значимой и более вариабельной (35% в СР и 61,5% в Украине), аналогичная ситуация зафиксирована в отношении триметоприма/сульфаметоксазола (77,6% в СР и 60,4% в Украине). В СР резистентность к ампициллину составила 12,2%, при этом частота выявления штаммов, продуцирующих β-лактамазу, оказалась равна 5,1%, а обнаружения BLNAR-штаммов – 7,1%. Резистентность к ампициллину в Украине была несколько ниже (8,3%) и обусловлена наличием небольшого количества штаммов, продуцирующих β-лактамазу (7,3%), и одного BLNAR-штамма (1,0%). В 2011-2013 гг. рассматриваемые показатели тоже были невысокими: тогда выявили 4,5% штаммов, продуцирующих β-лактамазу, а BLNAR-штаммов вообще не обнаружили. Кроме того, показатели чувствительности H. influenzae к АБ в Украине, зафиксированные в настоящем исследовании, оставались на уровне 100% и снизились всего на 2% по сравнению с данными, полученными в 2011-2013 гг. в рамках предыдущего исследования SOAR. Исключение составил кларитромицин, чувствительность к которому в 2014-2016 гг. по критериям CLSI оценена всего в 61,5%, тогда как в 2011-2013 гг. она достигала 98,5%.
Несмотря на то что антибактериальная активность в отношении H. influenzae оказалась достаточно однородной в обеих странах, при сравнении уровней чувствительности, определенных при помощи различных контрольных точек, указанная сопоставимость утрачивалась. Например, в соответствии с контрольными точками CLSI 97% штаммов гемофильной палочки являлись чувствительными к азитромицину, но при использовании стандартов ФК/ФД и EUCAST этот показатель уменьшался до ≤2,1%. Аналогичная ситуация зафиксирована для цефаклора при применении контрольных точек CLSI и ФК/ФД, а также для цефуроксима при использовании контрольных точек CLSI, ФК и EUCAST. Наиболее показательными в этом отношении являлись данные, полученные в Украине при применении цефаклора: в соответствии с контрольными точками CLSI 86,0% штаммов S. pneumoniae были чувствительны к этому АБ, тогда как при использовании контрольных точек ФК/ФД и EUCAST данный показатель снижался до 28,0 и 0% соответственно. Эти различия не только приводят в замешательство практикующих врачей, но и затрудняют использование данных по АБР в научных целях и в целях рационального использования антибактериальных препаратов.
Легкая стезя известных ошибок или нехоженые тропы новых решений?
Недавно опубликованные результаты исследования SOAR, проводимого с использованием оригинальных молекул, с одной стороны, подтвердили довольно благоприятную обстановку в нашей стране относительно АБР. С другой стороны, принимая во внимание неутешительные прогнозы проекта RAR и безрадостную статистику ВОЗ, можно смело утверждать, что Украина находится на распутье. От того, как будут действовать система здравоохранения в целом и каждый практикующий врач в отдельности, какое сформируется общественное мнение, зависит наше будущее. Если мы пойдем легкой, проторенной дорогой повального и повсеместного использования АБ, повторяя ошибки Словакии, нас ждут быстрое развитие резистентности к антибактериальным препаратам и рост смертности от АБР. Если же украинцы найдут в себе силы выбрать путь рациональной АБТ, контролированного и адекватного использования АБ в медицине, животноводстве, сельском хозяйстве, вполне вероятно, что нас будет ожидать другой сценарий, отличный от возврата в «темные века медицины». Первым шагом на этом сложном пути может стать рациональная АБТ инфекционных заболеваний НДП, в частности ВБП.
Амоксициллина/клавуланат (например, оригинальный препарат Аугментин, GlaxoSmithKline, Великобритания) демонстрирует свою высокую эффективность в отношении 2 основных возбудителей внебольничных инфекций дыхательных путей – S. pneumoniae и H. influenzae – в ходе 2 исследований SOAR 2011-2013 гг. и 2014-2016 гг. Так, чувствительность S. рneumoniae к амоксициллину/клавуланату в соответствии с контрольными точками CLSI составила 100% в 2011-2013 гг. и 97,0% в исследовании 2014-2016 гг. Чувствительность H. influenzae в исследовании 2014-2016 гг. сопоставима с результатами, полученными в 2011-2013 гг. и составляет 100%.
Владея современными данными относительно АБР, зная результаты исследования SOAR, достаточно просто сделать правильный выбор противомикробного препарата, назначить адекватную терапию амбулаторным больным с внебольничными инфекциями дыхательных путей и тем самым внести свой вклад в предотвращение развития АБР не только в нашей стране, но и во всем мире.
Подготовила Татьяна Можина
Литература
- Tackling DrugResistant Infections Globally: final report and recommendations. THE REVIEW ON ANTIMICROBIAL RESISTANCE CHAIRED BY JIM O’NEILL. https://amrreview.org/sites/default/files/160525_Final%20paper_with%20cover.pdf
- High levels of antibiotic resistance found worldwide, new data shows. http://www.who.int/mediacentre/news/releases/2018/antibioticresistancefound/en/
- The top 10 causes of death. http://www.who.int/newsroom/factsheets/detail/thetop 10causesofdeath
- Torumkuney D. Results from the Survey of Antibiotic Resistance (SOAR) 201416 in Ukraine and the Slovak Republic.J AntimicrobChemother.2018; 73 Suppl 5: v28–v35. doi:10.1093/jac/dky069
Медична газета «Здоров’я України 21 сторіччя» № 9 (430), травень 2018 р.