12 червня, 2018
Інноваційні технології хірургічного лікування гострих шлунково-кишкових кровотеч
 18-21 квітня у Києві відбувся ювілейний Х Британсько-української симпозіум з анестезіології та інтенсивної терапії «Фокус на ефективності й комфорті», на якому були представлені доповіді провідних фахівців інтенсивної терапії як вітчизняного, так і міжнародного рівня. Ще однією перевагою симпозіуму був його міждисциплінарний формат. Своїм баченням проблеми ведення пацієнтів із гострими станами ділилися й хірурги. Неабияку увагу присутніх привернула доповідь професора кафедри хірургії № 3 Національного медичного університету ім. О.О. Богомольця (НМУ) (м. Київ), доктора медичних наук Євгена Миколайовича Шепетька, що стосувалася сучасних реалій і перспектив діагностики й лікування шлунково-кишкових кровотеч (ШКК).
18-21 квітня у Києві відбувся ювілейний Х Британсько-української симпозіум з анестезіології та інтенсивної терапії «Фокус на ефективності й комфорті», на якому були представлені доповіді провідних фахівців інтенсивної терапії як вітчизняного, так і міжнародного рівня. Ще однією перевагою симпозіуму був його міждисциплінарний формат. Своїм баченням проблеми ведення пацієнтів із гострими станами ділилися й хірурги. Неабияку увагу присутніх привернула доповідь професора кафедри хірургії № 3 Національного медичного університету ім. О.О. Богомольця (НМУ) (м. Київ), доктора медичних наук Євгена Миколайовича Шепетька, що стосувалася сучасних реалій і перспектив діагностики й лікування шлунково-кишкових кровотеч (ШКК).
В Україні щороку госпіталізується понад 50 тис хворих із гострими ШКК. У такій розвиненій країні, як США, цей показник перевищує 300 тисяч. Висока частота та захворюваність (до 80 на 100 тис населення) супроводжується високою смертністю – до 8,7% у перші 30 днів з моменту госпіталізації. У Київському центрі шлунково-кишкових кровотеч за більш ніж 35-річний період було проліковано понад 37 тис пацієнтів із ШКК і накопичено достатньо великий досвід лікування таких хворих.
Найбільш частою причиною ШКК визначено виразкову хворобу. Серед інших причин варто зазначити ерозивний гастродуоденіт (ЕГД) та медикаментозні виразки (13,4%), пухлини (10%), цироз печінки (7,8%), синдром Мелорі – Вейса (7,8%) та інші рідкісні захворювання. До рідких причин кровотечі відносяться: дивертикули травного каналу, неспецифічний коліт, ентеропатії та кишковий дисбактеріоз, проростання пухлини в травний канал, судинні нориці, опіки стравоходу і шлунка, ятрогенні чинники, хвороба Рандю – Ослера, геморагічний васкуліт, гострий лейкоз, гемофілія, лімфогранулематоз, хвороба Шенлейн – Геноха, черевний тиф, лептоспіроз, травми.
Якщо порівнювати частоту ШКК у різні періоди (1982-2006, 2007-2012, 2012-2015 рр.), то слід зазначити, що частота пухлинних кровотеч практично не змінилась. Частота кровотеч при портальній гіпертензії збільшилась у 2,2 разу, при синдромі Мелорі – Вейса – у 1,6 разу. Це свідчить про несприятливий вплив соціально-економічних факторів, зокрема алкоголізму.
Кількість операцій із приводу виразкової хвороби в Україні в період із 2000 по 2014 рік знизилася на 63%. Таке зниження пояснюється в першу чергу визнанням хелікобактерної природи виразкової хвороби й широким впровадженням антихелікобактерної терапії.
Сьогодні вибір лікування хворих із пептичними виразками шлунка змістився на користь консервативної медикаментозної терапії, яка завдяки впровадженню сучасних противиразкових препаратів, насамперед блокаторів протонної помпи, забезпечує хороші результати лікування.
Однак це мало вплинуло на кількість виразкових кровотеч, частка яких у загальній структурі ускладнень виразкової хвороби становить 20-51%. Зменшилася кількість як планових, так і ургентних оперативних втручань із певною стабілізацією показників в останні 2-3 роки.
Лікування хворих із гострими ШКК – це складна проблема, що потребує залучення значної кількості спеціалістів (ендоскопістів, хірургів, анестезіологів) і їхньої тісної співпраці. З огляду на високий рівень летальності після екстрених операцій великої популярності набула активно-вичікувальна тактика, в якій саме лікарям-ендоскопістам відводиться найважливіша роль.
Сучасна концепція хірургічного лікування гострокровоточивих гастродуоденальних виразок (ГГВ) ґрунтується на наступних положеннях:
- розробка та впровадження ефективних засобів ендоскопічного гемостазу (ЕГ);
- застосування сучасної гемостатичної та інфузійно-трансфузійної терапії;
- застосування внутрішньовенних інгібіторів протонної помпи (езомепразол, омепразол, пантопразол) із рН-моніторингом;
- удосконалення активно-індивідуалізованої тактики з математичним прогнозуванням ризику раннього рецидиву кровотечі (РК);
- компенсаторна ерадикаційна (антихелікобактерна) терапія згідно з Маастрихтськими консенсусами;
- удосконалення пілорусзберігаючого напрямку в хірургії ГГВ (застосування функціонально вигідних операцій);
- використання сучасних технологій у хірургічному лікуванні гострокровоточивих ШКК (апаратні методи, ультразвуковий скальпель, зварювальний апарат, гемопоетичні стовбурові клітини в пацієнтів, яким протипоказана гемотрансфузія).
Хірургічне лікування ГГВ є складною й остаточно не вирішеною проблемою. Київський міський центр шлунково-кишкових кровотеч і кафедра хірургії № 3 НМУ ім. О.О. Богомольця має досвід лікування 34 556 хворих із ШКК за період з 1982 по 2014 рік. У дослідження включено три періоди спостереження за пацієнтами з гострими виразковими ШКК (ГВШКК):
І період (2006-2008 рр.) – 1696 пацієнтів (виразка шлунка – 646, 38,1%, виразка ДПК – 1050, 61,9%);
ІІ період (2009-2011 рр.) – 1321 пацієнт (виразка шлунка – 425, 32,2%, виразка ДПК – 896, 67,8%);
ІІІ період (2012-2014 рр.) – 1062 пацієнти (виразка шлунка – 388, 36,5%, виразка ДПК – 674, 63,5%).
Аналіз отриманих даних дозволяє зробити висновок про збільшення частки осіб похилого віку з ШКК. За ступенем крововтрати не було суттєвої різниці між порівнюваними групами.
Провідним діагностичним методом при ШКК є езофагогастродуоденоскопія (ЕГДС), яка має проводитися у всіх пацієнтів. ЕГДС дає можливість:
- верифікувати джерело кровотечі та його локалізацію;
- визначити стигмати активності кровотечі;
- провести зупинку кровотечі за допомогою ендоскопічних методів гемостазу;
- при зупиненій кровотечі провести ендоскопічну профілактику її рецидиву;
- визначити ступінь надійності гемостазу і спрогнозувати ймовірність ризику РК.
Для ендоскопічної характеристики джерела кровотечі використовують класифікацію активності кровотечі за Forrest (1973). Відповідно до цієї класифікації виділяють наступні типи кровотеч.
FI. Кровотеча, що продовжується:
- FIА – струминна;
- FIb – просочування.
FII. Кровотеча, що зупинилася:
- FIIa – тромбована судина (2 мм, тромб червоний, чорний, білий);
- FIIb – фіксований згусток (>2 мм, червоний, чорний, білий);
- FIIc – дрібні тромбовані судини (чорні крапки).
FIII. Відсутня кровотеча: дефект під фібрином.
РК є найбільш серйозною проблемою у веденні пацієнтів із ШКК виразкової етіології. Критерій ЕГ при ендоскопічному дослідженні вважається основним компонентом, на якому ґрунтується стратегія подальшого лікування пацієнта. РК максимально вірогідний протягом першої доби. Отже, велике значення для вибору подальшої хірургічної тактики і прогнозу раннього РК має визначення перерахованих вище ендоскопічних стигмат виразкових кровотеч.
Фахівцями Київського міського центру шлунково-кишкових кровотеч було розроблено алгоритм активної індивідуалізованої тактики хірургічного лікування ГВШКК, що ґрунтується на застосуванні невідкладних (превентивних) операцій у перші 6-12 год (до 24 год) після госпіталізації за нестабільного гемостазу й високого ризику РК (РКК) з використанням методики прогнозування РКК на основі покрокового дискримінантного аналізу.
Інтегральний показник включає такі змінні, як розмір виразки (Х1), стан гемостазу у виразці (Х2), ступінь тяжкості кровотечі (Х3) і вік пацієнта (Х4). Так, при діаметрі виразки до 1 см Х1=1, 1,1-2 см – Х1=2, >2 см – Х1=3. Стан гемостазу у виразці: Х2=1, якщо дно виразки вкрите фібрином (Forrest III); Х2=2, якщо на дні виразки видно малу тромбовану судину (Forrest IIС); Х2=3, якщо на дні виразки виявлено велику тромбовану судину (Forrest IIа); Х2=4, якщо на дні виразки видно згусток крові (Forrest IIb).
Ступінь тяжкості кровотечі: Х3=1 при кровотечі помірної тяжкості, Х3=2 при кровотечі помірної тяжкості та Х3=3, якщо кровотеча тяжка. Вік: Х4=1, якщо вік пацієнта ≤60 років, і Х4=2, якщо вік пацієнта >60 років.
Інтегральний показник розраховується за формулою:
ІП = (3×Х1) + (2×Х2) + Х3 + Х4.
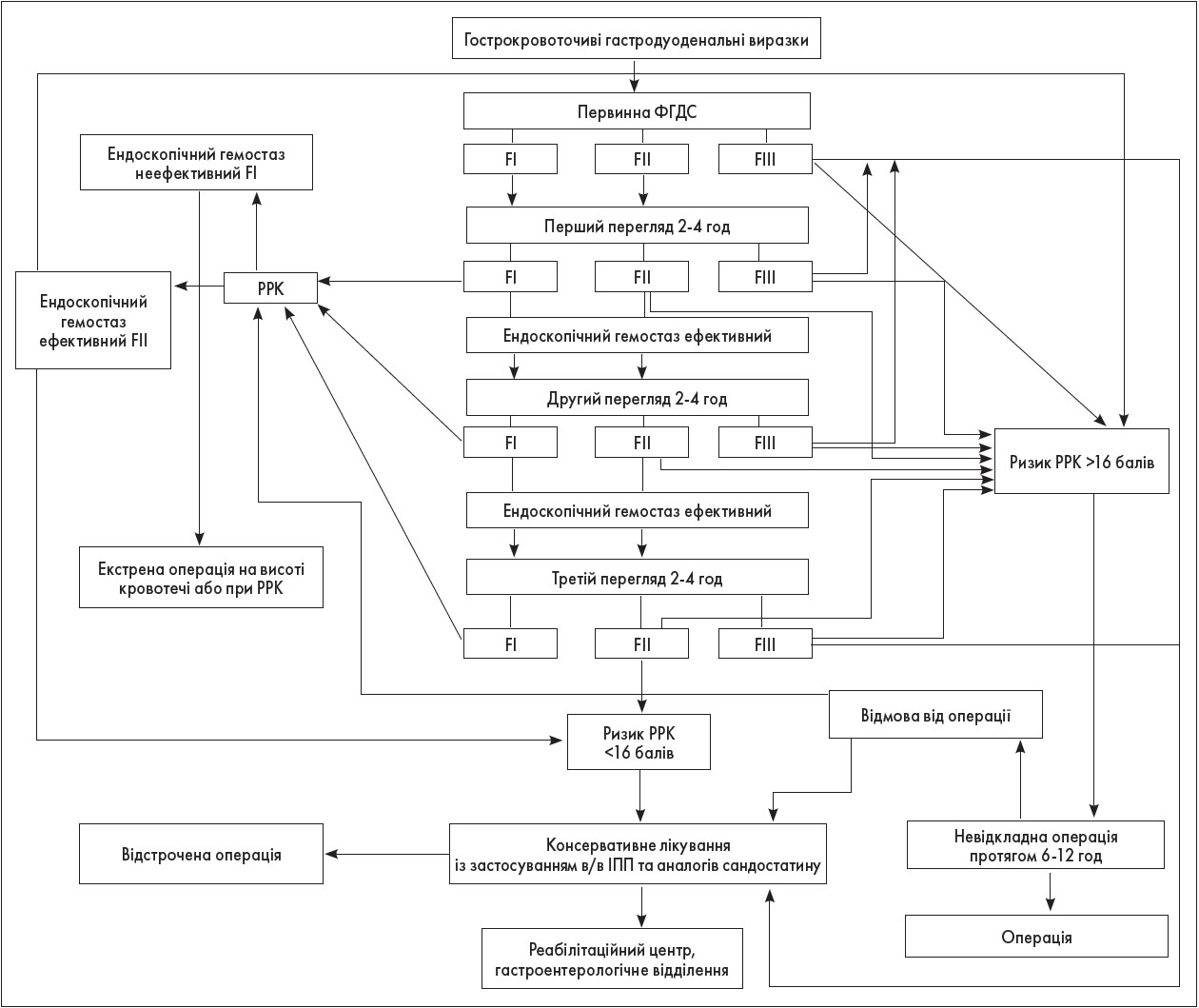
При інтегральному показнику <10 балів ризик виникнення РК низький (5-6%), від 10 до 16 балів – середній (до 34%), >16 балів – дуже високий (до 89%). Відповідно, чим вищий РРК, тим частіше необхідно проводити повторний ендоскопічний моніторинг (рис.). Це дозволяє виявити кровотечу ще до розвитку клінічних ознак і покращує прогноз терапії.
Таким чином, алгоритм тактики хірургічного лікування ГВШКК полягає у виявленні пацієнтів із високим РРК (≥16 балів). Таким пацієнтам показана активна хірургічна тактика з виконанням превентивних операцій, направлених на запобігання РК. Саме такий підхід сприяє зниженню як загальної, так і післяопераційної летальності. Безумовно, ЕГ лежить в основі лікування пацієнтів із ГВШКК.
Для цього можуть бути використані різні методи ЕГ (електро-, радіочастотна, аргоноплазмова коагуляція, лазерна фотокоагуляція), ефективність яких відрізняється в тих чи інших випадках. На жаль, не у всіх лікувальних закладах присутній весь перелік відповідного обладнання. Роль ендоскопіста полягає в оптимальному використанні арсеналу наявних у нього засобів для ефективного запобігання РК.
а сьогодні кількість оперативних втручань при ГВШКК суттєво знизилась. Переважно це невідкладні операції, метою яких є запобігання РК. 2016 року оперативна активність при ГВШКК склала всього 2,7%. Для порівняння: до 2006 року цей показник становив близько 37%.
При тяжких гастродуоденальних кровотечах і нестабільному стані пацієнта слід тимчасово утриматися від проведення ендоскопії й почати консервативну терапію з метою корекції та стабілізації гемодинаміки. У стратегії інфузійно-трансфузійної терапії при тяжкому геморагічному шоці показана трансфеморальна катетеризація аорти.
Проведення інфузійної терапії двома шляхами, внутрішньовенно й внутрішньоартеріально, зі співвідношенням вена:артерія = 1:5 або 1:7 дає можливість швидко стабілізувати гемодинаміку й запобігти розвитку серцевої недостатності внаслідок перевантаження правих відділів серця, що може мати місце при швидкому введенні інфузійних розчинів лише внутрішньовенно.
Важливу роль у профілактиці РК відіграє пригнічення шлункового кислотоутворення. Згідно з даними низки авторів, нормальний процес згортання крові відбувається при рН шлункового вмісту на рівні 6,7-7,0. При збільшенні кислотності відбувається інгібування агрегації тромбоцитів, а також лізис утвореного фібринового згустку через зростання пептичної активності. Високоефективним у даному випадку вважається призначення внутрішньовенних форм інгібіторів протонної помпи (ІПП). Для запобігання «нічному кислотному прориву» можуть бути рекомендовані дві схеми введення цих препаратів.
Схема № 1: ІПП 80 мг внутрішньовенно болюсно при госпіталізації, а потім внутрішньовенно крапельно 8 мг/год протягом 72 год (80 мг+192 мг/добу = 272 мг у 1-шу добу і в подальші 2 доби – болюсно 40 або 80 мг+192 мг/добу, тобто 272 або 232 мг).
Схема № 2: ІПП 80 мг внутрішньовенно болюсно при госпіталізації, а потім 80 мг внутрішньовенно болюсно 2 рази на добу протягом 3-5 діб. У подальшому рекомендується перехід на таблетовані форми препаратів.
У разі неефективності ЕГ слід виконати хірургічне втручання. На сьогодні широко застосовуються органозберігаючі методики оперативних втручань. Один із способів хірургічного лікування кровоточивих парапапілярних виразок передбачає виконання селективної проксимальної ваготомії, поперечної пілорусзберігаючої дуоденопластики з видаленням країв виразки, папілосфінктеропластики, селективної проксимальної ваготомії, транспапілярного дренування холедоха через зону виразки, розташовану поблизу великого дуоденального сосочка.
Інноваційні мініінвазивні технології включають поєднане використання лапароскопічних та ендоскопічних методик. Також розроблено методи реімплантації фатерового сосочка при гострокровоточивих юкстапапілярних виразках.
Впровадження в клініку модельованих органощадних операцій зі збереженням васкуляризованого та іннервованого пілороантрального сегмента шлунка, виконаних при виразках шлунка, органощадних антрум-резекцій при низьких постбульбарних та юкстапапілярних виразках та органозберігаючих операцій при ускладнених кровоточивих дуоденальних виразках дозволило знизити рівень післяопераційної летальності в 2,4 разу.
Другою за частотою причиною ШКК є ЕГД. Його морфологічним субстратом є поєднання субепітеліальних геморагій і пласких ерозій. Вони можуть виникнути як ускладнення при тяжких захворюваннях (атеросклероз, цукровий діабет, ниркова недостатність, сепсис, опік, перенесена напередодні складна операція, травма, отруєння різними речовинами тощо), прийомі деяких лікарських препаратів (НПЗП, кортикостероїди, деякі антибіотики, дигоксин, препарати заліза, калію, цитостатики тощо) й уживанні алкоголю. В основі патогенезу ЕГД лежить дисбаланс між активністю факторів агресії та захисту слизової оболонки шлунка.
До клінічних особливостей ЕГД слід віднести відсутність кореляції між тяжкістю суб’єктивних розладів, наявністю і ступенем вираженості ушкодження слизової оболонки, схильність до спонтанної зупинки кровотеч при усуненні впливу етіологічного чинника. Гостре виразкування слизової оболонки шлунка та ДПК розвиваються протягом найближчих 3-5 діб після дії провокуючих чинників (операція, шок, сепсис, обширні опіки тощо).
У 75-100% пацієнтів відділень інтенсивної терапії в перші 24 год після госпіталізації виявляють ушкодження слизової оболонки шлунково-кишкового тракту (стрес-виразки). У 5-25% із них розвиваються явні гастродуоденальні кровотечі. Загальна летальність в оперованих пацієнтів при розвитку гострого ерозивно-виразкового пошкодження шлунка, ускладненого кровотечею, є досить високою й сягає 80%.
Ризик гострого виразкування й кровотечі можна зменшити шляхом застосування ІПП. Сьогодні доведено, що належний рівень кислотності шлункового соку (рН>6) є ефективним засобом зупинки ШКК і профілактики раннього РК.
Важливим питанням є продовження терапії НПЗП у пацієнтів, в яких виникла ШКК.
Згідно з положеннями міжнародного консенсусу щодо ведення пацієнтів із неварикозними ШКК із верхніх відділів травного тракту за необхідності прийому НПЗП слід керуватися наступними рекомендаціями.
Е1. У пацієнтів із попередньою виразковою кровотечею, які потребують продовження лікування традиційними НПЗП на тлі прийому ІПП або селективних інгібіторів ЦОГ‑2 НПЗП без захисту досі асоціюється з клінічно значущим ризиком повторних виразкових кровотеч.
Е2. У пацієнтів із попередньою виразковою кровотечею, які потребують продовження прийому НПЗП, рекомендується лікування селективними інгібіторами ЦОГ‑2 НПЗП у поєднанні з ІПП. Це значно зменшує ризик повторної кровотечі порівняно з призначенням інгібіторів ЦОГ‑2 без такого захисту.
У пацієнтів, які отримували низькі дози ацетилсаліцилової кислоти (АСК) і в яких розвинулася виразкова кровотеча, терапія АСК може бути відновлена, як тільки ризик прогнозованих серцево-судинних ускладнень перевищить ризик кровотечі. Зазвичай АСК можна призначати на 3-5-ту добу після розвитку кровотечі. У пацієнтів з попередніми виразковими кровотечами, які потребують профілактики серцево-судинних ускладнень, монотерапія клопідогрелем асоціюється з більш високим РРК, ніж терапія АСК у поєднанні з ІПП.
У консервативній терапії ерозивно-виразкових ГШКК доцільно застосовувати гемостатичні препарати, ІПП та Н2-блокатори, антациди (альмагель, фосфалюгель), серотоніну адипінат у дозі 4 мг/кг, простагландини (місопростол), сандостатин. ЕГ може включати ін’єкційні, аплікаційні методики та хімічну коагуляцію або лазерну фотокоагуляцію, ендоскопічну локальну озонотерапію, ендоскопічну локальну імунотерапію (Ig A).
Синдром Мелорі – Вейса зумовлений розривом слизової оболонки в ділянці стравохідно-шлункового переходу. Патогенез цього захворювання пояснюється транзиторним збільшенням градієнта тиску між просвітом шлунка й грудної порожнини, що досягає максимального значення на рівні стравохідно-шлункового переходу.
До провокуючих факторів відносяться блювання, ікавка, кашель, збільшення ваги, напруження при дефекації, пологи, тупа травма живота, астматичний статус, ендоскопічне дослідження, реанімація (непрямий масаж серця, штучне дихання). Характерною ознакою синдрому Мелорі – Вейса є початок блювання без крові з подальшою появою крові у блювотних масах. Однак у третини хворих вже в перших порціях блювотних мас виявлялася кров, а у 5-10% це захворювання проявлялося тільки меленою.
Кровотеча при синдромі Мелорі – Вейса в більшості випадків зупинялася спонтанно, а РК розвивався рідко (близько 8% випадків). Основним методом лікування при цій патології є ЕГ.
Особливу складність представляє лікування кровотеч із варикозно-розширених вен (ВРВ) стравоходу та шлунка при синдромі портальної гіпертензії, оскільки ці кровотечі дуже часто є профузними. В лікуванні кровотеч із ВРВ доволі ефективна методика паравазального й інтравазального склерозування, а також комбінація клішування з інтравазальною склеротерапією. Хороший ефект забезпечує метод лікування стравохідних флебектазій із накладанням латексних кілець. Виконати гемостаз у випадку профузної кровотечі часто є складним завданням навіть для досвідчених ендоскопістів.
Таким чином, застосування сучасних ендоскопічних методик дозволяє суттєво поліпшити результати лікування хворих із ШКК, а розроблені алгоритми ендоскопічного моніторингу дають змогу вчасно попередити розвиток РК у пацієнтів високого ризику.
Підготував В’ячеслав Килимчук
Тематичний номер «Хірургія, Ортопедія, Травматологія, Інтенсивна терапія» № 2 (32), травень 2018 р.