14 червня, 2018
Неалкогольная жировая болезнь поджелудочной железы: современное состояние вопроса
 Научно-технический прогресс не только изменил условия и образ жизни человека, но и принес с собой специфические заболевания, число которых с каждым десятилетием возрастает. Казалось бы, совершенно недавно врачи узнали о коварстве метаболического синдрома и неалкогольной жировой болезни печени (НАЖБП), как появляется новая нозология – стеатоз поджелудочной железы (ПЖ). Поначалу ее постигла такая же участь, как и метаболический синдром и НАЖБП: в начале 2000-х гг. стеатоз ПЖ считали надуманной проблемой, мифом. Однако прошло всего 15-17 лет – и отношение к этой патологии существенно изменилось: доказана связь неалкогольной жировой болезни ПЖ (НАЖБПЖ) с другими заболеваниями, высказана гипотеза о прогрессирующем течении стеатоза с вероятным развитием аденокарциномы ПЖ, разрабатываются новые методы диагностики и эффективные способы лечения. В рамках данной статьи мы попытаемся осветить произошедшие перемены в области панкреатологии, посвященной этой «новой» нозологии.
Научно-технический прогресс не только изменил условия и образ жизни человека, но и принес с собой специфические заболевания, число которых с каждым десятилетием возрастает. Казалось бы, совершенно недавно врачи узнали о коварстве метаболического синдрома и неалкогольной жировой болезни печени (НАЖБП), как появляется новая нозология – стеатоз поджелудочной железы (ПЖ). Поначалу ее постигла такая же участь, как и метаболический синдром и НАЖБП: в начале 2000-х гг. стеатоз ПЖ считали надуманной проблемой, мифом. Однако прошло всего 15-17 лет – и отношение к этой патологии существенно изменилось: доказана связь неалкогольной жировой болезни ПЖ (НАЖБПЖ) с другими заболеваниями, высказана гипотеза о прогрессирующем течении стеатоза с вероятным развитием аденокарциномы ПЖ, разрабатываются новые методы диагностики и эффективные способы лечения. В рамках данной статьи мы попытаемся осветить произошедшие перемены в области панкреатологии, посвященной этой «новой» нозологии.
Первое описание стеатоза ПЖ, сделанное Oligvie и соавт. в 1933 г., связывало избыточное отложение жира в ПЖ с морбидным ожирением: при анализе секционного материала жировая инфильтрация ПЖ выявлена у 17% больных ожирением, тогда как у нормостеников это состояние описывали только в 9% случаев (Н. Tariq et al., 2016). Другое исследование жирового перерождения ПЖ, представленное Olsen в 1978 г., продемонстрировало корреляцию между распространенностью указанной патологии и увеличением возраста пациентов. Несколько позже эти данные подтвердил В. Stamm (1984), который, анализируя посмертные изменения ПЖ, установил, что распространенность липоматоза увеличивается с возрастом, а жировая инфильтрация >25% ткани ПЖ ассоциируется с высоким риском развития сахарного диабета (СД) 2-го типа и генерализованного атеросклеротического поражения сосудов. Впоследствии появилась теория о связи стеатоза ПЖ с инсулинорезистентностью. Van Geenen и соавт. (2010) предположили, что инсулинорезистентность, усиливая периферический липолиз, увеличивает приток свободных жирных кислот в ПЖ. Это способствует развитию стеатоза ПЖ, предшествующего возникновению стеатоза печени и НАЖБП. Именно эти авторы высказали мнение о целесообразности введения и повсеместного использования унифицированной дефиниции: они ввели и стали активно применять новый термин «НАЖБПЖ». До этого времени в литературе использовались самые разнообразные понятия: «жирная ПЖ», «псевдогипертрофический липоматоз», «жировое перерождение ПЖ», «жировая инфильтрация ПЖ», «неалкогольный жировой стеатопанкреатит».
В целом ряде фундаментальных и клинических исследований, проведенных на протяжении последних нескольких лет, зафиксирована сильная взаимосвязь между ожирением и развитием стеатоза ПЖ. Увеличение заболеваемости НАЖБПЖ связывают со значительным ростом распространенности ожирения в различных возрастных группах (дети, подростки, взрослое население). Учитывая неутешительные статистические данные, приведенные ВОЗ в 2017 г. (табл. 1), ведущие эксперты в области гастроэнтерологии прогнозируют возрастание распространенности стеатоза ПЖ.
 Высказывается предположение, что недавно появившийся термин globesity, введенный ВОЗ и подчеркивающий глобальный, всемирный масштаб распространения ожирения, будет использоваться в отношении таких патологий, как НАЖБП и НАЖБПЖ (R. Catanzaro et al., 2016).
Высказывается предположение, что недавно появившийся термин globesity, введенный ВОЗ и подчеркивающий глобальный, всемирный масштаб распространения ожирения, будет использоваться в отношении таких патологий, как НАЖБП и НАЖБПЖ (R. Catanzaro et al., 2016).
Среди других факторов, провоцирующих развитие стеатоза ПЖ (табл. 2), большое внимание уделяют возрасту пациента и наличию СД 2-го типа (Т. Khoury et al., 2017; Т. Alempijevic et al., 2017).
К другим возможным причинам относят наследственные заболевания, такие как муковисцидоз, синдромы Швахмана–Даймонда (врожденная гиперплазия экзокринной части ПЖ), Йохансона–Близзарда (врожденная недостаточность экзокринной функции ПЖ со множественными аномалиями развития), гетерозиготные мутации лизосомной кислой липазы. Н. Tariq и соавт. (2016) дополняют перечень возможных этиологических факторов, предложенный V. Prachayakul, токсическим воздействием алкоголя (при условии употребления алкогольных напитков >14 г в неделю).
В настоящее время существует несколько теорий возникновения и развития НАЖБПЖ, в большинстве своем они подобны гипотезе формирования и прогрессирования НАЖБП. В отношении естественного течения стеатоза ПЖ проводится параллель c жировой инфильтрацией печени: считается, что континуум НАЖБПЖ начинается с отложения жира в ПЖ, прогрессирует вследствие активного воспалительного процесса до развития фиброза и, вероятно, до аденокарциномы ПЖ (R. Carter et al., 2014; Н. Tariq et al., 2016; Т. Khoury et al., 2017; Т. Alempijevic et al., 2017).
Многие из этих ученых полагают, что развитие рака ПЖ в исходе жировой инфильтрации вполне вероятно, учитывая общность эмбриологического происхождения ПЖ и печени, для которой доказано формирование гепатоцеллюлярной карциномы в конечной точке прогрессирования НАЖБП. Эта гипотеза подтверждается результатами исследований, согласно которым НАЖБПЖ является фактором риска возникновения аденокарциномы ПЖ (R. Carter et al., 2014).
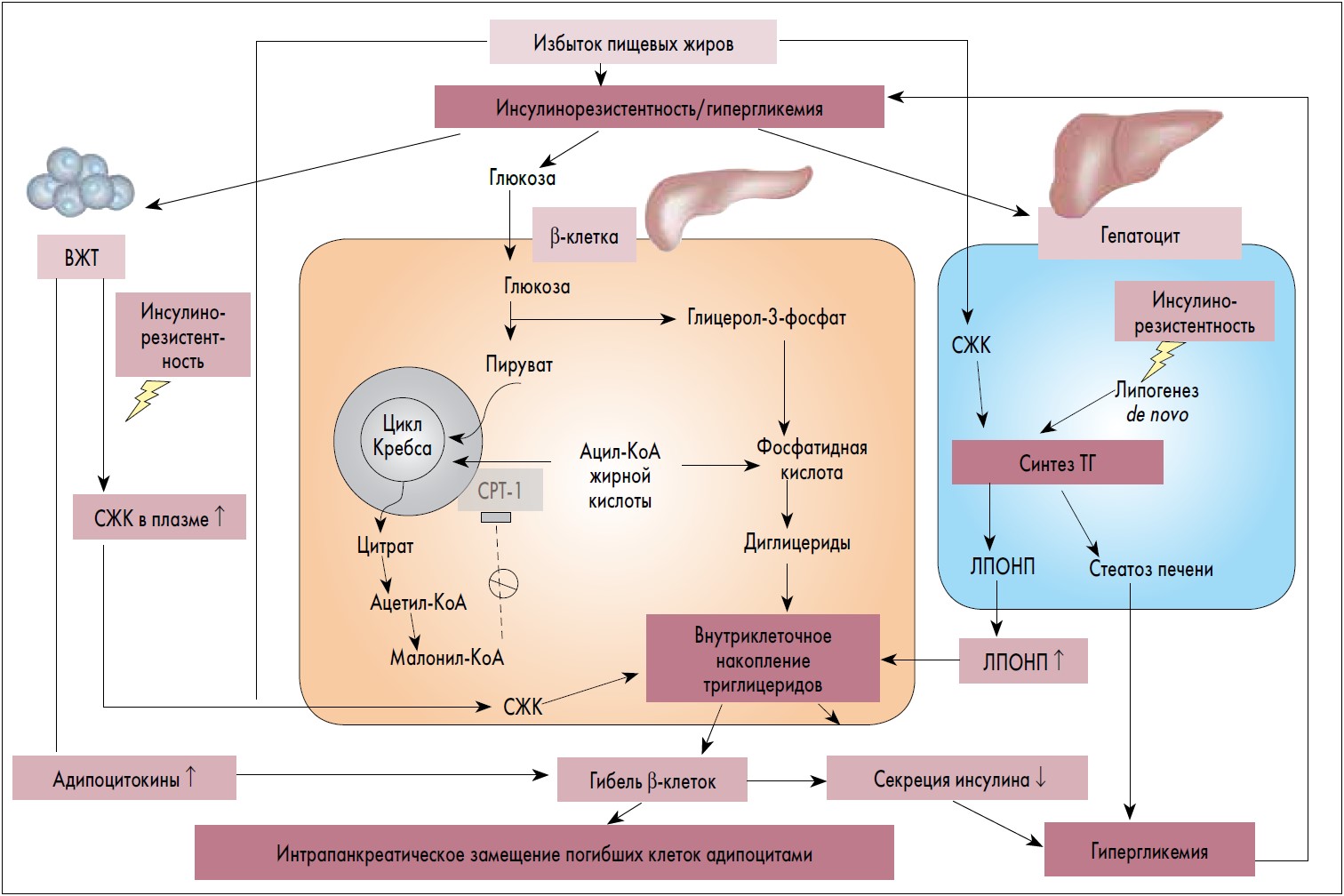
Согласно теории, предложенной T. Yu и соавт. (2017, рис.), первоначально НАЖБП, формирующаяся на фоне ожирения и увеличения количества висцеральной жировой ткани, создает предпосылки для внутриклеточного накопления триглицеридов в паренхиме ПЖ, что приводит к гибели β-клеток, их замещению адипоцитами, вторичной гипергликемии и усугублению метаболических нарушений.
Рис. Возможные взаимосвязи между дисгликемией, НАЖБПЖ и дисфункцией β-клеток (по T. Yu et al., 2017)
Избыточная калорийность пищевого рациона, чрезмерное насыщение пищи жирами на протяжении длительного времени, а также гиперинсулинемия способствуют развитию стеатоза печени, что обусловливает усиление экспорта липопротеинов очень низкой плотности (ЛПОНП), которое, в свою очередь, приводит к избыточному поступлению жира в островки ПЖ. В β-клетках на фоне гипергликемии снижается активность карнитин-пальмитоилтрансферазы‑1 (СРТ‑1) и увеличивается концентрация малонил-коэнзима А (КоА), снижается активность процессов β-окисления и происходит внутриклеточное накопление триглицеридов. Кроме этого, инсулинорезистентность обусловливает изменение липолиза триглицеридов (ТГ) и высвобождение свободных жирных кислот (СЖК) из висцеральной жировой ткани (ВЖТ), что приводит к увеличению концентрации циркулирующих СЖК. Хроническое воздействие избытка СЖК на β-клетки ассоциируется с увеличением внутриклеточного содержания ТГ, снижением экспрессии и уменьшением синтеза инсулина. Более того, адипоцитокины и СЖК могут усиливать повреждение β-клеток, что в итоге также приводит к ухудшению секреции инсулина и индуцирует замещение паренхимы ПЖ адипоцитами. Если накопление жира в ткани ПЖ превышает допустимый порог (так называемый порог толерантности), то развивается гипергликемия, замыкающая порочный круг нарушенного метаболизма глюкозы.
В ряде исследований в отношении особенностей возникновения стеатоза ПЖ показано, что накопление жира в ПЖ строго ассоциировано с увеличением индекса массы тела, инсулинорезистентностью, метаболическим синдромом, НАЖБП. Зафиксирована сильная прямая взаимосвязь между наличием СД и развитием стеатоза ПЖ, и наоборот: доказано, что пациентам с жировой инфильтрацией ПЖ свойственен более высокий риск возникновения СД по сравнению лицами, не имеющими СД (R. Carter et al., 2014; Н. Tariq et al., 2016; Т. Alempijevic et al., 2017). В вышеперечисленных работах доказывается, что стеатоз ПЖ протекает с последующей утратой некоторого количества β-клеток и значительным снижением их функции, это, вероятно, и обусловливает развитие СД. С другой стороны, на фоне уже имеющегося СД жировое замещение поврежденной ткани ПЖ может способствовать отложению избыточного количества жира в паренхиме органа. Кроме того, увеличение уровня малонового коэнзима А, вызванное гипергликемией, сопровождается ингибированием активности карнитин-пальмитоилтрансферазы‑1, что обусловливает снижение активности процессов β-окисления в митохондриях и стимуляцию внутриклеточного накопления триглицеридов (Н. Tariq et al., 2016; Т. Yu et al., 2017).
Клинически НАЖБПЖ может характеризоваться бессимптомным или ярко выраженным, манифестным течением. При незначительном или умеренном накоплении жира в ПЖ субъективные и объективные проявления заболевания отсутствуют. Иногда у пациентов со стеатозом ПЖ обнаруживают симптом Тужилина – красные возвышающиеся пятнышки округлой формы (сосудистые аневризмы), не исчезающие при надавливании и расположенные на верхней половине туловища и животе. Как правило, этот симптом считается характерным для хронического панкреатита, но он не является специфическим. При значительной жировой инфильтрации паренхимы ПЖ появляются симптомы внешнесекреторной недостаточности и стеаторея. Однако, учитывая один общеизвестный факт (для удовлетворения потребностей процессов пищеварения в липазе и других ферментах панкреатического сока необходимо всего 10% нормально функционирующей паренхимы), можно утверждать, что подавляющее большинство случаев стеатоза ПЖ протекает бессимптомно, а заболевание чаще всего обнаруживают случайно в ходе инструментального обследования.
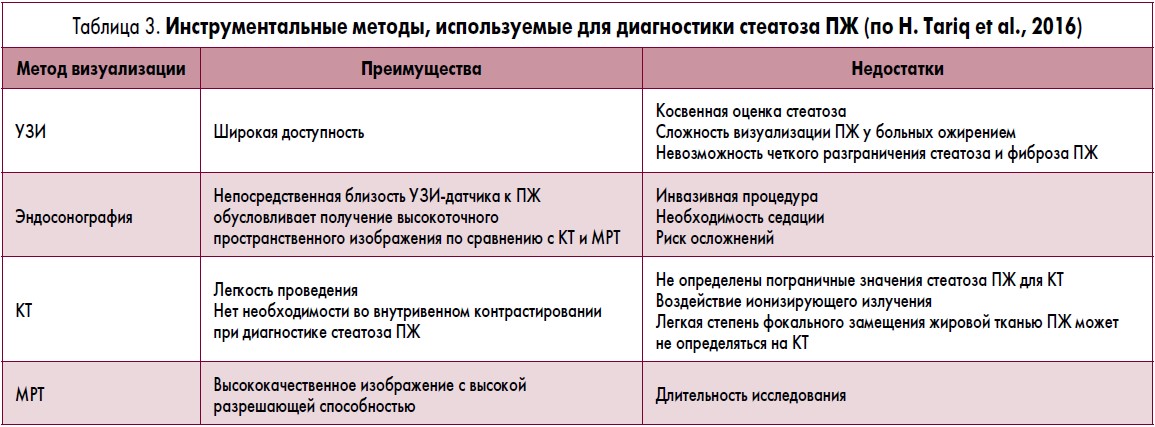
В недавнем прошлом инструментальная диагностика стеатоза ПЖ была возможна только in vivo при анализе образцов ткани, полученной в ходе аутопсии. С появлением современных и более сложных методов визуализации для диагностики НАЖБПЖ стали использовать ультразвуковое исследование (УЗИ), эндосонографию, компьютерную томографию (КТ), магнитно-резонансную томографию – МРТ (табл. 3).
Безусловно, наиболее широко использующимся методом диагностики НАЖБПЖ является УЗИ. Ультразвуковыми признаками стеатоза ПЖ являются диффузное увеличение эхогенности органа при сохранении однородной структуры, четкости контуров и возможном незначительном увеличении ПЖ в размерах. Обычно такие изменения обозначаются в ультразвуковом заключении как диффузные изменения ПЖ. В настоящее время эхогенность ПЖ оценивают косвенно, сравнивая ее с эхогенностью печени и почек. В норме эхогенность ПЖ такая же или несколько превосходит аналогичный показатель со стороны печени, тогда как при НАЖБП эхогенность печени выше, чем у почечной паренхимы. Данный факт отмечен еще в работе Lee и соавт. (2009), которые зафиксировали рост инсулинорезистентности, количества висцерального жира, триглицеридов, АЛТ в зависимости от степени инфильтрации адипоцитов паренхимы ПЖ. Эти авторы одними из первых установили факт одновременного существования НАЖБП и НАЖБПЖ и пришли к выводу, что стеатоз ПЖ может являться первоначальным маркером эктопического расположения жира, развивающейся инсулинорезистентности – ключевых элементов стеатоза печени и/или метаболического синдрома. К сожалению, фиброз ПЖ при УЗИ также проявляется повышением эхогенности, что делает невозможным применение УЗИ в качестве высокоточного скринингового метода диагностики стеатоза ПЖ.
По мнению Al-Haddad и соавт. (2009), а также Н. Tariq и соавт. (2016), эндосонография позволяет получить высокоточные изображения ПЖ и достоверно подтвердить стеатоз. Эти ученые утверждают, что разрешающая способность данного метода в диагностике жировой инфильтрации ПЖ может превосходить КТ и МРТ. Однако целый ряд недостатков (табл. 3), присущий эндосонографии, не позволяет использовать этот метод в качестве скринингового.
КТ с/без контрастирования также используется в диагностике стеатоза ПЖ. Плотность ПЖ, инфильтрированной большим количеством адипоцитов, выраженная в единицах Хаунсфилда (Hounsfield, HF), снижается и становится примерно равной таковой у селезенки. Пограничное значение HF для диагностики стеатоза ПЖ пока еще не определено (Н. Tariq et al., 2016).
Наилучшим способом диагностики стеатоза ПЖ является МРТ. Современные технологии позволяют не только оценить размеры органа и изменения его структуры, но и определить содержание липидов, а при протонной магнитно-резонансной спектроскопии – количественно оценить содержание триглицеридов (I. Lingvay et al., 2009). Разработаны различные МРТ-методики для определения количества жира в ПЖ. Например, Wong и соавт. (2014), использовав МРТ-технологии, установили, что распространенность стеатоза ПЖ у здоровых китайских волонтеров составляет 16,1% (95% доверительный интервал – ДИ – 13,3-18,8%). Вместе с тем до настоящего времени не разработаны унифицированные критерии МРТ-диагностики стеатоза ПЖ.
Учитывая тот факт, что каждый инструментальный метод диагностики имеет свои преимущества и недостатки, на протяжении последних нескольких лет активно исследовалась возможность диагностики стеатоза ПЖ по результатам лабораторных исследований. В одном из недавно опубликованных метаанализов 17 исследований (n=11 967) установлена взаимосвязь между количеством жира в паренхиме ПЖ и уровнем триглицеридов (r=0,38; 95% ДИ 0,31-0,46), HbA1c (r=0,39; 95% ДИ 0,30-0,48), инсулина (r=0,38; 95% ДИ 0,33-0,43), значением индекса НОМА (r=0,37; 95% ДИ 0,30-0,44), а также снижением холестерина липопротеинов высокой плотности (r= –0,33; 95% ДИ от –0,35 до –0,31). Перечисленные показатели R. Singh и соавт. (2017) предложили использовать в качестве биологических маркеров накопления жира в ПЖ. Вполне возможно, что в скором будущем будет разработана специальная лабораторная панель диагностики стеатоза ПЖ.
В настоящее время убедительно доказано, что стеатоз ПЖ ассоциируется с развитием метаболического синдрома, ожирения, увеличением уровня гликемии натощак, HbA1c, появлением дислипидемии (Wu и соавт., 2013). Эти данные подтверждены в более новой работе: метаанализ 9 исследований с участием относительно здоровых лиц, которым было выполнено МРТ-исследование (n=1209), выявил зависимость между наличием НАЖБПЖ и возрастанием риска развития артериальной гипертензии (относительный риск – ОР – 1,67; 95% ДИ 1,32-2,10; р<0,0001), СД (ОР 2,08; 95% ДИ 1,44-3,00; р=0,0001), метаболическим синдромом (ОР 2,37; 95% ДИ 2,07-2,71; р<0,0001). Авторы этого метаанализа предлагают в дальнейшем при проведении проспективных исследований использовать новое пограничное МРТ-значение для количества жира в ПЖ – 6,2% (R. Singh et al., 2017).
Функциональные последствия стеатоза ПЖ пока окончательно не изучены. Несмотря на то что накопление жира в островках ПЖ сопровождается снижением секреции инсулина, экзокринная недостаточность ПЖ при НАЖБПЖ исследована недостаточно широко. Подавляющее большинство литературных источников утверждает, что стеатоз ПЖ сопровождается снижением количества и функции β-клеток, которое обусловливает развитие СД 2-го типа. Установленная взаимосвязь между стеатозом ПЖ и метаболическим синдромом позволила некоторым авторам высказать мнение, что стеатоз ПЖ на самом деле является пятым компонентом метаболического синдрома (В. Romana et al., 2018).
Smits и van Geenen полагают, что стеатоз ПЖ, сформировавшийся на фоне ожирения, ассоциирован с высокой заболеваемостью и более тяжелым течением острого панкреатита за счет выраженного дисбаланса адипоцитокинов. Кроме того, в недавнем исследовании отмечено достоверное увеличение риска развития рака ПЖ при НАЖБПЖ: зафиксирована сильная прямая корреляционная взаимосвязь между панкреатической интраэпителиальной неоплазией и вне- (р<0,01), интралобулярным (р<0,0001) отложением жира в ПЖ (V. Rebours et al., 2015).
В настоящее время практические рекомендации по диагностике и лечению НАЖБПЖ еще не разработаны, поэтому единый подход к лечению данной патологии отсутствует. Некоторые авторы считают, что больным стеатозом ПЖ требуются такие же рекомендации, как и пациентам с НАЖБП: увеличить физическую активность, ограничить калорийность пищевого рациона, нормализовать массу тела (В. Romana et al., 2018). При этом V. Oskarsson и соавт. (2015) считают необходимым увеличить количество рыбы в рационе больных стеатозом ПЖ, поскольку в проспективном когортном исследовании (39 267 мужчин и 32 191 женщин), проведенном этими учеными, показано, что насыщение рациона питания рыбой (≤2-3 порции рыбных блюд в неделю) ассоциировано со значительным снижением риска развития некалькулезного панкреатита (р=0,017). V. Oskarsson полагает, что данная модификация пищевого рациона будет целесообразна при стеатозе ПЖ.
Другие авторы настаивают на проведении заместительной терапии ферментными препаратами при появлении клинических симптомов и лабораторных признаков экзокринной недостаточности ПЖ.
В лабораторных исследованиях in vitro изучалась эффективность троглитазона, телмисартана и ситаглиптина, берберина и коричной кислоты в лечении стеатоза ПЖ. При проведении клинических исследований большие надежды связывались с эксенатидом (аналогом глюкагонподобного пептида‑1), однако результаты недавно опубликованного проспективного рандомизированного исследования оказались неоднозначными. А. Dutour и соавт. (2016), наблюдавшие за больными ожирением и СД 2-го типа, течение которого не контролировалось приемом пероральных гипогликемических средств, дополнительно назначали пациентам 26-недельный прием эксенатида. После завершения курса терапии анализировали изменения размеров эпикардиальной жировой ткани, содержания триглицеридов в миокарде, печени и ПЖ спустя 45 мин после приема стандартизованного завтрака посредством 3Т-МРТ и протонной магнитно-резонансной спектроскопии. Оказалось, что прием эксенатида способствовал достоверному снижению массы тела, а также значительному уменьшению размера эпикардиальной жировой ткани (–8,8±2,1%), снижению содержания триглицеридов в печени (–23,8±9,5%) по сравнению с пациентами контрольной группы, не получавшими данный препарат (соответственно, –1,2±1,6% и +12,5±9,6%; р=0,007). Однако терапия эксенатидом не повлияла на уровень триглицеридов в ткани ПЖ. Поэтому в настоящее время продолжается поиск фармацевтических препаратов, способных уменьшить выраженность и степень стеатоза ПЖ.
Стеатоз ПЖ, при котором происходит замещение паренхимы ПЖ адипоцитами и развивается жировая инфильтрация, представляет собой чрезвычайно распространенное заболевание, которое легко диагностируется, но в большинстве случаев не учитывается практикующими врачами. Основываясь на вышеприведенных литературных данных, стеатоз ПЖ можно считать ранним маркером эктопического накопления жировой ткани и инсулинорезистентности при метаболическом синдроме, а также прогностическим маркером острого панкреатита или рака ПЖ. При проведении дифференциальной диагностики фиброза ПЖ с применением УЗИ необходимо учитывать вероятность жировой инфильтрации печени. Стеатоз печени может являться причиной необъяснимой экзокринной недостаточности ПЖ. В таком случае для ее коррекции понадобится проведение заместительной терапии ферментными препаратами.
Список литературы находится в редакции.
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 2 (48), травень 2018 р.