20 червня, 2018
Лікування пацієнтів із атопічним дерматитом

Рекомендації Американської академії алергії, астми та імунології1,
Американської колегії з проблем алергії, астми та імунології2,
Об’єднаного комітету з питань алергії, астми та імунології3 (лютий 2013 р.)
 Атопічний дерматит (АД) – генетично зумовлене хронічне запальне захворювання шкіри, яким уражені 10-20% дітей і 1-3% дорослого населення. Найчастіше АД проявляється до 5 років (хоча у 20% пацієнтів він розвивається в зрілому віці) і є першим проявом атопії у багатьох пацієнтів, які згодом страждають на алергічний риніт, астму або обидва ці захворювання (так званий «атопічний марш»). Основні відмінні риси захворювання – свербіж, розчухування, хронічне і або рецидивуюче екзематозне ураження. Для немовлят і дітей молодшого віку характерне ураження обличчя, шиї і шкіри розгинальних поверхонь. У дітей старшого віку і дорослих ураження шкіри часто супроводжується ліхенізацією шкіри згинальних складок кінцівок. Фактори, які можуть посилити симптоми АД, включають температуру, вологість, подразники, інфекції, продукти харчування, аеро- і контактні алергени, емоційне напруження. Приблизно у третини дітей розвиток АД пов’язаний із харчовою алергією або харчовою сенсибілізацією (наявністю специфічних IgE без клінічних ознак харчової алергії).
Атопічний дерматит (АД) – генетично зумовлене хронічне запальне захворювання шкіри, яким уражені 10-20% дітей і 1-3% дорослого населення. Найчастіше АД проявляється до 5 років (хоча у 20% пацієнтів він розвивається в зрілому віці) і є першим проявом атопії у багатьох пацієнтів, які згодом страждають на алергічний риніт, астму або обидва ці захворювання (так званий «атопічний марш»). Основні відмінні риси захворювання – свербіж, розчухування, хронічне і або рецидивуюче екзематозне ураження. Для немовлят і дітей молодшого віку характерне ураження обличчя, шиї і шкіри розгинальних поверхонь. У дітей старшого віку і дорослих ураження шкіри часто супроводжується ліхенізацією шкіри згинальних складок кінцівок. Фактори, які можуть посилити симптоми АД, включають температуру, вологість, подразники, інфекції, продукти харчування, аеро- і контактні алергени, емоційне напруження. Приблизно у третини дітей розвиток АД пов’язаний із харчовою алергією або харчовою сенсибілізацією (наявністю специфічних IgE без клінічних ознак харчової алергії).
Діагноз АД базується радше на клінічній картині, ніж на результатах діагностичного тестування, однак раціональне використання шкірних проб або лабораторних тестів на наявність IgE до відповідних алергенів є чутливим способом визначення факторів, що провокують алергію. Часто необхідне проведення подвійних сліпих харчових провокацій для визначення причетності певного харчового продукту до розвитку симптомів.
Для ефективного ведення пацієнта з АД необхідні:
- уникнення тригерного чинника;
- заходи з відновлення бар’єрної функції шкіри;
- терапія протизапальним препаратом.
Визначати індивідуальний тригерний чинник, якого слід уникати, необхідно на основі ретельного вивчення анамнезу і результатів тестування на специфічні IgE. Бар’єрна функція може бути поліпшена шляхом ретельної гідратації і застосування зволожувальних засобів, наприклад, приймання теплої ванни протягом щонайменше 10 хвилин з подальшим негайним застосуванням зволожувального крему.
Що ж до фармакотерапії пацієнтів з АД протизапальними препаратами, тут можливі варіанти. Адекватним вибором для більшості пацієнтів є місцеві кортикостероїди, ефективність застосування яких залежить від урахування індивідуальних особливостей, а саме тяжкості дерматиту, локалізації та розмірів уражених ділянок шкіри, а також від віку пацієнта.
У разі клінічних загострень може знадобитися тимчасовий перехід на більш потужний топічний препарат. У дорослих і дітей (≥ 2 років) з АД протизапальними препаратами другої лінії терапії є інгібітори кальциневрину – такролімус і пімекролімус. Їхня дія полягає у припиненні активації лімфоцитів та інших запальних клітин, що робить ці засоби невід’ємною складовою лікування АД.
До інших методів терапії пацієнтів із тяжкими або резистентними формами АД належать застосування вологих і оклюзійних пов’язок, фототерапії, системної терапії імунодепресантами (циклоспорин) і антиметаболітами. У деяких випадках може знадобитися короткострокова госпіталізація, яка дає змогу зменшити вплив факторів довкілля й емоційних тригерів; провести інтенсивне навчання пацієнтів; здійснити діагностичне тестування (шкірні тести, виявлення харчової сенсибілізації); застосувати за наявності показань внутрішньовенне введення антибіотиків і агресивне місцеве лікування.
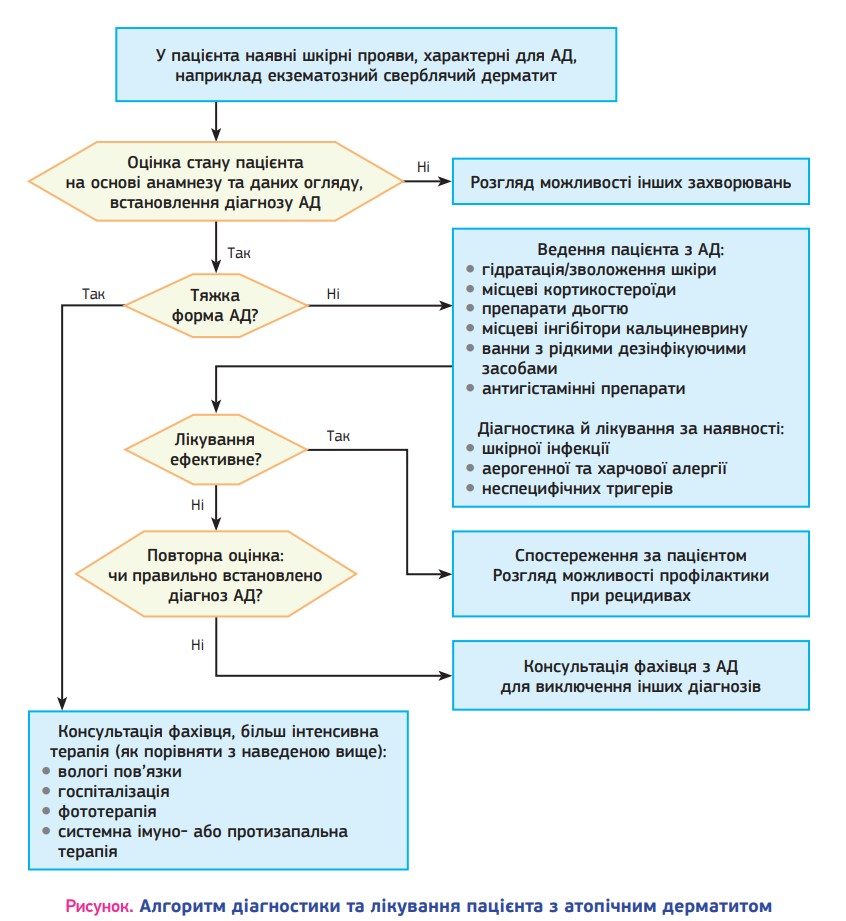
Основні етапи діагностування та ведення пацієнта з атопічним дерматитом (АД) представлено на рисунку.
Визначення
1. Атопічний дерматит являє собою спадкове хронічне запальне захворювання шкіри, що зазвичай проявляється в першому півріччі життя і в дитинстві, але може зберегтися або розвинутися й у зрілому віці. (рівень доказовості C)
Імунопатологічні й генетичні аспекти
2. Більшість пацієнтів із АД мають підвищений рівень сироваткових IgE, що корелює з клінічними показниками тяжкості захворювання. (C)
3. Призначаючи лікування, слід брати до уваги, що вогнища гострого ураження шкіри при АД містять складну суміш запальних цитокінів. Зокрема в них виявляють Т-хелперні (Th) клітини: Th2, що продукують інтерлейкіни IL-4, IL-5 та IL-13, і Th22, які виробляють IL-22; у значній кількості хронічних уражень ідентифікують також Th1-клітини, які експресують інтерферон γ. (C)
4. Загальноприйнятою є точка зору, що розвиток AД, принаймні частково, зумовлений дефектами шкірних бар’єрів, набутими або генетичними. Результати досліджень мишачих моделей АД дають вагомі підстави припускати, що ці дефекти бар’єрів провокують адаптивну імунну відповідь на шкірні антигени.
5. Слід брати до уваги, що неадекватна вроджена імунна реакція на шкірні мікроби є частково відповідальною за сприйнятливість до інфекцій і колонізацію шкіри пацієнтів з АД Staphylococcus aureus, а також багатьма вірусами. (C)
6. При лікуванні пацієнтів важливо пам’ятати, що АД є комплексним захворюванням, зумовленим взаємодією численних генів схильності до цього захворювання з мікросередовищем (наприклад, запалення тканин) і макросередовищем організму господаря. (B)
Клінічний діагноз
7. Діагностувати АД слід на основі сукупності клінічних ознак. Важливою для діагностування є наявність свербежу і хронічних/рецидивуючих екзематозних пошкоджень шкіри типових вигляду і локалізації у пацієнтів із проявами атопії в анамнезі. (C)
8. При фізикальному обстеженні слід звертати увагу на гострі й підгострі ураження шкіри, які наявні найчастіше у немовлят і дітей молодшого віку та супроводжуються сильним свербежем, еритематозними папуловезикулярними пошкодженнями з екскоріаціями і серозним ексудатом (D). Для хронічного АД характерні ліхенізація, папули і екскоріації. (D)
Терапія першої лінії
9. Інтенсивність ведення і лікування пацієнта з АД визначається тяжкістю захворювання і його впливом на якість життя пацієнта і членів його сім’ї. (A)
10. Слід встановити разом із пацієнтом мету лікування, яка може включати зменшення частоти і тяжкості загострень, збільшення тривалості періодів без рецидивів. (D)
11. Необхідно застосовувати систематичний комплексний підхід, який передбачає зволоження шкіри, лікування місцевими протизапальними препаратами, протисвербіжну й антибактеріальну терапію, усунення факторів, що погіршують стан. Слід проводити оцінку успішності вибраного підходу і за необхідності змінювати план лікування. (А)
Зволоження шкіри
12. При АД знижується бар’єрна функція шкіри, що призводить до підвищеної втрати води і висушування шкіри, тому слід рекомендувати пацієнтам зволожувати шкіру прийманням теплої ванни протягом не менше 10 хвилин із подальшим застосуванням зволожувального крему. (D)
13. Застосування зволожувальних засобів необхідно рекомендувати як терапію першої лінії. (D)
Місцеві кортикостероїдні препарати
14. Якщо застосування одних лише зволожувальних засобів недостатньо для контролю АД, слід рекомендувати пацієнту терапію місцевими кортикостероїдами. (А)
15. Кортикостероїди низької активності рекомендовано використовувати для підтримувальної терапії, помірної і високої активності – для короткотривалого лікування клінічного загострення. (A)
16. Не слід призначати сильнодіючі фторовані кортикостероїди для використання на шкірі обличчя, повік, статевих органів і ділянках попрілостей або у дітей раннього віку. (D)
17. Кортикостероїди надвисокої активності рекомендовано призначати тільки протягом дуже короткого строку (1-2 тижні), не застосовуючи їх на шкірі обличчя і ділянках шкірних складок. (D)
18. Призначаючи місцеві стероїди, клініцисти повинні пам’ятати, що ступінь поглинання кортикостероїдів через шкіру, а отже, і потенціал для розвитку системних побічних ефектів безпосередньо залежать від площі задіяної поверхні шкіри, товщини шкіри, використання оклюзійних пов’язок і ступеня активності кортикостероїдів. (D)
Інгібітори кальциневрину для місцевого застосування
Препарати такролімусу
19. Є докази на користь застосування мазі, що містить такролімус, ефективної і безпечної для лікування дорослих і дітей від 2 років із АД, – у більшості пацієнтів свербіж зменшується протягом 3 днів після початку терапії. (A)
20. Слід розглянути можливість використання мазі з такролімусом, оскільки, на відміну від місцевих стероїдів, вона не викликає атрофію шкіри при лікуванні екземи на обличчі, повіках і складках шкіри, яка розвивається за браком відповіді на терапію місцевими стероїдами низької активності. (A)
21. Необхідно попереджати пацієнтів, що протягом першого тижня місцевого застосування такролімусу можуть проявлятися минущі локалізовані відчуття печіння і свербежу. Це може обмежити застосування препарату в деяких осіб. (A)
22. Після досягнення контролю над загостренням можна розглянути можливість застосування такролімусу в формі мазі двічі на день, а надалі двічі на тиждень на ділянках, схильних до екземи, з метою профілактики загострення. (A)
Препарати пімекролімусу
23. Слід розглянути можливість використання для місцевого лікування крему, що містить пімекролімус – інгібітор кальциневрину, який є безпечним, сприяє зменшенню кількості загострень, знижує потребу в кортикостероїдах, не викликає атрофію шкіри, дає змогу контролювати свербіж. (A)
Препарати дьогтю
24. Хоча препарати дьогтю широко використовуються для лікування хворих із АД, їхню ефективність не підтверджено результатами рандомізованих контрольованих досліджень. (A)
25. Розроблено нові препарати на основі кам’яновугільного дьогтю, які є більш прийнятними з точки зору запаху і забруднення одягу, ніж «старі». (B)
26. Препарати дьогтю не слід використовувати при гострому запаленні шкіри, оскільки це може призвести до її додаткового подразнення. (D)
Антигістамінні препарати
27. У деяких пацієнтів застосування антигістамінних препаратів може бути корисним для полегшення свербежу, пов’язаного з АД. (С)
28. Зазвичай місцеві антигістамінні препарати не рекомендовані через потенційну небезпеку сенсибілізації шкіри. (C)
Вітамін D
29. Пацієнтам із АД, можливо, буде корисний додатковий прийом вітаміну D, особливо при недостатньому рівні його споживання. (B)
Ванни з рідкими дезінфікуючими засобами
30. Слід розглянути додаткове застосування ванн із дезінфекуючими засобами двічі на тиждень для зменшення тяжкості АД, особливо у пацієнтів із рецидивуючими інфекціями шкіри. (A)
Виявлення та усунення провокуючих факторів
31. Слід рекомендувати уникнення поширених подразників (мила, косметичних засобів, шерсті та хімічних речовин), які викликають свербіж, що зумовлює розчухування (так званий цикл «свербіж-розчухування»). (B)
32. Можна також порекомендувати контроль температури і вологості для запобігання свербежу, викликаному надмірним теплом, вологістю й потовиділенням. (D)
33. Можливі тригери АД можна визначити за допомогою шкірних тестів, лабораторних досліджень наявності специфічних IgE, а в деяких випадках – за допомогою нашкірних алергічних проб (патч-тестів) для виявлення негайних або сповільнених реакцій на білкові алергени. Слід визначати тільки потенційно значущі алергени, оскільки тестування, особливо щодо харчових продуктів, має низьку специфічність. (В)
34. Необхідно пам’ятати, що у немовлят і дітей раннього віку тригерами АД найчастіше є харчові алергени. (D) Щодо дітей віком до 5 років із проявами АД від помірних до тяжких запропоновано розглядати можливість обмеженого тестування на визначення харчового алергену, якщо АД проявляється постійно, незважаючи на оптимальне ведення та місцеве лікування або якщо в анамнезі відзначено алергічну реакцію негайного типу після прийому певної їжі.
35. Не слід рекомендувати широку елімінаційну дієту лише на основі позитивних результатів шкірного тесту або визначення IgE, оскільки це загрожує розвитком харчової недостатності. Окрім того, навіть при численних позитивних результатах шкірних тестів більшість пацієнтів при проведенні перорального провокаційного тесту будуть реагувати лише на кілька продуктів. (B)
36. Через здатність викликати загострення АД слід звести до мінімуму вплив таких джерел аероалергенів, як кліщі домашнього пилу, тварини, пилок рослин. (A)
Мікроорганізми
37. Слід пам’ятати, що інфікування шкіри S. aureus є постійною проблемою у пацієнтів із проявами АД від помірних до тяжких, і в їхній шкірі наявні IgE проти токсинів стафілокока. (B)
38. Короткий курс відповідного системного антибіотика слід призначати тільки пацієнтам, клінічно інфікованим S. aureus. У регіонах із високою частотою метицилін-стійкого S. aureus доцільно проводити бактеріальне дослідження зразка шкіри пацієнта і в очікуванні його результатів починати лікування із застосуванням кліндаміцину, доксицикліну або триметоприм-сульфаметоксазолу. (A)
39. Перебіг AД можуть ускладнювати рецидивуючі вірусні інфекції шкіри, такі як вірус простого герпесу, збудники бородавок і контагіозного молюска. Слід діагностувати і своєчасно лікувати розсіяний герпес або герпетиформну екзему, застосовуючи системні противірусні засоби. (B)
40. Не слід проводити імунізацію пацієнтів із АД або членів сім’ї, які з ними контактують, проти натуральної віспи, оскільки в них може бути наявна поширена потенційно смертельна шкірна інфекція, що має назву вакцинальна екзема і схожа за проявами на герпетиформну екзему. (C)
41. Слід брати до уваги небезпеку грибкових інфекцій, які можуть ускладнити перебіг AД і спричинювати загострення. Діагностувати наявність дерматофітів можна з використанням КОН-тесту або грибкової культури. Дріжджові гриби роду Malassezia, інфікування якими є особливою проблемою в молодих пацієнтів зі стійкою екземою шкіри голови і шиї, можуть бути діагностовані клінічно або із застосуванням КОН-тесту; можна також визначати наявність IgE до різних видів Malassezia. (C)
Якість життя та емоційний стрес
42. АД значно впливає на якість життя пацієнта і його сім’ї, підвищуючи ризик розвитку психологічних розладів. Слід розпитувати хворого про стресові й емоційні чинники, які можуть викликати загострення і сприяти імунній активації, появі свербежу й розчухування. (C)
43. Потрібно оцінювати порушення сну. Якість сну може поліпшити протизапальна терапія; слід також розглянути можливість застосування терапевтичних засобів або направити хворого до сомнолога/психолога в тяжких випадках і якщо сон не поліпшується в стадії ремісії. (C)
Навчання пацієнта
44. Для досягнення ефективного контролю над АД слід пояснити пацієнтам і членам їхніх сімей хронічну природу захворювання; розповідати про вплив чинників, що викликають загострення; консультувати щодо безпеки препаратів і можливих побічних реакцій. Слід також забезпечити наочну демонстрацію технологій догляду за шкірою, надати письмовий план лікування й інформацію про організацію підтримки хворих. (D)
Ведення проблемних пацієнтів із атопічним дерматитом
Консультація фахівця з атопічного дерматиту
45. Пацієнтів зі стійкими до терапії першої лінії формами АД слід направляти до фахівця з AД. (D)
Вологі пов’язки
46. Застосування вологих обгортувальних пов’язок у поєднанні з місцевими кортикостероїдами слід рекомендувати для лікування хворих на стійкі форми АД. (А) Вологі пов’язки сприяють відновленню шкірного бар’єру, підвищують ефективність місцевих стероїдів при одночасному використанні і захищають шкіру від постійного розчухування, що дає змогу більш швидко загоюватися ураженням з екскоріацією. (B)
Системні імуномодулювальні препарати
47. Показано, що застосування таких імуномодуляторів, як циклоспорин, мофетілу мікофенолат, азатіоприн, інтерферон-γ і кортикостероїди, корисне у пацієнтів із тяжкими стійкими формами АД, однак слід брати до уваги можливість серйозних побічних реакцій. (A)
Фототерапія
48. Терапія ультрафіолетовим світлом може бути корисною у випадках резистентного АД. Найбільш ефективним є застосовування вузького спектра ультрафіолетових променів типу B, яке практикують у США. (А)
Госпіталізація
49. Госпіталізація може поліпшити стан пацієнта з АД завдяки ізоляції від алергенів і подразників навколишнього середовища, усуненню стресових чинників, а також завдяки отриманню пацієнтом і тими, хто ним опікується, нових знань щодо поліпшення сну, вирішення психосоціальних проблем, корекції лікування і поліпшення прихильності до лікувального режиму. (D)
Алерген-специфічна імунотерапія
50. Отримані на сьогодні дані досліджень дають змогу в деяких випадках розглядати можливість застосування в пацієнтів із АД, чутливих до аероалергенів, імунотерапії алергеном кліща домашнього пилу. (B)
Експериментальні методи лікування атопічного дерматиту
51. Нині досліджується можливість застосовувати внутрішньовенне введення імуноглобуліну, препарати омалізумаб і ритуксимаб для лікування пацієнтів із AД. Оскільки ефективність цих методів ще не доведена, застосовувати їх не рекомендовано.
1 AAAAI – The American Academy of Allergy, Asthma and Immunology.
2 ACAAI – The American College of Allergy, Asthma and Immunology.
3 The Joint Council of Allergy, Asthma and Immunology.
Реферативний огляд підготовано за матеріалами Schneider L., Tilles S., Lio P., Boguniewicz M. et al. Atopic dermatitis: A practice parameter update 2012. J. Allergy Clin. Immunol. 2013; 131: 295-9 (http://www.jcaai.org)