21 червня, 2018
Замена антидепрессанта у пациентов с большим депрессивным расстройством: выбираем препарат
Согласно клиническим данным 40-60% пациентов с большим депрессивным расстройством (БДР) не отвечают адекватно на первую линию фармакотерапии, то есть не достигают ≥50% снижения показателей по клиническим шкалам оценки депрессии (Rush et al., 2006). Кроме того, успешному лечению БДР часто препятствует плохая переносимость антидепрессантов: несоблюдение назначений или прекращение приема антидепрессантов из-за развития побочных реакций – две основные причины неудачной терапии депрессии (A. K. Ashton et al., 2005; P. S. Masand, 2003).
В среднем половина пациентов (46-52%) прекращает прием антидепрессантов на шестом месяце фармакотерапии (R.A. Sansone, L.A. Sansone, 2012). В исследовании, в котором 60% пациентов полностью прекратили лечение антидепрессантами, среди причин отказа упоминались недостаточная эффективность (44%), недовольство ощущениями, которые вызывает препарат (36%), недостаточный интерес к сексу (22%), повышенная утомляемость (17%) и увеличение массы тела (15%) (A.K. Ashton et al., 2005).
Систематический обзор данных клинических исследований показал, что лечение сертралином, венлафаксином, циталопрамом, пароксетином, флуоксетином, имипрамином, фенелзином, дулоксетином, эсциталопрамом и флувоксамином было ассоциировано с сексуальными нарушениями, частота которых была значительно выше, чем в группе плацебо, и составляла от 25 до 80% (A. Serretti, A. Chiesa, 2009). Таким образом, значительная доля пациентов с БДР нуждается в замене антидепрессанта в ходе лечения.
Пациентам с БДР, которые не отвечают на терапию препаратами первой линии либо плохо ее переносят, рекомендована замена антидепрессанта (переключение терапии). В современной практике переключение терапии – распространенная стратегия в случае неэффективности или плохой переносимости антидепрессанта. Так, анализ британской клинической базы данных показал, что замена антидепрессантов происходит в 39% случаев (F. Lamy et al., 2015).
Согласно результатам недавнего многоцентрового исследования, проведенного в Испании, примерно 40% пациентов, не отвечавших на начальную терапию, переключили на другой антидепрессант, в 24% случаях был назначен второй антидепрессант, остальные пациенты получали адъювантную терапию для усиления эффектов антидепрессантов – аугментацию (18%) или у них применялись смешанные стратегии терапии (19%) (M. Garcia-Toro et al., 2012). При обзоре фармакологических стратегий при БДР в США были получены сопоставимые результаты (J.F. Goldberg et al., 2015).
Для принятия решения о переключении на другой антидепрессант в распоряжении клинициста имеется ограниченное число данных, на основании которых можно выбрать препарат замены (American Psychiatric Association, 2010; B.N. Gaynes et al., 2012; National Collaborating Centre for Mental Health, 2010; P. Santaguida et al., 2012; A. Tadic et al., 2016). Недавний метаанализ показал, что имеется всего несколько рандомизированных контролируемых исследований, оценивающих замену антидепрессанта в связи с неэффективностью лечения, а высококачественные данные в поддержку замены по сравнению с продолжением использования первоначально назначенного антидепрессанта отсутствуют (T. Bschor et al., 2016).
Лишь в нескольких прямых сравнительных исследованиях оценивали эффективность и переносимость различных антидепрессантов как препаратов замены у лиц, прекративших терапию из-за неэффективности или побочных эффектов (S. Kasper, G. Hajak, 2013; A.J. Lenox-Smith, Q. Jiang, 2008; S.A. Montgomery et al., 2014; A.J. Rush et al., 2006). Только в одном исследовании было проведено прямое сравнение препаратов замены у пациентов с сексуальной дисфункцией, связанной с приемом антидепрессантов (A.K. Ashton et al., 2005).
Вортиоксетин как препарат замены при неудачной терапии БДР
Вортиоксетин – одобренный мультимодальный антидепрессант, механизм действия которого отличается от такового селективных ингибиторов обратного захвата серотонина (СИОЗС) и норадреналина (СИОЗН). Вортиоксетин обладает уникальным механизмом действия: препарат ингибирует 5-HT-транспортер и является антагонистом 5-НТ3-, 5-HT7- и 5-HT1D-, частичным агонистом 5-HT1B-, агонистом 5-HT1A-рецепторов (B. Bang-Andersen et al., 2011; L. Westrich et al., 2012). Эти взаимодействия приводят к модуляции передачи нейротрансмиссии в нескольких системах, преимущественно серотониновой, но также, возможно, в системах норадреналина, дофамина, гистамина, ацетилхолина, ГАМК и глутамата (C. Sanchez et al., 2015).
Вортиоксетин оценивали как препарат замены путем прямого и косвенного сравнения у пациентов с неадекватным ответом на терапию СИОЗС и СИОЗН, а также у пациентов, прекративших лечение из-за развития сексуальной дисфункции.
Прямое сравнение терапии вортиоксетином и агомелатином
В проспективном рандомизированном двойном слепом 12-недельном исследовании с гибкой дозировкой REVIVE (S.A. Montgomery et al., 2014) (NCT01488071) оценивалась эффективность вортиоксетина в сравнении с агомелатином у пациентов с БДР, не отвечавших адекватно на терапию СИОЗС и СИОЗН в течение минимум 6 нед. Соответствующие критериям лица переводились на вортиоксетин (10 или 20 мг/сут, n=252) или агомелатин (25 или 50 мг/сут, n=241).
Агомелатин был выбран в качестве препарата сравнения потому, что, как и вортиоксетин, имеет механизм действия, отличный от СИОЗС и СИОЗН (S.M. Stahl, 2014). Антидепрессантный эффект агомелатина, как полагают, обусловлен его действием как агониста рецепторов мелатонина МТ1 и МТ2 и как антагониста серотониновых рецепторов 5-HT2C (B. Guardiola-Lemaitre et al., 2014).
В первичном анализе эффективности среднее изменение суммарной оценки относительно исходного уровня по шкале оценки депрессии Монтгомери – Асберг (MADRS) на 8-й неделе терапии составило -16,5 баллов для вортиоксетина и -14,4 – для агомелатина.
Различие средних изменений оценок при лечении данными препаратами составило -2,2 балла (95% доверительный интервал (ДИ): от -3,5 до -0,8; р=0,0018), что указывает на более высокую эффективность вортиоксетина (European Medicines Agency, 2000). На 12-й неделе вортиоксетин сохранял преимущества со статистически значимым различием средних изменений суммарной оценки относительно исходного уровня по шкале MADRS в -2,0 балла (р<0,01).
Описанная эффективность согласовалась с конечными точками (S.A. Montgomery et al., 2014). На 8-й неделе в группе, получавшей вортиоксетин, на терапию отвечали 61,5% (улучшение ≥50% относительно исходного уровня по шкале MADRS), тогда как в группе агомелатина – 47,3% пациентов (р<0,01). Ремиссия (суммарная оценка по шкале MADRS ≤10) в группе вортиоксетина отмечалась у 40,5%, тогда как в группе агомелатина – у 29,5% пациентов (р<0,01).
Различия в группах сохранялись и на 12-й неделе: ответ на вортиоксетин отмечался у 69,8%, тогда как на агомелатин – у 56% пациентов (р<0,01). Ремиссия отмечалась у 55,2% пациентов в группе вортиоксетина и у 39,4% – в группе агомелатина (р<0,001). Эти результаты свидетельствуют о статистически более высокой вероятности достижения ремиссии в группе вортиоксетина по сравнению с группой агомелатина (разница рисков, РР -11%; р<0,01) (рис. 1).
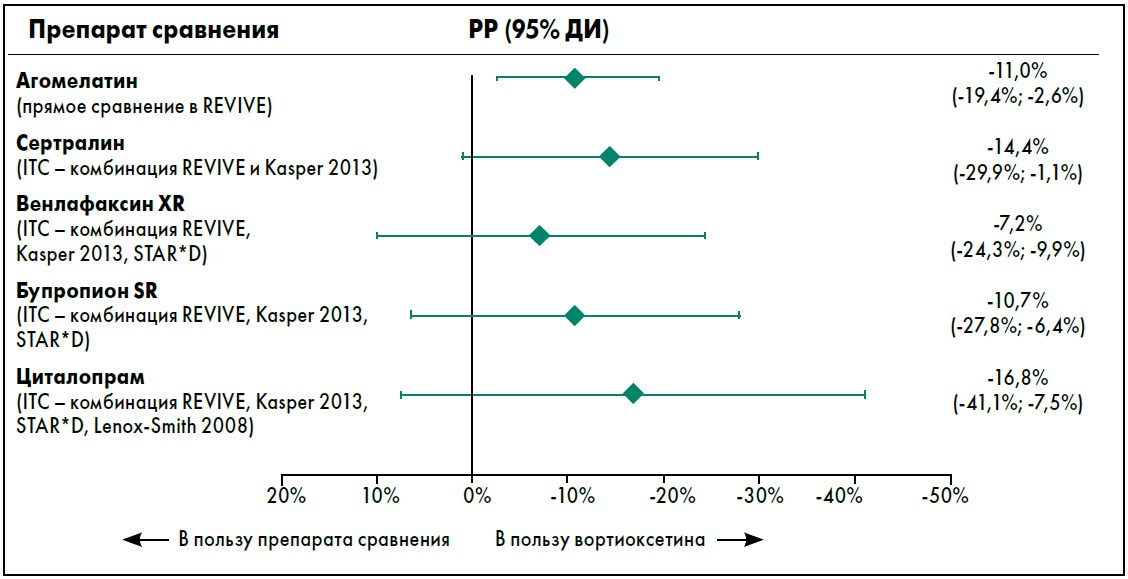 Рис. 1. Разница рисков в отношении ремиссии: вортиоксетин vs препараты сравнения. Адаптировано из M. Brignone et al. (2016)
Рис. 1. Разница рисков в отношении ремиссии: вортиоксетин vs препараты сравнения. Адаптировано из M. Brignone et al. (2016)
Кроме того, вортиоксетин имел преимущества при самостоятельной оценке пациентами изменений относительно исходного уровня на 8-й неделе лечения. Средние изменения суммарного балла относительно исходного уровня (± стандартная ошибка, СО) по шкале самооценки дезадаптации Шихана (SDS) составили -9,28 (±5,3) балла в группе вортиоксетина и -7,06 (±0,55) балла в группе агомелатина (р<0,01).
Снижение балла по шкале Шихана относительно исходного уровня является показателем функционального улучшения; таким образом, на фоне приема вортиоксетина оно было более выражено. В пользу вортиоксетина говорили также изменения баллов по шкале SDS в отдельных сферах жизни: работа, социальная деятельность, семья (р<0,01) (S.A. Montgomery et al., 2014).
Средние изменения относительно исходного уровня (±СО) показателей общего состояния здоровья на основании Европейского опросника для оценки качества жизни (EuroQol 5 Dimensions) составили 20,6 (±1,2) в группе вортиоксетина и 15,6 (±1,3) в группе агомелатина (р<0,01) (более высокие показатели соответствуют лучшему состоянию здоровья).
Средние изменения относительно исходного уровня (±СО) суммарного балла на основании шкалы семейного функционирования при депрессии (Depression and Family Functioning Scale) составили -10,8 (±0,7) в группе вортиоксетина и -7,9 (±0,7) в группе агомелатина (р<0,01) (снижение балла относительно исходного уровня указывает на улучшение) (S.A. Montgomery et al., 2014).
Непрямое сравнение терапии вортиоксетином и другими антидепрессантами
С целью оценки относительной эффективности и переносимости вортиоксетина в сравнении с другими препаратами был проведен систематический обзор литературы и построена сеть доказательств для косвенного сравнения (indirect treatment comparisons, ITC) методов терапии. Основные использованные методы оценки и частично результаты опубликовали ранее M. Brignone и соавт. (2016).
При косвенном сравнении ориентировались на два показателя: уровень ремиссии (определялся как балл ≤10 по шкале MADRS или ≤7 по шкале оценки депрессии Гамильтона – Hamilton Depression Rating Scale, HAM-D) и уровень прекращения лечения в связи с развитием побочных эффектов.
В сеть доказательств были включены вортиоксетин, агомелатин, венлафаксин, сертралин, бупропион и циталопрам, и использованы данные четырех исследований (рис. 2): исследования REVIVE (S.A. Montgomery et al., 2014); ретроспективного анализа рандомизированного контролируемого исследования, сравнивающего агомелатин с сертралином (S. Kasper, G. Hajak, 2013); исследования STAR*D монотерапии сертралином, венлафаксином пролонгированного высвобождения (XR) и бупропионом замедленного высвобождения (SR) после неудачного лечения циталопрамом (A.J. Rush et al., 2006); рандомизированного контролируемого исследования, сравнивающего венлафаксин XR с циталопрамом после неудачного лечения СИОЗС (A.J. Lenox-Smith, Q. Jiang, 2008).
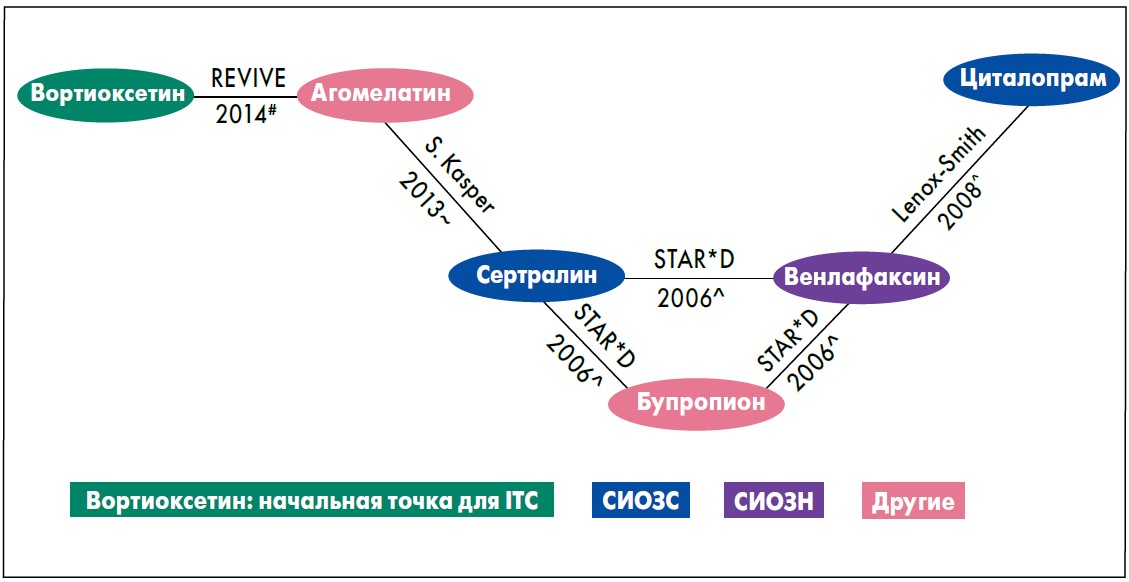 Рис. 2. Базовая сеть для косвенного сравнения терапии
Рис. 2. Базовая сеть для косвенного сравнения терапии
В сеть доказательств включались только исследования с активным препаратом сравнения (не плацебо), которые оценивали переключение пациентов на другой антидепрессант. Косвенное сравнение проводили методом Bucher (H.C. Bucher et al., 1997).
Косвенное сравнение терапий показало более высокую вероятность ремиссии для вортиоксетина в сравнении с сертралином (РР -14,4%), венлафаксином XR (РР -7,2%), бупропионом SR (РР -10,7%) и циталопрамом (РР -16,8%) (рис. 1).
Таким образом, для пациентов с БДР, которых переключили с терапии СИОЗС и СИОЗН, более высокая эффективность вортиоксетина в сравнении с агомелатином была статистически достоверной и клинически значимой. Кроме того, на основании косвенного сравнения можно предположить более высокую эффективность вортиоксетина как препарата замены в сравнении с другими широко применяемыми антидепрессантами (сертралином и циталопрамом как СИОЗС, венлафаксином как СИОЗН и бупропионом как атипичным антидепрессантом).
Относительная переносимость/безопасность вортиоксетина как препарата замены
Прямое сравнение терапии у пациентов с переключением из-за недостаточной эффективности
В исследовании REVIVE оценивалась переносимость вортиоксетина и агомелатина у пациентов с БДР, не отвечавших адекватно на начальную терапию СИОЗС и СИОЗН, а также частота прекращения лечения из-за побочных явлений. Наиболее распространенными побочными явлениями, связанными с лечением (отмечены у ≥5% пациентов в любой группе терапии), были тошнота, головная боль, головокружение, сонливость (S.A. Montgomery et al., 2014).
Только тошнота встречалась в группе вортиоксетина чаще, чем агомелатина (16,2 и 9,1% соответственно). В связи с развитием побочных явлений от терапии отказались 5,9% пациентов в группе вортиоксетина и 9,5% – в группе агомелатина (S.A. Montgomery et al., 2014).
У пациентов, получавших вортиоксетин, вероятность прекращения терапии в связи с развитием побочных явлений была ниже, чем у пациентов, получавших агомелатин (РР 3,6%) (рис. 3).
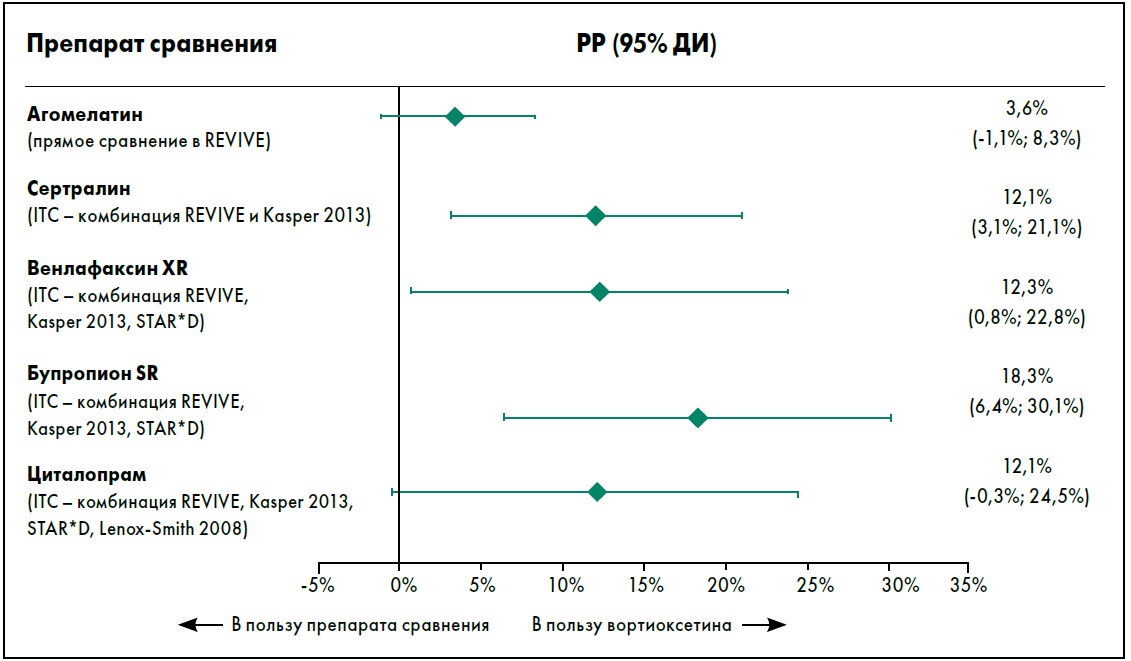 Рис. 3. Разница рисков прекращения терапии в связи с развитием побочных явлений: вортиоксетин vs препараты сравнения. Адаптировано из M. Brignone et al. (2016)
Рис. 3. Разница рисков прекращения терапии в связи с развитием побочных явлений: вортиоксетин vs препараты сравнения. Адаптировано из M. Brignone et al. (2016)
Ретроспективный анализ данных исследования REVIVE показал, что профили переносимости вортиоксетина и агомелатина не зависели от того, с какого именно антидепрессанта происходило переключение на другую терапию (G. Papakostas et al., 2014). При этом частота тошноты при терапии вортиоксетином ниже у пациентов, которых переключили с других антидепрессантов, чем у пациентов, ранее не получавших лечения.
В связи с тем, что данные о переносимости терапии вортиоксетином в исследовании REVIVE сходны с теми, которые наблюдаются во всей популяции пациентов с БДР (D.S. Baldwin et al., 2016), и не зависят от предыдущего лечения (G. Papakostas et al., 2014), профиль переносимости, наблюдаемый во всей популяции пациентов с БДР, может быть применим и для пациентов, которые переключились на вортиоксетин с другого антидепрессанта.
Потенциал такого обобщения изучали с помощью ретроспективного анализа побочных явлений у пациентов с БДР, получавших терапию антидепрессантом в связи с текущим большим депрессивным эпизодом до включения в одно из 12 краткосрочных исследований в рамках программы клинических исследований вортиоксетина (E. Alvarez et al., 2012; D.S. Baldwin et al., 2012; J.P. Boulenger et al., 2014; N. Henigsberg et al., 2012; P.L. Jacobsen et al., 2015; R. Jain et al., 2013; C. Katona et al., 2012; A.R. Mahableshwarkar et al., 2015; A.R. Mahableshwarkar et al., 2015; A.R. Mahableshwarkar et al., 2013; R.S. McIntyre et al., 2014; A. Nishimura et al., 2014).
Профиль побочных явлений у пациентов, ранее получавших лечение, был сходен с тем, что наблюдался среди всех участников исследования, однако частота многих наиболее распространенных побочных явлений была ниже у тех, кто ранее получал лечение.
Показатели преждевременного прекращения терапии также были сходными в группе пациентов, переключенных с другого антидепрессанта, и среди всех участников исследования.
Непрямое сравнение терапии
При косвенном сравнении терапии переносимость оценивали как РР отказа от терапии в связи с развитием побочных эффектов. РР были статистически достоверно ниже для вортиоксетина в сравнении с сертралином (12,1%), венлафаксином XR (12,3%) и бупропионом SR (18,3%), а также количественно ниже для циталопрама (12,1%) (рис. 3). При использовании сети доказательств для косвенного сравнения терапии было показано, что вортиоксетин характеризуется более высокой эффективностью и лучшей переносимостью, чем различные антидепрессанты сравнения, широко назначаемые в клинической практике.
Переносимость пациентами, у которых переключение терапии связано с сексуальной дисфункцией
В двойном слепом исследовании в параллельных группах с гибкой дозировкой (P.L. Jacobsen et al., 2015) участвовали пациенты, которые ранее принимали СИОЗС на протяжении как минимум 8 нед и предъявляли жалобы на тяжелую сексуальную дисфункцию, связанную с терапией.
Пациенты были рандомизированы в группы, получавшие вортиоксетин (10 или 20 мг/сут, n=225) или эсциталопрам (10 или 20 мг/сут, n=222) в течение 8 нед. Симптомы БДР у пациентов были успешно купированы еще в период приема СИОЗС (циталопрам, пароксетин, сертралин): исходный суммарный балл по шкале MADRS (±СО) составлял для группы вортиоксетина 7,9±6,28, эсциталопрама – 8,3±6,53, со средним исходным уровнем по шкале общего клинического впечатления о тяжести заболевания (CGI-S) ≤3, что соответствует ремиссии.
В качестве первичной конечной точки рассматривались изменения относительно исходного уровня оценки по опроснику изменений сексуальной функции (Changes in Sexual Functioning Questionnaire Short Form – CSFQ‑14), где более высокий балл соответствует лучшей функции (A. Keller et al., 2006). На 8-й неделе среднее увеличение балла по шкале CSFQ‑14 было значительно выше в группе вортиоксетина (предел среднего ± СО 8,8±0,64) в сравнении с группой эсциталопрама (6,6±0,64; р=0,013). При этом улучшение сексуальной функции при терапии вортиоксетином не зависело от возраста, пола и исходной тяжести депрессии (рис. 4).
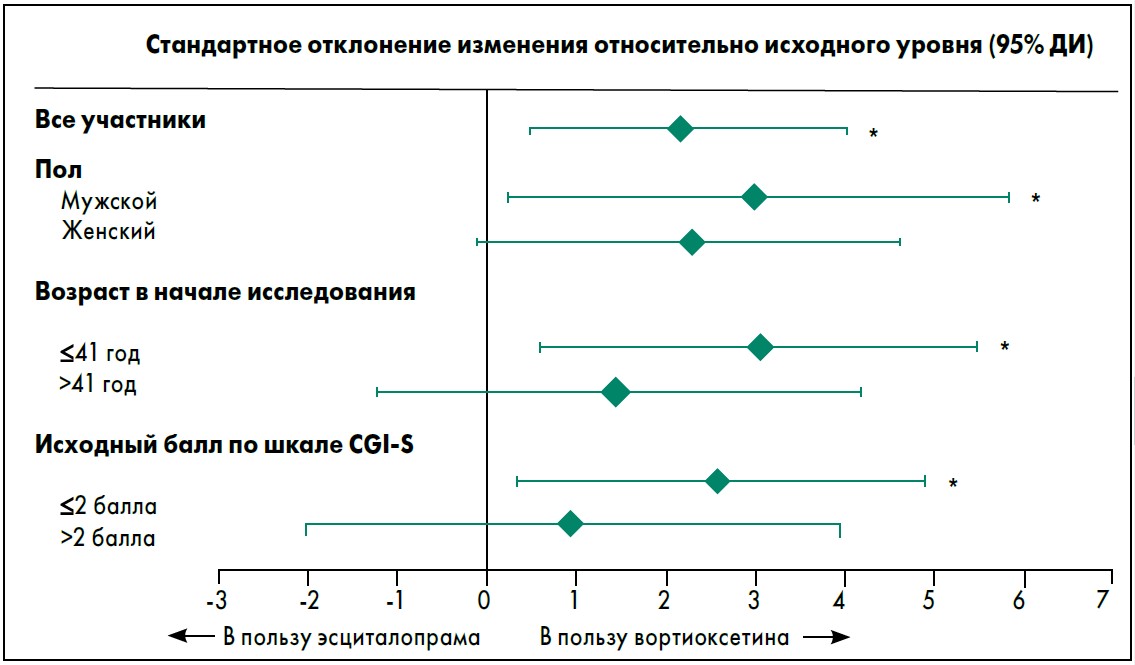 Рис. 4. Изменения балла по шкале CSFQ-14 относительно исходного уровня на 8-й неделе исследования: вортиоксетин и эсциталопрам. Адаптировано из P.L. Jacobsen et al. (2015)
Рис. 4. Изменения балла по шкале CSFQ-14 относительно исходного уровня на 8-й неделе исследования: вортиоксетин и эсциталопрам. Адаптировано из P.L. Jacobsen et al. (2015)
В группе вортиоксетина чаще, чем в группе эсциталопрама, отмечались тошнота (25,0 vs 5,4%), головная боль (9,4 vs 7,7%), головокружение (8,0 vs 5,0%) и зуд генерализованный (5,8 vs 0% соответственно). Частота раздражительности (7,2 vs 4,9%), усталости (5,4 vs 4,5%) и тревожности (5,4 vs 2,2%) была выше в группе эсциталопрама в сравнении с группой вортиоксетина. Тошнота при приеме вортиоксетина носила временный характер: средняя продолжительность – 7-7,5 суток. В связи с побочными явлениями от терапии отказались 9,4% пациентов в группе вортиоксетина и 6,3% – в группе эсциталопрама.
У пациентов, хорошо отвечавших на предыдущий антидепрессант, эффективность терапии на 8-й неделе сохранялась в обеих группах (в группе вортиоксетина ремиссия составляла 78,7%, в группе эсциталопрама – 77,3%; р=0,902) (P.L. Jacobsen et al., 2015).
Эти данные позволяют предположить, что пациенты с непереносимой сексуальной дисфункцией, получающие СИОЗС/СИОЗН, могут улучшить сексуальную функцию путем переключения на вортиоксетин без потери эффективности лечения БДР.
Выводы
- С учетом распространенности БДР и его негативного влияния на здоровье, экономическую производительность и качество жизни пациентов решение проблемы неэффективности или плохой переносимости антидепрессантов, используемых в первой линии терапии, является важной задачей здравоохранения и насущной потребностью психофармакологии.
- Пациенты, не отвечающие на лечение СИОЗС и СИОЗН, могут нуждаться в использовании новых препаратов с другим механизмом действия.
- Результаты прямых и косвенных сравнений вортиоксетина с некоторыми антидепрессантами, используемыми в первой линии терапии БДР, демонстрируют его более высокую эффективность и лучшую переносимость у пациентов с предыдущей неудачной терапией.
- В целом вортиоксетин демонстрирует благоприятный профиль безопасности и переносимости, в особенности в отношении изменений массы тела, сна и сексуальной дисфункции.
- Вортиоксетин является рациональным выбором для переключения пациентов с БДР с неадекватным ответом и/или непереносимыми побочными реакциями, наблюдающимися на фоне терапии СИОЗС или СИОЗН.
Обзор подготовлен по материалам статьи Thase M. E., Danchenko N., Brignone M., et al. Comparative evaluation of vortioxetine as a switch therapy in patients with major depressive disorder. European Neuropsychopharmacology,
2017; 27 (8): 773-781.
Подготовила Екатерина Ткаченко
Тематичний номер «Неврологія, Психіатрія, Психотерапія» № 2 (45) червень 2018 р.


